2. 安徽医科大学第二附属医院医学检验科,合肥 230601
2. Clinical laboratory department, the Second Affiliated Hospital, Anhui Medical University, Hefei, China 230601, China
误吸被定义为胃或口咽内容物进入喉和下呼吸道,引起气道梗阻、化学性肺炎、感染性肺炎等不同的临床征象[1]。目前,通过气管镜采集下呼吸道菌群测序的研究表明,宿主防御反应可使肺部微生物不断地迁移和清除[2-3],进而维持正常情况下肺内相对无菌环境,而误吸打破了这种平衡,进而引起不同的临床表现[4]。近年来吸入性肺炎的发生率不断增加,占社区获得性肺炎病例的7%~24%[5],已成为住院医疗患者的第二大常见诊断,病死率高达29.4%[6]。因此深入探讨吸入性肺炎患者的治疗措施,对改善该群患者的预后具有重要临床价值。
吸入性肺炎的进展取决于误吸颗粒的体积、频次、化学特征。50%的健康人在睡眠中虽也微误吸少量微生物,但没有导致临床显著的后果[7],因为只有吸入大量酸性胃液、大量低毒力病原微生物或异物才会导致肺损伤及感染[8-9],而且其前提是患者本身存在意识障碍、低血糖、谵妄、阿片类药物使用等导致误吸防御机制(声门闭合、咳嗽反射、黏液纤毛清除和肺泡巨噬细胞吞噬等[2-3])受损[10-11],才可能造成大容量的宏误吸。此外,不同的特征吸入物可导致不同的肺损伤,比如吸入pH低于2.5盐酸导致支气管黏膜脱上皮化、肺水肿、出血和中性粒细胞浸润[12];吸入的脂质也可引起低热和呼吸困难[13]。吸入物是引起肺损伤的源头,若能尽早清除误吸的化学物质或含有微生物团块,有望减轻肺损伤进展。
气管镜检查广泛应用于临床呼吸道疾病的诊断和治疗,已成为ICU医生评估肺部病情、引流气道分泌物、采样病原学、治疗肺部感染必备助力[14-16]。临床实践中发现,晚期气管镜灌洗时肺部往往充血水肿,治疗效果差;故本研究比较了是否早期给与气管镜灌洗的两组患者的基本资料特征、临床相关参数、病原学结果及预后指标,旨在评估早期气管镜-支气管灌洗是否能改善吸入性肺炎患者临床结局。
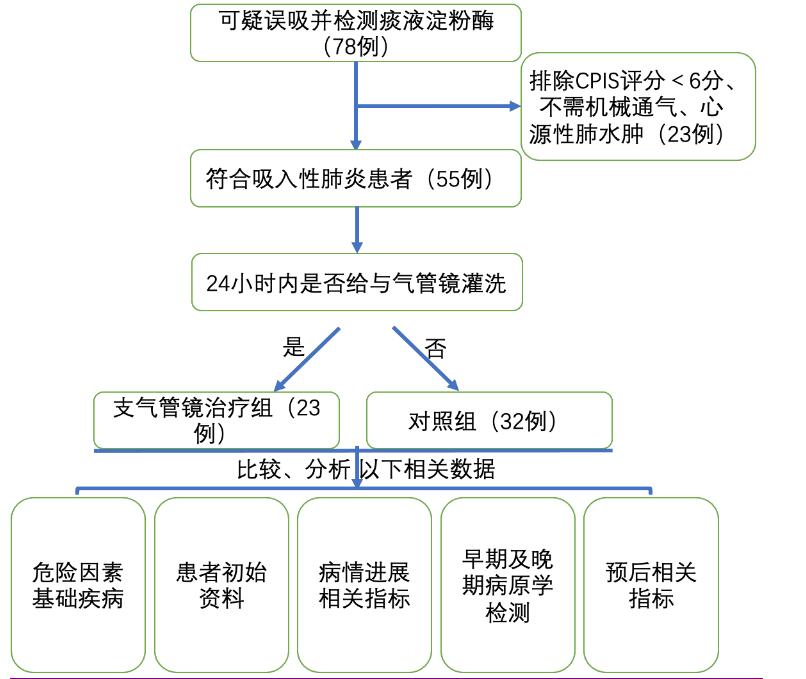
1 资料与方法 1.1 一般资料调取2020年1月至2021年4月安徽医科大学第二附属医院医疗信息系统中因可疑误吸留取痰液淀粉酶(AMS)患者信息,进一步通过病例及护理系统收集患者体温、呼吸频率、血气、痰液量及性状、胸片或胸部CT、痰液送检病原学结果,进行临床肺部感染评分(CPIS)≥6分同时评估是否符合吸入性肺炎诊断标准。排除标准:(1)不需要进行有创机械通气;(2) CPIS评分<6分;(3)排除心源性肺水肿,具体流程见图 1。本研究经安徽医科大学第二附属医院伦理委员会审核通过(NO.20121003)。
|
| 图 1 吸入性肺炎纳入流程及分组 Fig 1 Flow chart of enrollment and grouping of aspiration pneumonia |
|
|
CPIS评分标准:①平均12 h体温(℃):0分(36~38)、1分(38~39)、2分(>39或<36)②白细胞(×109/L):0分(4~11)、1分(11~16)、2分(>17或<4)③分泌物(×109/L):0分(无-少量)、1分(大量、非脓性)、2分(大量脓痰)④氧合指数[250 mmHg (1 mmHg=0.133 kPa)为界值):0分(>250)、2分(≤250)⑤X片:0分(无渗出)、1分(单个象限)、2分(≥2个象限)⑥痰或灌洗液培养(×109/L):0分(无菌生长)、2分(临床考虑致病菌生长2分)。
吸入性肺炎诊断标准[17]:⑴有误吸高危因素(≥1个):吞咽障碍、意识障碍、呕吐、心肺复苏、上气道受损、困难插管、其他影响咳嗽排痰因素(如食管手术、胸部损伤等);⑵肺炎及可能肺炎[17]:①以下症状≥3种(新的/加重的咳嗽、呼吸频率增加、氧饱和度降低、发热 > 38℃、白细胞增多或白细胞减少、化脓性分泌物、胸部啰音或支气管呼吸音)加上胸片显示斑片状浸润、肺叶实变或胸腔积液,诊断为肺炎; ②以上症状≥3种,但无胸片或胸片显示上述特征者,可能为肺炎。本文纳入患者除了符合上述⑴⑵诊断外,同时必须满足临床肺部感染评分CPIS≥6分。
1.2 研究方法 1.2.1 分组若在误吸导致病情加重24 h内气管镜灌洗为气管镜灌洗组、24以上给与气管镜或未给与气管镜灌洗均为对照组。
1.2.2 观察指标(1)基本资料:年龄、性别、体重指数;误吸危险因素、心率、呼吸频率、体温、痰液量、胸部正位X片评分(分四个象限:累积一个象限+1分,总分0~4分)、氧合指数(P/F)、C反应蛋白(CRP)、降钙素原(PCT)、白细胞介素6(IL-6)、外周血白细胞(WBC)、格拉斯哥昏迷指数(GCS)、急性生理学及慢性健康状况评分系统Ⅱ(APECHE Ⅱ)、CPIS评分、全身炎症反应(SIRS)评分(SIRS评分标准:体温、HR、RR或PCO2、WBC每一项符合+1分,总分0到4分)。
1.2.3 病情进展观察指标第3天及第5天的体温、呼吸频率、P/F、WBC、CRP、PCT、IL-6、胸片、需要镇静镇静时间、CPIS评分、APECHEⅡ评分,及第3天与第5天与第1天的差值(△1-3 d APECHEⅡ、△1-5 d APECHEⅡ);病程中血管活性药物比例、机械通气天数、CRRT比率。
1.2.4 预后指标有创机械通气时间,因吸入性肺炎ICU住院时间和总住院时间(以考虑符合吸入性肺炎诊断当日作为起始时间),出院时患者病死率。
1.2.5 病原学结果早期(3 d以内)及晚期(4~7 d)病原学阳性数量、格兰阴性杆菌、阳性球菌、真菌占送检患者比例。
1.3 统计学方法采用SPSS 26.0(SPSS Inc, Chicago, IL)及Graphpad Prism 8(GraghPad Prism Software Inc, USA)统计学软件进行统计分析。计量资料中,正态性分布的数据以均数±标准差(x±s)表示,比较前先进行方差齐性检验,方差齐采用独立样本t检验,方差不齐采用Mann-Whitney U检验。计数资料采用χ2检验。以P < 0.05为差异有统计学意义。
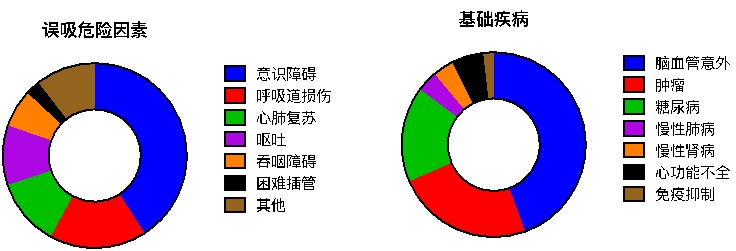
2 结果 2.1 误吸危险因素与基础疾病分析在纳入危险因素中意识障碍占56.4%,存上气道受损(口鼻腔损伤出血、气管梗阻、食道手术等)占23.6%,心肺复苏16.4%、呕吐14.5%、吞咽障碍9.1%;同时存在两个及以上的危险因素占34.5%。合并基础病中,脑血管以外占43.6%、肿瘤占23.6%,糖尿病占16.4%、慢性心、肺、肾及免疫抑制患者的比例在1.8%~5.5%范围(见图 2)。
|
| 图 2 误吸危险因素及基础疾病比例 Fig 2 Proportion of aspiration risk factors and underlying diseases |
|
|
早期气管镜灌洗组≥2个危险因素的患者比例较对照组显著增加(P<0.05),其他单个高危因素或基础疾病比例在两组间差异无统计学意义(P均>0.05)。见表 1。
| 危险因素/基础疾病 | 组别 | |||
| 病例总数(n=55) | 气管镜组(n=23) | 对照组(n=32) | P值 | |
| 危险因素(n, %) | ||||
| 吞咽障碍 | 5 (9.1) | 2 (8.7) | 3 (9.4) | 1.000 |
| 意识障碍 | 31 (56.4) | 12 (52.2) | 19 (59.4) | 0.595 |
| 呕吐 | 8 (14.5) | 2 (8.7) | 6 (18.8) | 0.446 |
| 心肺复苏 | 9 (16.4) | 5 (21.7) | 4 (12.5) | 0.467 |
| 上气道受损 | 13 (23.6) | 7 (30.4) | 6 (18.8) | 0.446 |
| 困难插管 | 2 (3.6) | 1 (4.3) | 1 (3.1) | 1.000 |
| 其他 | 8 (14.5) | 4 (17.4) | 4 (12.5) | 0.707 |
| ≥2个高危因素 | 19 (34.5) | 12 (52.2) | 7 (21.9) | 0.020 |
| 基础疾病(n, %) | ||||
| 肿瘤 | 13 (23.6) | 4 (17.4) | 9 (28.1) | 0.522 |
| 糖尿病 | 9 (16.4) | 6 (26.1) | 3 (9.4) | 0.143 |
| 脑血管以外 | 24 (43.6) | 8 (34.8) | 16 (50.0) | 0.262 |
| 慢性肺病 | 2 (3.6) | 1 (4.3) | 1 (3.1) | 1.000 |
| 慢性肾病 | 2 (3.6) | 1 (4.3) | 1 (3.1) | 1.000 |
| 心功能不全 | 3 (5.5) | 2 (8.7) | 1 (3.1) | 0.565 |
| 免疫抑制 | 1 (1.8) | 0 (0.0) | 1 (3.1) | 1.000 |
共纳入吸入性肺炎患者55例,男性42例,女性13例,24 h内给与气管镜灌洗23例,24 h内未进行气管镜灌洗32例,两组患者年龄、性别、BMI以及初始痰液淀粉酶、体温、心率、呼吸频率、CRP、PCT、IL-6、WBC、中性粒细胞、胸部正位X线片、GCS、APECHEⅡ、CPIS、SIRS差异无统计学意义(P均>0.05),初始氧合指数在气管镜灌洗组显著高于对照组(P<0.05)。见表 2。
| 基本特征 | 组别 | ||
| 气管镜组(n=23) | 对照组(n=32) | P值 | |
| 体重指数(kg/m2) | 1.66 (0.84) | 1.65 (0.84) | 0.801 |
| 年龄(岁) | 62.17(17.59) | 66.47(15.88) | 0.348 |
| 女性,(n, %) | 6 (26.09) | 7 (21.88) | 0.530 |
| 入科体温, (℃) | 38.10 (1.07) | 38.26(1.11) | 0.594 |
| 痰淀粉酶(U/L) | 1216.00 (437.50, 3270.50) | 1933.00 (147.00, 14668.00) | 0.087 |
| 心率(次/min) | 117.83(22.99) | 122.34(31.15) | 0.558 |
| 呼吸频率(次/min) | 32 (25, 34) | 24(20, 29) | 0.713 |
| 氧合指数(mmHg) | 119.00 (105.50, 171.25) | 186.00(148.45, 215.00) | 0.008 |
| WBC(×109/L) | 14.05 (7.64) | 12.98 (7.30) | 0.600 |
| Neu(×109/L) | 12.81 (7.46) | 11.56 (7.19) | 0.533 |
| CRP(mg/L) | 107.67 (100.75) | 146.81 (96.42) | 0.171 |
| PCT(ng/mL) | 0.89 (0.16, 1.76) | 1.36(0.19, 7.67) | 0.335 |
| IL-6(pg/mL) | 146.20(23.20, 1429.55) | 63.80 (32.60, 253.00) | 0.389 |
| GCS评分 | 12.00(3.00, 15.00) | 8.00(6.00, 13.00) | 0.701 |
| APECHEⅡ | 23.23(9.20) | 21.38(5.75) | 0.367 |
| X1 | 2.00 (2.00, 3.00) | 2.00 (1.50, 3.00) | 0.270 |
| CPIS | 9.00(8.00, 10.00) | 9.00(8.00, 10.00) | 0.410 |
| SIRS | 4.00(3.00, 4.00) | 4.00 (3.00, 4.00) | 0.448 |
较对照组比较,气管镜灌洗3 d后患者APECHEⅡ评分及治疗5 d后CPIS评分显著下降(P均<0.05);第3天、第5天氧合指数亦有下降趋势,体温、呼吸频率、白细胞、CRP、IL-6、PCT、X线片、血管活性药物比例、CRRT、CPIS3d差异无统计学意义(P均>0.05)。见表 3。
| 进展指标 | 组别 | ||
| 气管镜组(n=23) | 对照组(n=32) | P值 | |
| 3 d体温(℃) | 37.86(0.94) | 38.06(0.97) | 0.475 |
| 5 d体温(℃) | 38.21(1.02) | 37.99(1.74) | 0.429 |
| 3 d RR(次/min) | 24.84(5.84) | 25.25(6.70) | 0.830 |
| 5 d RR(次/min) | 26.36 (5.08) | 24.70(6.12) | 0.391 |
| 3 d P/F(mmHg) | 183.75 (173.75, 223.00) | 242.50 (205.00, 332.50) | 0.183 |
| 5 d P/F(mmHg) | 180.50 (156.25, 221.75) | 250.00 (180.00, 335.00) | 0.057 |
| 3 d WBC(×109/L) | 12.72 (5.93) | 10.16 (5.74) | 0.153 |
| 5 d WBC(×109/L) | 10.64 (4.74) | 11.24(4.42) | 0.701 |
| 3 d CPR(mg/L) | 136.22(88.37) | 15174(79.10) | 0.538 |
| 5 d CRP(mg/L) | 116.76(109.62) | 128.99 (97.45) | 0.733 |
| 3 d PCT(ng/mL) | 0.78(0.23, 2.59) | 0.63 (0.18, 2.10) | 0.584 |
| 5 d PCT(ng/mL) | 0.64(0.12, 1.11) | 0.39 (0.17, 1.14) | 0.522 |
| 3 d IL-6(pg/mL) | 42.50 (15.20, 131.85) | 62.60(22.20, 93.00) | 0.823 |
| 5 d IL-6(pg/mL) | 32.10 (19.65, 123.95) | 29.30(17.60, 48.50) | 0.377 |
| 3 d胸X片 | 2.00 (2.00, 3.00) | 1.00 (1.00, 2.00) | 0.156 |
| 5 d胸X片 | 2.00 (2.00, 3.00) | 1.00 (0.00, 2.00) | 0.135 |
| 镇静≥3d, (n, %) | 11 (47.8) | 15 (46.9) | 0.944 |
| △1-3 d APECHEⅡa | 15.00 (10.00, 16.75) | 12.00(7.00, 12.00) | 0.037 |
| △1-5 d APECHEⅡa | 14.00 (7.25, 17.5) | 11.00(7.00, 15.00) | 0.614 |
| 血管活性药物, (n, %) | 14 (60.9) | 25 (78.1) | 0.165 |
| 机械通气>3 d, (n, %) | 10 (43.5) | 21 (65.6) | 0.102 |
| CRRT(n, %) | 4 (17.4) | 6 (18.8) | 1.000 |
| 3 d CPIS | 8.00(8.00, 9.00) | 8.00(7.00, 9.00) | 0.148 |
| 5 d CPIS | 9.00(8.00, 11.00) | 6.00(6.00, 9.00) | 0.024 |
| 注:3 d:第3天;5 d:第5天;a最小值为负值,调整为0,其他值相应增量调整;△1-3d为初始APECEⅡ比较,APECHⅡ在第三天相对下降幅度;△1-5d为初始APECEⅡ比较,APECHⅡ在第五天相对下降幅度。计量资料应用均数(标准差)或中位数(四分位25%,75%)表示 | |||
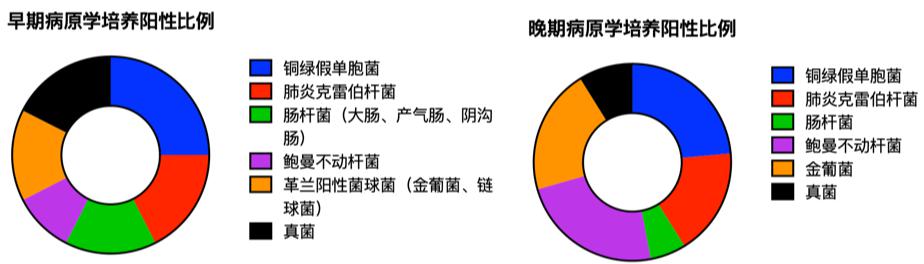
早期(3 d内)病原学培养阳性率85.2%,细菌阳性率72.9%,真菌阳性率14.6%;铜绿假单胞菌20.8%、肺炎克雷伯杆菌14.6%、肠杆菌(12.5%)、鲍曼不动杆菌(8.3%)、金葡菌和链球菌占(12.5%),见图 3;在气管镜灌洗组与对照组分布差异无统计学意义(P均>0.05)。晚期(4~7 d内)病原学培养阳性率88.6%,细菌阳性率85.7%,真菌阳性率2.9%;晚期细菌培养阳性率在气管镜干预组显著降低(P<0.05),其余分布与对照组比较差异无统计学意义(P均>0.05)。较早期培养结果比较,晚期菌群变化与早期不完全一致比例达50%。见表 4。
|
| 图 3 吸入性肺炎早期及晚期病原学分布占比图 Fig 3 Proportion of etiological distribution at the early and later stage of aspiration pneumonia |
|
|
| 指标 | 组别 | |||
| 总数(n=48) | 气管镜组(n=22) | 对照组(n=26) | P值 | |
| 早期病原学(n, %) | ||||
| 1~3 d病原学培养阳性 | 41 (85.2) | 17 (77.3) | 24 (92.3) | 0.141 |
| 1~3 d培养细菌阳性 | 35 (72.9) | 16 (72.7) | 19 (73.1) | 0.978 |
| 铜绿假单胞菌 | 10 (20.8) | 6 (27.3) | 4 (15.4) | 0.478 |
| 肺炎克雷伯杆菌 | 7 (14.6) | 1 (4.5) | 6 (23.1) | 0.219 |
| 肠杆菌(大肠、产气肠、阴沟肠) | 6 (12.5) | 5 (22.7) | 1 (3.6) | 0.072 |
| 鲍曼不动杆菌 | 4 (8.3) | 3 (13.6) | 1 (3.6) | 0.308 |
| 革兰阳性菌球菌(金葡菌、链球菌) | 6 (12.5) | 2 (9.0) | 4 (15.4) | 0.575 |
| 1~3 d培养真菌阳性 | 7 (14.6) | 2 (8.7) | 5 (15.6) | 0.447 |
| 晚期病原学 | n=35 | n=11 | n=24 | P |
| 4~7 d病原学培养阳性 | 31 (88.6) | 8 (72.7) | 23 (95.8) | 0.046 |
| 4~7 d培养细菌阳性 | 30 (85.7) | 8 (72.7) | 22 (88.0) | 0.137 |
| 4~7 d培养真菌阳性 | 1 (2.9) | 0 (0) | 1 (4.2) | 1.000 |
早期给与气管镜灌洗组患者有创机械通气天数明显缩短(中位数6.00 d vs. 7.00 d),ICU住院时间(平均7.91 d vs. 14.00 d)以及总住院时间(平均19.96 d vs. 31.34 d)显著下降(P均<0.05);两组患者病死率差异无统计学意义(P>0.05)。见表 5。
| 预后指标 | 组别 | |||
| 气管镜组(n=23) | 对照组(n=32) | P值 | ||
| 死亡(n, %) | 4 (17.4) | 4 (12.5) | 0.707 | |
| ICU LOS(d) | 7.91(7.17) | 14.00(10.71) | 0.022 | |
| TLOS(d) | 19.96(16.31) | 31.34(19.58) | 0.027 | |
| 机械通气时间(d) | 6.00(2.00, 12.00) | 7.00(4.00, 10.00) | 0.041 | |
| 注:计量资料应用均数(标准差)或中位数(四分位25%,75%)表示 | ||||
本研究发现对于机械通气吸入性肺炎患者,早期气管镜灌洗可以改善患者氧合,降低临床肺部感染评分,减少呼吸机支持时间,降低后期细菌培养阳性比率,减少ICU住院时间和总住院时间,病死率未见显著差异。
参考既往文献纳入危险因素,本研究发现意识障碍(56.4%)、呼吸道受损(23.6%)、心肺复苏(16.4%)是误吸患者最常见的危险因素。意识障碍可由麻醉药、全麻药、某些抗抑郁药和酒精等多种因素引起,抗抑郁药物可使误吸比率增加1.5倍[18]。而本研究更多可能是脑血管以外导致患者意识障碍,脑血管意外的基础病占43.6%,平均昏迷指数评分(GCS)10.85,故存在脑血管意外多存在意识障碍,对于该群患者应在早期胃肠减压;研究也显示早期胃肠减压可改善该类患者的生存[19]。有研究报道存在多种误吸风险的患者,吸入性肺炎发生率、病死率和其他不良结局的发生率增加,当合并吞咽困难时,吸入性肺炎的比值比(OR)增加了9.4倍,但当同时存在脑血管疾病时,OR上升到12.9[20]。心脏骤停是误吸另一个重要的临床高危因素,研究报道65%的患者在心搏骤停事件发生后3天内出现肺炎,可能的机制是在复苏过程中吸入胃内容物,或在面罩通气和插管过程中吸入口腔分泌物[21-22],而低温治疗使早发性肺炎的优势比提高了接近2倍[23]。有两种或两种以上危险因素的患者复发性肺炎发生率增加,30 d和6个月病死率增加,发病率与危险因素的数量同步上升[24]。本研究显示较多患者合并多种危险因素,同时合并两种以上危险因素比例达34.5%,且在气管镜早期干预组明显高于对照组;然而气管镜组患者通气时间、住院时间却低于对照组,表明早期气管镜灌洗具有显著治疗效果。
基本资料分析显示两组患者基本特征大多差异无统计学意义,而治疗组患者氧合指数显著下降,可能是误吸导致吸入性化学性肺炎、感染性肺炎和气道阻塞发,从而导致广泛的肺部病变,影响患者的氧合;微误吸虽然被证明含有一定数量的微生物,但一般不会导致临床显著的后果[7]。只有吸入大量酸性胃液或接种大量低毒力病原微生物才会导致肺损伤或ARDS[8]。目前急性肺损伤或ARDS的程度根据氧合指数来判断,而气管镜灌洗组早期氧合指数显著降低,故气管镜灌洗组在发病早期可能存在更为严重的肺损伤,然而经早期气管镜灌洗后,第5日再次评估CPIS评分,治疗组评分显著降低,氧合指数较对照组有限制下降趋势,进一步表明早期气管镜灌洗对误吸患者具有良好的效果。
本研究早期送检标本阳性培养率达85.2%,后期标本送检阳性率达88.6%;均为格兰阳性球菌和格兰阴性杆菌,未见厌氧菌。这与20世纪70年代报道不相符,在不含口腔分泌物(气管吸出物、胸膜液和血液培养)的菌群中分离到的优势菌为黑原拟杆菌和核梭杆菌,二者均为无芽孢的专性厌氧杆菌[25];尽管当时住院患者金葡菌和革兰氏阴性杆菌分离率较高,肺炎克雷伯氏菌是最常见的分离细菌,仍有87%的患者培养出厌氧菌[26]。而本研究显示误吸早期最常见的病原体为铜绿假单胞菌(20.8%),其次是肺炎克雷伯杆菌、鲍曼不动杆菌;格兰阳性球菌仍然以金葡菌和链球菌最为常见(12.5%)。铜绿假单胞菌在本院误吸患者中多见,这可能与医生更多经验性选择三代头孢、碳青霉烯类、含酶抑制剂抗生素有关。另外厌氧菌少见,也可能与目前抗生素具有抗厌氧菌的效果,导致厌氧菌阳性培养率下降。
化学性肺炎可能会继发后期感染。吸入性细菌性肺炎的特征是目击或怀疑有误吸,临床上出现咳嗽,发热,呼吸急促,胸部CT或X片发现继发于感染原因的新发肺泡浸润。误吸导致化学性肺炎有类似的表现,但没有感染原因,但可发生继发性感染[11]。本研究显示有初始培养无病原学生长后期培养阳性的患者占后期感染患者的13%,后期与早期培养病原学不一致高达50%,表明早期化学性肺炎亦可继发后期细菌感染,考虑可能与较多因素有关:(1)早期吸入细菌量较低,早期培养未能检测出,可能误吸早期机体免疫防御体系尚能够迅速清除病原体[27],但由于误吸入呼吸道化学成分改变局部免疫状态,导致机体防御力低下,难以清除持续增殖的细菌;(2)细菌繁殖环境改变:原来呼吸道及肺部是细菌生长营养匮乏的环境,误吸导致其变成含有丰富黏液、蛋白渗出物等,微环境改变为富含促进细菌生长富含营养物质,病原体进一步繁殖导致后期培养阳性[27]。基于化学性肺炎存在潜在感染风险,这可能导致临床医生过度使用使抗生素[28]。事实上,如果误吸为酸性胃液,临床行气管镜灌洗时不难发现,在误吸24 h后再次行气管镜灌洗,往往仅能看到气道红肿显著,气管镜灌洗疗效差;而在早期灌洗可显著减轻气道红肿,改善患者影像学及氧合情况;同时本研究调查结果显示后期再次发生肺部感染率高达50%,笔者推荐早期进行肺泡灌洗、希望能清除大量误吸的化学物质、降低细菌量,防治早期和后期继发的肺部感染,本研究结果也显示气管镜灌洗后后期病原学培养阳性率显著低于对照组。尽管这未能改变病死率,可能的原因是感染不仅仅是细菌复制或细菌基因产物的结果; 也是宿主反应以及由此产生的炎症和组织损伤的结果[29-30],机体的免疫状态、组织损伤程度同样影响临床结局。
预防性支气管灌洗有望改善吸入性肺炎的临床预后。研究显示对于气管切开且有大量气道分泌物的ICU住院患者,进行预防性气管镜灌洗可以肺炎降低发病率和病死率,甚至可以缩短在ICU的住院时间,从而降低治疗费用[31]。对已经出现吸入性损伤患者的研究中也发现[32],接受支气管镜灌洗的患者,其机械通气疗程明显缩短、ICU住院时间及总住院时间也显著减少,并有降低整体医院成本、改善病死率的趋势。对于COPD患者进行无创通气联合气管镜灌洗与直接插管有创通气患者比较,前者感染并发症明显降低[33]。同样予以气管镜灌洗可通过清除气道内黏液物质及免疫物质,改善难治性哮喘和肺泡蛋白沉积症[34-35]。这些研究均表明,预防或治疗性支气管镜治疗可以使存在气道炎症及肺部炎症的患者受益。同样,通过早期支气管镜检查和灌洗ICU内诊断吸入性肺炎的患者,清除吸入的炎症和污染物质,有可能改善临床结果。这在本研究中得到证实:早期气管镜灌洗后第3天APECHEII下降更为显著,并可显著降低误吸患者带呼吸机时间,实现尽早脱机,进而缩短ICU住院时间及总住院时间。对于误吸患者不能及时行气管镜治疗的原因较多,其中临床上的“周末现象”可能就是延迟气管镜灌洗的原因之一。研究发现周末ICU入院患者住院时间延长、实现病情稳定需要更久[36],以及周末入ICU与增加的病死率有关[37]。非工作日气管镜治疗可能受限于ICU设备或人员等资源的可用性,比如周末非办公时间涉及到气管镜检查的医师、护士是否值班,周末气管镜循环消毒、灭菌团队是否充足等。
本研究有一些局限性。首先,本研究是一项单中心、回顾性研究。尽管笔者回顾了近期一年多的医疗记录,与既往研究相比,病例跨度时限短,避免了医疗技术的进步带来的差异,但由于是单中心回顾性性研究,难以匹配更多影响吸入性肺炎预后的因素,如胆碱酯酶、营养评分等[38],需要前瞻性RCT进一步验证研究结论。其次,本文纳入“可能为肺炎”临床诊断的患者,有一定的局限性,比如体温、白细胞等可能受到其他因素的影响,如合并症或基础病、激素治疗、原发病的影响。再次,本中心前期研究显示,痰液淀粉酶对于筛选误吸具有一定临床价值,故根据淀粉酶去筛选吸入性肺炎患者,但可能没有从存在误吸的高危因素所有患者去筛选更为全面,故55例患者不代表所有吸入性肺炎患者。
综上所述,对于吸入性肺炎患者早期行支气管镜灌洗有利于改善患者氧合、降低ICU及总住院时间等临床指标,但需要进一步的大规模随机对照试验来确定早期支气管镜在这些人群中的治疗作用。
利益冲突 所有作者声明无利益冲突
作者贡献声明 鹿中华、孙昀:研究设计、论文撰写;余维丽、韩宁、周强、陈虎:数据收集及整理;付路、余维丽:统计学分析;胡秋源、曹利军:论文修改。
| [1] | Marik PE. Aspiration pneumonitis and aspiration pneumonia[J]. N Engl J Med, 2001, 344(9): 665-671. DOI:10.1056/NEJM200103013440908 |
| [2] | O'Dwyer DN, Dickson RP, Moore BB. The lung microbiome, immunity, and the pathogenesis of chronic lung disease[J]. J Immunol, 2016, 196(12): 4839-4847. DOI:10.4049/jimmunol.1600279 |
| [3] | Dickson RP, Martinez FJ, Huffnagle GB. The role of the microbiome in exacerbations of chronic lung diseases[J]. Lancet, 2014, 384(9944): 691-702. DOI:10.1016/S0140-6736(14)61136-3 |
| [4] | Mandell LA, Niederman MS. Aspiration pneumonia[J]. N Engl J Med, 2019, 380(7): 651-663. DOI:10.1056/nejmra1714562 |
| [5] | Reza Shariatzadeh M, Huang JQ, Marrie TJ. Differences in the features of aspiration pneumonia according to site of acquisition: community or continuing care facility[J]. J Am Geriatr Soc, 2006, 54(2): 296-302. DOI:10.1111/j.1532-5415.2005.00608.x |
| [6] | Lindenauer PK, Strait KM, Grady JN, et al. Variation in the diagnosis of aspiration pneumonia and association with hospital pneumonia outcomes[J]. Annals ATS, 2018, 15(5): 562-569. DOI:10.1513/annalsats.201709-728oc |
| [7] | Gleeson K, Eggli DF, Maxwell SL. Quantitative aspiration during sleep in normal subjects[J]. Chest, 1997, 111(5): 1266-1272. DOI:10.1378/chest.111.5.1266 |
| [8] | Son YG, Shin J, Ryu HG. Pneumonitis and pneumonia after aspiration[J]. J Dent Anesth Pain Med, 2017, 17(1): 1-12. DOI:10.17245/jdapm.2017.17.1.1 |
| [9] | Shen L. Empyema associated with vegetable foreign body aspiration[J]. World J Emerg Med, 2021, 12(2): 162-164. DOI:10.5847/wjem.j.1920-8642.2021.02.015 |
| [10] | Morrow RL, Bassett K, MacLure M, et al. Outcomes associated with hospital admissions for accidental opioid overdose in British Columbia: a retrospective cohort study[J]. BMJ Open, 2019, 9(5): e025567. DOI:10.1136/bmjopen-2018-025567 |
| [11] | Neill S, Dean N. Aspiration pneumonia and pneumonitis: a spectrum of infectious/noninfectious diseases affecting the lung[J]. Curr Opin Infect Dis, 2019, 32(2): 152-157. DOI:10.1097/QCO.0000000000000524 |
| [12] | Teabeaut JR. Aspiration of gastric contents; an experimental study[J]. Am J Pathol, 1952, 28(1): 51-67. |
| [13] | Betancourt SL, Martinez-Jimenez S, Rossi SE, et al. Lipoid pneumonia: spectrum of clinical and radiologic manifestations[J]. AJR Am J Roentgenol, 2010, 194(1): 103-109. DOI:10.2214/AJR.09.3040 |
| [14] | Lee HW, Min J, Park J, et al. Clinical impact of early bronchoscopy in mechanically ventilated patients with aspiration pneumonia[J]. Respirology, 2015, 20(7): 1115-1122. DOI:10.1111/resp.12590 |
| [15] | 王川江, 徐昉. 机械通气合并重症肺部感染患者胸部CT定位下床旁无痛纤维支气管镜气道灌洗临床价值[J]. 中华急诊医学杂志, 2015, 24(4): 374-379. DOI:10.3760/cma.j.issn.1671-0282.2015.04.007 |
| [16] | 邵飞飞, 梁琦强, 肖纬, 等. 支气管肺泡灌洗对重症肺炎抗生素使用的影响[J]. 中华急诊医学杂志, 2019, 28(12): 1529-1532. DOI:10.3760/cma.j.issn.1671-0282.2019.12.014 |
| [17] | Anderson CS, ARIMA H, Lavados P, et al. Cluster-randomized, crossover trial of head positioning in acute stroke[J]. N Engl J Med, 2017, 376(25): 2437-2447. DOI:10.1056/NEJMoa1615715 |
| [18] | Herzig SJ, LaSalvia MT, Naidus E, et al. Antipsychotics and the risk of aspiration pneumonia in individuals hospitalized for nonpsychiatric conditions: a cohort study[J]. J Am Geriatr Soc, 2017, 65(12): 2580-2586. DOI:10.1111/jgs.15066 |
| [19] | Dennis M, Lewis S, Cranswick G, et al. FOOD: a multicentre randomised trial evaluating feeding policies in patients admitted to hospital with a recent stroke[J]. Health Technol Assess, 2006, 10(2): 1-120. DOI:10.3310/hta10020 |
| [20] | van der Maarel-Wierink CD, Vanobbergen JN, Bronkhorst EM, et al. Meta-analysis of dysphagia and aspiration pneumonia in frail Elders[J]. J Dent Res, 2011, 90(12): 1398-1404. DOI:10.1177/0022034511422909 |
| [21] | Perbet S, Mongardon N, Dumas F, et al. Early-onset pneumonia after cardiac arrest: characteristics, risk factors and influence on prognosis[J]. Am J Respir Crit Care Med, 2011, 184(9): 1048-1054. DOI:10.1164/rccm.201102-0331OC |
| [22] | Takenaka I, Aoyama K. Prevention of aspiration of gastric contents during attempt in tracheal intubation in the semi-lateral and lateral positions[J]. World J Emerg Med, 2016, 7(4): 285-289. DOI:10.5847/wjem.j.1920-8642.2016.04.008 |
| [23] | Johnson NJ, Carlbom DJ, Gaieski DF. Ventilator management and respiratory care after cardiac arrest: oxygenation, ventilation, infection, and injury[J]. Chest, 2018, 153(6): 1466-1477. DOI:10.1016/j.chest.2017.11.012 |
| [24] | Noguchi S, Yatera K, Kato T, et al. Impact of the number of aspiration risk factors on mortality and recurrence in community-onset pneumonia[J]. Clin Interv Aging, 2017, 12: 2087-2094. DOI:10.2147/CIA.S150499 |
| [25] | Bartlett JG, Gorbach SL. The triple threat of aspiration pneumonia[J]. Chest, 1975, 68(4): 560-566. DOI:10.1378/chest.68.4.560 |
| [26] | Wang JL, Chen KY, Fang CT, et al. Changing bacteriology of adult community-acquired lung abscess in Taiwan: Klebsiella pneumoniaeversus anaerobes[J]. Clin Infect Dis, 2005, 40(7): 915-922. DOI:10.1086/428574 |
| [27] | Dickson RP, Erb-Downward JR, Falkowski NR, et al. The lung microbiota of healthy mice are highly variable, cluster by environment, and reflect variation in baseline lung innate immunity[J]. Am J Respir Crit Care Med, 2018, 198(4): 497-508. DOI:10.1164/rccm.201711-2180OC |
| [28] | Dragan V, Wei YL, Elligsen M, et al. Prophylactic antimicrobial therapy for acute aspiration pneumonitis[J]. Clin Infect Dis, 2018, 67(4): 513-518. DOI:10.1093/cid/ciy120 |
| [29] | Casadevall A, Pirofski LA. The damage-response framework of microbial pathogenesis[J]. Nat Rev Microbiol, 2003, 1(1): 17-24. DOI:10.1038/nrmicro732 |
| [30] | Casadevall A, Pirofski LA. Host-pathogen interactions: redefining the basic concepts of virulence and pathogenicity[J]. Infect Immun, 1999, 67(8): 3703-3713. DOI:10.1128/IAI.67.8.3703-3713.1999 |
| [31] | Vejdan AK, Khosravi M. BAL for pneumonia prevention in tracheostomy patients: a clinical trial study[J]. Pak J Med Sci, 2013, 29(1): 148-151. DOI:10.12669/pjms.291.1971 |
| [32] | Carr JA, Phillips BD, Bowling WM. The utility of bronchoscopy after inhalation injury complicated by pneumonia in burn patients: results from the National Burn Repository[J]. J Burn Care Res, 2009, 30(6): 967-974. DOI:10.1097/BCR.0b013e3181bfb77b |
| [33] | Scala R, Naldi M, Maccari U. Early fiberoptic bronchoscopy during non-invasive ventilation in patients with decompensated chronic obstructive pulmonary disease due to community-acquired-pneumonia[J]. Crit Care, 2010, 14(2): R80. DOI:10.1186/cc8993 |
| [34] | Lang DM, Simon RA, Mathison DA, et al. Safety and possible efficacy of fiberoptic bronchoscopy with lavage in the management of refractory asthma with mucous impaction[J]. Ann Allergy, 1991, 67(3): 324-330. |
| [35] | Rodrigo D, Rathnapala A, Senaratne W. Therapeutic limited bronchoalveolar lavage with fiberoptic bronchoscopy as a bridging procedure prior to total lung lavage in a patient with pulmonary alveolar proteinosis: a case report[J]. J Med Case Rep, 2015, 9: 93. DOI:10.1186/s13256-015-0574-z |
| [36] | Milevski SV, Lloyd M, Janus E, et al. Impact of weekend admission and changes in treating team on patient flow and outcomes in adults admitted to hospital with community-acquired pneumonia[J]. Intern Med J, 2021, 51(10): 1681-1690. DOI:10.1111/imj.15252 |
| [37] | Uusaro A, Kari A, Ruokonen E. The effects of ICU admission and discharge times on mortality in Finland[J]. Intensive Care Med, 2003, 29(12): 2144-2148. DOI:10.1007/s00134-003-2035-1 |
| [38] | 田玮, 丁宁. 影响老年吸入性肺炎患者短期预后的危险因素分析[J]. 中华急诊医学杂志, 2019, 28(6): 743-747. DOI:10.3760/cma.j.issn.1671-0282.2019.06.016 |
 2022, Vol. 31
2022, Vol. 31




