2 北京中医药大学脓毒症研究所 北京 100700
2 Institute of Sepsis, Beijing University of Chinese Medicine, Beijing 100700, China
脓毒症是机体对感染的反应失调引发的严重器官功能障碍,诊治不及时,可发展至脓毒性休克,是重症感染患者死亡的主要原因。早期识别脓毒性休克、准确评估病情严重程度、客观判断预后,及时给予积极有效的治疗对降低脓毒症病死率至关重要[1]。因此寻找在诊断上敏感性与特异性均较高,并且对预后有一定预测价值的理想指标是目前的研究热点之一。肝素结合蛋白(heparin-binding protein, HBP)在细胞分化及成熟的过程中储存在中性粒细胞中,当机体受到感染后,HBP迅速对感染应答,是脓毒症相关器官功能障碍的早期预警因子[2]。在一项前瞻性国际多中心队列研究中发现,HBP在感染患者出现脓毒症前数小时已经明显升高,预测效能高于白细胞计数(white blood cell count, WBC)、C-反应蛋白(C-reactive protein, CRP)、降钙素原(procalcitonin, PCT),是早期预测脓毒症的最佳生物标志物[3]。本研究通过比较HBP与其他脓毒症常用生物指标,探讨HBP及HBP联合序贯器官衰竭(sequential organ failure assessment, SOFA)评分评估是否发生脓毒性休克的早期诊断价值,同时评估对死亡风险的早期预测价值。
1 资料与方法 1.1 一般资料选择2019年10月至2020年4月在北京中医药大学东直门医院急诊科及急诊重症监护病房(EICU)就诊的65例年龄≥65岁老年脓毒症患者,按照Sepsis 3.0定义分为脓毒症组与脓毒性休克组[4],又依据28 d是否存活分为存活组和死亡组。排除标准:器官移植患者、恶性肿瘤晚期、免疫缺陷患者。本研究通过北京中医药大学东直门医院伦理委员会批准;所有受试者均自愿加入本研究并签署知情同意书,意识障碍者由家属知情同意并代签字。
1.2 观察指标记录所有患者性别、年龄、感染部位、28 d结局,在诊断脓毒症24 h内采集血标本,检测HBP、WBC、CRP、PCT,并在24 h内完成SOFA评分。
1.3 检测方法所有入组患者采集静脉血3管,每管各2 mL。一管使用1:9枸橼酸钠抗凝管抽取血液后2 h内使用1500RCF离心机(北京白洋320A)离心10 min,小心析出血浆,使用免疫荧光法检测HBP(中翰盛泰生物技术公司),检测仪器为Jet-iStar800 (FIC-Q100)。一管为无抗凝剂血,静置30 min后分离血清,使用双抗夹心免疫化学发光法检测PCT(化学发光测定仪,中国亚辉龙)。一管为肝素抗凝血,使用阻抗法检测WBC(美国贝克曼公司),散射比浊法检测CRP(美国贝克曼公司)。
1.4 统计学方法使用SPSS 22.0进行数据分析。计数资料比较采用χ2检验。所有计量资料以均数±标准差(Mean±SD)表示,符合正态分布的采取独立样本t检验,不符合正态分布的采取Mann-Whitney U检验。对组间有统计学差异的指标绘制ROC曲线,评价各指标对脓毒性休克及死亡结局的预测价值。双侧检验,以P<0.05为差异有统计学意义。
2 结果 2.1 基线资料65例患者中肺部感染例54例,腹腔感染7例,皮肤软组织感染2例,泌尿系感染2例。脓毒症组与脓毒性休克组,存活组和死亡组之间性别、年龄差异均无统计学意义(P>0.05),见表 1。
| 组别 | 例数(n) | 性别 | 年龄(岁) | |
| 男性(n) | 女性(n) | |||
| 以是否发生休克分组 | ||||
| 脓毒症组 | 41 | 17 | 24 | 78.8±6.5 |
| 脓毒性休克组 | 24 | 11 | 13 | 78.5±9.5 |
| χ2/ t值 | 0.118 | 1.141 | ||
| P值 | 0.731 | 0.888 | ||
| 以28 d不同结局分组 | ||||
| 存活组 | 55 | 23 | 32 | 79.2±6.9 |
| 死亡组 | 10 | 5 | 5 | 76.0±11.2 |
| χ2/ t值 | 0.231 | 0.870 | ||
| P值 | 0.631 | 0.404 | ||
脓毒性休克组患者的SOFA评分、HBP、CRP和PCT均显著高于脓毒症组(均P<0.05,表 2)。死亡组患者的SOFA评分、HBP和PCT均显著高于存活组(P<0.05),见表 3。
| 指标 | 脓毒症组(n=41) | 脓毒性休克组(n=24) | F/Z值 | P值 |
| SOFA评分 | 6.0±3.0 | 10.0±3.0 | -4.299 | 0.000 |
| HBP | 103.3±56.8 | 146.7±75.4 | 0.352 | 0.049 |
| WBC | 15.2±3.5 | 17.3±6.0 | 6.543 | 0.126 |
| CRP | 99.40±40.5 | 127.5±52.5 | 2.950 | 0.018 |
| PCT | 6.2±9.6 | 16. 7±14.7 | -3.963 | 0.000 |
| 指标 | 存活组(n=55) | 死亡组(n=10) | F/Z值 | P值 |
| SOFA评分 | 6.7±3.0 | 12.2±2.8 | -4.148 | 0.000 |
| HBP | 98.2±49.9 | 200.8±64.8 | 0.758 | 0.000 |
| WBC | 15.7±4.1 | 17.5±7.0 | 3.963 | 0.266 |
| CRP | 109.0±48.7 | 114.3±37.3 | -0.673 | 0.501 |
| PCT | 7.6±9.2 | 23.6±20.0 | -3.218 | 0.001 |
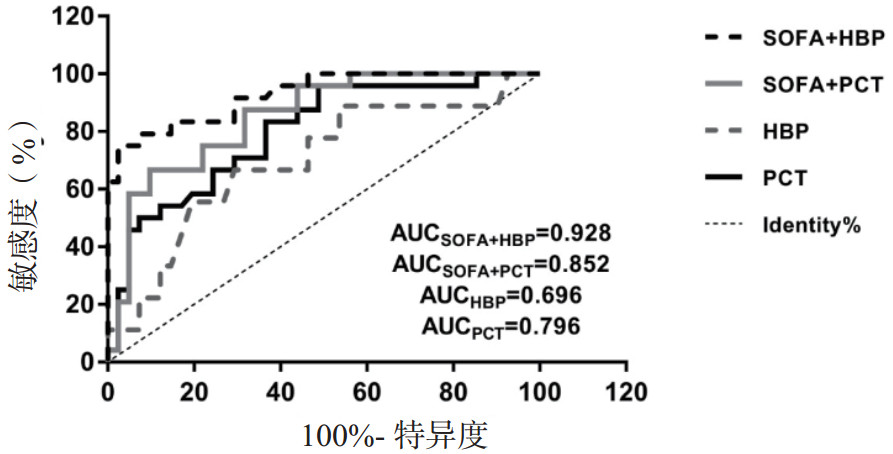
ROC曲线显示HBP联合SOFA评分诊断脓毒性休克的ROC曲线下面积(0.928)大于PCT联合SOFA评分(0.852)、PCT(0.796)和HBP(0.696),见图 1和表 4。
|
| 图 1 HBP、PCT及二者联合SOFA诊断脓毒性休克的ROC曲线 Fig 1 ROC curves of HBP, PCT and their combination with SOFA for diagnosing septic shock |
|
|
| 指标 | AUC | SE | P值 | 95%CI | 最佳临界值 | 灵敏度(%) | 特异度(%) | 约登指数 |
| HBP | 0.696 | 0.100 | 0.067 | 0.500~0.893 | 127.500 | 66.7 | 70.7 | 0.374 |
| PCT | 0.796 | 0.057 | 0.000 | 0.685~0.907 | 2.395 | 95.8 | 51.2 | 0.470 |
| SOFA+PCT | 0.852 | 0.047 | 0.000 | 0.759~0.944 | 66.7 | 90.2 | 0.569 | |
| SOFA+HBP | 0.928 | 0.032 | 0.000 | 0.866~0.991 | 75.0 | 97.6 | 0.726 |
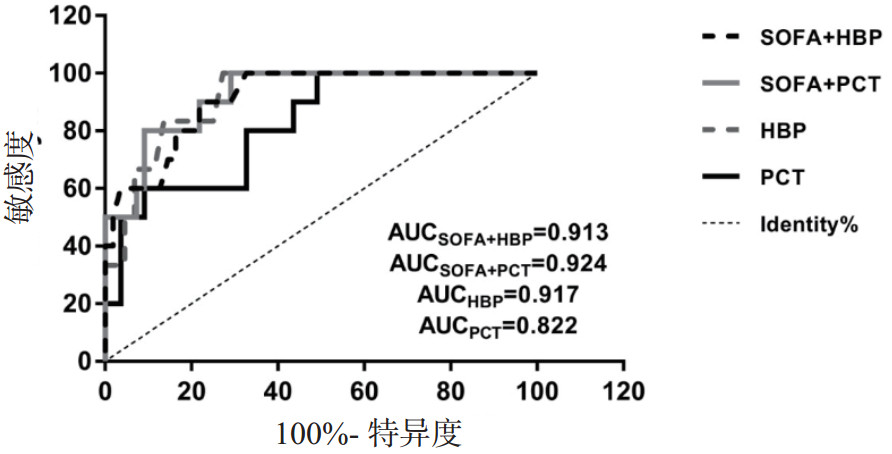
PCT联合SOFA评分预测28 d死亡的ROC曲线下面积(0.924)大于HBP(0.917)、HBP联合SOFA评分(0.913)和PCT(0.822)(图 2和表 5)。
|
| 图 2 HBP、PCT及二者联合SOFA预测死亡风险的ROC曲线 Fig 2 ROC curves of HBP, PCT and their combination with SOFA for predicting death |
|
|
| 指标 | AUC | SE | P值 | 95%CI | 最佳临界值 | 灵敏度(%) | 特异度(%) | 约登指数 |
| HBP | 0.917 | 0.047 | 0.001 | 0.825~1.000 | 127.5 | 100.0 | 72.7 | 0.727 |
| PCT | 0.822 | 0.066 | 0.001 | 0.692~0.952 | 18.4 | 60.0 | 90.9 | 0.509 |
| SOFA+PCT | 0.924 | 0.038 | 0.000 | 0.850~0.997 | 100.0 | 70.9 | 0.709 | |
| SOFA+HBP | 0.913 | 0.041 | 0.001 | 0.833~0.992 | 90.0 | 78.2 | 0.682 |
脓毒症是威胁人类健康的重要疾病之一,老年患者病死率高达30%~60 %,但因早期识别困难,约有20%~30%的患者来院时未表现出严重的器官功能障碍,诊治不及时病情进展十分迅速,病死率居高不下,因此尽早识别、评估病情严重程度以及积极的判断预后,对脓毒症的诊治具有十分重要的临床价值[5-6]。
本研究发现HBP和PCT对脓毒性休克和脓毒症患者死亡风险的早期预警价值较高,但WBC及CRP表现不佳。降钙素原是甲状腺激素降钙素的前体,正常情况下含量很低,人体受到细菌感染后迅速升高,可以反应脓毒症严重程度,被用来指导抗生素的使用[7]。HBP主要是在细菌感染后产生,甲型流感病毒H1N1导致的脓毒症患者及钩端螺旋体感染者体内HBP也明显增加[8],心肺复苏术后及心源性休克患者同样升高[9-10]。HBP是一种衍生自中性粒细胞的颗粒蛋白,中性粒细胞被趋化因子活化后其囊泡迅速分泌出胞,释放HBP,导致内皮细胞骨架重排和细胞收缩,从而增加内皮通透性,并作为诱导剂将更多白细胞募集到感染部位,进一步增强免疫反应[11]。动物试验进一步证实HBP增加血管内皮通透性[12],其机制与蛋白激酶C和rho激酶被激活有关[13]。血管内皮通透性增加和过度激活的免疫应答正是脓毒症器官功能障碍及休克的重要发病机制[14-15]。既往研究发现,HBP在脓毒症早期具有较好的预测价值,并且与循环衰竭密切相关[16-17];也发现脓毒性休克患者较未休克患者HBP及PCT显著增高,这与既往多项研究结果一致[18-19];但在Adam的研究中,脓毒性休克与未休克组HBP差异无统计学意义,这可能与该项试验未将恶性肿瘤化疗后导致白细胞减少的患者排除有关[20]。笔者还发现28 d死亡者较存活者的HBP及PCT均显著升高。
运用ROC曲线进一步检测两个指标及分别联合SOFA评分后对脓毒性休克早期诊断及28 d死亡风险的预测效能,结果得出诊断脓毒性休克时单独应用HBP(AUC=0.696)逊色于PCT(AUC=0.796)。当HBP联合SOFA评分后,效能明显提升(AUC=0.928),优于SOFA联合PCT(AUC=0.852)。在一项前瞻性研究中,HBP对感染患者发生脓毒症的预测效能要优于PCT,但并未在脓毒性休克与未休克患者之间进行观察,而且未对死亡风险进行预测[3]。本研究发现在预测死亡风险时,HBP(AUC=0.917)优于PCT(AUC=0.822),SOFA联合PCT时效能最大(AUC=0.924),优于SOFA联合HBP(AUC=0.913)。证实HBP在早期判断脓毒症预后时效能很好,这一结果在Fredrik及Jonas等研究中也得到证实[7, 16]。PCT在预测死亡风险时相对逊色,既往试验得出入院时的PCT可以提示脓毒症发生器官功能障碍和休克的存在,但相较于动态变化,单次检测结果与死亡相关性相对较低[21]。PCT联合SOFA评分对脓毒症预后的预测效能最好,可能是因为PCT与SOFA评分具有显著正相关性[22, 23]。脓毒症是涉及炎症反应、免疫应答、代谢、凝血系统及器官功能紊乱的复杂病理生理过程,很难找到单一指标在早期诊断、判断严重程度及评估预后方面同时具有理想的特异性与敏感性[24]。本次研究发现,联合指标普遍比单一指标表现更好,能明显提升检验效能,但是在预测脓毒症死亡风险时,虽然HBP及HBP联合SOFA评分均具有很好的临床价值,但是后者却稍稍逊色于前者,这与预期结果不符。既往研究显示HBP与SOFA评分中的循环衰竭、肺损伤、肾损伤均有正相关性[17, 25],此次结果与预期不符是否与患者选择、检测时间及样本量较小有关,仍需进一步深入研究。
本研究的不足之处在于这是一次单一横断面研究,没有进行连续性观察,所以仅能提示对老年脓毒症患者病情严重程度及死亡风险的早期预测价值,对于脓毒症发展过程中各指标的变化还需更进一步深入研究。
综上所述,HBP联合SOFA评分对老年脓毒症患者发生脓毒性休克及死亡风险均有较好的预测价值。
利益冲突 所有作者均声明不存在利益冲突。
| [1] | Seymour CW, Gesten F, Prescott HC, et al. Time to treatment and mortality during mandated emergency care for Sepsis[J]. N Engl J Med, 2017, 376(23): 2235-2244. DOI:10.1056/nejmoa1703058 |
| [2] | Ya ng, Liu GH, He QN, et al. A promising candidate: heparin-binding protein steps onto the stage of Sepsis prediction[J]. J Immunol Res, 2019, 2019: 1-11. DOI:10.1155/2019/7515346 |
| [3] | Adam L, Ryan A, John HB. Heparin-binding protein measurement improves the prediction of severe infection with organ dysfunction in the emergency department[J]. Crit Care Med, 2015, 43(11): 2378-2386. DOI:10.1097/CCM.0000000000001265 |
| [4] | Singer M, Deutschman CS, Seymour CW, et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3)[J]. JAMA, 2016, 315(8): 801-810. DOI:10.1001/jama.2016.0287 |
| [5] | 中国医疗保健国际交流促进会急诊医学分会, 中华医学会急诊医学分会. 中国脓毒症早期预防与阻断急诊专家共识[J]. 中华急诊医学杂志, 2020, 29(7): 885-895. DOI:10.3760/cma.j.issn.1671-0282.2020.07.001 |
| [6] | 陈振英, 何小军. 2018中国脓毒症研究发展蓝皮书及未来展望[J]. 中华急诊医学杂志, 2019, 28(10): 1332-1334. DOI:10.3760/cma.j.issn.1671-0282.2019.10.032 |
| [7] | 降钙素原急诊临床应用专家共识组. 降钙素原(PCT)急诊临床应用的专家共识[J]. 中华急诊医学杂志, 2012, 21(9): 944-951. DOI:10.3760/cma.j.issn.1671-0282.2012.09.005 |
| [8] | Kaukonen KM, Linko R, Herwald H, et al. Heparin-binding Protein (HBP) in Critically Ill Patients With Influenza A(H1N1) Infection[J]. Clin Microbiol Infect, 2013, 19(12): 1122-1128. DOI:10.1111/1469-0691.12156 |
| [9] | Pan T, Long GF, Chen C, et al. Heparin-binding protein measurement improves the prediction of myocardial injury-related cardiogenic shock[J]. BMC Cardiovasc Disord, 2020, 20: 124. DOI:10.1186/s12872-020-01406-3 |
| [10] | Ristagno G, Group FS, Masson S, et al. Elevated plasma heparin-binding protein is associated with early death after resuscitation from cardiac arrest[J]. Crit Care, 2016, 20: 251. DOI:10.1186/s13054-016-1412-4 |
| [11] | Fisher J, Linder A. Heparin-binding protein: a key player in the pathophysiology of organ dysfunction in Sepsis[J]. J Intern Med, 2017, 281(6): 562-574. DOI:10.1111/joim.12604 |
| [12] | Chen SL, Xie WL, Wu K, et al. Suilysin stimulates the release of heparin binding protein from neutrophils and increases vascular permeability in mice[J]. Front Microbiol, 2016, 7: 1338. DOI:10.3389/fmicb.2016.01338 |
| [13] | Bentzer P, Fisher J, Kong HJ, et al. Heparin-binding protein is important for vascular leak in Sepsis[J]. ICMx, 2016, 4: 33. DOI:10.1186/s40635-016-0104-3 |
| [14] | Cheng BL, Hoeft AH, Book M, et al. Sepsis: pathogenesis, biomarkers, and treatment[J]. Biomed Res Int, 2015, 2015: 1-2. DOI:10.1155/2015/846935 |
| [15] | Chen XH. Sepsis and immune response[J]. World J Emerg Med, 2011, 2(2): 88. DOI:10.5847/wjem.j.1920-8642.2011.02.002 |
| [16] | Kahn F, Tverring J, Mellhammar L, et al. Heparin-binding protein as a prognostic biomarker of Sepsis and disease severity at the emergency department[J]. Shock, 2019, 52(6): e135-e145. DOI:10.1097/shk.0000000000001332 |
| [17] | 刘杨, 马少林, 王学斌. 血清肝素结合蛋白在脓毒症休克中的预测作用[J]. 中华急诊医学杂志, 2014, 23(1): 79-83. DOI:10.3760/cma.j.jssn.1671-0882.2014.01.019 |
| [18] | Chew MS, Linder A, Santen S, et al. Increased plasma levels of heparin-binding protein in patients with shock: a prospective, cohort study[J]. Inflamm Res, 2012, 61(4): 375-379. DOI:10.1007/s00011-011-0422-6 |
| [19] | Zhou YX, Liu Z, Huang J, et al. Usefulness of the heparin-binding protein level to diagnose Sepsis and septic shock according to Sepsis-3 compared with procalcitonin and C reactive protein: a prospective cohort study in China[J]. BMJ Open, 2019, 9(4): e026527. DOI:10.1136/bmjopen-2018-026527 |
| [20] | Linder A, Åkesson P, Inghammar M, et al. Elevated plasma levels of heparin-binding protein in intensive care unit patients with severe Sepsis and septic shock[J]. Crit Care, 2012, 16(3): R90. DOI:10.1186/cc11353 |
| [21] | Tydén J, Herwald H, Sjöberg F, et al. Increased plasma levels of heparin-binding protein on admission to intensive care are associated with respiratory and circulatory failure[J]. PLoS One, 2016, 11(3): e0152035. DOI:10.1371/journal.pone.0152035 |
| [22] | Yunus I, Fasih A, Wang YZ. The use of procalcitonin in the determination of severity of Sepsis, patient outcomes and infection characteristics[J]. PLoS One, 2018, 13(11): e0206527. DOI:10.1371/journal.pone.0206527.[LinkOut |
| [23] | Guan J, Lin ZF, Hong LE. Dynamic change of procalcitonin, rather than concentration itself, is predictive of survival in septic shock patients when beyond 10 ng/mL[J]. Shock, 2011, 36(6): 570-574. DOI:10.1097/shk.0b013e31823533f9 |
| [24] | Fan YW. A pulmonary source of infection in patients with Sepsis-associated acute kidney injury leads to a worse outcome and poor recovery of kidney function[J]. World J Emerg Med, 2020, 11(1): 18. DOI:10.5847/wjem.j.1920-8642.2020.01.003 |
| [25] | Tydén J, Herwald H, Hultin M, et al. Heparin-binding protein as a biomarker of acute kidney injury in critical illness[J]. Acta Anaesthesiol Scand, 2017, 61(7): 797-803. DOI:10.1111/aas.12913 |
 2020, Vol. 29
2020, Vol. 29




