创伤是青壮年人群的首要死因,约30%~40%的创伤死亡因大量失血所致,失血也是严重创伤后“可预防性死亡”的主要原因。及时、快速控制出血,纠正失血性休克对严重创伤的救治至关重要,不仅可以有效减少严重创伤后继发性损伤所致的并发症,还可以大大降低“可预防性死亡”[1]的发生。中国医师协会急诊医师分会、中国人民解放军急救医学专业委员会、中国医师协会急诊医师分会急诊外科专业委员会针对创伤失血性休克紧急救治的关键问题,于2017年12月在国内首次推出了《创伤失血性休克中国急诊专家共识》[2],为中国急诊医生对此类患者进行诊疗工作提供了系统、全面的参考依据。随着时间的推移,在创伤失血性休克诊疗领域涌现了大量临床与基础研究,一些观念发生了变化。为此,编写组在第一版《共识》的基础上,以创伤救治流程的时间轴为主线,围绕创伤失血性休克诊疗关键问题,更新并依据最新临床证据总结推荐意见;通过全国急诊领域专家的共同讨论,以文献、数据的质量和每项推荐意见的收益与风险之间的平衡为基础进行了分级。临床证据的分级标准依据GRADE(grading of recommendations assessment, development and evaluation)评价系统制定,具体见表 1。
| 推荐等级 | 各等级代表的意义 | 收益、风险与负担之间的关系 | 支持证据的文献质量 |
| 1A | 推荐力度大;证据质量高 | 收益明显大于风险和负担,反之亦然 | 无重要限制的随机对照研究或具有压倒性证据的观察研究 |
| 1B | 推荐力度大;证据质量中等 | 收益明显大于风险和负担,反之亦然 | 有重要限制的随机对照研究或具有高质量证据的观察研究 |
| 1C | 推荐力度大;证据质量低或极低 | 收益明显大于风险和负担,反之亦然 | 观察性研究或病例分析 |
| 2A | 推荐力度小;证据质量高 | 收益与风险、负担持平 | 无重要限制的随机对照研究或具有压倒性证据的观察研究 |
| 2B | 推荐力度小;证据质量中等 | 收益与风险、负担持平 | 有重要限制的随机对照研究或具有高质量证据的观察研究 |
| 2C | 推荐力度小;证据质量低或极低 | 无法评估收益、风险与负担之间的关系;收益、风险与负担之间可能持平 | 观察性研究或病例分析 |
本共识不再将创伤失血性休克的病理生理基础单独以章节形式描述,而是将这些知识点融入到推荐意见的支撑文献之中;对时间依赖性较强的救治环节进行了简化,如创伤失血性休克的识别;强化了致命性出血控制要点的阐述;细化了液体复苏目标、液体选择、决策转变依据;对创伤性凝血病的范畴进行了拓展,新增对创伤性凝血病高凝状态表型的阐述;明确了创伤镇痛的阶梯化方案;力求推荐意见的可操作性与实用性。
本共识主要关注创伤失血性休克的早期救治,由于篇幅所限,并没有对创伤整体治疗其他要点进行展开。
2 创伤失血性休克快速识别及严重程度评价标准 2.1 创伤失血性休克的概念创伤失血性休克目前没有一个公认的(统一的)概念,本共识制定组认为创伤失血性休克概念[2]是指创伤造成机体大量失血所致有效循环血量减少、组织灌注不足、细胞代谢紊乱和器官功能受损的临床症候群。休克常常合并低血压[定义为收缩压 < 90 mmHg(1 mmHg=0.133 kPa),脉压 < 30 mmHg[3],或原有高血压者收缩压自基线下降≥40 mmHg]。
2.2 创伤失血性休克的快速识别与程度评价创伤失血性休克可以发生在接诊前,也可以发生在医疗救治的过程中;从休克发生到死亡的中位时间仅有2 h, 早期识别失血性休克和迅速采取止血措施是拯救生命的关键[4]。为了争取更长的诊疗时间窗,降低死亡率与并发症的发生,识别创伤失血性休克不能仅仅基于以上诊断标准,应该引入更多的临床指标加以量化,同时评估和预判失血的严重程度,以指导救治工作。目前有多个公认的评价系统可以用于创伤失血性休克的识别与严重程度评价。
休克指数(shock index,SI)是脉搏(bpm)与收缩压(systolic pressure, SBP)的比值,是反映血流动力学的临床指标之一,具有所需临床变量少、可以快速获得、计算简单等特点,可用于失血量粗略评估及休克程度分级[5](表 2)。SI可能因患者心血管储备能力、血管顺应性等因素存在个体差异,而导致错误评价,在应用时应充分考虑到年龄、基础疾病、基础代谢能力等因素(如:儿童、运动员、老年患者)。脉压(收缩压-舒张压)的降低也是快速判断血流动力学、预测患者急诊手术与大量输血可靠的临床指标之一,一项回顾性研究提示脉压<30 mmHg与患者是否存在休克、是否需要紧急手术密切相关[3]。
美军将神志和脉搏异常作为战场环境下快速识别失血性休克以及启动输血治疗的评价标准:没有头部损伤的伤员,发生神志异常或者精神状态改变,和(或)桡动脉搏动减弱或者消失[6]。
高级创伤生命支持(advanced trauma life support,ATLS)休克分级标准是目前被广泛认可的创伤失血性休克多因素、严重程度评价标准,它通过综合心率、血压、呼吸频率、尿量、神经系统症状等多因素对潜在失血量进行分级,但德国研究者对此提出了质疑[7],他们将该标准中的心率、血压、神经系统症状三个参数作为“严格”的分级标准,用于3万余例创伤数量的回顾性分析,发现该标准不能发挥良好的休克分级作用。
值得注意的是:严重创伤患者发生失血性休克的风险是持续存在的,首诊阶段采用复杂变量的休克分级标准可能降低休克识别的效率,而在持续治疗的过程中,就需要动态观察更多能够反映循环或灌注不足的临床指标的变化趋势。
推荐意见1:在灾难、战争环境下或其他无法获取患者(非脑外伤)生命体征时采用神志异常和(或)桡动脉搏动减弱或消失两个指标快速建立创伤失血性休克的初步诊断(1C)。
推荐意见2:在可获取患者生命体征时,可首先采用休克指数(SI)≥1或者脉压<30 mmHg作为建立创伤失血性休克诊断以及判断其严重程度的标准(1C)。
推荐意见3:在持续救治过程中,应尽可能全面的获取致伤机制并动态监测患者的心率、血压、脉压、脉搏、呼吸、尿量、意识状态、血气分析(血碱缺失及血乳酸水平)等可能反映循环或灌注不足的临床指标,并结合致伤机制对创伤后失血程度进行综合分析,建立临床诊断(1B)。
3 院前评估与紧急救治 3.1 首次评估与出血控制出血是严重创伤后“可预防性死亡”的主要原因,通过对控制出血的重视可大大提高严重创伤的整体救治成功率,降低“可预防性死亡”的发生[1]。因此在传统创伤首次评估(ABCDE原则)的基础上,突出致命性出血的早期识别与控制(hemorrhage control):对于可见的头颅躯干部体表活动性出血、肢体活动性出血应在第一时间进行有效控制,同时动态评估止血效果;一些不可见的但是可预期的出血也应该在第一时间采取有效措施予以控制,如:多发长骨干骨折、严重骨盆骨折。严重创伤早期评估与救治应按照CABCDE原则:C-出血控制(hemorrhage Control),A-气道(Air way),B-通气(Breathing),C-循环(Circulation),D-神经功能障碍(Disability),E-暴露与环境控制(Exposure & Environments)。
局部压迫是最为快速的止血方式,绝大多数的体表活动性出血可以通过局部压迫或加压包扎获得良好的止血效果[8]。对于创口较小或者存在潜行伤道时,局部压迫止血可能无法确切的压闭出血的血管或创面,导致止血效果不佳,可考虑采用填塞法或填塞法结合加压包扎的方法进行止血。鼓励使用具有辅助止血效果的敷料作为包扎材料以提高院前控制出血的效果。对于创道细长的贯穿伤,特别是颈部难以控制的盲管伤,可将Foley导管直接插入伤口,通过扩张前端球囊达到控制出血的目的[9-10]。
止血带适用于四肢致命性出血的快速控制[包括穿通伤(穿透性、贯通性)、爆炸伤、大面积软组织毁损伤、创伤性截肢][8];在某些特殊环境下,无法及时探明出血部位、评价出血严重程度时也可使用止血带控制四肢出血,但应在条件允许的情况下进行及时评估是否有必要继续使用止血带。没有证据支持对于四肢闭合性损伤或者非致命性出血使用止血带。止血带的并发症包括:神经损伤、肢体远端缺血再灌注损伤、创面感染风险增高、骨筋膜室综合征、肢体远端丢失(非必要的截肢),止血带使用时间超过2 h并发症率会明显上升[11];止血带的并发症还与是否严格按照适应证使用止血带相关,因为在面对不可控的致命性出血时,医生需要在挽救生命和挽救肢体间做出正确的选择[11];采用间断松开止血带的方式来延缓缺血性损伤,从而延长止血带使用时间的做法在院前急救环境是不恰当的,因再灌注时间需要至少30 min才能达到延缓缺血性损伤的作用,而不可控性出血持续30 min以上可能会直接威胁患者生命[12];松开止血带的操作有突然增加出血或再灌注损伤的风险,即便是在有条件的院内情况下也应做好充分的快速控制出血的准备[13]。
止血带使用时的注意事项:
【部位】绑扎在出血部位近心端10 cm以上非关节部位,如出血部位不明确,应将止血带打在肢体根部。
【松紧度】止血带的松紧度应取决于是否能有效控制创面出血,如无法通过一条止血带达到止血效果,应在其近心端再绑扎一条止血带。
【标注】止血带控制出血后应清晰标明开始使用时间,并暴露于体表,避免掩盖。
【解除条件】在具备确切创面止血能力或条件前,不可松动止血带;应该尽可能缩短等待确定性止血的时间,从而最大限度降低肢体功能障碍或截肢的风险。
严重高能量损伤所致的骨盆复杂性骨折,可导致骨折周围的多灶性出血(骨折断端出血、盆腔血管出血等),是多发伤主要死亡原因之一。在院前可使用骨盆带固定,通过限制骨盆活动,部分复位骨折、限制盆腔体积的方式达到降低出血速度的目的,在院内可根据骨盆骨折的类型决定是否行骨盆复位支架外固定手术[14]。
值得强调的是,不是所有的致命性出血都可以在现场进行处理,如:体腔内血管损伤、实质性脏器损伤、心脏损伤、部分颈部大血管损伤很难在第一现场进行及时控制;许多致命性出血部位常因体位或者衣物遮盖而被掩盖,应尽可能暴露伤者体表以免遗漏;通过近心端动脉压迫而达到区域性控制出血的方法(指压法),只适合于短时间内控制出血,为其他止血手段的实施争取时间或提供相对清晰的视野,随着时间的延长侧支循环的开放或压迫着力点移位等原因导致止血失败的发生;无论采用何种方式进行紧急止血,都需要动态评估止血效果,同时也不能因此而拖延患者获得确定性止血的时机。
推荐意见4:在院前首次接诊伤员时应首先排查可见的或可预期的致命性出血,对活动性出血,要立即采取快捷有效的止血措施,尽量减少受伤和出血控制之间的时间间隔;然后(或同时)开始常规的初次评估与救治(即CABCDE原则)(1A)。
推荐意见5:局部压迫或指压法(区域控制出血)只能作为临时措施,应快速替换为止血效率更高,便于伤者转运的止血方式(1A)。
推荐意见6:对于肢体活动性出血局部压迫无效或者特殊环境下无法及时探明出血部位时,可使用止血带控制致命性出血(1A)。止血带使用后须尽快将患者转运至有条件进行确定性止血的医疗机构、尽快实施确定性止血手术,止血带使用超过2 h可能会增加并发症的发生,是否撤出止血带取决于是否将威胁患者的生命(1B)。
推荐意见7:对于有疑似因骨盆骨折所致的致命性出血时,使用骨盆带或外固定支架并限制骨盆活动,以达到降低出血速度的目的(1B)。
推荐意见8:无论采用何种紧急止血措施,都应动态评估止血效果(1A)。
3.2 人工气道与通气支持由于人工气道特别是气管插管操作对操作者的要求较高,不建议在院前常规建立人工气道。对于清醒、有自主呼吸者,以清除气道异物、维持气道通畅为主。只有当存在明确的气道阻塞、GCS≤8分、合并有重度失血性休克、自主通气量不足或低氧血症时,才考虑建立人工气道[15]。院前可考虑声门上人工气道,在声门上气道无法耐受或无法获得有效通气效果时考虑经声门或声门下人工气道;但近期的一项队列研究发现:对于心脏骤停的患者,建立声门上人工气道的预后并不优于气管内插管[16]。因此,有条件的院前救治团队或院内急诊环境下,应考虑快速诱导麻醉插管(RSI)[17]。
创伤失血性休克患者人工通气治疗的初期,通常采用高浓度氧通气,以快速纠正组织缺氧。然而长时间的高浓度氧的吸入可能导致微循环改变及氧自由基损伤的发生,同时有研究表明,适当降低外周氧饱和度目标的通气策略对创伤患者的预后无明显影响,因此,在血红蛋白浓度纠正后应尽快将目标动脉血氧分压调整为正常水平(60~120 mmHg)[16, 18]。
在绝大多数情况下,过度通气可能增加创伤患者的死亡率,人工通气应根据PaCO2调整通气量,目标PaCO2应为35~40 mmHg。过度通气可以减少脑血流,从而在一定时间内降低颅内压力,在伤者出现单侧或双侧瞳孔扩大或去大脑状态等临床表现,提示即将死亡或发生不可逆性脑损伤时,可通过过度通气短暂延缓颅内压增高趋势,为医生实施其他确切降低颅内压的治疗措施争取时机。创伤失血性休克的患者存在急性呼吸窘迫综合征(ARDS)的风险,早期应使用低潮气量和适度呼气末正压通气(PEEP)的保护性通气策略[19]。
推荐意见9:以“最大限度避免低氧血症”作为院前开放气道与人工通气操作的最终目的。在有条件的情况下采用快速诱导麻醉插管(1A)。
推荐意见10:人工通气时应尽可能避免长时间高氧浓度通气;尽量采用低潮气量的策略(约6 mL/kg),只有在脑外伤、颅内压进行性增高、为延缓脑疝发生时采用过度通气策略(1B)。
3.3 院前液体复苏与急救药品的使用院前救治的主要目的是发现并控制快速致死性因素,就创伤失血性休克而言,首要的问题还是控制出血,院前液体复苏与急救药品的使用应充分考虑救治、转运的时效性和实用性,建议采用限制性液体复苏和延迟性液体复苏策略,具体详见后文(5、液体复苏;8、创伤凝血病的防治)。
3.4 医疗救助与转运的时效性大宗病历回顾性分析显示:院前救治时间的增加与创伤病死率的增加相关[20];尤其是锐性、开放性损伤的患者[21]。院前无法对所有类型的致命性出血进行有效控制,因此将伤者快速转运至有止血条件、具备损伤控制性手术、确定性手术、血管内介入手术等综合能力较强的创伤中心(尽量减少受伤和出血控制之间的时间间隔),可以显著改善预后[22]。但是对创伤与失血耐受性差的高龄患者,在无法快速送达创伤中心时,应当适当降低首诊医院资质门槛[23]。这就要求城市建立切实有效的创伤救治网络,并大力发展基层医院对创伤的综合救治能力。
推荐意见11:尽量将严重创伤患者转运至就近且具备相应救治能力的创伤中心。对于对创伤耐受性较差的患者更应注重就近转运的原则(1B)。
4 院内评估与紧急救治 4.1 创伤失血性休克的早期识别与初步评估首诊患者,应在接诊时按照推荐意见2建立失血性休克的诊断,按照推荐意见2、3初步评估创伤失血性休克的严重程度。
4.2 强化出血控制技术的应用院内阶段,快速识别与控制致命性出血仍是创伤失血性休克患者治疗的首要任务。应在接诊时按照推荐意见4~7,对可见的致命性出血进行快速排查与控制。合并有致命性出血的患者,对于明确出血病灶、且简易止血措施无法达到确切止血效果者,应考虑手术确定性止血的可能,并权衡选择恰当的干预方式;对于出血区域明确、但病灶无法确定者,在有条件时应考虑选择临时区域血管阻断,并快速明确出血病灶予以干预,条件不允许时,可考虑手术探查。
(1)损伤控制性策略与损伤控制性外科
损伤控制性策略是一种理念,源自美国海军舰艇水面下船体损伤的应急救援,引入创伤外科领域后形成了损伤控制性外科(damage control surgery,DCS)的理念,即:对于严重创伤特别是合并有低体温(T≤ 35℃)、酸中毒(pH值≤ 7.2)、无法控制的大出血、重建手术较大耗时较长的患者,采取分期手术的策略称为损伤控制性手术策略[24]。由于以往将“damage control surgery”中的“surgery”翻译为“手术”,因此错误的将其理解为一种术式。完整的DCS包括第一阶段尽量简化的手术,以控制出血、控制污染为目的;第二阶段为ICU治疗,其核心内容是优化血流动力学、复温、纠正酸碱失衡、纠正凝血功能障碍、改善重要脏器功能以及必要的精细化评估;第三阶段为再次重建修复手术。DCS必须严格掌握适应证,过度应用DCS可能导致患者死亡率的增加[25]。此外,单纯从第一阶段手术角度出发来讨论损伤控制理念是不正确的,损伤控制性理念并不一味追求在第一阶段完成姑息性手术,也并不排斥Ⅰ期重建修复手术[26],创伤医生应该权衡不同术式对患者全身状态的影响,既不贪恋“完美”的Ⅰ期手术,也不能一味放弃Ⅰ期重建修复的可能。
(2)血管内介入
躯干难以压迫的出血(肢体躯干交界部位、体腔内)可能是此阶段面临的最大问题。血管内介入适合动脉血供相对单一、侧支循环相对不太丰富、栓塞后果不严重的动脉性出血。可选择的方式包括永久性栓塞与球囊临时性阻断[如复苏性主动脉血管内球囊阻断术(resuscitative endovascular balloon occlusion of the aorta, REBOA)]。永久性栓塞应尽量考虑告高选择栓塞的可能性[27],避免广泛的缺血与脏器坏死;临时性球囊阻断可以在无放射影像定位下使用,该技术通过股总动脉的血管内通路置入球囊导管,实现主动脉临时阻断,从而达到暂时止血的目的。文献Meta分析发现,REBOA相对于传统主动脉临时夹闭技术,可以显著降低难以控制的躯干出血患者的病死率[28-29]。REBOA技术将主动脉分为三个区(即:Ⅰ区,左侧锁骨下动脉至腹腔干;Ⅱ区,腹腔干至肾动脉;Ⅲ区,肾开口以远至髂动脉分叉上)。对于腹腔内出血阻断Ⅰ区;在无腹部出血的情况下,阻断Ⅲ区可用于控制盆腔出血。REBOA技术的禁忌证包括心脏压塞和主动脉夹层,或者在穿透性颈部、胸部创伤和钝性心脏、主动脉损伤[30]。虽然REBOA可以挽救生命,但它也可能导致重大并发症;REBOA可导致危及器官和肢体的并发症,如假性动脉瘤、Ⅰ区阻断可能导致脊髓下段缺血及不可逆的神经功能损伤、Ⅲ区阻断可能导致下肢缺血坏死,实施前必须充分权衡并发症与失血性死亡风险之间的取舍,且只能在主动脉Ⅰ区与Ⅲ区实施阻断[30]。绝大多数情况下血管内介入应作为确定性手术的辅助手段,为手术操作创造手术时机、降低手术难度、减少术中出血。通过血管内介入栓塞止血后应动态评估控制出血的效果、尽早评价残留缺血病灶对整体的影响,并明确手术治疗的方式与时机。
(3)早期确定性手术
同上所述,任何时候都不能放弃Ⅰ期重建修复手术的可能,也不能将早期姑息性手术作为手术医生经验与能力不足的补救措施。有时Ⅰ期重建修复手术的创伤明显小于姑息性手术,同样的手术选择不同的术式也存在较大的差异(如:脾破裂切除,对于有经验的腔镜医生,腹腔镜手术可能在一定程度上减少手术创伤而不增加手术并发症,但对于缺乏此类经验的医生,传统开放手术可能更为适合),手术治疗策略的选择也与创伤医生自身能力、医疗环境有极大的关系,因此建议提高创伤外科医生综合救治能力,提升创伤中心建设效能,从而在必要时做出更为符合患者利益的决策。
(4)术中止血药的局部使用
一项纳入1000例腔镜手术的国内多中心前瞻性随机对照研究提示:将白眉蛇毒血凝酶8 kU溶于10 mL生理盐水中,用于术中创面局部喷洒,能够有效减少术后创面渗血和术后引流量,对患者的凝血功能没有明显影响[31]。
(5)麻醉风险在手术决策中的意义
没有临床证据支持麻醉高风险的创伤失血性休克患者可以因麻醉高风险而拒绝或者延迟手术时机。实际工作中严重创伤失血性休克的患者往往都存在常规麻醉风险评估较高的现象,而研究表明,缩短创伤失血性休克患者的术前等待时间,尽早实施确切止血与损伤控制可以显著改善创伤失血性休克患者的预后[1]。
(6)严重骨盆骨折所致失血的综合处理
没有临床证据证明,在面对严重骨盆骨折合并严重失血性休克时,血管内介入、剖腹止血填塞、骨折复位固定这三种基本治疗措施间存在绝对的优劣之分。
骨盆骨折可首选适度闭合复位及外固定措施[32],目的为闭合松质骨断面、稳定骨盆环、避免骨盆环反复移位活动、控制静脉和松质骨出血。外固定方式可选择外固定支架、C形夹、骨盆带,无论采取何种外固定方式,在对骨盆环进行加压操作时应注意压缩操作对骨盆环闭合的影响,避免加重移位或造成二次损伤。腹膜前、腹膜外或腹膜后填塞可减少或控制静脉出血,减少骨盆栓塞的需要[33],在骨盆骨折已相对稳定、血流动力学无好转、排除动脉型出血后可行骨盆填塞。对于骨折稳定的动脉性出血应考虑血管内介入栓塞。临时性血管内阻断可以为更为精确的血管内介入栓塞或者手术止血争取手术时机,但该操作应与其他影像学检查同时进行,避免不必要的手术时机的延误,同时应注意其并发症的风险。对于严重的骨盆损伤,应充分考虑单一治疗措施失败的可能,血管内介入与紧急手术可同时进行[34],这就要求加强创伤急诊手术室甚至杂交手术室的建设。
推荐意见12:对严重创伤患者合并有重度失血性休克、持续活动性出血,存在低体温(体温≤ 35℃)、酸中毒(pH值≤ 7.2)、凝血功能障碍风险,且Ⅰ期完全的重建修复手术难以快速控制出血、耗时较长、手术范围较广、手术打击较大者采用损伤控制策略,阶段性手术治疗;制订分阶段手术决策时应充分考虑Ⅰ期重建修复手术的可能以及替代Ⅰ期重建修复手术的手术方式是否真正能缩短手术时间、减少手术打击(1B)。
推荐意见13:对血流动力学稳定的患者进行Ⅰ期重建修复手术,除非存在严重污染以及存在可预期的因感染所致的重建修复失败的可能(1C)。
推荐意见14:术中可在已实施确定性止血的前提下,在有潜在渗血风险的创面上局部使用凝血酶类药物,以降低术后渗血风险(2C)。
推荐意见15:将血管内介入治疗作为创伤止血综合策略之一,适用于难以快速手术止血的动脉性出血,达到彻底控制出血、降低手术难度、减少术中出血的目的。在选择血管内介入治疗时,应充分考虑血管栓塞的并发症,并做好相应应对计划(1B)。
推荐意见16:在有条件的医院,对于不可压迫的致命性躯干出血可采用复苏性主动脉血管内球囊阻断术等方式进行临时性控制出血,为急诊确定性止血手术争取必要的时间(1B)。
推荐意见17:对于严重骨盆骨折应采取综合治疗措施。在有条件的地区,应加强急诊杂交手术室的建设,减少对患者不必要的搬动,缩短整体治疗时间(1B)。
推荐意见18:对于创伤失血性休克患者应适当降低麻醉风险对手术决策的影响,最大限度尽早开展确定性止血治疗(1A)。
4.3 创伤失血性休克的进一步评估推荐意见19:初步评估一旦完成,并且已对患者实施紧急处理,可以进行二次评估。若参与抢救的救治人员充足,可以在紧急处置的同时进行伤员的二次评估。二次评估包括:(向患者、患者家属或院前救治者询问了解)患者的病史及受伤机制、系统详细地查体、必要的实验室与影像学检查。在进一步评估中,仍旧需要关注患者大出血问题(1A)。
(1)病史补充、体格检查与监护
所有创伤患者在二次评估中都应尽可能完善病史(受伤机制、伤后症状、既往史)、完善从头到脚的全面检查,并予以必要的监护。
(2)实验室检查
① 血常规:由于大量失血后机体“自体输液”代偿机制需要一定的时间,因此患者首次血红蛋白(hemoglobin, Hb)/红细胞压积(hematocrit, HCT)即便正常,也不能排除失血的可能。初始Hb或HCT下降[35]或动态下降[36]可以反应患者失血量情况,对输血补液治疗起着决定性作用。
② 血气分析:动脉血乳酸与碱缺失,动态监测血乳酸[37]和碱缺失水平[38]对休克的早期诊断、指导治疗及预后评估有重要意义。当创伤与饮酒有关时,乳酸测定的可靠性可能较低。乙醇代谢通过乳酸脱氢酶诱导丙酮酸转化为乳酸,导致血液中乳酸水平升高;此时,碱基缺失可能比乳酸更能预测预后[39]。
③ 凝血功能指标:早期和动态监测凝血功能对了解创伤休克病情变化和治疗方法方案选择意义重大[40],检测指标主要包括血小板计数、凝血酶原时间(PT)、部分凝血活酶时间(APTT)和国际标准化比值(INR)等。
血栓弹力图(thromboelastography, TEG)是全血凝固的实时测试,可提供凝血功能的动态信息,有条件时使用TEG可进行更有效的监测[41],且TEG不受氨甲环酸给药的影响[42]。
尽管上述指标对了解创伤后凝血功能状态有一定的意义,但也存在一定的局限性,详见TIC章节。
④ 人绒毛膜促性腺激素(HCG):育龄期女性创伤患者如合并妊娠可能影响治疗与检查决策;因此需对此类患者常规进行血HCG检测。
⑤ 生化指标:监测电解质和肝肾功能,可及时发现肝肾功能损害,对指导治疗及稳定内环境至关重要。
⑥ 血型鉴定、病毒四项(乙肝、梅毒、艾滋、丙肝):留取第一份血标本的同时检测,为下一步输血或手术提前做好准备。
推荐意见20:伤员到达诊室后,评估的同时,抽血化验血常规、血气分析、凝血功能指标、血HCG、生化指标、血型鉴定、病毒四项作为实验室检查指标,且动态复查血常规、血气分析、凝血功能指标、生化指标等检查以掌握患者病情变化及危重程度分级(1B)。
(3)影像学检查
① CT扫描:患者入院进行CT扫描可大大提高救治效率[43]。全身计算机断层扫描(whole-body computed tomography, WBCT)是指对患者头、胸和腹部同时进行CT扫描,目前WBCT在外伤急救中的适应证仍在争论中,一项前瞻性研究对1271名患者的特定身体区域的放射学检查进行比较发现,在等效的身体区域中,WBCT检测到的损伤结果比选择性CT多(1.8∶0.6,P < 0.001)。与WBCT相比,选择性CT可能会低估特定身体区域的损伤严重程度,在22.0%的病例中,WBCT后损伤严重程度评分较检查前增加;88.4%的病例中,WBCT增加了1个以上的阳性发现(平均3.4)[44]。因此,针对多发伤的患者,特别是交通伤、高空坠落伤、受力部位不清楚创伤、严重钝性创伤或多发伤的成年患者作为影像学手段,可以行WBCT检查以避免对患者受伤部位的漏诊。需要注意的是,CT检查需对患者进行转移搬动,有加重患者创伤出血的可能,且检查时间相对较长,对于危重患者的选择需要谨慎。
② 创伤重点超声评估(focused assessment with sonography for trauma,FAST):是一种重要的检查方法[45],一般指由临床医生对创伤患者进行床旁超声快速评估的操作,根据腹腔及心包是否存在游离液体,判断腹部及心脏损伤是否存在,以及损伤的具体情况。对腹部外伤患者进行FAST检查,检查出患者腹腔内出血的特异度高达94%~98%,敏感度为73%~99%,准确性为90%~98%[46]。近期的一项系统评价显示,在院前救治环节,超声对气胸、胸腹腔内游离积液具有良好的敏感度与特异度[47]。但是,超声检查具有一定的局限性,患者病情比较复杂,实施超声检查操作者的技术和经验等主观因素也对检查结果有影响,其阴性并不能完全排除腹腔内和腹膜后出血。对怀疑存在出血的患者,如果血流动力学稳定或对容量复苏有反应,应考虑进行CT扫描。
推荐意见21:进一步评估中建议采用创伤重点超声评估(FAST)作为首选影像学检查手段,对高能量暴力损伤、致伤机制不明的昏迷患者、严重钝性损伤或多发伤的患者应进行全身CT扫描(1B)。
5 液体复苏 5.1 液体复苏的目标与策略创伤失血性休克复苏应遵循休克治疗阶段化目标原则[48],即急救阶段、优化阶段、稳定阶段与降阶梯治疗阶段;而就复苏而言,主要的工作集中在急救阶段与优化阶段。
急救阶段治疗目标为积极控制出血,最大限度维持生命体征平稳,保证血压、心输出量在安全范围。针对该阶段的治疗,美军通过总结实战救治经验,提出了损伤控制性复苏(damage control resuscitation,DCR)理念,包括允许性低血压、止血复苏、损伤控制性手术,强调控制出血前减少复苏液体量、注意维护凝血功能;DCR理念同样适合于非战争环境[49],在降低死亡率的同时也可以大大降低复苏用血量[50]。研究表明,非颅脑外伤的创伤大出血患者,手术前维持收缩压为80~90 mmHg是有益的[51];严重颅脑损伤(GCS≤8分)的患者,维持平均动脉压(MAP)为≥80 mmHg[52],或维持收缩压 > 110 mmHg[53]可以显著降低脑继发性损伤率与死亡率。快速控制出血是DCR的关键,缩短接诊—确定性控制出血的时间可以显著改善患者预后[54],是否完成致命性出血的控制也是决定液体复苏目标、策略转换的关键点。
一旦获得确定性止血,治疗目标应逐渐向优化调整阶段转换,以增加组织氧供、改善微循环灌注,优化心输出量、静脉血氧饱和度(SVO2)及血乳酸水平等体现有效循环与微循环灌注的临床指标[55]。
在院前救治阶段,过于积极的复苏策略对大量失血的创伤患者是不利的,以德国创伤外科学会创伤数据库资料为研究对象的一系列回顾性分析发现:无论是儿童[56]还是成年[57]患者,院前大量补液都可能导致并发症(特别是创伤性凝血病)以及死亡率的升高;即便是对于合并颅脑伤的严重多发伤患者,提高院前液体复苏量(大于1500 mL),也并不能改善患者的预后[58]。
推荐意见22:出血未能得到有效控制的创伤失血性休克患者推荐使用允许性低血压的液体复苏策略:无颅脑外伤的患者维持SBP在80~90 mmHg之间;严重颅脑损伤(GCS≤8分)患者,维持SBP > 110 mmHg,或MAP≥80 mmHg;复苏应以缩短确定性止血手术的等待时间为根本目的(1C)。
推荐意见23:在院前救治中,对创伤失血性休克的患者采取延迟性复苏或更为严格的限制性液体复苏策略(以维持SBP 80 mmHg或者可触及桡动脉搏动为目标)(1B)。
5.2 液体复苏通道院前:首选外周静脉通路,但救治环境、患者自身血管条件、穿刺耗时等因素都可能造成外周静脉通道无法快速建立。骨髓腔穿刺置管可以作为外周静脉通道的替代选择,一项随机对照研究发现;在院前环境下,与常规静脉穿刺相比,骨髓腔穿刺具有操作时间短、成功率高、漏液发生率低、整体生存率高等优势[59]。
院内:应在建立有效的外周静脉通路的同时尽早着手建立中心静脉通道的准备,首选上腔静脉属支;对于出血可能来自下腔静脉属支的伤者(如:严重骨盆骨折),通过下腔静脉属支补液可能无法获得良好的扩容效果,同时有增加出血的风险。若中心静脉通道建立困难可考虑胫骨或胸骨骨髓腔穿刺通道。
推荐意见24:良好静脉通路是液体复苏的前提,推荐院前首选外周静脉通路,院内应尽早建立中心静脉通路。在静脉通道建立困难或紧急条件下,可使用骨髓腔穿刺输液(1C)。
5.3 复苏液体的选择可用于创伤失血性休克液体复苏治疗的液体种类可分为血制品(全血、血浆)、晶体液、人工或天然胶体。
(1)全血与成分血
创伤失血性休克患者丢失的主要是等比例全血,因此理论上使用全血进行复苏是最为“生理”的。早在美国南北战争期间就将全血作为战创伤复苏的主要液体,然而由于并发症与经济性的关系,逐渐被成分输血所替代;近年来美军将降低免疫活性处理的全血应用于战创伤早期复苏(包括现场与战地医院环节),基于这些经验,全血在非战争环境下创伤早期复苏中的应用也逐渐增多,作为成分输血的一种替代方式,可以缩短等待输注时间;相对于等比例成分输血,在病死率和并发症率指标上差异并无统计学意义[60],近期一项3期院前血制品复苏的RCT研究显示,在院前救治阶段采用初始剂量2 U红细胞进行复苏相对于初始剂量1 L 0.9%氯化钠,其病死率与微循环改善程度(乳酸清除率)差异亦无统计学意义[61],其应用价值、并发症率、效价关系仍然有待进一步的验证。
(2)血浆
一项随机试验显示:严重失血性休克患者,在直升机救援现场及途中,优先给予2 U冰冻血浆,可以较常规复苏策略获得更低的30 d病死率、维持更好的凝血状态[62]。该研究中的血浆剂量很低,相比其有限的扩容作用,血浆在伤后短期内输注可以改善患者凝血功能、减缓持续出血、减少炎症反应与内皮活化等因素可能是导致患者预后改善的重要原因。且从研究对象的纳入标准分析,该研究中的研究对象已达到大量输血(massive transfusions,MTs)指征,因此可以将该研究理解为大量输血方案的前置。
(3)胶体与晶体的选择
晶体与胶体作为复苏液体的争论一直在持续,近期针对德国创伤外科学会创伤数据库的回顾性分析发现:人工合成胶体用于创伤失血性休克的液体复苏,并没给患者带来预期的疗效,且可能是有害的[63]。胶体对肾功能、凝血功能存在影响,并可能诱发过敏反应,不适用于脓毒症患者或有急性肾损伤风险的患者。鉴于使用胶体可能导致潜在的不利风险,不推荐使用胶体复苏。
平衡晶体液可避免高氯性酸中毒发生,改善重要脏器血流灌注,耐受性良好,是一种有效的晶体复苏液体,尤其对于活动性出血患者在院前环境无法获得成分血的情况和血源紧张的院内情况下,可采用平衡晶体液扩容。一项单中心多交叉研究对比发现在急诊使用平衡晶体液较生理盐水发生肾脏不良事件的概率更低[64]。乳酸是创伤失血性休克早期监测的重要指标,有担心乳酸林格液的输注可能会显著改变血中乳酸水平,影响复苏效果的判别,有趣的是,在对正常人群的研究中发现,1 h输注1 L乳酸林格钠不会改变血乳酸水平[65];只有在快速输注30 mL/kg剂量(70 kg健康人约输2100 mL)的乳酸林格钠时,才可能导致血乳酸水平的增高,而同样剂量的生理盐水也可以导致血乳酸的升高,且与输注乳酸林格钠无明显差异[66]。一项动物实验显示:在对新西兰兔失血性休克复苏过程中,碳酸氢钠林格氏液在维持酸碱平衡和组织保护方面比生理盐水更有效[67],采用新的缓冲体系、更贴近细胞外液电解质组份的复苏液体可能成为新的研究方向。对于颅脑创伤的患者应避免低渗溶液复苏,回顾性研究PROMMTT[68]显示,与0.9%氯化钠溶液相比,颅脑创伤患者使用乳酸林格液复苏可能导致死亡率增高。近期的一项RCT研究显示:重症患者复苏过程中选择平衡晶体液或0.9%氯化钠溶液,两组间患者的死亡率无明显差异[69]。因此,选择何种晶体液作为复苏的首选液体还有待进一步的研究与探索。
推荐意见25:建议对创伤失血性休克患者首先使用等渗晶体溶液进行液体治疗;建议使用平衡的电解质溶液或者0.9%氯化钠溶液(初始剂量0.5~1.0 L)(1A);建议限制使用胶体;对于颅脑创伤的患者建议避免使用低渗复苏液;建议在有条件的情况下,对存在大量输血可能性的患者,尽早使用2 U血浆,并尽快衔接MTs治疗(详见推荐意见26、27)(1B)。
5.4 大量输血治疗(1)如何启动MTs治疗
一般认为患者急性失血量达自身血容量的30%~50%时,需要MTs治疗。MTs治疗的概念为:24 h内输注≥10 U红细胞或1 h内输注3~4 U以上红细胞[70]。依靠临床经验启动MTs可能造成血制品的浪费与输血并发症的增加[70];即便是启动了MTs程序,如果未能在6 h内达到满意的复苏,患者的预后往往较差[71];因此,如何及时、准确的启动或终止MTs需要客观的预测方案作为决策支持。目前MTs尚未形成非常明确的共识,尤其是针对MTs何时终止的决策。近期一项纳入了544例患者的回顾性队列研究显示[72],SI≥1在预测创伤患者休克程度以及用血需求上优于血液消耗量评估(assessment of blood consumption, ABC)≥2。
(2)MTs治疗中的血制品选择
如前所述,MTs时选择全血还是成分血仍有较多争议,部分国外创伤中心再次将低免疫活性的全血作为血制品的首选[73],但基于我国国情,目前获得与使用全血很难在短时间内推广;因此,本共识组仍推荐等比例成分血。
在一项纳入680名严重创伤大出血患者进行成分比例输血的研究中发现,24 h内,血浆、血小板和红细胞按1:1∶1输注的患者比1∶1∶2输注的患者止血率更高,减少了早期失血死亡的比例[74]。但对于血浆、血小板和红细胞的输注比例为1∶1∶1是否是最佳的比例,仍有很多的专家表示存在异议[75]。一项纳入168例创伤受试者的随机对照研究显示,院前血浆输注可引起低钙血症,而严重低钙血症与生存率降低和大量输血需求显著相关[76],提示采用血制品复苏的患者应注意钙离子的补充。
通过经验,而不是实验室检查结果指导的输血复苏方案存在一定的盲目性,研究显示使用旋转血栓弹性测定法(ROTEM)[77]、TEG指导复苏治疗[78],可改善患者总体死亡率,并更为合理地使用血浆、血小板、纤维蛋白原等血制品。因此在院内条件下应强化并尽早过渡到“目标导向性输血复苏治疗”,即依据TEG、血常规、血凝、生化等检验结果制定的个体化输血方案[79]。
推荐意见26:急诊科或创伤中心,应以相对简单指标为标准,建议根据自身用血条件拟定创伤失血大量输血启动预案(1B)。
推荐意见27:大量输血方案实施的初始阶段,推荐血浆、血小板和红细胞比例控制在1∶1∶1(相当于来自同一个采血单位的成分血,例如200mL全血可分离约100mL血浆、1 U血小板、1 U红细胞)与1∶1∶2之间(1A);一旦接受血制品输注应注意钙离子的补充,维持钙离子浓度≥1.00 mmol/L(1A);并且应尽早过渡到依据血栓弹力图、血常规、血凝功能、生化等检验结果制定的目标导向性输血方案(1B)。
5.5 升压药与正性肌力药物一项在日本人群中进行的大样本回顾性队列研究显示,创伤失血性休克患者在最初24 h内使用血管加压药,增加创伤失血性休克死亡风险[80]。在一项随机、双盲安慰剂对照临床试验中发现,在成人(18~65岁)创伤失血性休克患者中使用精氨酸加压素维持平均动脉压≥65 mmhg可减少血制品,但不减少晶体的用量,对死亡率也没有改善[81]。但血压过低(如MAP低于50 mmHg或SBP低于70 mmHg)可能导致重要脏器灌注压持续下降、甚至危及生命,此时可以考虑使用升压药[82]。创伤失血性休克通常首选去甲肾上腺素用于恢复动脉压[83]。
推荐意见28:不推荐常规使用升压药物或正性肌力药物(1B)。对于危及生命的失血性休克(MAP低于50 mmHg或SBP低于70 mmHg)使用血管加压药,首选去甲肾上腺素(1C)。
6 温度管理体温过低(核心体温 < 35 ℃)与严重创伤失血性休克患者并发酸中毒、低血压和凝血障碍(死亡三角)密切相关,最终导致患者并发症率及病死率的增高。低温可严重影响血小板功能、凝血功能[84],而这一现象很难在实验室检查中观察到(因实验室检查的标本离体后常常被设置在37℃的条件下进行实验操作)。过低的体温管理目标还可能导致救治过程中血制品的用量增加。
积极的体温管理包括保温(脱离低温环境、更换湿衣物、维持体表干燥、覆盖保温材料等避免患者热量过度丢失的方法)、复温(提高环境温度、输注液体加热以及调温毯等体外加热装置)以及核心温度动态监测,并以核心温度目标作为体温管理措施实施的主要依据。
推荐意见29:应将核心温度作为体温管理的量化标准;建议早期应用保温、复温措施,除非有低温脑保护的要求,应将复温目标设置为正常体温(36~37 ℃)(1C)。
7 疼痛管理对严重创伤患者进行疼痛管理是非常必要的工作[85],但是绝大多数镇痛药物都会对血流动力学与呼吸兴奋性造成一定的影响,特别是阿片类强镇痛药;对于创伤失血性休克患者而言,在没有良好的生命支持措施的前提下可能加重病情;而以快速疼痛分层为基础的阶梯化疼痛管理策略可以更好的降低并发症的发生[86]。对轻到中度疼痛的患者首选非甾体类解热镇痛剂口服(如:对乙酰氨基酚500 mg,Q8h,可重复两次,或美洛昔康15 mg,Qd);对于中度到重度疼痛的患者首选氯胺酮30 mg(或0.3 mg/kg)缓慢静脉或静脉推注,20 min以上可重复1次,一旦疼痛被有效控制或出现眼球震颤应停止使用;对于中度到重度疼痛的患者在无休克或呼吸窘迫的情况下可使用枸橼酸芬太尼50 μg(或0.5~1.0 μg/kg)缓慢静推,30 min后可重复1次;对于中度到重度疼痛的创伤失血性休克患者需要行有创操作(明显增加患者疼痛)时应在充分的血流动力学支持及做好气道保护与插管准备后,调整增加镇痛药物的剂量。强镇痛药物的使用后应注意血流动力学、呼吸兴奋性改变以及低剂量条件下的致幻作用的保护[6]。
推荐意见30:建议在对创伤患者行镇痛治疗前应常规开展疼痛评估,采用快速简便的疼痛评估方法(如VAS法或面部表情法);建议对于创伤患者采用阶梯化的选择镇痛策略;镇痛药物应选择对血流动力学与呼吸兴奋性影响较小的药物,使用后应密切监测血流动力学与自主呼吸兴奋性,并做好纠正血流动力学不稳定及人工通气的准备(2C)。
8 创伤性凝血病的防治创伤性凝血病(trauma-induced coagulopathy, TIC)目前尚无统一的标准定义,一般认为TIC是一组继发于创伤的多因素所致的凝血功能障碍;TIC的发病机制复杂、表型多样:在组织损伤与休克的协同作用下,导致低凝状态(“早期TIC”)的因素包括凝血酶生成障碍、血小板功能障碍、纤维蛋白原缺乏或功能障碍、纤溶过度激活以及内皮功能障碍,而导致高凝状态(“晚期TIC”)的因素包括凝血酶生成过度、内皮损伤、血小板过度激活或衰竭、高纤维蛋白原血症和纤溶功能障碍[87]。“早期TIC”主要表现为低凝状态所致的出血以及早期出血相关死亡,而“晚期TIC”主要表现为高凝状态相关的静脉内血栓形成、多器官功能障碍以及栓塞相关的迟发性死亡;“早期TIC”和“晚期TIC”可能同时存在于同一患者的病程之中,患者可能在几分钟或几小时内发生从低凝状态到高凝状态的转变,这一过程也可能迁延数日[88-89]。
影响TIC表型和病程的因素可分为三类:①创伤因素:包括损伤严重程度、损伤的组织类型、失血性休克程度、损伤机制和受伤时间;②患者因素:包括年龄、性别、合并症(如心血管疾病)、创伤前使用的抗凝剂、凝血功能的遗传差异;③复苏治疗因素:包括使用的液体类型、血制品成分、复苏辅助药品使用(如TXA)和手术干预的时间;尽管TIC不同于其他类型的凝血病,在上述三类因素的影响下呈现出多种表型,但如果凝血功能持续异常,最终也将像其他凝血病一样进入暴发性凝血功能衰竭和DIC的共同途径[87, 90]。
传统的基于血浆的凝血实验(PT或INR和APTT)并不能很好地反映创伤患者的实际凝血功能状态,基于全血的凝血实验[弹性凝血实验(viscoelastic haemostatic assays,VHAs)]在一定程度上弥补了传统凝血实验的不足,目前被用于目标导向止血复苏的VHAs有TEG或ROTEM,其优点在于反映了血栓形成的各个阶段,但它们无法监测血流产生的剪切力对凝血的影响,也无法反映炎症反应与免疫系统对凝血的作用,不能可靠地量化血小板功能和纤溶水平[91]。因此在采用上述指标指导复苏时,应充分考虑其局限性,并做好动态评估,及时调整复苏方案。
创伤早期有效控制出血是预防TIC的关键,在未获得有效控制出血前采取适当的损伤控制性复苏、合理选择复苏液体减少TIC的发生(同推荐意见4、12~18、22、23、25~27)。
除此之外,TIC早期的纤溶亢进一直是研究和治疗策略的热点。CRASH-2试验表明,成人创伤患者早期使用氨甲环酸(伤后3 h内使用负荷剂量为1 g、给药时间至少10 min,然后继续静脉滴注给药1 g并维持8 h以上)可降低大出血与死亡风险[92]。CRASH-3试验表明,轻到中度颅脑创伤患者早期使用氨甲环酸可改善生存预后[93]。尽管CRASH-2、CRASH-3均未发现氨甲环酸的应用与静脉血栓性并发症的关系,但上述两项研究缺乏对静脉血栓性并发症的筛查;同时CRASH-2的结果显示创伤3 h后使用氨甲环酸会增加病死率,提示氨甲环酸应在伤后早期使用,且对于有纤溶过程明显受抑的患者应该慎用[94]。尿胰蛋白酶乌司他丁(ulinastatin),一直被认为能够稳定溶酶体膜、清除氧自由基及抑制炎症介质释放,从而减轻细胞和组织损伤。近期一项小样本随机对照研究显示,乌司他丁可以显著降低体外循环心脏手术患者的术后失血,其疗效与氨甲环酸相似[95];该结论有待更大样本量的随机对照多中心研究加以证实。
止血复苏策略目前尚存在较为明显的区域差异。例如,欧洲大出血和凝血病管理指南强调纤维蛋白原的补充,而美国止血复苏策略更倾向于优先使用血浆和血小板。上述血制品资源可能存在严重的区域差异,因此应根据现有条件与可获取资源合理运用。
如前所述,TIC是多因素所致的创伤后特有的凝血功能障碍,对于因基础疾病而长期服用抗凝或抗血小板凝集药物的患者或合并有原发性凝血功能障碍的患者(如血友病),伤后发生TIC的风险也会显著增高。因此,在创伤早期救治阶段应尽可能的获取此类药物的服用史及基础凝血功能障碍等病史,并根据伤后凝血功能水平予以相应的拮抗治疗。如:使用维生素K1或凝血酶原复合物逆转维生素K依赖的口服抗凝药(如华法林);使用鱼精蛋白拮抗肝素;Idarucizumab单克隆抗体逆转达比加群;Andexanet单克隆抗体逆转沙班类Ⅹa因子抑制剂;对于服用抗血小板药且持续出血的患者,如存在血小板功能障碍,或伴颅内出血且需要手术的患者,可输注浓缩血小板;对于血友病患者,如存在明显出血倾向或需接受手术治疗前应予以相应凝血因子的补充。
发生严重“早期TIC”的患者发生“晚期TIC”的风险更高。低灌注加重组织损伤、严重创伤患者的主动或被动制动都可能是“晚期TIC”发生的重要原因;在出血和低灌注得到解决后,大多数患者的凝血功能将从低凝状态过渡到高凝状态[87],从高纤溶状态过渡到低纤溶状态[96]。“晚期TIC”的发生机制尚不完全明确,目前所知的是复苏后血栓强度增加和纤溶障碍(VHAs测量值)是创伤后静脉栓塞性并发症的危险因素[97]。
推荐意见31:建议强化对TIC的重视,TIC的不同表型(低凝状态或高凝状态)都可能导致不良预后的发生(1A);TIC的预防关键在于创伤早期有效控制出血(详见推荐意见4、12~18、22、23、25~27)
推荐意见32:建议动态监测创伤失血性休克患者的血常规、凝血功能(血浆凝血功能、VHAs),以指导复苏(同推荐意见27),同时动态评估TIC的发生以及表型变化(1C)。
推荐意见33:建议成人创伤患者早期使用氨甲环酸(伤后3 h内使用负荷剂量为1 g、给药时间至少10 min,然后继续静脉滴注给药1 g并维持8 h以上);不建议在创伤3 h后或有明确纤溶抑制的患者使用氨甲环酸(1A)。
推荐意见34:建议在接诊患者时主动询问抗凝、抗血小板药物服用史以及基础凝血功能障碍等病史,根据凝血功能状态与治疗决策,选择必要的拮抗或补充治疗(1C)。
推荐意见35:建议强化创伤失血性休克患者血栓性并发症的Ⅲ级预防(1C)。
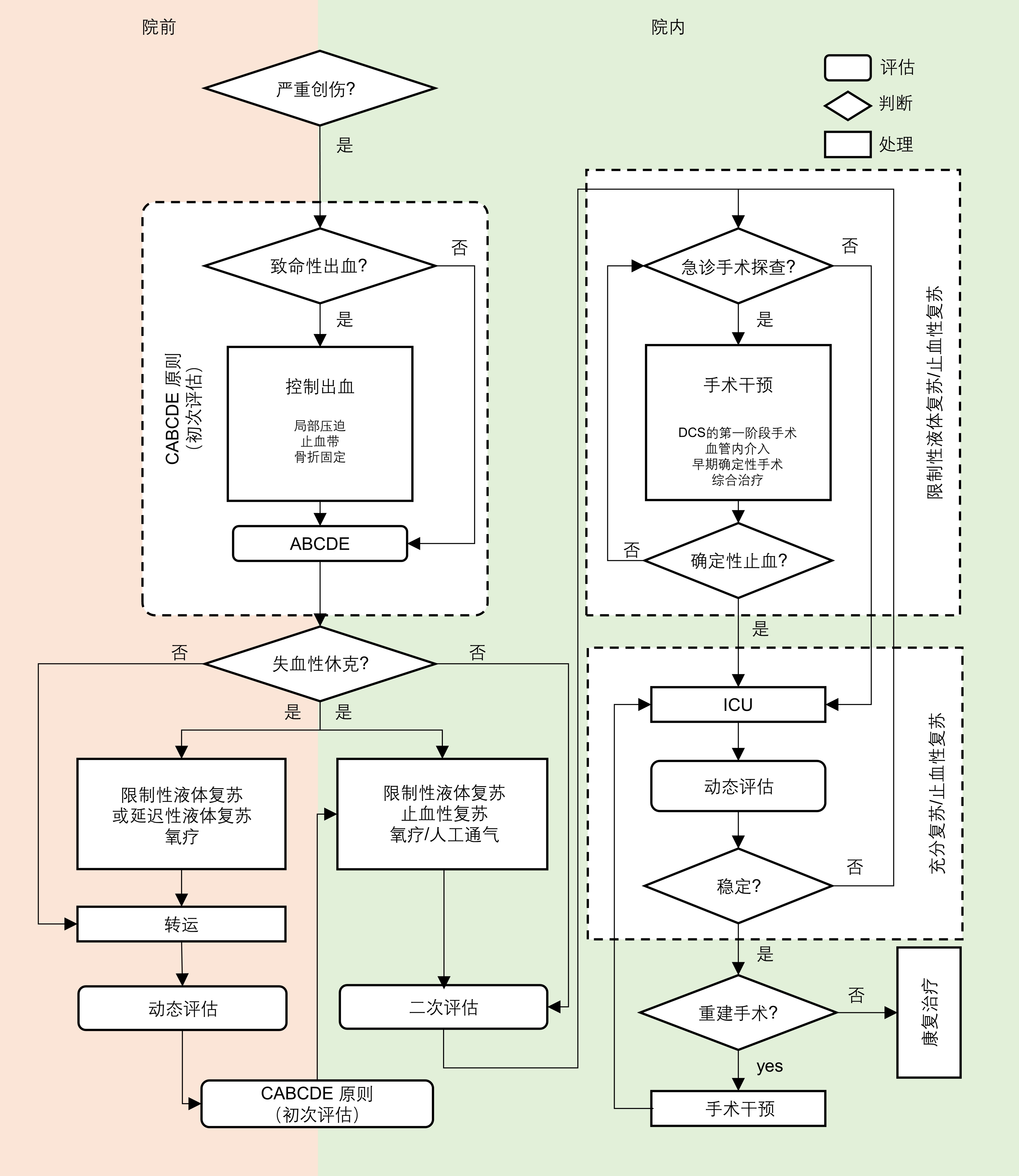
9 总结积极预防、早期识别、合理治疗创伤失血性休克是提高严重创伤患者救治成功率的关键。随着严重创伤病程的发展以及临床救治场景的变化,创伤失血性休克诊治的要点也会发生相应的变化(见图 1);任何情况下,首次接诊伤者的医生都应遵循CABCDE原则对患者进行快速的初次评估;在院前救治阶段,急诊医生应在第一时间发现并有效控制可控制的出血,在确定性止血措施起效前应采用限制性或延迟性液体复苏策略;一旦伤者到达医院,接诊医生应对伤者进行两阶段评估,以避免错失第一时间控制致命性出血的机会;对尚未明确诊断或暂无急诊手术指征的患者应制定个性化的动态评估计划。尽管在液体复苏、TIC的预防和治疗、影像学检查选择、手术时机与方式选择等方面存在不同程度的争论,临床医生常常处于两难境地;然而在绝大多数情况下,能否及时有效控制致命性出血都是简化临床问题、明确治疗目标的关键。
|
| 图 1 创伤失血性休克诊疗决策流程图 |
|
|
本共识根据现有文献基础,结合专家团队的临床实践经验,以严重创伤救治时间轴为主线,制定和推荐了创伤失血性休克评估、止血、复苏、手术、体温管理、疼痛管理、TIC防治等关键临床问题的决策选择,临床医生还应结合伤者病情、病程、医疗机构能力等因素,权衡治疗风险和患者获益后采用。
执笔作者:陈翔宇、刘红升、向强、刘双庆
参与共识制定专家组成员(按姓名拼音顺序)
白祥军、曹钰、柴湘平、柴艳芬、陈飙、陈聪、陈锋、陈凤英、陈海鸣、陈威、陈翔宇、崇巍、党星波、邓颖、丁邦晗、董士民、窦清理、杜同海、杜贤进、范晨芳、费军、封启明、高峰、果应非、韩小彤、何小军、侯利民、黄亮、冀兵、蒋龙元、金红旭、康健、李德忠、李立宏、李培武、李湘民、李小刚、李小民、李永武、李占飞、梁显泉、林炳锵、蔺际龑、刘斌、刘红升、刘明华、刘双庆、刘宇鹏、刘笑然、卢中秋、吕传柱、马俊麒、毛恩强、穆叶赛·尼加提、聂时南、潘险锋、裴俏、彭娜、彭鹏、钱传云、秦历杰、桑锡光、单爱军、商德亚、邵艳霞、沈开金、司君利、宋海晶、苏琴、唐华民、唐柚青、唐玉彬、唐忠志、田英平、田兆兴、王成、王海涛、王培戈、王琦、王锐、王瑞兰、王威、王旭东、王振杰、吴国平、吴海英、吴利东、向强、邢吉红、徐峰、徐贵森、徐军、徐宪辉、许硕贵、许铁、燕宪亮、闫柏刚、闫乐媛、杨灿菊、杨立山、姚爱明、姚咏明、尹文、于学忠、张东山、张海涛、张建波、张剑峰、张茂、张为、张伟、张文武、张新超、章福彬、赵刚、赵敏、赵小纲、赵晓东、郑粉双、周人杰、周荣斌、朱海燕、朱华栋、朱加应、朱长举、左永波
利益冲突 所有作者声明无利益冲突
| [1] | Celso B, Tepas J, Langland-Orban B, et al. A systematic review and meta-analysis comparing outcome of severely injured patients treated in trauma centers following the establishment of trauma systems[J]. J Trauma, 2006, 60(2): 371-378. DOI:10.1097/01.ta.0000197916.99629.eb |
| [2] | 中国医师协会急诊分会, 中国人民解放军急救医学专业委员会, 中国人民解放军重症医学专业委员会, 等. 创伤失血性休克诊治中国急诊专家共识[J]. 中华急诊医学杂志, 2017, 26(12): 1029-1038. DOI:10.3760/cma.j.issn.1671-0282.2017.12.004 |
| [3] | Warren J, Moazzez A, Chong V, et al. Narrowed pulse pressure predicts massive transfusion and emergent operative intervention following penetrating trauma[J]. Am J Surg, 2019, 218(6): 1185-1188. DOI:10.1016/j.amjsurg.2019.08.022 |
| [4] | Cannon JW. Hemorrhagic shock[J]. N Engl J Med, 2018, 378(4): 370-379. DOI:10.1056/NEJMra1705649 |
| [5] | Olaussen A, Blackburn T, Mitra B, et al. Review article: shock index for prediction of critical bleeding post-trauma: a systematic review[J]. Emerg Med Australas, 2014, 26(3): 223-228. DOI:10.1111/1742-6723.12232 |
| [6] | Drew B, Montgomery HR, Butler FK Jr. Tactical combat casualty care (TCCC) guidelines for medical personnel: 05 November 2020[J]. J Spec Oper Med, 2020, 20(4): 144-151. DOI:10.55460/RBRA-WMWV |
| [7] | Mutschler M, Nienaber U, Brockamp T, et al. A critical reappraisal of the ATLS classification of hypovolaemic shock: does it really reflect clinical reality?[J]. Resuscitation, 2013, 84(3): 309-313. DOI:10.1016/j.resuscitation.2012.07.012 |
| [8] | Bulger EM, Snyder D, Schoelles K, et al. An evidence-based prehospital guideline for external hemorrhage control: American College of Surgeons Committee on Trauma[J]. Prehosp Emerg Care, 2014, 18(2): 163-173. DOI:10.3109/10903127.2014.896962 |
| [9] | Van Waes OJ, Cheriex KC, Navsaria PH, et al. Management of penetrating neck injuries[J]. Br J Surg, 2012, 99(Suppl 1): 149-154. DOI:10.1002/bjs.7733 |
| [10] | Nowicki JL, Stew B, Ooi E. Penetrating neck injuries: a guide to evaluation and management[J]. Ann R Coll Surg Engl, 2018, 100(1): 6-11. DOI:10.1308/rcsbull.2018.6 |
| [11] | Eilertsen KA, Winberg M, Jeppesen E, et al. Prehospital tourniquets in civilians: a systematic review[J]. Prehosp Disaster Med, 2021, 36(1): 86-94. DOI:10.1017/S1049023X20001284 |
| [12] | Doyle GS, Taillac PP. Tourniquets: a review of current use with proposals for expanded prehospital use[J]. Prehosp Emerg Care, 2008, 12(2): 241-256. DOI:10.1080/10903120801907570 |
| [13] | Levy MJ, Pasley J, Remick KN, et al. Removal of the prehospital tourniquet in the emergency department[J]. J Emerg Med, 2021, 60(1): 98-102. DOI:10.1016/j.jemermed.2020.10.018 |
| [14] | Coccolini F, Stahel PF, Montori G, et al. Pelvic trauma: WSES classification and guidelines[J]. World J Emerg Surg, 2017, 12: 5. DOI:10.1186/s13017-017-0117-6 |
| [15] | Mayglothling J, Duane TM, Gibbs M, et al. Emergency tracheal intubation immediately following traumatic injury: an Eastern Association for the Surgery of Trauma practice management guideline[J]. J Trauma Acute Care Surg, 2012, 73(5 Suppl 4): S333-S340. DOI:10.1097/TA.0b013e31827018a5 |
| [16] | Page D, Ablordeppey E, Wessman BT, et al. Emergency department hyperoxia is associated with increased mortality in mechanically ventilated patients: a cohort study[J]. Crit Care, 2018, 22(1): 9. DOI:10.1186/s13054-017-1926-4 |
| [17] | Bernard SA, Nguyen V, Cameron P, et al. Prehospital rapid sequence intubation improves functional outcome for patients with severe traumatic brain injury: a randomized controlled trial[J]. Ann Surg, 2010, 252(6): 959-965. DOI:10.1097/SLA.0b013e3181efc15f |
| [18] | Derek K, Chu MD, et al. Mortality and morbidity in acutely ill adults treated with liberal versus conservative oxygen therapy (IOTA): a systematic review and meta-analysis[J]. Lancet, 2018, 391(10131): 1693-1705. DOI:10.1016/S0140-6736(18)30479-3 |
| [19] | Davis DP. Early ventilation in traumatic brain injury[J]. Resuscitation, 2008, 76(3): 333-340. DOI:10.1016/j.resuscitation.2007.08.004 |
| [20] | Ruelas OS, Tschautscher CF, Lohse CM, et al. Analysis of prehospital scene times and interventions on mortality outcomes in a national cohort of penetrating and blunt trauma patients[J]. Prehosp Emerg Care, 2018, 22(6): 691-697. DOI:10.1080/10903127.2018.1448494 |
| [21] | Nasser AAH, Nederpelt C, El Hechi M, et al. Every minute counts: the impact of pre-hospital response time and scene time on mortality of penetrating trauma patients[J]. Am J Surg, 2020, 220(1): 240-244. DOI:10.1016/j.amjsurg.2019.11.018 |
| [22] | Harmsen AM, Giannakopoulos GF, Moerbeek PR, et al. The influence of prehospital time on trauma patients outcome: a systematic review[J]. Injury, 2015, 46(4): 602-609. DOI:10.1016/j.injury.2015.01.008 |
| [23] | Caputo LM, Salottolo KM, Slone DS, et al. The relationship between patient volume and mortality in American trauma centres: a systematic review of the evidence[J]. Injury, 2014, 45(3): 478-486. DOI:10.1016/j.injury.2013.09.038 |
| [24] | Benz D, Balogh ZJ. Damage control surgery: current state and future directions[J]. Curr Opin Crit Care, 2017, 23(6): 491-497. DOI:10.1097/MCC.0000000000000465 |
| [25] | Ball CG. Damage control surgery[J]. Curr Opin Crit Care, 2015, 21(6): 538-543. DOI:10.1097/MCC.0000000000000252 |
| [26] | Roberts DJ, Bobrovitz N, Zygun DA, et al. Evidence for use of damage control surgery and damage control interventions in civilian trauma patients: a systematic review[J]. World J Emerg Surg, 2021, 16(1): 10. DOI:10.1186/s13017-021-00352-5 |
| [27] | Hagiwara A, Fukushima H, Murata A, et al. Blunt splenic injury: usefulness of transcatheter arterial embolization in patients with a transient response to fluid resuscitation[J]. Radiology, 2005, 235(1): 57-64. DOI:10.1148/radiol.2351031132 |
| [28] | Manzano Nunez R, Naranjo MP, Foianini E, et al. A meta-analysis of resuscitative endovascular balloon occlusion of the aorta (REBOA) or open aortic cross-clamping by resuscitative thoracotomy in non-compressible torso hemorrhage patients[J]. World J Emerg Surg, 2017, 12: 30. DOI:10.1186/s13017-017-0142-5 |
| [29] | Kinslow K, Shepherd A, McKenney M, et al. Resuscitative endovascular balloon occlusion of aorta: a systematic review[J]. Am Surg, 2022, 88(2): 289-296. DOI:10.1177/0003134820972985 |
| [30] | Jamal L, Saini, Quencer K, et al. Emerging approaches to pre-hospital hemorrhage control: a narrative review[J]. Ann Transl Med, 2021, 9(14): 1192. DOI:10.21037/atm-20-5452 |
| [31] | 张沂南, 叶雄俊, 闫伟, 等. 注射用白眉蛇毒血凝酶局部应用对泌尿外科腹腔镜手术: 创面止血效果的多中心研究[J]. 泌尿外科杂志(电子版), 2020, 12(3): 13-20. DOI:10.3969/j.issn.1674-7410.2020.03.003 |
| [32] | Toth L, King KL, McGrath B, et al. Efficacy and safety of emergency non-invasive pelvic ring stabilisation[J]. Injury, 2012, 43(8): 1330-1334. DOI:10.1016/j.injury.2012.05.014 |
| [33] | Tötterman A, Madsen JE, Skaga NO, et al. Extraperitoneal pelvic packing: a salvage procedure to control massive traumatic pelvic hemorrhage[J]. J Trauma, 2007, 62(4): 843-852. DOI:10.1097/01.ta.0000221673.98117.c9 |
| [34] | Matsumoto H, Hara Y, Yagi T, et al. Impact of urgent resuscitative surgery for life-threatening torso trauma[J]. Surg Today, 2017, 47(7): 827-835. DOI:10.1007/s00595-016-1451-0 |
| [35] | Thorson CM, van Haren RM, Ryan ML, et al. Admission hematocrit and transfusion requirements after trauma[J]. J Am Coll Surg, 2013, 216(1): 65-73. DOI:10.1016/j.jamcollsurg.2012.09.011 |
| [36] | Thorson CM, Ryan ML, van Haren RM, et al. Change in hematocrit during trauma assessment predicts bleeding even with ongoing fluid resuscitation[J]. Am Surg, 2013, 79(4): 398-406. |
| [37] | Kobayashi L, Coimbra R, Goes AMO Jr, et al. American Association for the Surgery of Trauma-World Society of Emergency Surgery guidelines on diagnosis and management of peripheral vascular injuries[J]. J Trauma Acute Care Surg, 2020, 89(6): 1183-1196. DOI:10.1097/TA.0000000000002967 |
| [38] | Mutschler M, Nienaber U, Brockamp T, et al. Renaissance of base deficit for the initial assessment of trauma patients: a base deficit-based classification for hypovolemic shock developed on data from 16, 305 patients derived from the TraumaRegister DGU®[J]. Crit Care, 2013, 17(2): R42. DOI:10.1186/cc12555 |
| [39] | Herbert HK, Dechert TA, Wolfe L, et al. Lactate in trauma: a poor predictor of mortality in the setting of alcohol ingestion[J]. Am Surg, 2011, 77(12): 1576-1579. |
| [40] | Mohamed M, Majeske K, Sachwani GR, et al. The impact of early thromboelastography directed therapy in trauma resuscitation[J]. Scand J Trauma Resusc Emerg Med, 2017, 25(1): 99. DOI:10.1186/s13049-017-0443-4 |
| [41] | Albert V, Subramanian A, Pati HP, et al. Efficacy of thromboelastography (TEG) in predicting acute trauma-induced coagulopathy (ATIC) in isolated severe traumatic brain injury (iSTBI)[J]. Indian J Hematol Blood Transfus, 2019, 35(2): 325-331. DOI:10.1007/s12288-018-1003-4 |
| [42] | Dixon AL, McCully BH, Rick EA, et al. Tranexamic acid administration in the field does not affect admission thromboelastography after traumatic brain injury[J]. J Trauma Acute Care Surg, 2020, 89(5): 900-907. DOI:10.1097/TA.0000000000002932 |
| [43] | Murao, Yamakawa K, Kabata D, et al. Effect of earlier door-to-CT and door-to-bleeding control in severe blunt trauma: a retrospective cohort study[J]. J Clin Med, 2021, 10(7): 1522. DOI:10.3390/jcm10071522 |
| [44] | Magyar CTJ, Maeder F, Diepers M, et al. Detailed information gain and therapeutic impact of whole body computed tomography supplementary to conventional radiological diagnostics in blunt trauma emergency treatment: a consecutive trauma centre evaluation[J]. Eur J Trauma Emerg Surg, 2022, 48(2): 921-931. DOI:10.1007/s00068-020-01502-1 |
| [45] | Do WS, Chang R, Fox EE, et al. Too fast, or not fast enough? The FAST exam in patients with non-compressible torso hemorrhage[J]. Am J Surg, 2019, 217(5): 882-886. DOI:10.1016/j.amjsurg.2019.02.012 |
| [46] | Moore CL, Copel JA. Point-of-care ultrasonography[J]. N Engl J Med, 2011, 364(8): 749-757. DOI:10.1056/NEJMra0909487 |
| [47] | Mercer CB, Ball M, Cash RE, et al. Ultrasound use in the prehospital setting for trauma: a systematic review[J]. Prehosp Emerg Care, 2021, 25(4): 566-582. DOI:10.1080/10903127.2020.1811815 |
| [48] | Barbar SD, Clere-Jehl R, Bourredjem A, et al. Timing of renal-replacement therapy in patients with acute kidney injury and Sepsis[J]. N Engl J Med, 2018, 379(15): 1431-1442. DOI:10.1056/NEJMoa1803213 |
| [49] | Samuels JM, Moore HB, Moore EE. Damage control resuscitation[J]. Chirurgia, 2017, 112(5): 514. DOI:10.21614/chirurgia.112.5.514 |
| [50] | Cole E, Weaver A, Gall L, et al. A decade of damage control resuscitation: new transfusion practice, new survivors, new directions[J]. Ann Surg, 2021, 273(6): 1215-1220. DOI:10.1097/SLA.0000000000003657 |
| [51] | Leibner E, Andreae M, Galvagno SM, et al. Damage control resuscitation[J]. Clin Exp Emerg Med, 2020, 7(1): 5-13. DOI:10.15441/ceem.19.089 |
| [52] | Abdelmalik PA, Draghic N, Ling GSF. Management of moderate and severe traumatic brain injury[J]. Transfusion, 2019, 59(s2): 1529-1538. DOI:10.1111/trf.15171 |
| [53] | Geeraerts T, Velly L, Abdennour L, et al. Management of severe traumatic brain injury (first 24hours)[J]. Anaesth Crit Care Pain Med, 2018, 37(2): 171-186. DOI:10.1016/j.accpm.2017.12.001 |
| [54] | Eastridge BJ, Holcomb JB, Shackelford S. Outcomes of traumatic hemorrhagic shock and the epidemiology of preventable death from injury[J]. Transfusion, 2019, 59(s2): 1423-1428. DOI:10.1111/trf.15161 |
| [55] | Siegemund M, Hollinger A, Gebhard EC, et al. The value of volume substitution in patients with septic and haemorrhagic shock with respect to the microcirculation[J]. Swiss Med Wkly, 2019, 149: w20007. DOI:10.4414/smw.2019.20007 |
| [56] | Hussmann B, Lefering R, Kauther MD, et al. Influence of prehospital volume replacement on outcome in polytraumatized children[J]. Crit Care, 2012, 16(5): R201. DOI:10.1186/cc11809 |
| [57] | Hussmann B, Lefering R, Waydhas C, et al. Does increased prehospital replacement volume lead to a poor clinical course and an increased mortality? A matched-pair analysis of 1896 patients of the Trauma Registry of the German Society for Trauma Surgery who were managed by an emergency doctor at the accident site[J]. Injury, 2013, 44(5): 611-617. DOI:10.1016/j.injury.2012.02.004 |
| [58] | Hussmann B, Schoeneberg C, Jungbluth P, et al. Enhanced prehospital volume therapy does not lead to improved outcomes in severely injured patients with severe traumatic brain injury[J]. BMC Emerg Med, 2019, 19(1): 1-9. DOI:10.1186/s12873-019-0221-x |
| [59] | 王坤, 杨萍芬, 严浩. 骨髓腔穿刺输液在院外创伤失血性休克患者抢救中的应用效果[J]. 中国急救复苏与灾害医学杂志, 2020(3): 288-290. DOI:10.3969/j.issn.1673-6966.2020.03.011 |
| [60] | Crowe E, DeSantis SM, Bonnette A, et al. Whole blood transfusion versus component therapy in trauma resuscitation: a systematic review and meta-analysis[J]. J Am Coll Emerg Physicians Open, 2020, 1(4): 633-641. DOI:10.1002/emp2.12089 |
| [61] | Crombie N, Doughty HA, Bishop JRB, et al. Resuscitation with blood products in patients with trauma-related haemorrhagic shock receiving prehospital care (RePHILL): a multicentre, open-label, randomised, controlled, phase 3 trial[J]. Lancet Haematol, 2022, 9(4): e250-e261. DOI:10.1016/S2352-3026(22)00040-0 |
| [62] | Sperry JL, Guyette FX, Brown JB, et al. Prehospital plasma during air medical transport in trauma patients at risk for hemorrhagic shock[J]. N Engl J Med, 2018, 379(4): 315-326. DOI:10.1056/NEJMoa1802345 |
| [63] | Hilbert-Carius P, Schwarzkopf D, Reinhart K, et al. Synthetic colloid resuscitation in severely injured patients: analysis of a nationwide trauma registry (TraumaRegister DGU)[J]. Sci Rep, 2018, 8(1): 11567. DOI:10.1038/s41598-018-30053-0 |
| [64] | Semler MW, Self WH, Wanderer JP, et al. Balanced crystalloids versus saline in critically ill adults[J]. N Engl J Med, 2018, 378(9): 829-839. DOI:10.1056/NEJMoa1711584 |
| [65] | Didwania A, Miller J, Kassel D, et al. Effect of intravenous lactated Ringer's solution infusion on the circulating lactate concentration: part 3. Results of a prospective, randomized, double-blind, placebo-controlled trial[J]. Crit Care Med, 1997, 25(11): 1851-1854. DOI:10.1097/00003246-199711000-00024 |
| [66] | Zitek T, Skaggs ZD, Rahbar A, et al. Does intravenous lactated ringer's solution raise serum lactate?[J]. J Emerg Med, 2018, 55(3): 313-318. DOI:10.1016/j.jemermed.2018.05.031 |
| [67] | Wang L, Lou JS, Cao JB, et al. Bicarbonate Ringer's solution for early resuscitation in hemorrhagic shock rabbits[J]. Ann Transl Med, 2021, 9(6): 462. DOI:10.21037/atm-21-97 |
| [68] | Rowell SE, Fair KA, Barbosa RR, et al. The impact of pre-hospital administration of lactated ringer's solution versus normal saline in patients with traumatic brain injury[J]. J Neurotrauma, 2016, 33(11): 1054-1059. DOI:10.1089/neu.2014.3478 |
| [69] | Zampieri FG, Machado FR, Biondi RS, et al. Effect of intravenous fluid treatment with a balanced solution vs 0.9% saline solution on mortality in critically ill patients: the BaSICS randomized clinical trial[J]. JAMA, 2021, 326(9): 1-12. DOI:10.1001/jama.2021.11684 |
| [70] | Foster JC, Sappenfield JW, Smith RS, et al. Initiation and termination of massive transfusion protocols: current strategies and future prospects[J]. Anesth Analg, 2017, 125(6): 2045-2055. DOI:10.1213/ANE.0000000000002436 |
| [71] | Callcut RA, Cripps MW, Nelson MF, et al. The Massive Transfusion Score as a decision aid for resuscitation: learning when to turn the massive transfusion protocol on and off[J]. J Trauma Acute Care Surg, 2016, 80(3): 450-456. DOI:10.1097/TA.0000000000000914 |
| [72] | Kheirbek T, Martin TJ, Cao J, et al. Prehospital shock index outperforms hypotension alone in predicting significant injury in trauma patients[J]. Trauma Surg Acute Care Open, 2021, 6(1): e000712. DOI:10.1136/tsaco-2021-000712 |
| [73] | Black JA, Pierce VS, Kerby JD, et al. The evolution of blood transfusion in the trauma patient: whole blood has come full circle[J]. Semin Thromb Hemost, 2020, 46(2): 215-220. DOI:10.1055/s-0039-3402426 |
| [74] | Holcomb JB, Tilley BC, Baraniuk S, et al. Transfusion of plasma, platelets, and red blood cells in a 1: 1: 1 vs a 1: 1: 2 ratio and mortality in patients with severe trauma: the PROPPR randomized clinical trial[J]. JAMA, 2015, 313(5): 471-482. DOI:10.1001/jama.2015.12 |
| [75] | Kelly JM, Callum JL, Rizoli SB. 1: 1: 1 - Warranted or wasteful? Even where appropriate, high ratio transfusion protocols are costly: early transition to individualized care benefits patients and transfusion services[J]. Expert Rev Hematol, 2013, 6(6): 631-633. DOI:10.1586/17474086.2013.859520 |
| [76] | Moore HB, Tessmer MT, Moore EE, et al. Forgot calcium? Admission ionized-calcium in two civilian randomized controlled trials of prehospital plasma for traumatic hemorrhagic shock[J]. J Trauma Acute Care Surg, 2020, 88(5): 588-596. DOI:10.1097/ta.0000000000002614 |
| [77] | Prat NJ, Meyer AD, Ingalls NK, et al. Rotational thromboelastometry significantly optimizes transfusion practices for damage control resuscitation in combat casualties[J]. J Trauma Acute Care Surg, 2017, 83(3): 373-380. DOI:10.1097/TA.0000000000001568 |
| [78] | Wikkelsø A, Wetterslev J, Møller AM, et al. Thromboelastography (TEG) or thromboelastometry (ROTEM) to monitor haemostatic treatment versus usual care in adults or children with bleeding[J]. Cochrane Database Syst Rev, 2016, 2016(8): CD007871. DOI:10.1002/14651858.CD007871.pub3 |
| [79] | McQuilten ZK, Crighton G, Brunskill S, et al. Optimal dose, timing and ratio of blood products in massive transfusion: results from a systematic review[J]. Transfus Med Rev, 2018, 32(1): 6-15. DOI:10.1016/j.tmrv.2017.06.003 |
| [80] | Aoki M, Abe T, Saitoh D, et al. Use of vasopressor increases the risk of mortality in traumatic hemorrhagic shock: a nationwide cohort study in Japan[J]. Crit Care Med, 2018, 46(12): e1145-e1151. DOI:10.1097/ccm.0000000000003428 |
| [81] | Sims CA, Holena D, Kim P, et al. Effect of low-dose supplementation of arginine vasopressin on need for blood product transfusions in patients with trauma and hemorrhagic shock: a randomized clinical trial[J]. JAMA Surg, 2019, 154(11): 994-1003. DOI:10.1001/jamasurg.2019.2884 |
| [82] | Spahn DR, Bouillon B, Cerny V, et al. The European guideline on management of major bleeding and coagulopathy following trauma: fifth edition[J]. Crit Care, 2019, 23(1): 98. DOI:10.1186/s13054-019-2347-3 |
| [83] | Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis campaign: international guidelines for management of Sepsis and septic shock: 2016[J]. Crit Care Med, 2017, 45(3): 486-552. DOI:10.1097/CCM.0000000000002255 |
| [84] | Kutcher ME, Howard BM, Sperry JL, et al. Evolving beyond the vicious triad: differential mediation of traumatic coagulopathy by injury, shock, and resuscitation[J]. J Trauma Acute Care Surg, 2015, 78(3): 516-523. DOI:10.1097/TA.0000000000000545 |
| [85] | Prevaldi C, Paolillo C, Locatelli C, et al. Management of traumatic wounds in the Emergency Department: position paper from the Academy of Emergency Medicine and Care (AcEMC) and the World Society of Emergency Surgery (WSES)[J]. World J Emerg Surg, 2016, 11: 30. DOI:10.1186/s13017-016-0084-3 |
| [86] | Schauer SG, Naylor JF, Maddry JK, et al. Trends in prehospital analgesia administration by US forces from 2007 through 2016[J]. Prehosp Emerg Care, 2019, 23(2): 271-276. DOI:10.1080/10903127.2018.1489022 |
| [87] | Moore HB, Gando S, Iba T, et al. Defining trauma-induced coagulopathy with respect to future implications for patient management: communication from the SSC of the ISTH[J]. J Thromb Haemost, 2020, 18(3): 740-747. DOI:10.1111/jth.14690 |
| [88] | Moore HB, Walsh M, Kwaan HC, et al. The complexity of trauma-induced coagulopathy[J]. Semin Thromb Hemost, 2020, 46(2): 114-115. DOI:10.1055/s-0040-1702202 |
| [89] | Moore EE, Moore HB, Kornblith LZ, et al. Trauma-induced coagulopathy[J]. Nat Rev Dis Primers, 2021, 7(1): 30. DOI:10.1038/s41572-021-00264-3 |
| [90] | Duque P, Calvo A, Lockie C, et al. Pathophysiology of trauma-induced coagulopathy[J]. Transfus Med Rev, 2021, 35(4): 80-86. DOI:10.1016/j.tmrv.2021.07.004 |
| [91] | Petros S. Trauma-induced coagulopathy[J]. Hamostaseologie, 2019, 39(1): 20-27. DOI:10.1055/s-0039-1677853 |
| [92] | CRASH- trial collaborators, Shakur H, Roberts I, et al. Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): a randomised, placebo-controlled trial[J]. Lancet, 2010, 376(9734): 23-32. DOI:10.1016/S0140-6736(10)60835-5 |
| [93] | CRASH-trial collaborators. Effects of tranexamic acid on death, disability, vascular occlusive events and other morbidities in patients with acute traumatic brain injury (CRASH-3): a randomised, placebo-controlled trial[J]. Lancet, 2019, 394(10210): 1713-1723. DOI:10.1016/S0140-6736(19)32233-0 |
| [94] | Moore EE, Moore HB, Gonzalez E, et al. Rationale for the selective administration of tranexamic acid to inhibit fibrinolysis in the severely injured patient[J]. Transfusion, 2016, 56(Suppl 2): S110-S114. DOI:10.1111/trf.13486 |
| [95] | Zhang P, Lv H, Qi X, et al. Effect of ulinastatin on post-operative blood loss and allogeneic transfusion in patients receiving cardiac surgery with cardiopulmonary bypass: a prospective randomized controlled study with 10-year follow-up[J]. J Cardiothorac Surg, 2020, 15(1): 98. DOI:10.1186/s13019-020-01144-9 |
| [96] | Moore HB, Moore EE. Temporal changes in fibrinolysis following injury[J]. Semin Thromb Hemost, 2020, 46(2): 189-198. DOI:10.1055/s-0039-1701016 |
| [97] | Coleman JR, Kay AB, Moore EE, et al. It's sooner than You think: blunt solid organ injury patients are already hypercoagulable upon hospital admission - Results of a bi-institutional, prospective study[J]. Am J Surg, 2019, 218(6): 1065-1073. DOI:10.1016/j.amjsurg.2019.08.024 |
 2023, Vol. 32
2023, Vol. 32


