重症监护室(intensive care unit, ICU)是收治急危重症患者的主要场所,大部分进入ICU的患者都存在不同程度的低氧血症,病情较重的患者同时存在急性呼吸衰竭、急性呼吸窘迫综合征或外伤、其他疾病引起的呼吸功能障碍,严重时将危及生命。因此,急危重症患者早期辅助呼吸,维持血氧饱和度等一线治疗措施极其重要。目前重症监护室用于辅助呼吸的治疗措施主要包括鼻导管及面罩吸氧、经鼻高流量氧疗(high-flow oxygen through nasal cannula, HFNC)和无创或有创机械通气(mechanical ventilation)。对于不需要立即行机械通的患者,常规吸氧气治疗有明显的缺点,许多患者由于加热和湿化不足,导致对面罩吸氧或鼻导管吸氧的容忍度降低[1], 而经鼻高流量氧疗使空气与氧气混合,提供充分加热和湿化的气体流量高达60 L/min,降低了患者的呼吸频率和呼吸做功,减少对呼吸支持的需求,近年来作为危重患者的一种替代呼吸支持手段,一直受到关注。HFNC已经成为一种新型、有效的早期治疗呼吸衰竭与各种潜在疾病的模式[2]。一项纳入38例患者的前瞻性单中心研究也表明患者使用HFNC后呼吸频率、心率、呼吸困难评分降低,血氧饱和度增加,而院内获得性肺炎发生率也显著降低[3]。但并不是所有低氧血症患者都应首先考虑HFNC治疗,目前机械通气仍是住院患者中常用的抢救工具。由于各种病因接受机械通气的患者数量正在增加,机械通气包括气管内插管通气和经口插管通气,作为机械呼吸的输送管道,气管插管还可以保护气道,通过管道抽吸分泌物,并允许进行包括支气管镜检查在内的操作及治疗手段。机械通气有助于稳定低氧血症和高碳酸血症患者的呼吸衰竭,减少吸气做功,促进休克患者血流重分配[4]。对于ICU患者是否优先使用经鼻高流量氧疗,或何时应将HFNC治疗转换为机械通气还存在争议,虽然高流量氧疗可以为低氧血症患者提供一种替代方案[5],有极高的临床获益性,但由于大部分重症患者病情不稳定导致治疗手段不断变换,过分依赖HFNC会延误患者行机械通气等进一步治疗,导致病情恶化。因此何时使用不同的辅助呼吸设备也亟待预测,因此本文通过研究本院经鼻高流量氧疗患者来预测更换为机械通气的风险概率,为临床医生提供一种简单、有效的预测模型,提高患者的预后生存。
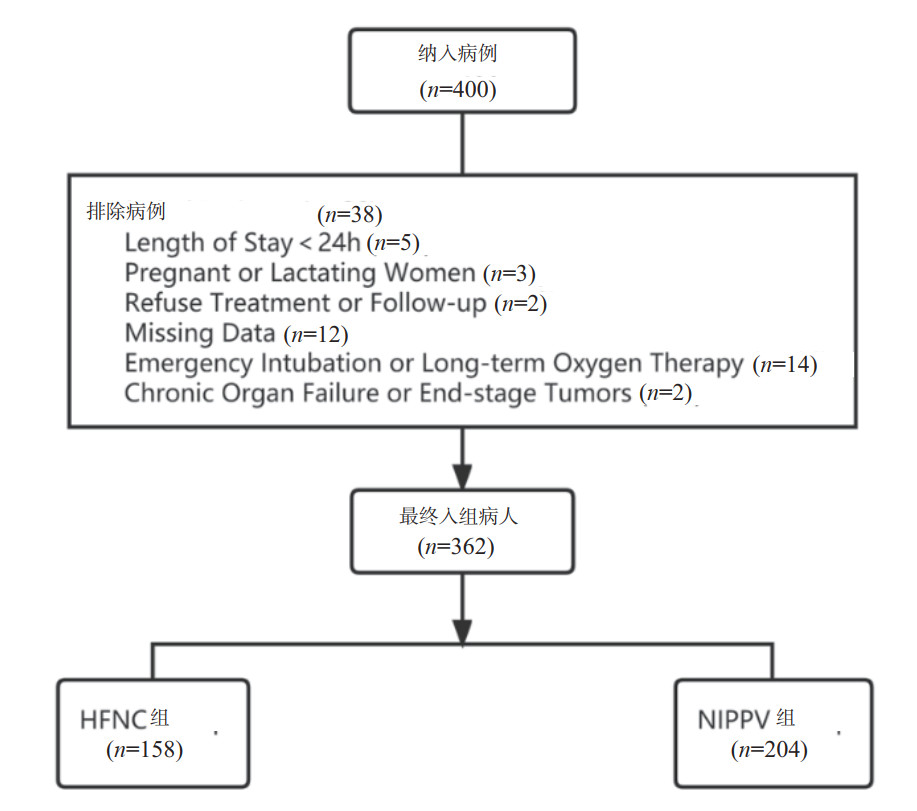
1 资料与方法 1.1 一般资料收集2019年1月至2021年12月兰州大学第二医院重症医学科收治的362例行经鼻高流量氧疗的患者进行回顾性分析,纳入流程(见图 1)。记录患者从入院到出院前是否行无创正压机械通气为主要结局指标,根据机械通气与否将患者分为经鼻高流量氧疗组(HFNC组)及氧疗失败行机械通气组(NIPPV组)插管时间点不纳入统计分析,凡是符合机械通气适应证并行插管治疗患者均纳入NIPPV组。次要结局指标为ICU住院时长与总住院时长。
|
| 图 1 患者纳入流程图 Fig 1 Patients inclusion flow chart |
|
|
纳入标准:①年龄≥18岁;②氧合指数(PaO2/ FiO2) < 300 mmHg的低氧血症的患者;③入院24 h之内开始使用经鼻高流量氧疗的患者;④住院时间≥24 h。排除标准:①年龄<18岁;②行高流量氧疗前急诊气管插管或气管切开术后或长期接受家庭氧疗患者;③各项指标不完善、拒绝治疗或随访的患者;④有慢性器官衰竭或恶性肿瘤终末期的患者;⑤妊娠期或哺乳期妇女;⑥入院时间<24 h或自动出院患者;⑦氧合指数(PaO2/ FiO2)≥300 mmHg。本研究符合医学伦理学标准,并经本院伦理委员会批准(伦理号:2022A-190)。
1.3 研究方法收集患者一般资料(性别和年龄),临床数据[(入院24 h内的生命体征、急性生理学及慢性健康状况评分(acute physiology and chronic health evaluationⅡ, APACHEⅡ)、血气指标、炎症指标、急性合并症、实验室检查结果及住院时长等)]。血气指标包括(pH、PO2、PCO2、Lac、AG);计算ROX指数;实验室检查包括炎症指标[降钙素原(procalcitonin, PCT)、C反应蛋白(C-reaction protein, CRP)、白细胞计数(white blood cell, WBC)、中性粒细胞比率(neutrophilic granulocyte, NE%)];生化指标包括(K+、Ca2+、Glu);合并症包括[急性呼吸衰竭、心力衰竭、肾衰竭、脑水肿、弥散性血管内凝血(disseminated intravascular coagulation, DIC)、多器官功能障碍综合征(multiple organ dysfunction syndrome, MODS)、消化道出血及肝衰竭]。所有生理生化指标纳入入院24 h内首次测量值进行分析。
1.4 统计学方法采用SPSS 25.0软件进行数据分析。患者分为HFNC组(n=158)及NIPPV组(n=204),将两组人群进行统计分析,正态分布的计量资料以(x±s)表示,两组间比较采用两独立样本t检验;偏态分布的计量资料以M(Q1,Q3)表示,两组间比较采用Mann Whitney U检验;计数资料以百分数表示,两组间比较采用χ2检验;通过单因素及多因素分析探讨影响患者是否需行机械通气的独立危险因素,使用GraphPad Prism 8绘制二元Logistic回归分析可视化图,并建立Logistic模型公式。采用R软件(版本4.1.3)中的car、rms、pROC、DecisionCurve等安装包对列线图进行构建及验证,计算C-index,绘制各个指标及预测模型的ROC曲线、校准曲线与DCA进行模型的预测效能及价值的评估。以P<0.05差异为有统计学意义。
2 结果 2.1 HFNC组与NIPPV组临床特征的比较本研究最终纳入了362例患者,其中HFNC组纳入158例患者,NIPPV组纳入204例患者(如图 1)。通过比较,两组患者的性别、年龄、基本生命体征、大部分血气指标与合并症之间的差异无统计学意义(P>0.05);而两组患者APACHE Ⅱ评分、ROX指数、AG、血糖、PCT、WBC、两组间是否合并急性呼吸衰竭及ICU和总住院时间之间的差异有统计学意义(P<0.05)。其中NIPPV组患者中合并急性呼吸衰竭人数、ICU和总住院时间、APACHE Ⅱ评分、PCT和WBC值均高于HFNC组;而ROX指数比HFNC组低(见表 1)。
| 一般特征 | HFNC组(n=158) | NIPPV组(n=204) | P值 |
| 性别(男/女) | 101/57 | 143/61 | 0.214 |
| 年龄(岁)a | 64(49, 74) | 58(46, 72) | 0.187 |
| 生命体征 | |||
| 体温(℃)a | 36.7(36.4, 37.1) | 36.6(36.3, 37.2) | 0.651 |
| 心率(次/min)b | 97±25 | 103±24 | 0.058 |
| APACHE Ⅱ评分a | 16(13, 21) | 35(30, 41) | <0.001 |
| 血气指标a | |||
| pH | 7.41(7.34, 7.47) | 7.41(7.35, 7.47) | 0.594 |
| PO2(mmHg) | 63(52, 77) | 68(53, 84) | 0.238 |
| PCO2(mmHg) | 39(32, 49) | 38(33, 46) | 0.620 |
| Lac(mmol/L) | 1.7(1.1, 3.2) | 2.3(1.2, 4.0) | 0.053 |
| AG(mmol/L) | 14.8(9.7,23.2) | 12.7(7.45,18.48) | 0.015 |
| ROX指数 | 8.62(5.96,10.29) | 4.30(3.80, 10.52) | 0.000 |
| 生化指标 | |||
| K+(mmol/L)b | 3.85±0.55 | 3.89(3.38,4.30) | 0.752 |
| Ca2+(mmol/L)a | 2.02(1.07, 2.28) | 1.94(1.07,2.29) | 0.701 |
| GLu(mmol/L)a | 6.96(5.70, 9.01) | 7.75(6.10, 10.33) | 0.009 |
| 炎症指标a | |||
| PCT(ng/ml) | 0.73(0.19, 3.23) | 1.15(0.44, 7.20) | 0.005 |
| CRP(mg/L) | 39.97(3.13, 124.76) | 33.86(2.25, 132.67) | 0.454 |
| WBC(×109/L) | 9.56(6.57, 13.23) | 10.63(7.56, 15.95) | 0.021 |
| NE% | 0.87(0.79, 0.91) | 0.87(0.83, 0.91) | 0.096 |
| 合并症(例,%) | |||
| 呼吸衰竭 | 83(52.5) | 138(67.6) | 0.003 |
| 心力衰竭 | 65(41.1) | 64(31.3) | 0.054 |
| 肾衰竭 | 35(22.1) | 59(28.9) | 0.145 |
| 脑水肿 | 12(7.5) | 15(7.3) | 0.931 |
| DIC | 5(3.1) | 10(4.9) | 0.411 |
| MODS | 17(10.7) | 26(12.7) | 0.563 |
| 消化道出血 | 9(5.6) | 18(8.8) | 0.261 |
| 肝衰竭 | 34(21.5) | 51(25.0) | 0.438 |
| ICU住院时间(d)a | 6(4, 10) | 10(6, 19) | <0.001 |
| 总住院时间(d)a | 10(5, 16) | 17(9, 27) | <0.001 |
| 注:a为M(Q1,Q3),b为x±s | |||
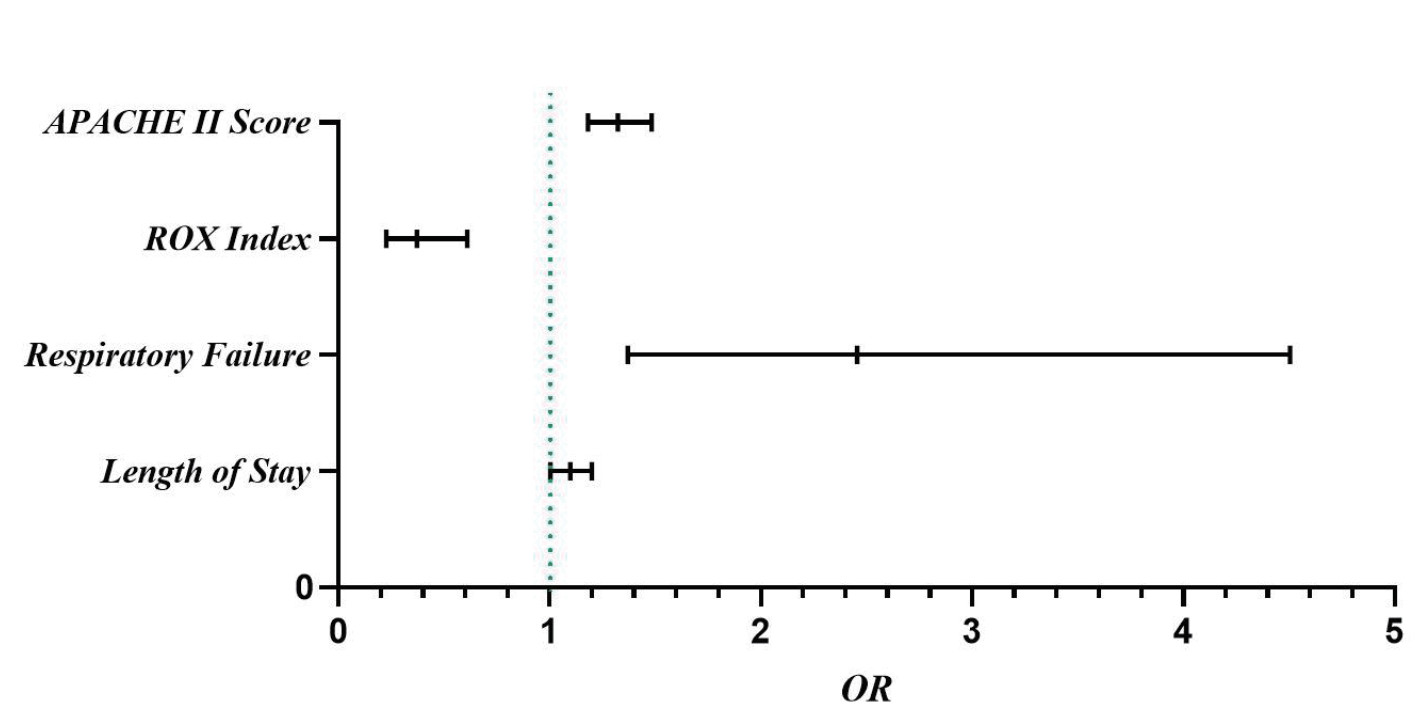
将纳入的362例患者进行单因素分析后得到影响因素进行二元Logistic回归分析,以患者最终是否行机械通气为因变量(进行机械通气:Y=1,未行机械通气:Y=0),将两组间单因素分析中有意义的指标作为自变量,进行多因素回归分析。结果表明,APACHE Ⅱ评分(OR=1.323, 95%CI: 1.818~1.483)、ROX指数(OR=0.371, 95%CI: 0.226~0.609)、总住院时长(OR=1.097, 95%CI: 1.003~1.200)及合并急性呼吸衰竭(OR=2.456, 95%CI: 1.368~4.506)是经鼻高流量氧疗患者最终改行机械通气的独立危险因素(如图 2),将以上4项指标进行数学分析建立Logistic模型公式,如下所示:
|
| 图 2 二元Logistic回归分析可视化图 Fig 2 Visualization of binary Logistic regression analysis |
|
|
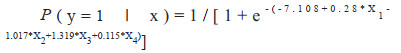
|
(注:X1:APACHEⅡ评分,X2:ROX指数,X3:是否合并呼吸衰竭,X4:住院时长)
通过带入X1~X4对应的数值可大致估算患者的风险概率。
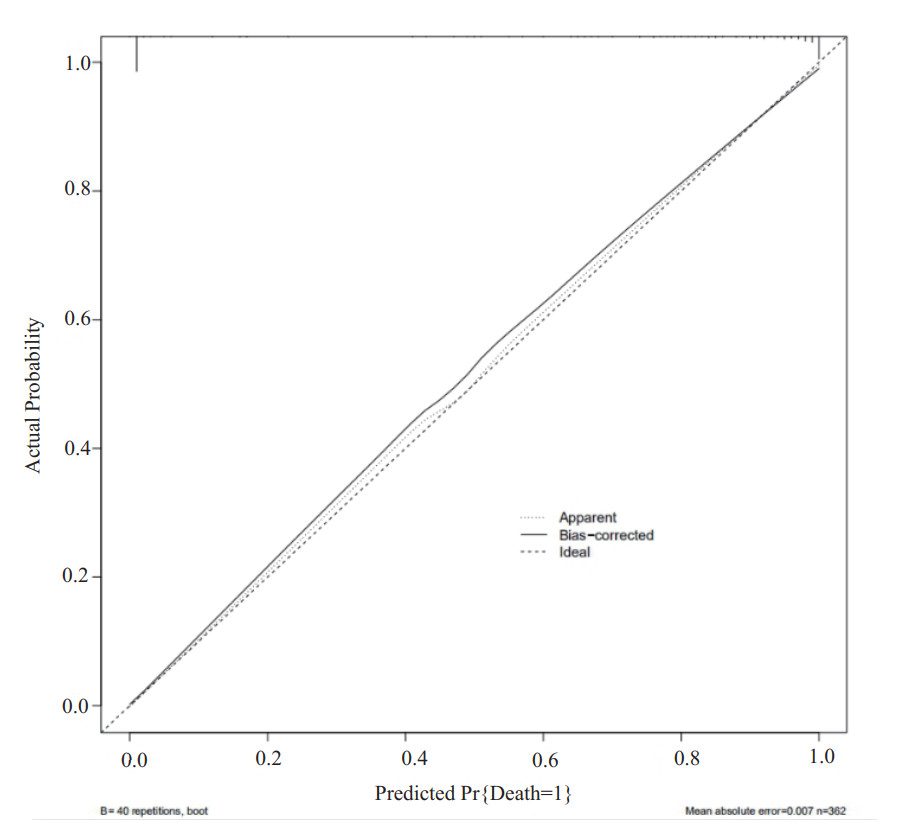
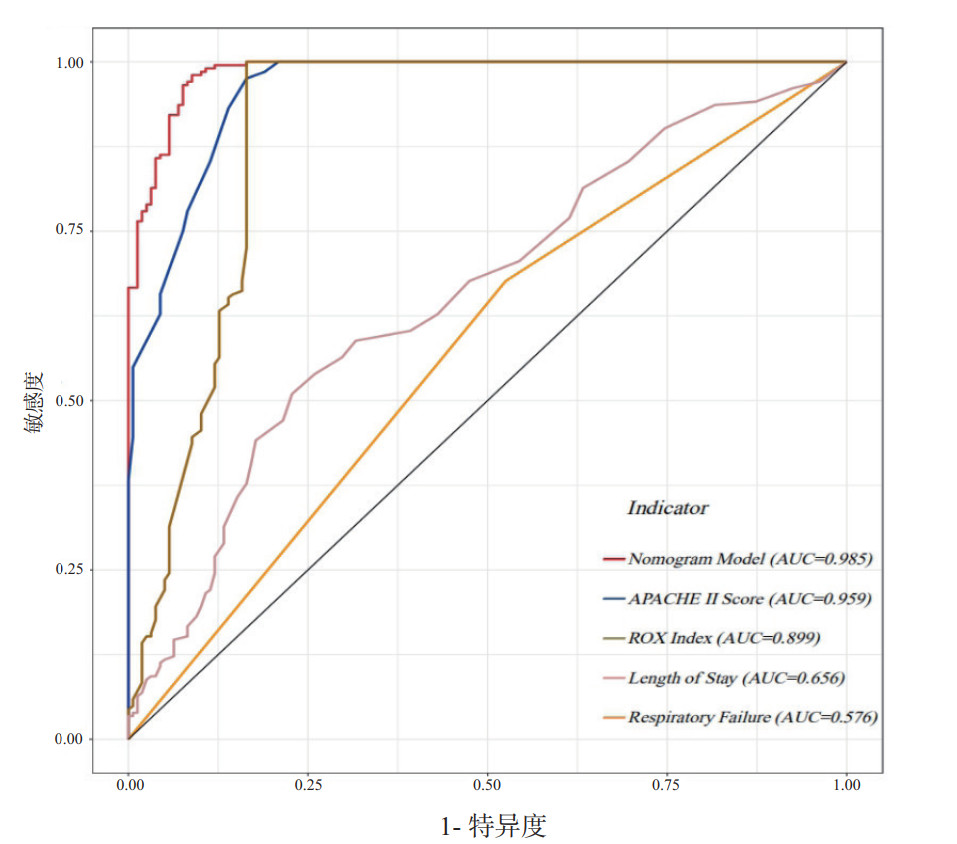
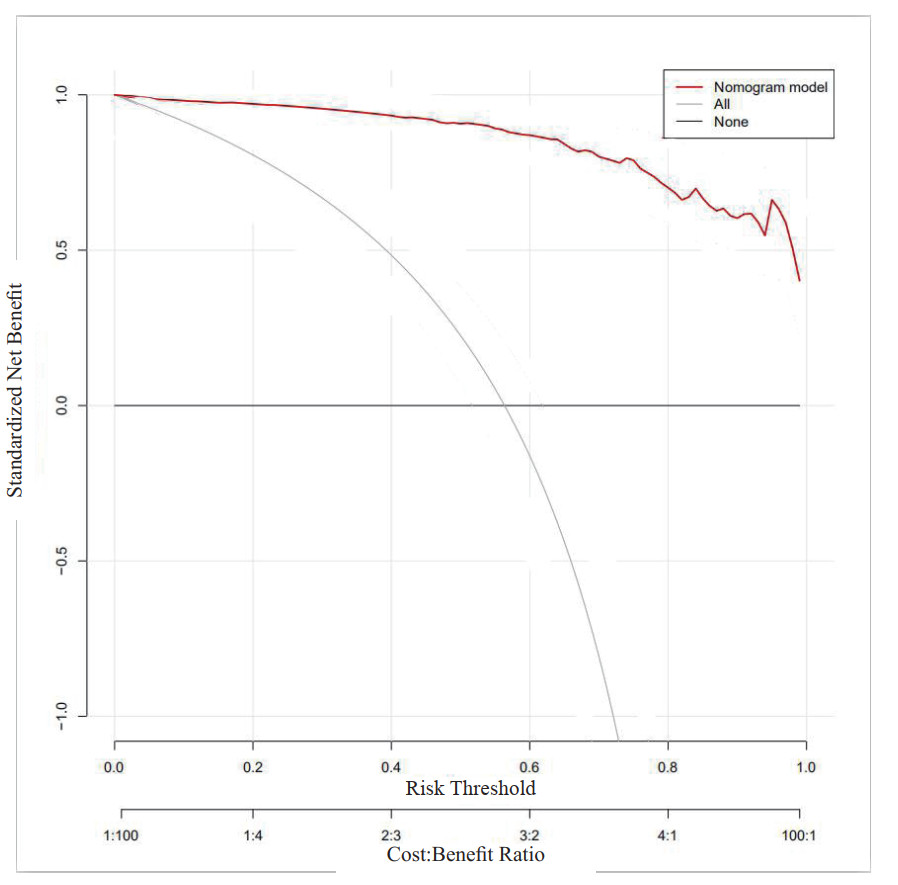
2.3 预测HFNC患者机械通气风险概率列线图的建立与验证将多因素分析筛选出的全部独立影响因素纳入到预测模型中,使用R软件建立预测模型(见图 3),图中从上到下对应的指标分别为单项得分、APACHE Ⅱ评分分值、ROX指数、呼吸衰竭、总住院时长、总分、风险概率。每一项后面对应一条标尺,标尺上对应相应数值,将患者对应指标相应的分值相加便可大致观测到患者行机械通气的概率。利用Bootstrap法对模型进行内部验证,结果显示该预测模型的C-index为0.985,表明该模型的预测效能较好;绘制模型的校准曲线(图 4),其中X轴代表预测的风险概率,Y轴代表实际的风险概率,图中可见预测曲线贴近于对角线,实际曲线与理想曲线拟合较好,表明预测概率与实测值基本一致;绘制各个独立指标与模型的ROC曲线,并计算曲线下面积AUC(图 5),由图可知,列线图、APACHEⅡ评分、ROX指数、总住院时长及是否合并急性呼吸衰竭的曲线下面积分别为0.985、0.959、0.899、0.656和0.576,表明该预测模型与单独指标相比其预测准确性更高;最后将该模型进行决策曲线分析,计算模型的临床价值及其对实际决策的影响,y轴表示计算出的收益,x轴是取不同的概率的Pt,即成本收益比。如图所示,除了红色波浪线外,还有一条灰色曲线和灰色实线,它们代表两种极端情况。灰色实线表示所有样本都是阴性(Pi < Pt),所有人都没干预,净获益为0。斜的虚线表示所有样本都是阳性,所有人都接受了干预,净获益是个斜率为负值的反斜线,其他的曲线就与它们相比较。红色波浪线离两线交叉点越远表明临床获益越大,由图可见该预测模型有较大的临床获益[6-7](见图 6)。

|
| 图 3 预测ICU经鼻高流量氧疗患者机械通气风险的列线图 Fig 3 Nomogram graph for predicting the risk of NIPPV in ICU patients undergoing HFNC therapy |
|
|
|
| 图 4 预测模型的校准曲线图 Fig 4 Calibration curves of the prediction model |
|
|
|
| 图 5 预测模型与不同独立影响因素的ROC曲线分析 Fig 5 ROC curve analysis of prediction model and different independent influencing factors |
|
|
|
| 图 6 预测模型的决策曲线分析 Fig 6 Analysis of the decision curve of the prediction model |
|
|
低氧血症、呼吸功能障碍目前仍是急危重症监护患者存在的主要问题,传统鼻导管吸氧及面罩吸氧对急危重症患者效果不显著,而高流量氧疗通过鼻插管将加热和湿化的氧气输送到鼻腔,这些高流速的气体在上呼吸道产生低水平的正压,通过从上呼吸道冲洗呼出的二氧化碳来减少生理死腔,降低呼吸做功。而吸入氧气的比例(FiO2%)可以通过改变驱动气体中氧气的比例来调节[8-10]。近年来HFNC被用于临床辅助患者呼吸,改善氧合上取得了显著的效果,并有研究表明在不同病因导致的呼吸衰竭患者中使用高流量氧疗,比通过面罩吸氧或鼻导管吸氧更舒适和有效[11]。并且一项回顾性研究表明使用经鼻高流量氧疗在冠状病毒疾病引起的呼吸功能障碍患者中与较低的有创机械通气率相关[12]。有关的荟萃分析也显示与常规氧疗法(COT)或无创机械通气(NIV)相比,HFNC降低了气管插管率、机械通气率和呼吸支持设备的更换[13]。尤其对危重患者而言,鼻腔湿化高流量氧疗也有显著的益处[14]。然而在疾病发展过程中,往往因为抢救患者而不得不使用机械通气改善氧合,HFNC在一线抢救中存在些许不足之处,为了及时识别患者病情,早期做好机械通气抢救措施,需要构建一个预测模型帮助临床工作者早期做好插管准备。而本实验通过分析研究本院重症监护室362例使用经鼻高流量氧疗患者的基本资料、临床特征及实验室指标,最终纳入APACHE Ⅱ评分、ROX指数、总住院时长及是否合并急性呼吸衰竭四个独立指标用于构建列线图。
急性生理学和慢性健康评分(APACHEⅡ)在构建模型中占有较大权重,APACHEⅡ评分目前已在重症监护室得到广泛应用,并且已经应用了30多年[15-16]。APACHEⅡ评分系统包括12分的急性生理评分、年龄评分和慢性健康评估,这些在大多数急诊及重症监护室都很容易获得。此外,该评分计算简单、便捷,可以促进急诊分诊系统和危重症患者的指导治疗选择,是急危重症科常用的评估患者病情及判断预后的方法[17]。一项前瞻性实验表明在在重症监护室APACHE Ⅱ≤ 20分的患者中,所有患者均获得了成功的辅助通气治疗,而APACHEⅡ>20分的患者最终行机械通气的概率增加[18]。另有研究比较和分析了不同APACHEⅡ分值患者在使用高流量氧疗与机械通气治疗急性呼吸衰竭和低氧血症的疗效。APACHEⅡ评分<24分的急性呼吸衰竭患者,使用经鼻高流量氧疗和无创正压通气在预防呼吸衰竭方面差异无统计学意义。然而,使用HFNC的患者较使用NIPPV的患者腹胀的发生率降低[19]。本实验也显示APACHEⅡ评分越高,患者的单项得分也越高,对应的机械通气风险比率越大。
ROX指数即呼吸频率-氧合指数(SpO2 /FiO2与呼吸频率的比值)作为判断HFNC成功的早期预测指标之一,分值越低表明插管的风险较高。近期相关研究[20-21]开发和验证了ROX指数,以预测HFNC治疗在肺炎相关急性呼吸衰竭患者在开始治疗后24 h内是否成功,其结果表明ROX指数在开始行经HFNC后第2、6和12小时可用于预测HFNC治疗成功的拔管患者。故ROX指数被提出来指导使用HFNC时何时给予气管插管[22]。目前无创正压通气和高流量吸氧仍是ICU呼吸衰竭患者在有创通气前的两种呼吸支持的方式。研究表明两者的气管插管率没有差别,但HFNC组的90 d病死率低于NIPPV组。近年来,HFNC的应用越来越多,而若因HFNC使用导致延迟插管,则会增加患者的病死率。
随着住院时间的延长,ICU患者极易发生院内感染,尤其是老龄化趋势,使越来越多的老年人、免疫抑制的ICU患者病情更加复杂,导致院内感染的整体负担和复杂性增多,使患者的病情加重,增加医疗负担[23]。美国麻醉科重症监护室一项进行了3年的回顾性研究阐明ICU患者住院时间越长,其医院感染发生率越高,使用辅助呼吸设备的可能性越大,但可以通过感染控制措施使与设备有关的感染率降低[24]。
由各种原因导致的引起的低氧血症甚至呼吸功能衰竭一直是急诊及重症监护病房患者面临的主要临床挑战。大多数ICU患者都会发展为急性呼吸衰竭,甚至急性呼吸窘迫综合征(ARDS),导致快速进行性呼吸困难、呼吸急促和低氧血症,以及无法解释心力衰竭或液体超负荷引起的呼吸衰竭。其病因是由于肺部或肺外损伤导致炎症介质的释放,促进肺泡和微循环中炎症细胞的积聚。炎症细胞损伤血管内皮和肺泡上皮,导致肺水肿,肺透明膜形成,肺顺应性降低,气体交换减少。大多数病例与重症肺炎或脓毒症有关[25]。急性呼吸衰竭是重症监护病房住院患者的十分之一,机械通气的四分之一。严重患者的住院病死率为46% ~60%。因此早期支持性的治疗十分必要,包括机械通气、预防应激性溃疡和静脉血栓栓塞、营养支持和基础损伤的治疗,密切监测患者生命体征,积极预测患者预后[26]。
本研究通过单因素及多因素分析得出影响重症监护室经鼻高流量氧疗患者最终行机械通气的4个独立危险因素(APACHEⅡ评分、ROX指数、总住院时长、急性呼吸衰竭),并通过将以上因素联合构建列线图得出用来预测风险概率的模型,经过内部验证计算C-index为0.985、绘制校准曲线,显示了预测模型与实际观测的结果拟合较好,通过ROC曲线与DCA曲线,也显示出了模型同其他独立指标相比更具准确度与有效性,并且该模型具有一定的临床获益性。
本实验建立的预测重症监护室经鼻高流量氧疗患者机械通气风险概率的列线图具有较高的预测效能,有助于临床医生评估患者病情并给予合理恰当的治疗措施,改善患者愈后。但本研究存在一定的不足之处:首先,纳入的数据仅为本院重症医学科使用HFNC的患者,数据样本相对较少,且为单中心回顾性研究,因此得出的结论有一定的局限性;其次,本研究仅对于患者住院期间是否行机械通气作为结局事件进行分析,未做远期随访,对患者生存结局预测缺乏数据支撑;第三,鉴于两组患者用药情况及辅助治疗分析复杂、困难,也未作为预测指标纳入影响因素分析中,因此所建模型较为粗略,只可作为入住ICU初期的一个基础预测方法;最后,该预测模型经过内部验证后虽显示出良好的预测效能及准确性,但未进行外部验证来评估模型的适用性及可靠性,存在一定的缺陷。综上,为证实本实验构建的列线图的临床价值,为临床医生提供准确可靠、简单易行的预测方法,还需要进一步开展样本量大,设计严谨的前瞻性研究及外部验证来进一步完善该实验,得到更有价值的预测模型。
利益冲突 所有作者声明无利益冲突
作者贡献声明 种萌:设计实验、数据收集,统计分析;牛亚芳,马鑫:数据收集、文献查询;马莉:论文修改
| [1] | Luo MS, Huang GJ, Wu L. High flow nasal cannula compared with conventional oxygen therapy for acute hypoxemic respiratory failure[J]. Intensive Care Med, 2019, 45(8): 1167-1168. DOI:10.1007/s00134-019-05652-8 |
| [2] | Nishimura M. High-flow nasal cannula oxygen therapy in adults: physiological benefits, indication, clinical benefits, and adverse effects[J]. Respir Care, 2016, 61(4): 529-541. DOI:10.4187/respcare.04577 |
| [3] | Sztrymf B, Messika J, Bertrand F, et al. Beneficial effects of humidified high flow nasal oxygen in critical care patients: a prospective pilot study[J]. Intensive Care Med, 2011, 37(11): 1780. DOI:10.1007/s00134-011-2354-6 |
| [4] | Walter JM, Corbridge TC, Singer BD. Invasive mechanical ventilation[J]. South Med J, 2018, 111(12): 746-753. DOI:10.14423/SMJ.0000000000000905 |
| [5] | Frat JP, Thille AW, Mercat A, et al. High-flow oxygen through nasal cannula in acute hypoxemic respiratory failure[J]. N Engl J Med, 2015, 372(23): 2185-2196. DOI:10.1056/NEJMoa1503326 |
| [6] | Rousson V, Zumbrunn T. Decision curve analysis revisited: overall net benefit, relationships to ROC curve analysis, and application to case-control studies[J]. BMC Med Inform Decis Mak, 2011, 11: 45. DOI:10.1186/1472-6947-11-45 |
| [7] | Kerr KF, Brown MD, Zhu KH, et al. Assessing the clinical impact of risk prediction models with decision curves: guidance for correct interpretation and appropriate use[J]. J Clin Oncol, 2016, 34(21): 2534-2540. DOI:10.1200/JCO.2015.65.5654 |
| [8] | Chanques G, Riboulet F, Molinari N, et al. Comparison of three high flow oxygen therapy delivery devices: a clinical physiological cross-over study[J]. Minerva Anestesiol, 2013, 79(12): 1344-1355. |
| [9] | Corley A, Caruana LR, Barnett AG, et al. Oxygen delivery through high-flow nasal cannulae increase end-expiratory lung volume and reduce respiratory rate in post-cardiac surgical patients[J]. Br J Anaesth, 2011, 107(6): 998-1004. DOI:10.1093/bja/aer265 |
| [10] | Parke RL, Eccleston ML, McGuinness SP. The effects of flow on airway pressure during nasal high-flow oxygen therapy[J]. Respir Care, 2011, 56(8): 1151-1155. DOI:10.4187/respcare.01106 |
| [11] | Pham TMT, O'Malley L, Mayfield S, et al. The effect of high flow nasal cannula therapy on the work of breathing in infants with bronchiolitis[J]. Pediatr Pulmonol, 2015, 50(7): 713-720. DOI:10.1002/ppul.23060 |
| [12] | Bonnet N, Martin O, Boubaya M, et al. High flow nasal oxygen therapy to avoid invasive mechanical ventilation in SARS-CoV-2 pneumonia: a retrospective study[J]. Ann Intensive Care, 2021, 11(1): 37. DOI:10.1186/s13613-021-00825-5 |
| [13] | Zhao HY, Wang HX, Sun F, et al. High-flow nasal cannula oxygen therapy is superior to conventional oxygen therapy but not to noninvasive mechanical ventilation on intubation rate: a systematic review and meta-analysis[J]. Crit Care, 2017, 21(1): 184. DOI:10.1186/s13054-017-1760-8 |
| [14] | Cuquemelle E, Pham T, Papon JF, et al. Heated and humidified high-flow oxygen therapy reduces discomfort during hypoxemic respiratory failure[J]. Respir Care, 2012, 57(10): 1571-1577. DOI:10.4187/respcare.01681 |
| [15] | Knaus WA, Draper EA, Wagner DP, et al. APACHE Ⅱ: a severity of disease classification system[J]. Crit Care Med, 1985, 13(10): 818-829. DOI:10.1097/00003246-198510000-00009 |
| [16] | Huang NC, Lin SL, Hung YM, et al. Severity assessment in acute paraquat poisoning by analysis of APACHE Ⅱ score[J]. J Formos Med Assoc, 2003, 102(11): 782-787. |
| [17] | Xu SY, Hu H, Jiang Z, et al. APACHE score, Severity index of paraquat poisoning, and serum lactic acid concentration in the prognosis of paraquat poisoning of Chinese patients[J]. Pediatr Emerg Care, 2015, 31(2): 117-121. DOI:10.1097/PEC.0000000000000351 |
| [18] | Matic I, Titlic M, Dikanovic M, et al. Effects of APACHE Ⅱ score on mechanical ventilation; prediction and outcome[J]. Acta Anaesthesiol Belg, 2007, 58(3): 177-183. |
| [19] | Shang XK, Wang YG. Comparison of outcomes of high-flow nasal cannula and noninvasive positive-pressure ventilation in patients with hypoxemia and various APACHE Ⅱ scores after extubation[J]. Ther Adv Respir Dis, 2021, 15: 17534666211004235. DOI:10.1177/17534666211004235 |
| [20] | Roca O, Caralt B, Messika J, et al. An index combining respiratory rate and oxygenation to predict outcome of nasal high-flow therapy[J]. Am J Respir Crit Care Med, 2019, 199(11): 1368-1376. DOI:10.1164/rccm.201803-0589OC |
| [21] | Lee YS, Chang SW, Sim JK, et al. An integrated model including the ROX index to predict the success of high-flow nasal cannula use after planned extubation: a retrospective observational cohort study[J]. J Clin Med, 2021, 10(16): 3513. DOI:10.3390/jcm10163513 |
| [22] | Mauri T, Carlesso E, Spinelli E, et al. Increasing support by nasal high flow acutely modifies the ROX index in hypoxemic patients: a physiologic study[J]. J Crit Care, 2019, 53: 183-185. DOI:10.1016/j.jcrc.2019.06.020 |
| [23] | Kollef MH, Torres A, Shorr AF, et al. Nosocomial infection[J]. Crit Care Med, 2021, 49(2): 169-187. DOI:10.1097/CCM.0000000000004783 |
| [24] | Dereli N, Ozayar E, Degerli S, et al. Three-year evaluation of nosocomial infection rates of the ICU[J]. Braz J Anesthesiol Engl Ed, 2013, 63(1): 73-78. DOI:10.1016/j.bjane.2012.03.004 |
| [25] | Saguil A, Fargo MV. Acute respiratory distress syndrome: diagnosis and management[J]. Am Fam Physician, 2020, 101(12): 730-738. |
| [26] | Ayzac L, Girard R, Baboi L, et al. Ventilator-associated pneumonia in ARDS patients: the impact of prone positioning[J]. Intensive Care Med, 2016, 42(5): 871-878. DOI:10.1007/s00134-015-4167-5 |
 2022, Vol. 31
2022, Vol. 31




