杭州G20峰会将细菌耐药写入公报:“抗生素耐药性严重威胁公共健康、经济增长和全球经济稳定[1]。”其与抗菌药物的不合理应用相关,临床工作者需高度关注[2-3]。血浆标志物降钙素原(procalcitonin,PCT)有助于区分细菌性和非细菌性感染,将其纳入感染性疾病的总体评估指标可以为患者提供诊疗决策[4];同时可以安全地减少抗菌药物处方率,缩短抗感染治疗疗程,降低细菌耐药率[5-11]。因此,早在2012年《中华急诊医学杂志》即组织“PCT急诊临床应用专家共识组”,共同发表了《降钙素原急诊临床应用的专家共识》[12],对提高急诊医师对PCT检测的重视程度并规范其临床应用发挥了重要作用。目前,PCT在临床最常见的成人下呼吸道感染性疾病(lower respiratory tract infections,LRTI)的应用中仍缺乏清晰的临床指导方案,有必要结合我国国情和LRTI的诊疗特点加强对PCT应用的指导。鉴于此,本共识组回顾借鉴该领域最新研究证据和进展,撰写此共识,以指导和规范PCT在成人LRTI中的临床应用。特别强调:PCT是一项辅助性诊断指标,不能仅根据这一孤立指标进行临床决策,必须结合LRTI患者的病史、临床表现、查体发现及其他辅助检查结果进行综合评估。
1 过程与推荐依据本共识是由来自全国急诊医学、呼吸病学、感染病学、微生物学等相关领域的专家所组成的多学科团队共同讨论制定,2021年1月,通过Delphi法各方达成了共识,并于3月完成第四轮讨论。
专家组讨论了PCT在成人LRTI不同病原体鉴别诊断中的证据,以及LRTI不同病种中PCT指导下的抗菌药物管理临床试验证据,依托国际相关指南和共识,结合中国人群临床诊疗的实践经验,针对PCT在LRTI的分级管理进行了充分的交流和探讨。此外,还交流和讨论了临床实际操作过程中可能面临的各项影响因素。在此基础上,提出了针对轻中度和重度LRTI患者PCT指导下的诊疗方案。此过程中,对系统评价/Meta分析以AMSTAR(a measurement tool to assess systematic reviews)做方法学质量评估。应用GRADE(grading of recommendations assessment, Development and evaluation)评级系统对每一结果作出正确的判断。
对有争议的问题公开讨论改进,通过逐一调整和反馈直到达成共识。最终,采用改良的Delphi流程[13],所有参加共识制定的成员对每项推荐意见投票:①强烈推荐、②弱推荐、③弃权、④弱不推荐、⑤强烈不推荐。
专家成员对推荐意见逐一进行了表决,在最终轮投票进行表决时达成一致。
2 PCT在LRTI患者分级管理中的应用 2.1 PCT简介1990年法国肿瘤学家Dr. Bohuon的团队在检测甲状腺肿瘤患者降钙素水平时发现了PCT的存在。1993年该团队首先提出PCT可以作为细菌感染的血清炎症标志物:细菌感染时,肝脏巨噬细胞和单核细胞、肺及肠道组织的淋巴细胞及神经内分泌细胞,在内毒素、肿瘤坏死因子-α(TNF-α)及IL-6等作用下会产生大量PCT[14];且细菌刺激机体后3 h即可测得,6~12 h后达到峰值[15]。健康人的血清PCT浓度低于0.05 µg/L;老年人、慢性疾病患者以及不足10%的健康人血清PCT浓度高于0.05 µg/L,最高可达0.1 µg/L,但一般不超过0.3 µg/L[12]。
2.2 依据LRTI不同感染类型和严重程度,采用不同PCT阈值进行感染分级管理[16-17]2020年《PCT指导抗菌药物管理亚太专家共识》指出:建议采用PCT 0.25 μg/L为阈值来评估非重症感染患者是否启用抗菌药物。对于轻中度社区、门急诊及住院的LRTI患者:建议动态监测PCT,采用每隔48~72 h的监测频率,同时结合临床资料,如PCT≥0.25 μg/L建议应用抗菌药物;初始PCT水平高者,如经治疗PCT < 0.25 μg/L或从峰值下降≥80%建议停用抗菌药物。
对于需要入住ICU的重度LRTI患者,进行经验性抗菌药物治疗同时应动态监测PCT,可采用每隔6~24 h的监测频率,以重新评估是否需要抗菌药物治疗。结合临床资料,如PCT≥0.5μg/L建议应用抗菌药物;初始PCT水平高者,如经治疗降低到PCT < 0.5 μg/L或PCT从峰值下降≥80%建议停用抗菌药物。在重症感染患者中,检测PCT的更重要的目的是停止应用抗菌药物,而不是决定是否启用抗菌药物治疗。
【推荐1】依据LRTI不同感染类型和严重程度,应采用不同PCT阈值进行感染分级管理。轻中度LRTI患者抗菌药物管理采用PCT 0.25 µg/L阈值指导,重度LRTI患者则采用PCT0.5 µg/L阈值指导,见表 1,2。
| 初步临床评估(包括微生物诊断) | 不确定细菌感染 | 高度怀疑细菌感染 | ||
| PCT值(µg/L) | < 0.25 | ≥0.25 | < 0.25 | ≥0.25 |
| PCT水平评估细菌感染可能性 | 低 | 高 | 低 | 高 |
| 细菌感染的总体评估 | 不太可能 | 有可能 | 可能 | 非常有可能 |
| 抗菌药物的应用 | 不推荐应用,需参考其他检查结果 | 基于临床综合情况判断用药 | 基于临床综合情况经验性用药,需参考其他检查结果 | 应用抗菌药物 |
| 随诊建议 | 根据临床感染证据变化,必要时复查PCT | 动态监测,PCT < 0.25 µg/L或从峰值下降80%后停药 | 在24 h内复测,如PCT < 0.25 µg/L停药 | 动态监测,PCT < 0.25 µg/L或从峰值下降80%后停药 |
| 初步临床评估(包括微生物诊断) | 不确定细菌感染 | 高度怀疑细菌感染 | ||
| PCT值(µg/L) | 应基于PCT基线水平及其他检验结果,s依据临床综合判断经验性用药 | |||
| < 0.5 | ≥0.5 | < 0.5 | ≥0.5 | |
| PCT水平评估细菌感染可能性 | 低 | 高 | 低 | 高 |
| 细菌感染的总体评估 | 不太可能 | 可能 | 可能 | 非常有可能 |
| 监测PCT值随访抗菌药物的应用 | 临床情况好转考虑停药 | 复测或动态监测,PCT < 0.5 µg/L或从峰值下降80%停药 | 临床情况好转考虑停药 | 考虑治疗失败,调整抗菌药物;继续动态监测,如PCT < 0.5 µg/L或从峰值下降80%停药 |
PCT在LRTI中可呈现多水平的变化,主要与感染病原体的类型、全身炎症反应的严重程度等相关。多种病原微生物可以引起LRTI,包括细菌、非典型病原体(支原体、衣原体、军团菌等)、病毒、真菌、结核、寄生虫等;不同病原微生物引起的LRTI,其PCT的临床诊断价值、意义以及阈值均不同,因此应采用不同PCT阈值进行管理(见表 3,表 4)。
| 降(μg/L) | 临床诊断意义 |
| < 0.1 | 无细菌感染 |
| 0.1至 < 0.25 | 不太可能存在细菌感染 |
| 0.25至 < 0.5 | 可能存在细菌感染 |
| ≥ 0.5 | 存在细菌感染 |
| 不同LRTI | PCT水平 | 以PCT指导临床结局 | 抗菌药使用建议 |
| 急性气管-支气管炎 | 0.25μg/L cutoff | 降低抗菌药物治疗时间和治疗费用 | PCT 0.25 µg/L可为急性气管-支气管炎患者选择抗菌药物提供指导作用 |
| 肺炎 | |||
| 社区获得性肺炎 | |||
| 轻中度 | 0.25μg/L cutoff | 降低抗菌药物处方率和暴露 | 0.25 µg/L作为阈值启用或停用抗菌药物 |
| 重度 | 0.5μg/L cutoff | 缩短抗菌药物治疗时间、减少抗菌药物用量,危重患者28天和1年病死率显著降低 | 0.5 µg/L作为阈值停用抗菌药物 |
| 院内获得性肺炎 | |||
| 轻中度 | 0.25μg/L cutoff | 平均抗菌药物治疗时间减少,住院时间缩短 | PCT < 0.1 µg/L和0.1~0.25 µg/L的患者,分别强烈不建议或不建议开始抗菌药物治疗,不应用抗菌药物的患者采取6~24 h后重复PCT检测 |
| 重度 | 0.5μg/L cutoff | 在区分细菌感染和病毒感染方面更具优势 | 在脓毒症患者中以0.5 µg/L为阈值联合CRP等项目作为抗菌药停药指标 |
| 呼吸机相关性肺炎 | 动态监测PCT水平 | 减少抗菌药物使用天数和总持续治疗时间 | PCT在0.25~0.5 µg/L之间或下降≥80%,鼓励停用抗菌药物;PCT ≥0.5 µg/L或下降 < 80%,不建议停用抗菌药物;PCT>1 µg/L强烈提示细菌感染未控制,强烈不建议停用抗菌药物 |
| 慢性支气管炎急性发作/慢性阻塞性肺疾病急性加重 | 0.25μg/L cutoff | 减少抗菌药物暴露量和住院时间 | PCT<0.25 µg/L不启动抗菌药物治疗,建议6~24 h后复测PCT。PCT≥0.25 µg/L启动抗菌药物治疗,之后依据指南持续应用5~7 d |
| 支气管扩张合并细菌感染 | 动态监测PCT水平 | 减少抗菌药物使用 | PCT < 0.1 μg/L强烈不建议应用抗菌药物;PCT < 0.25 μg/L不建议应用抗菌药物;PCT≥0.25 μg/L建议应用抗菌药物;PCT≥0.5 μg/L强烈推荐应用抗菌药物 |
美国CDC对1 735例成人社区获得性肺炎(community-acquired pneumonia, CAP)患者的研究结果显示,典型的细菌性肺炎PCT水平显著高于病毒性肺炎及其他病原体感染,以0.25 µg/L作为诊断阈值,鉴别细菌和非细菌感染的阴性预测值为92.4%[18]。
研究显示[19],G-菌感染所致PCT水平显著高于G+菌感染,考虑原因与G-菌缺少细胞壁以及释放大量内毒素有关;PCT大于4.49 µg/L,诊断G-菌感染特异度可达81.8%,阳性预测值为75.0%。因此,呼吸道的不同典型细菌性感染与PCT水平相关。
PCT水平还可以作为抗菌药物治疗效果的评估指标。PCT持续升高或治疗后不下降一般提示治疗效果不佳,需调整抗菌药物。相反,治疗后PCT下降可以作为抗菌药物治疗有效和停药的参考指标。
【推荐2】排除典型细菌性LRTI的诊断阈值采用PCT 0.25 μg/L,此阈值同时可作为启用和终止抗菌药物治疗的参考指标。
3.2 非典型病原体感染PCT在支原体、衣原体感染的LRTI患者中一般无明显升高。一项西班牙双中心CAP住院患者前瞻性研究发现[20],PCT≤0.5 μg/L时区分非典型病原体与典型细菌的敏感性为81%,阴性预测值高达97%(肺炎支原体中位数为0.34 μg/L,肺炎衣原体中位数为0.23 μg/L)。因此,PCT虽不能作为支原体、衣原体等非典型病原体所致LRTI的诊断指标,如果0.25 μg/L≤PCT≤0.5 μg/L提示可能存在细菌感染,推荐抗菌药物治疗;如未采用喹诺酮类、四环素类或大环内酯类抗感染药物,且观察治疗效果不佳者,结合临床表现提示可能存在非典型病原体如支原体、衣原体感染引起的LRTI。
瑞士巴塞尔大学医院一项回顾性研究纳入了2002年至2007年军团菌感染的CAP患者[21],超过93%患者PCT大于0.1 μg/L,超过86%患者大于0.25 μg/L;同时PCT对住院病死率和(或)需要入住ICU具有很高的预测准确性。因此,PCT>0.25 μg/L考虑典型细菌感染的同时也要考虑军团菌感染导致的LRTI。
3.3 病毒感染一项研究比较了多种生物标记物对于细菌和病毒感染的鉴别能力,包括PCT、IL-1 β、IL-6、IL-8、IL-10、IL-12、TNF- α、IFN-γ、sCD14等,结果发现PCT对于细菌感染的敏感性和特异性最佳,诊断细菌感染的ROC曲线下面积达0.952,细菌感染的PCT中位数为1.84 µg/L,而病毒感染的PCT中位数为0.05 µg/L[12]。另外一项纳入1 735名下呼吸道感染患者的多中心前瞻性研究发现,病毒感染时PCT浓度中位数<0.25 µg/L[18],而典型细菌感染则明显升高(≥2.5 µg/L)。PCT可以有效对细菌性病原体(包括典型细菌和非典型病原体)与病毒感染进行区分,其ROC曲线下面积为0.73[18]。
针对新型冠状病毒肺炎的研究发现,93%的非重症患者入院时PCT均小于0.25 µg/L[22];严重急性呼吸综合征(severe acute respiratory syndrome, SARS)患者与细菌或真菌感染的肺炎相比较PCT水平较低[23];中东呼吸综合征(middle east respiratory syndrome, MERS)患者在入院时均出现发热、肌痛、白细胞减少以及C反应蛋白轻度升高,但PCT则正常或维持在较低水平[24]。2009年甲型H1N1流感病毒流行期间的研究同样显示,94%的经H1N1核酸检测确诊的患者PCT均低于0.25 µg/L[25]。因此,PCT具有较高的细菌感染阴性预测值,且检测方便快速,可在得到病毒核酸检测结果前用于发热门诊及急诊患者的筛查和快速分流[26]。
【推荐3】结合临床症状采用PCT<0.25 μg/L阈值有助于支持单纯病毒所致LRTI的诊断。
3.4 其他病原体感染 3.4.1 真菌感染真菌性下呼吸道感染患者PCT可升高,但升高的程度常依真菌感染的侵及范围而异:侵袭性真菌感染时PCT增高明显,而局灶性感染者很少增高。同时,不同种类真菌感染导致的PCT变化亦可表现不同的特点。
加拿大一项大型多中心呼吸机相关性肺炎(ventilator-associated pneumonia, VAP)患者前瞻性研究中[27],针对ICU入院24 h内呼吸道念珠菌培养阳性与细菌培养阳性患者,进行了包括PCT在内的全身炎症标志物比较。研究发现念珠菌组和细菌组与对照组相比,PCT水平均有所升高;但PCT中位数水平念珠菌组(1.4 μg/L)显著高于细菌培养阳性组(0.8 μg/L)以及对照组(0.2 μg/L)(P = 0.02)。因此,临床评估PCT与呼吸道念珠菌感染之间的关系,如果PCT水平继续升高,可能意味着肺部念珠菌感染导致全身炎症反应持续加重。
波兰一项肺移植术后霉菌感染患者研究中发现,霉菌检测阳性的患者(青霉菌、曲霉菌和接合菌)PCT均有所升高,其值在(0.5±0.7) µg/L。提示PCT可以是霉菌感染的有用标记物,帮助医生做临床决策[28]。PCT水平的显著升高不仅要关注细菌感染,有免疫抑制因素者也要排除霉菌感染。
综上所述,PCT对真菌感染的诊断或鉴别诊断具有一定的临床价值,但应当结合宿主免疫状况、临床指征和其他检测项目进行综合科学评估。此外,长时间广谱抗菌药物治疗后PCT不能降至正常范围,且免疫受损的感染患者需要考虑合并真菌感染的可能。
3.4.2 结核感染临床上部分呼吸道细菌和真菌感染常需要与肺结核鉴别诊断,但在未取得病原学证据的情况下鉴别较困难。PCT在活动性结核病患者中有可能轻度升高,研究证实可将0.1~0.25 µg/L作为临界值[29]。肺结核患者PCT水平大多轻度升高,而细菌或真菌性呼吸道感染患者水平明显升高,以PCT≥0.25 μg/L为阈值,有助于细菌性和真菌性下呼吸道感染与肺结核鉴别诊断[29-30]。
3.4.3 寄生虫感染一项观察27名泰国疟疾患者在应用青蒿琥酯和甲氟喹治疗前后的PCT水平的研究表明,患者入院时PCT升高(中位数40 µg/L,范围0.04~662 µg/L),治疗后,中位数下降到1.3 µg/L(范围0.01~6.5 µg/L)。PCT水平与提示疾病严重程度的初始寄生虫密度相关(P<0.05)。因此,对疟疾患者动态监测PCT可以作为疾病严重程度的监测指标,并可能对预测病程进展和临床结局具有价值[31]。
4 PCT在不同类型LRTI分级管理中的应用 4.1 急性气管-支气管炎(acute tracheobronchitis,ATB)急性气管-支气管炎是由生物或非生物性因素引起的气管-支气管黏膜的急性炎症;是急性咳嗽的常见病因之一,中国和欧美对病史 < 3周者定义为急性[32]。此类疾病患者常见症状为发热、咳嗽、咳痰、气急等,胸部影像检查可见肺纹理增粗紊乱。临床医师往往会主动或由就诊者本人提出应用抗菌药物,从而造成抗菌药物过度应用,进而造成医疗成本增加。而本病最常见的病原体是病毒,冷空气、粉尘及刺激性气体也可引发。美国《2016年成人急性呼吸道感染抗菌药物指南》中指出[33],90%表现为咳嗽的患者是由于病毒感染所致,然而判断究竟是否为病毒感染是非常困难的。出现脓痰或者痰的颜色改变(如黄色、绿色)并不意味着细菌感染,也可能是由于炎症细胞或者脱落的黏膜上皮细胞造成。因此,目前大部分指南对于急性单纯性支气管炎都不建议常规应用抗菌药物。美国一项研究中纳入458名急性呼吸道感染患者[34],以PCT 0.25 μg/L为阈值指导治疗组上呼吸道感染或急性支气管炎患者的抗菌药物处方比标准治疗组显著减少了约80%(19% vs. 99%),而两组患者的预后差异无统计学意义。因此,PCT 0.25 μg/L可为急性气管-支气管炎患者应用抗菌药物提供指导作用,同时应监测病情,若病情加重或无效,应及时复查PCT及调整治疗方案[35]。
【推荐4】PCT 0.25 μg/L阈值可为急性气管-支气管炎患者应用抗菌药物提供指导作用,同时减少抗菌药物处方。
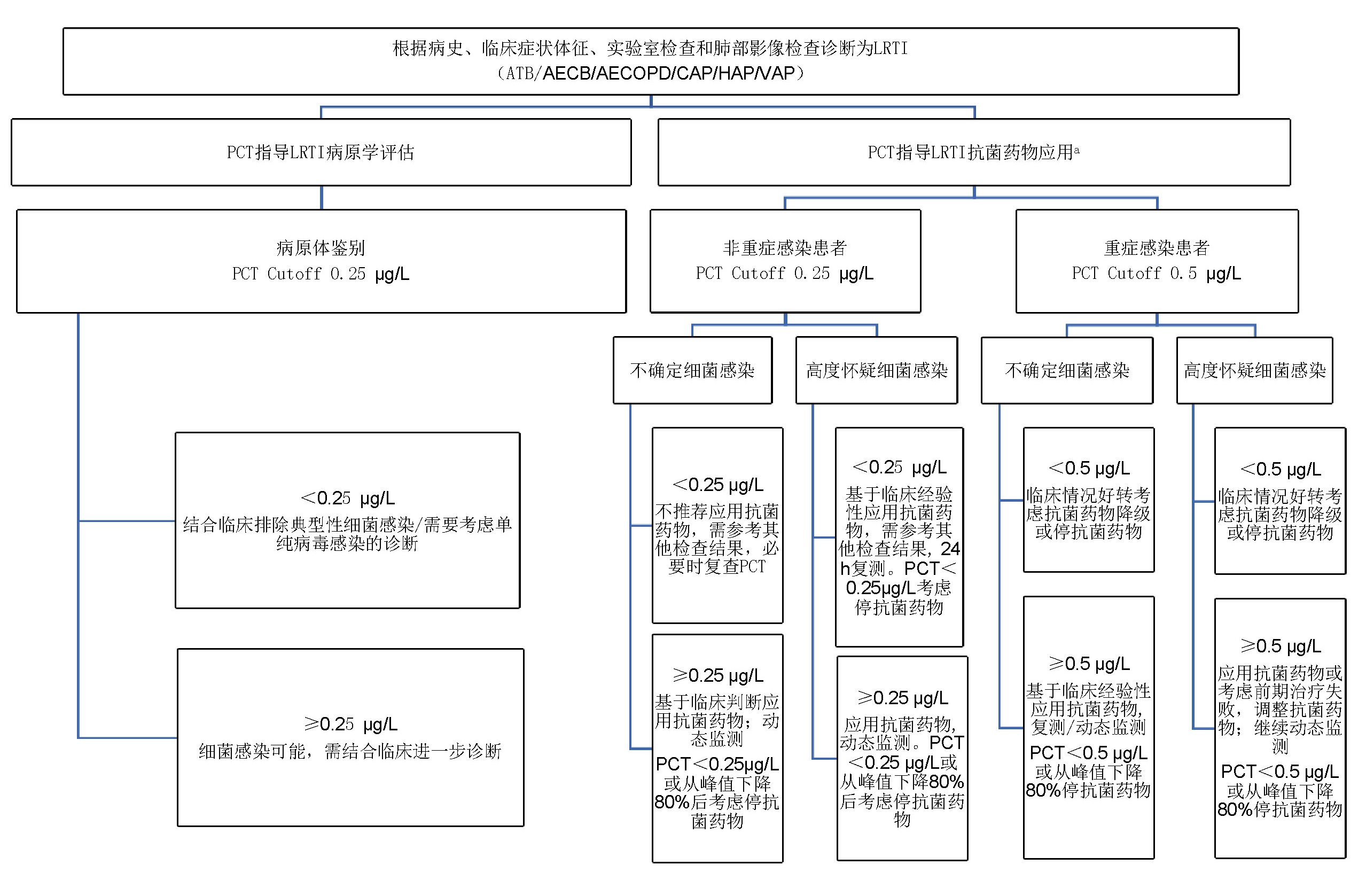
4.2 肺炎 4.2.1 社区获得性肺炎(community-acquired pneumonia,CAP)CAP是临床最常见的疾病之一,根据已有的高质量循证医学证据建议PCT指导抗菌药物管理概念在CAP患者中予以实施。见图 1。
|
| a以指导肺炎患者抗菌药物应用为例 图 1 降钙素原指导LRTI诊疗路径图 |
|
|
来自12个国家的26项随机试验的6 708名急性呼吸道感染患者中(包括CAP患者2 910例),以PCT 0.25 µg/L作为阈值与较低的抗菌药物使用率、较少的抗菌药物相关不良反应和改善总体生存率相关[36]。1 359例成人下呼吸道感染患者的ProHOSP多中心随机干预研究结果也显示,与对照组相比,其中925例成人CAP患者以PCT 0.25 µg/L作为阈值启用或停用抗菌药物,抗菌药物处方率下降了10%,抗菌药物暴露下降了32.4%。作为研究主要终点,患者急诊入院30天内总体不良结局风险差异PCT组明显低于对照组(-4.1%,95% CI),且不会增加患者全因死亡风险(-0.4%,95% CI)[37]。
4.2.1.2 重症CAP:PCT阈值为0.5 µg/L一项荷兰15家医院纳入1 575名入住ICU的感染患者(其中CAP患者994例)的前瞻性多中心、随机对照干预试验中,PCT指导组设置为浓度下降至峰值80%以上或<0.5 µg/L则推荐依据临床情况停止抗菌药物应用[8];标准治疗组则根据传统抗菌药物应用方案接受治疗。该试验表明,PCT指导下的抗菌药物治疗可以缩短治疗时间2 d和减少抗菌药物用量19%。与传统治疗方案相比,PCT指导下可减少危重感染患者抗菌药物应用时间和每日抗菌药物剂量,危重患者28 d和1年病死率也显著降低[8]。
4.2.2 院内获得性肺炎(hospital-acquired pneumonia,HAP) 4.2.2.1 轻中症HAP:PCT阈值为0.25 µg/L一项回顾性研究比较了美国宾夕法尼亚州匹兹堡两所教学医院实施PCT指导前后HAP患者的情况[38]。PCT < 0.1 µg/L和0.1~0.25 µg/L的患者,分别强烈不建议或不建议抗菌药物治疗,不应用抗菌药物的患者6~24 h后复测PCT。PCT在0.25~0.5 µg/L之间和PCT≥0.5 µg/L的患者,建议或强烈建议开始抗菌药物治疗。与非指导组相比,PCT指导组平均抗菌药物持续治疗时间减少(6.0 d vs 9.9 d;P<0.001),平均住院时间缩短(3.5 d vs 4.9 d;P = 0.006);PCT指导组<0.25 µg/L的患者比≥0.25 µg/L患者平均抗菌药物治疗时间明显更短(4.6 d vs 8.0 d;P<0.001)。
4.2.2.2 重症HAP:PCT阈值为0.5 µg/L在一项比较高剂量多黏菌素单药治疗与多黏菌素+美罗培南联合治疗多重耐药肺炎克雷伯菌引起的HAP和呼吸机相关性肺炎的前瞻性临床研究中[39],以PCT 0.5 µg/L为阈值联合CRP等指标作为抗菌药物停药指标,同时评估了各检测指标的差异,发现PCT的敏感性与CRP差异有统计学意义,且更具优势。
4.2.3 呼吸机相关性肺炎(ventilator-associated pneumonia,VAP)一项纳入101名VAP患者的多中心随机对照试验中[40],根据细菌感染的可能性进行分级,PCT < 0.25 µg/L提示不存在细菌感染可能,强烈建议停用抗菌药物;经抗菌药物治疗与初始相比,PCT在0.25~0.5 µg/L之间或下降≥80%,鼓励停用抗菌药物;经抗菌药物治疗与初始相比,PCT≥0.5 µg/L或下降 < 80%被认为细菌感染控制并不理想,不建议停用抗菌药物;PCT>1 µg/L强烈提示细菌感染未控制,强烈不建议停用抗菌药物。结论表明,VAP发生后28 d内PCT指导组可显著减少抗菌药物应用天数(13 d vs 9.5 d),抗菌药物治疗总持续时间减少了27%(P=0.038),从而帮助减少VAP患者的抗菌药物暴露时间。
对于VAP患者,指南建议在72 h后根据微生物学结果调整抗菌药物治疗。动态监测PCT水平可为减少抗菌药物治疗提供依据[40]。
【推荐5】PCT阈值可为不同严重程度的肺炎患者提供抗菌药物指导。轻中度肺炎患者采用0.25 μg/L阈值、重度肺炎患者采用0.5 μg/L阈值。当PCT下降幅度>80%时,鼓励停用抗菌药物。
4.3 慢性支气管炎急性发作(acute exacerbation of chronic bronchitis,AECB)/慢性阻塞性肺疾病急性加重(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)Stoltz等[41]对AECB的研究中,将PCT指导的抗菌药物治疗组(依据PCT水平>0.25 μg/L并结合临床判断)与标准治疗组对比,发现PCT指导的抗菌药物治疗组有效地减少了AECB患者抗菌药物处方,且不影响临床结局。
尽管细菌感染常被怀疑为AECOPD的病因,但研究表明很大比例归因于呼吸道病毒感染。AECOPD全球倡议指南中建议,当患者在三项主要症状包括呼吸困难加重、痰量增加和痰液脓性改变中存在两种症状,或者这两种症状之一是痰液脓性改变,或者是需要机械通气治疗的情况下可采用抗菌药物治疗。然而,上述标准仍可能会导致抗菌药物的过度应用,因为脓痰并不一定代表细菌感染,因此抗菌药物管理计划(antimicrobial stewardship programs,ASPs)建议利用PCT以帮助识别AECOPD细菌与病毒或非感染性病因,制定相应的指导方案来帮助纠正抗菌药物的过度应用。该方案推荐对于AECOPD入院患者,建议在24 h内检测PCT浓度:PCT<0.25 µg/L不启动抗菌药物治疗,同时建议6~24 h后复测PCT。PCT≥0.25 µg/L建议启动抗菌药物治疗,之后依据指南持续应用5~7 d。一项对1 062名AECOPD患者进行的随机对照试验的荟萃分析也证实,基于PCT的抗菌药物指导方案,根据PCT浓度在24 h内启动抗菌药物治疗与经验性治疗相比,显著减少了总抗菌药物暴露量,且住院时间明显缩短(2.8 d vs 3.7 d,P<0.01),与此同时并不增加治疗失败率、复发率或病死率等[42]。
【推荐6】PCT有助于识别AECB/AECOPD细菌与病毒或非感染性病因;PCT<0.25 µg/L不推荐启动抗菌药物治疗。
4.4 支气管扩张合并细菌感染PCT在支气管扩张合并细菌感染时血清浓度通常较低(与其他感染标记物类似),这可能反映了支气管扩张感染和炎症通常局限于气道腔内。英国一项支气管扩张患者对比研究中,采用依据PCT指导下的抗菌药物治疗方案:PCT < 0.25 μg/L不建议应用抗菌药物;PCT≥0.25 μg/L建议应用抗菌药物;结果发现,PCT可在支气管扩张患者中作为常用的炎症标志物帮助医生确立诊疗决策,同时可帮助临床显著减少抗菌药物应用,但不影响临床结局[43]。因此,支气管扩张患者如出现急性呼吸道症状伴有黄色、绿色黏痰等,应动态监测PCT确认是否存在细菌感染,依据PCT指导抗菌药物应用。
【推荐7】支气管扩张合并细菌感染患者PCT<0.25 μg/L不建议应用抗菌药物。
5 PCT在LRTI应用的检测需求和影响因素 5.1 PCT针对LRTI的检测需求部分LRTI因感染的局限,PCT检测结果可能升高不明显,诊断阈值也较脓毒症要低,这对检测系统的准确度和精密度要求更高。2020年亚太区PCT共识建议:PCT测定应确保高灵敏度和足够的精度[17]。《2019年PCT指导抗菌药物治疗优化临床应用国际专家共识》特别强调:在相关的阈值范围内,能够提供足够精密度的PCT检测才能用于安全的临床决策[16]。2017年美国FDA首次批准B·R·A·H·M·S PCT检测为LRTI患者抗菌药物治疗提供指导方案[44]。2019年我国国家药监局也首次批准采用赛默飞公司的时间分辨荧光免疫法PCT检测(灵敏度为0.06 μg/L),且将PCT 0.25 μg/L作为轻中度下呼吸道细菌感染鉴别诊断的阈值[45]。鉴于假阴性和假阳性检测结果可能影响患者治疗安全性,建议临床应用中尽可能避免低质量的超线性测定[17]。此外,为避免复杂血液成分的干扰,检测应采取血清/血浆样本。
由于PCT未实现国际标准化,在检测平台的选择上要注意其结果的溯源性,不同溯源的检测方法需要建立各自的参考区间和临床决定阈值。本共识中临床研究采用的阈值均基于B·R·A·H·M·S溯源体系的分析研究,因此建议PCT检测采用B·R·A·H·M·S溯源体系的检测平台(例如,赛默飞公司的时间分辨荧光免疫分析平台,罗氏公司、雅培公司、西门子公司、索灵公司的化学发光平台,生物梅里埃公司的酶联免疫荧光平台,奥森多公司增强化学发光平台),以确保检测的高灵敏度和精密度以及阈值和结果的适用性。
5.2 血清/血浆PCT检测的影响因素目前PCT检测的标本类型主要为血清和血浆,通常其血清和血浆离体浓度非常稳定,但某些临床因素下PCT可能会受到影响。某些非感染性疾病会导致PCT增高:例如外科手术和创伤、器官移植、肾功能不全、甲状腺髓样癌、自身免疫性疾病、胰腺炎等[46-52];中性粒细胞减少症的患者合并感染时PCT的上升会受到抑制,重症中性粒细胞减少症(<0.5×109/L)的患者PCT生成仅为正常的1/3~1/2[12];PCT在这些患者人群中的结果解释需谨慎。此外,如患者入院前已经接受抗菌药物治疗且有效,PCT初次检测也可能较低[53]。因此,针对不同个体,由于受到不同个体不同疾病临床特征影响,血清PCT的判读需结合临床分析。
【推荐8】PCT检测尚未实现国际公认的标准化,各厂家PCT需自行建立阈值;以确保提供安全有效的临床决策,临床采用的PCT阈值应基于大量临床研究和证据。
6 结论与展望PCT检测可以作为一项有效的辅助工具指导LRTI的诊断治疗以及合理应用抗菌药物、减少抗感染药物暴露、控制耐药菌过快增长。PCT的临床应用,应当依据LRTI的严重程度以及感染类型采用不同的PCT阈值来指导感染诊断和抗菌药物治疗。应提高对于PCT 0.25 μg/L阈值的重视程度,同时关注检测平台是否适用于LRTI的诊断,例如检测平台的灵敏度,线性范围及相关阈值上的精度。
专家组成员名单(按笔画顺序)丁邦晗 马青变 马岳峰 王弋 王军 王旭东 王选锭 邓义军 石松菁 卢中秋 叶贤伟 田英平 白建文 邢吉红 邢西迁 吕传柱 吕菁君 朱华栋 朱建军 朱海燕 朱继红 刘京铭 闫圣涛 孙同文 孙克玉 李文放 李圣青 李雯 李湘民 何小军 何新华 吴彩军 宋元林 宋振举 张文武 张劲松 张杰 张泓 张国强 张新超 陆远强 陈凤英 陈玉国 陈旭岩 陈晓辉 林兆奋 孟庆义 封启明 赵丽 赵晓东 赵剡 赵敏 赵斌 洪玉才 侯刚 聂时南 柴艳芬 徐军 徐峰 高艳霞 郭伟 郭树彬 郭俊 黄英姿 黄亮 黄曼 曹钰 龚平 康健 揭志军 蒋龙元 童朝阳 曾俊 谢苗荣 蔡文伟 裴红红 黎檀实 燕宪亮 魏捷
利益冲突 所有作者均声明不存在利益冲突
| [1] | Jee Y, Carlson J, Rafai E, et al. Antimicrobial resistance: a threat to global health[J]. Lancet Infect Dis, 2018, 18(9): 939-940. DOI:10.1016/S1473-3099(18)30471-7 |
| [2] | Musher DM, Thorner AR. Community-acquired pneumonia[J]. N Engl J Med, 2014, 371(17): 1619-1628. DOI:10.1056/nejmra1312885 |
| [3] | Jain S, Self WH, Wunderink RG, et al. Community-acquired pneumonia requiring hospitalization among US adults[J]. N Engl J Med, 2015, 373(5): 415-427. DOI:10.1056/nejmoa1500245 |
| [4] | Sager R, Kutz A, Mueller B, et al. Procalcitonin-guided diagnosis and antibiotic stewardship revisited[J]. BMC Med, 2017, 15(1): 15. DOI:10.1186/s12916-017-0795-7 |
| [5] | Mitsuma SF, Mansour MK, Dekker JP, et al. Promising new assays and technologies for the diagnosis and management of infectious diseases[J]. Clin Infect Dis, 2013, 56(7): 996-1002. DOI:10.1093/cid/cis1014 |
| [6] | Schuetz P, Raad I, Amin DN. Using procalcitonin-guided algorithms to improve antimicrobial therapy in ICU patients with respiratory infections and Sepsis[J]. CurrOpin Crit Care, 2013, 19(5): 453-460. DOI:10.1097/mcc.0b013e328363bd38 |
| [7] | Schuetz P, Wirz Y, Sager R, et al. Effect of procalcitonin-guided antibiotic treatment on mortality in acute respiratory infections: a patient level meta-analysis[J]. Lancet Infect Dis, 2018, 18(1): 95-107. DOI:10.1016/s1473-3099(17)30592-3 |
| [8] | de Jong E, van Oers JA, Beishuizen A, et al. Efficacy and safety of procalcitonin guidance in reducing the duration of antibiotic treatment in critically ill patients: a randomised, controlled, open-label trial[J]. Lancet Infect Dis, 2016, 16(7): 819-827. DOI:10.1016/s1473-3099(16)00053-0 |
| [9] | Christ-Crain M, Stolz D, Bingisser R, et al. Procalcitonin guidance of antibiotic therapy in community-acquired pneumonia: a randomized trial[J]. Am J Respir Crit Care Med, 2006, 174(1): 84-93. DOI:10.1164/rccm.200512-1922OC |
| [10] | Nobre V, Harbarth S, Graf JD, et al. Use of procalcitonin to shorten antibiotic treatment duration in septic patients: a randomized trial[J]. Am J Respir Crit Care Med, 2008, 177(5): 498-505. DOI:10.1164/rccm.200708-1238oc |
| [11] | Schroeder S, Hochreiter M, Koehler T, et al. Procalcitonin (PCT)-guided algorithm reduces length of antibiotic treatment in surgical intensive care patients with severe sepsis: results of a prospective randomized study[J]. Langenbeck's Arch Surg, 2009, 394(2): 221-226. DOI:10.1007/s00423-008-0432-1 |
| [12] | 降钙素原急诊临床应用专家共识组. 降钙素原(PCT)急诊临床应用的专家共识[J]. 中华急诊医学杂志, 2012, 21(9): 944-951. DOI:10.3760/cma.j.issn.1671-0282.2012.09.005 |
| [13] | Memtsoudis, S. G., et al. Consensus statement from the consensus conference on bilateral total knee arthroplasty group[J]. Clin OrthopRelat Res, 2013, 47(18): 2649-2657. |
| [14] | Assicot M, Gendrel D, Carsin H, et al. High serum procalcitonin concentrations in patients with Sepsis and infection[J]. Lancet, 1993, 341(8844): 515-518. DOI:10.1016/0140-6736(93)90277-n |
| [15] | 陆一鸣. 降钙素原PCT感染诊治新技术: 早期诊断、快速鉴别、及时评估感染程度、指导抗生素使用[J]. 中华实验和临床感染病杂志(电子版), 2013, 7(3): 463-465. |
| [16] | Schuetz P, Beishuizen A, Broyles M, et al. Procalcitonin (PCT)-guided antibiotic stewardship: an international experts consensus on optimized clinical use[J]. Clin Chem Lab Med, 2019, 57(9): 1308-1318. DOI:10.1515/cclm-2018-1181 |
| [17] | Lee CC, Kwa ALH, Apisarnthanarak A, et al. Procalcitonin (PCT)-guided antibiotic stewardship in Asia-Pacific countries: adaptation based on an expert consensus meeting[J]. Clin Chem Lab Med, 2020, 58(12): 1983-1991. DOI:10.1515/cclm-2019-1122 |
| [18] | Self WH, Balk RA, Grijalva CG, et al. Procalcitonin as a marker of etiology in adults hospitalized with community-acquired pneumonia[J]. Clin Infect Dis, 2017, 65(2): 183-190. DOI:10.1093/cid/cix317 |
| [19] | Yan ST, Zhang GQ, et al. Diagnostic and predictive value of critical illness scores and biomarkers in bloodstream infection-associated pneumonia[J]. Chin Crit Care Med, 2020, 32(6): 681-685. DOI:10.3760/cma.j.cn121430-20200428-00345 |
| [20] | Menéndez R, Sahuquillo-Arce JM, Reyes S, et al. Cytokine activation patterns and biomarkers are influenced by microorganisms in community-acquired pneumonia[J]. Chest, 2012, 141(6): 1537-1545. DOI:10.1378/chest.11-1446 |
| [21] | Haeuptle J, Zaborsky R, Fiumefreddo R, et al. Prognostic value of procalcitonin in Legionella pneumonia[J]. Eur J Clin Microbiol Infect Dis, 2009, 28(1): 55-60. DOI:10.1007/s10096-008-0592-5 |
| [22] | Huang CL, Wang YM, Li XW, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China[J]. Lancet, 2020, 395(10223): 497-506. DOI:10.1016/s0140-6736(20)30183-5 |
| [23] | Chua AP, Lee KH. Procalcitonin in severe acute respiratory syndrome (SARS)[J]. J Infect, 2004, 48(4): 303-306. DOI:10.1016/j.jinf.2004.01.015 |
| [24] | Rhee JY, Hong G, Ryu KM. Clinical implications of 5 cases of middle east respiratory syndrome coronavirus infection in a south Korean outbreak[J]. Jpn J Infect Dis, 2016, 69(5): 361-366. DOI:10.7883/yoken.JJID.2015.445 |
| [25] | Canavaggio P, Boutolleau D, Goulet H, et al. Procalcitonin for clinical decisions on influenza-like illness in emergency department during influenza a(H1N1)2009 pandemic[J]. Biomarkers, 2018, 23(1): 10-13. DOI:10.1080/1354750X.2016.1276626 |
| [26] | Rodríguez AH, Avilés-Jurado FX, Díaz E, et al. Procalcitonin (PCT) levels for ruling-out bacterial coinfection in ICU patients with influenza: a CHAID decision-tree analysis[J]. J Infect, 2016, 72(2): 143-151. DOI:10.1016/j.jinf.2015.11.007 |
| [27] | Williamson DR, Albert M, Perreault MM, et al. The relationship between Candida species cultured from the respiratory tract and systemic inflammation in critically ill patients with ventilator-associated pneumonia[J]. Can J Anaesth, 2011, 58(3): 275-284. DOI:10.1007/s12630-010-9439-5 |
| [28] | Zegleń S, Sioła M, Woźniak-Grygiel E, et al. Procalcitonin serum concentration in lung transplant recipients during mold colonization or infection[J]. Transplant Proc, 2011, 43(8): 3089-3091. DOI:10.1016/j.transproceed.2011.08.057 |
| [29] | Huang SL, Lee HC, Yu CW, et al. Value of procalcitonin in differentiating pulmonary tuberculosis from other pulmonary infections: a meta-analysis[J]. Int J Tuberc Lung Dis, 2014, 18(4): 470-477. DOI:10.5588/ijtld.13.0449 |
| [30] | 罗国辉, 曹华蕊, 肖军, 等. PCT在肺结核与真菌性肺部感染疾病鉴别中的意义[J]. 中国社区医师, 2014, 30(16): 108-109. DOI:10.3969/j.issn.1007-614x.2014.16.72 |
| [31] | Hollenstein U, Looareesuwan S, Aichelburg A, et al. Serum procalcitonin levels in severe plasmodium falciparum malaria[J]. Am J Trop Med Hyg, 1998, 59(6): 860-863. DOI:10.4269/ajtmh.1998.59.860 |
| [32] | Richard S. Irwin, Michael H Baumann, et al. Diagnosis and management of cough executive summary : ACCP evidence-based clinical practice guidelines[J]. Chest, 2006, 129(suppl): 1S-23S. DOI:10.1378/chest.129.1_suppl.1S |
| [33] | Aaron M. Harris, et al. Appropriate antibiotic use for acute respiratory tract infection in adults: advice for high-value care from the American college of physicians and the centers for disease control and prevention[J]. Ann Intern Med, 2016, 1646(6): 425-434. DOI:10.7326/M15-1840 |
| [34] | Matthias Briel, Philipp Schuetz, et al. Procalcitonin-guided antibiotic use vs a standard approach for acute respiratory tract infections in primary Care[J]. Arch Intern Med, 2008, 168(18): 2000-2007. DOI:10.1001/archinte.168.18.2000 |
| [35] | 李文, 郑玉琼, 钟云清. 降钙素原在急性气管-支气管炎中使用抗生素的指导意义[J]. 中国抗生素杂志, 2013, 38(7): 562-564. DOI:10.13461/j.cnki.cja.005224 |
| [36] | Schuetz P, Wirz Y, Mueller B. Procalcitonin testing to guide antibiotic therapy in acute upper and lower respiratory tract infections[J]. JAMA, 2018, 319(9): 925-926. DOI:10.1001/jama.2018.0852 |
| [37] | Schuetz P, Christ-Crain M, Thomann R, et al. Effect of procalcitonin-based guidelines vs standard guidelines on antibiotic use in lower respiratory tract infections: the ProHOSP randomized controlled trial[J]. JAMA, 2009, 302(10): 1059-1066. DOI:10.1001/jama.2009.1297 |
| [38] | Walsh TL, DiSilvio BE, Hammer C, et al. Impact of procalcitonin guidance with an educational program on management of adults hospitalized with pneumonia[J]. Am J Med, 2018, 131(2): 201. DOI:10.1016/j.amjmed.2017.08.039 |
| [39] | Abdelsalam MFA, Abdalla MS, El-Abhar HSE. Prospective, comparative clinical study between high-dose colistin monotherapy and colistin-meropenem combination therapy for treatment of hospital-acquired pneumonia and ventilator-associated pneumonia caused by multidrug-resistant Klebsiella pneumoniae[J]. J Glob Antimicrob Resist, 2018, 15: 127-135. DOI:10.1016/j.jgar.2018.07.003 |
| [40] | Stolz D, Smyrnios N, Eggimann P, et al. Procalcitonin for reduced antibiotic exposure in ventilator-associated pneumonia: a randomised study[J]. Eur Respir J, 2009, 34(6): 1364-1375. DOI:10.1183/09031936.00053209 |
| [41] | Siempos Ⅱ, Michalopoulos A, Falagas ME. Treatment of acute bacterial exacerbations of chronic bronchitis[J]. Expert Opin Pharmacother, 2009, 10(7): 1173-1182. DOI:10.1517/14656560902907734 |
| [42] | Bremmer DN, Moffa MA, Ma K, et al. Acute exacerbations of chronic obstructive pulmonary disease with a low procalcitonin concentration: impact of antibiotic therapy[J]. Clin Infect Dis, 2019, 68(5): 725-730. DOI:10.1093/cid/ciy552 |
| [43] | Loebinger MR, Shoemark A, Berry M, et al. Procalcitonin in stable and unstable patients with bronchiectasis[J]. Chronic Respir Dis, 2008, 5(3): 155-160. DOI:10.1177/1479972308088823 |
| [44] | B·R·A·H·M·S PCT sensitive KRYPTOR®. Food and Drug Administration, 2017. |
| [45] | 赛默飞世尔公司. 降钙素原检测试剂盒(时间分辨荧光免疫法)说明书[Z]. |
| [46] | Wu JY, Lee SH, Shen CJ, et al. Use of serum procalcitonin to detect bacterial infection in patients with autoimmune diseases: a systematic review and meta-analysis[J]. Arthritis Rheum, 2012, 64(9): 3034-3042. DOI:10.1002/art.34512 |
| [47] | Wu CW, Wu JY, Chen CK, et al. Does procalcitonin, C-reactive protein, or interleukin-6 test have a role in the diagnosis of severe infection in patients with febrile neutropenia? A systematic review and meta-analysis[J]. Support Care Cancer, 2015, 23(10): 2863-2872. DOI:10.1007/s00520-015-2650-8 |
| [48] | Schuetz P, Kutz A, Grolimund E, et al. Excluding infection through procalcitonin testing improves outcomes of congestive heart failure patients presenting with acute respiratory symptoms: results from the randomized ProHOSP trial[J]. Int J Cardiol, 2014, 175(3): 464-472. DOI:10.1016/j.ijcard.2014.06.022 |
| [49] | Meisner M, Lohs T, Huettemann E, et al. The plasma elimination rate and urinary secretion of procalcitonin in patients with normal and impaired renal function[J]. Eur J Anaesthesiol, 2001, 18(2): 79-87. DOI:10.1046/j.0265-0215.2000.00783.x |
| [50] | Dong R, Wan B, Lin S, et al. Procalcitonin and liver disease: a literature review[J]. J Clin Transl Hepatol, 2019, 7(1): 51-55. DOI:10.14218/jcth.2018.00012 |
| [51] | Avrillon V, Locatelli-Sanchez M, Folliet L, et al. Lung cancer may increase serum procalcitonin level[J]. Infect Disord Drug Targets, 2015, 15(1): 57-63. DOI:10.2174/1871526515666150320162950 |
| [52] | Maier M, Wutzler S, Lehnert M, et al. Serum procalcitonin levels in patients with multiple injuries including visceral trauma[J]. J Trauma, 2009, 66(1): 243-249. DOI:10.1097/ta.0b013e31817c966f |
| [53] | Yu CW, Juan LI, Hsu SC, et al. Role of procalcitonin in the diagnosis of infective endocarditis: a meta-analysis[J]. Am J Emerg Med, 2013, 31(6): 935-941. DOI:10.1016/j.ajem.2013.03.008 |
 2021, Vol. 30
2021, Vol. 30



