2. 苏州大学附属第一医院肾病内科 215006
1970年Thomas G. Baffes首次将体外膜肺氧合(extracorporeal membrane oxygenation,ECMO) 引入手术过程中的心肺支持,而后一直被用于循环手术及严重心源性休克的治疗。脓毒性休克(septic shock)的定义是脓毒症并发液体复苏无效的低血压或高乳酸血症。
目前美国危重医学会发布的指南建议液体和正性肌力药物支持效果不佳的难治性脓毒性休克的儿童和新生儿进行静脉动脉体外膜肺氧合(veno-arterial ECMO,V-A ECMO)[1]。最新的综述已经指出ECMO治疗的难治性脓毒性休克儿童的存活率有明显改善[2]。但是截至目前,使用ECMO治疗成人脓毒性休克的研究报道较少,本研究旨在使用Meta分析整合现有的ECMO治疗成人脓毒性休克的文献资料,找出与患者死亡有关的危险因素。
1 资料与方法 1.1 文献检索计算机检索PubMed、Embase、Web of Science、Cochrane library、知网、万方、中国生物医学文献数据库,检所时限为建库至2019年11月,英文检索方法为Extracorporeal Membrane Oxygenation,Sepsis的MeSH主题词,中文检索词为体外膜肺氧合,脓毒症或脓毒性休克。
1.2 文献纳入或排除标准文献的纳入标准:①入选患者均已确诊脓毒血症。②住院期间均使用ECMO,模式不限。③研究方法为随机对照研究、病例对照研究、队列研究。④发表语言不限。⑤年龄 > 16岁。⑥数据资料完整。排除标准:①无法获得全文或指标无法定量提取。②研究对象处于妊娠期。③分组方法非生存组/死亡组。④重复发表或文献质量较低。
1.3 资料提取包括文献第一作者、发表年份、发表的国家或地区、样本量;患者的性别、年龄、病史、ECMO模式、临床指标等。
1.4 文献质量评价RCT研究根据Cochrane系统评价手册5.0版本进行评价,队列研究及病例对照研究根据NOS量表进行评价,评价包含:疾病的定义和诊断是否恰当,病例是否具有代表性,对照组的定义及选取是否恰当,两组是否具有可比性,两组调查方法是否一致,应答率,暴露因素的调查和评估方法是否恰当,满分为9分,一般认为分数≥5分为高质量研究[3]。由2名研究者严格按照上述评价方法对文献质量进行评定,如遇分歧则由双方讨论或第三研究者裁定。
1.5 统计学方法采用Endnote进行文献管理,Revman 5.3统计软件进行Meta分析。对研究资料进行异质性检验,当I2≥50%或P < 0.1时采用随机效应模型合并资料,反之采用固定效应模型。研究设定生存组为对照组,死亡组为实验组。以P < 0.05为差异有统计学意义。
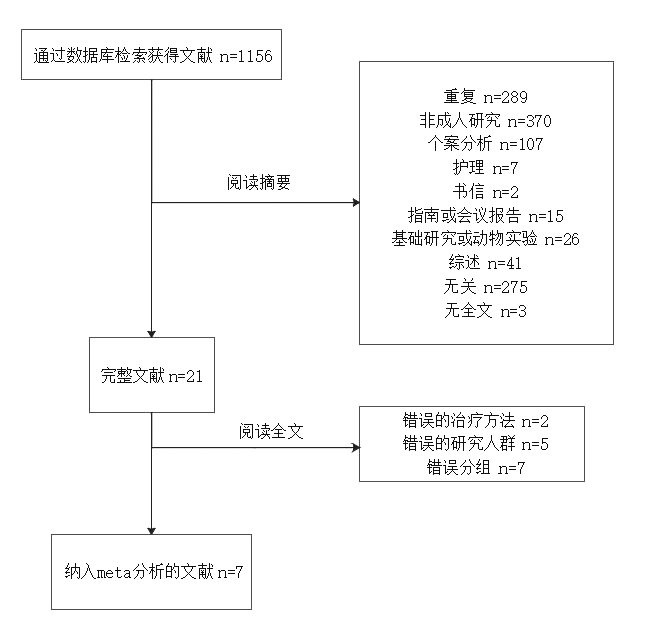
2 结果 2.1 文献检索结果共检索文献1 156篇,经过阅读摘要或全文后排除1 149篇,7篇完整文献纳入Meta分析。纳入的文献均为英文回顾性病例对照研究;发表时间2014—2019年;样本量8~151例,共计350例,其中男性229例,女性121例,生存患者89例,死亡患者261例,病死率36.08%~92.96%;发表地区均为亚洲。文献检索流程见图 1。纳入文献的基本资料见表 1。
|
| 图 1 文献检索及筛选流程图 |
|
|
| 第一作者 | 年份 | 样本量(例) | 生存/死亡(例) | 男性/女性(例) | 国家/地区 | 文献类型 | NOS评分 |
| Hyoung Soo Kim[4] | 2018 | 37 | 15/22 | 25/12 | 韩国 | 病例对照研究 | 6 |
| Sun Kyun Ro[5] | 2018 | 71 | 5/66 | 40/31 | 韩国 | 病例对照研究 | 5 |
| Taek Kyu Park[6] | 2014 | 32 | 7/25 | 21/11 | 韩国 | 病例对照研究 | 6 |
| Kyo Won Lee[7] | 2017 | 8 | 2/6 | 6/2 | 韩国 | 病例对照研究 | 4 |
| Aristine Cheng[8] | 2016 | 151 | 45/106 | 100/51 | 中国台湾 | 病例对照研究 | 6 |
| Lei Han[9] | 2019 | 23 | 5/18 | 14/9 | 中国 | 病例对照研究 | 5 |
| Myun Jin Choi[10] | 2016 | 28 | 10/18 | 23/5 | 韩国 | 病例对照研究 | 5 |
有1项研究报道年龄 > 75岁是患者死亡的独立危险因素[8]。而性别和体质量指数(body mass index,BMI)在纳入的七项研究中都没有显示出与患者死亡明显的相关性。Meta分析结果显示性别(OR=1.17,95%CI: 0.68~2.02,P=0.56)、年龄(OR=10.13,95%CI: -1.55~21.81,P=0.09)及BMI(OR=-0.95,95%CI: -2.53~0.63,P=0.24)均与使用ECMO治疗的脓毒性休克患者死亡无关。
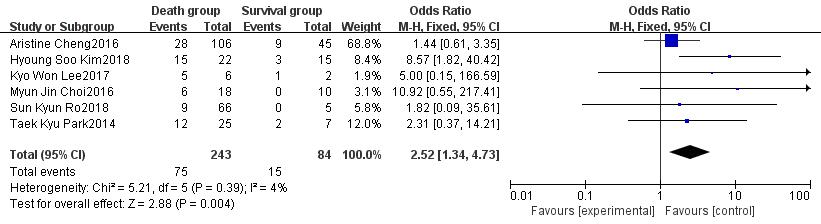
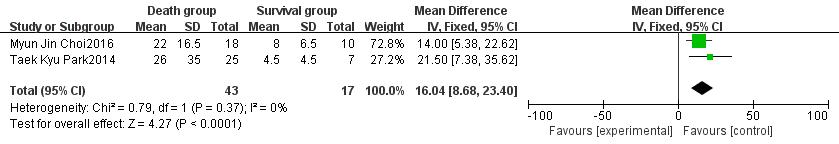
2.2.2 病史纳入的研究均未发现患者死亡与既往史,包括糖尿病(OR=0.99,95%CI: 0.55~180,P=0.98)、高血压病(OR=0.94,95%CI: 0.52~1.68,P=0.83)、慢性肾脏病(OR=0.38,95%CI: 0.11~1.34,P=0.13)有密切关系,但是涉及心脏骤停史的研究均指出心脏骤停是患者死亡的相关因素,其中有2项研究[6, 8]发现心脏骤停是患者死亡的独立危险因素,其中Park[6]的研究发现CPR的时长是患者死亡的独立危险因素。经文献合并后发现心脏骤停史(OR=2.52,95%CI: 1.34~4.73,P=0.004)与CPR时间(OR=16.04,95%CI: 8.68~23.4,P < 0.01)为患者死亡重要的危险因素,见图 2~3。
|
| 图 2 心脏骤停病史对ECMO治疗的脓毒性休克患者预后影响的森林图 |
|
|
|
| 图 3 CPR时间对ECMO治疗的脓毒性休克患者预后影响的森林图 |
|
|
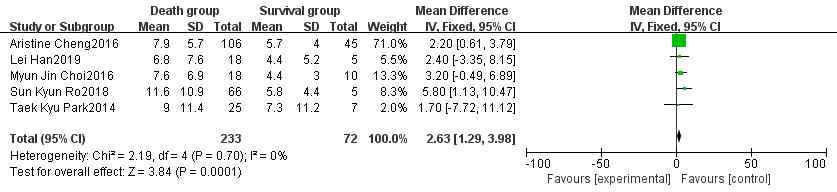
白细胞计数、肌酐、动脉血pH、乳酸均为ECMO使用前24 h内采血测得。其中Kim[4]的研究发现pH是患者死亡的独立危险因素,但经过文献合并后不支持该结果(OR=-0.09,95%CI: -2.99~2.80,P=0.95)。纳入分析的5项研究均发现乳酸水平与患者死亡密切相关,Meta分析的结果支持乳酸水平升高是脓毒性休克患者死亡的重要危险因素(OR=2.63,95%CI:1.29~3.98,P < 0.01),见图 4。而白细胞计数(OR=2.28,95%CI: -3.20~7.76,P=0.41)、肌酐水平(OR=0.21,95%CI: -0.66~1.07,P=0.64)与患者死亡无明显关联。
|
| 图 4 乳酸对ECMO治疗的脓毒性休克患者预后影响的森林图 |
|
|
纳入Meta分析的两项研究[4-5]均认为SAPSⅡ评分是患者死亡的独立危险因素,但是经合并后发现SAPSⅡ评分不是患者死亡的独立危险因素(OR=21.95,95%CI: -14.22~58.12,P=0.23)。有6项研究均发现SOFA评分与患者死亡相关,但经合并后不支持该结论(OR=1.13,95%CI: -0.33~2.59,P=0.13)。
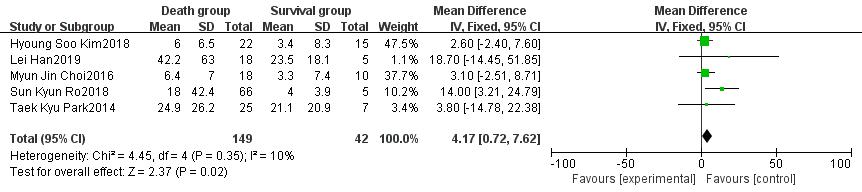
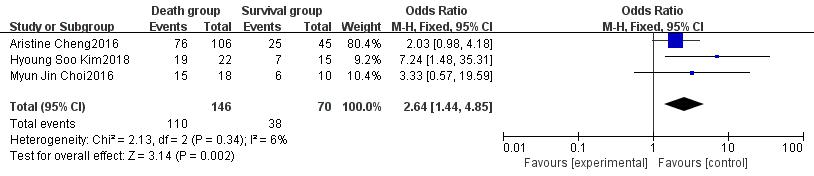
2.2.5 ECMO相关指标Cheng等[8]的研究发现患者发生休克至使用ECMO的时间与死亡密切相关,经合并后发现该时间为患者死亡的重要危险因素(OR=4.17,95%CI:0.72~7.62,P=0.02),见图 5。独立的研究和Meta分析都显示使用ECMO的时长与患者死亡无明显关联。有两项研究[8, 10]发现V-A模式是患者死亡的独立危险因素,经合并后支持该结果(OR=2.64,95%CI: 1.44~4.85,P=0.002),见图 6。
|
| 图 5 休克至使用ECMO时间对ECMO治疗的脓毒性休克患者预后影响的森林图 |
|
|
|
| 图 6 V-A模式对ECMO治疗的脓毒性休克患者预后影响的森林图 |
|
|
ECMO技术现在已经被公认是治疗儿童难治性脓毒性休克的有效手段[11],但是由于伦理学、并发症、费用以及预后等问题,ECMO技术在脓毒性休克的成人患者中的应用仍然存在争议[12]。本研究共纳入了7篇有关ECMO治疗成人脓毒性休克的完整文献,经Meta分析后发现乳酸水平、心脏骤停史、心肺复苏时间、休克至ECMO时间以及V-A模式与患者死亡密切相关,其中CPR时间是最重要的影响因素,而患者的一般情况(如性别、年龄、既往史以及BMI指数)与死亡结局无明显相关。
Kim等[4]的研究指出使用ECMO前的乳酸水平是患者住院期间死亡的独立危险因素,而这一指标也可以作为判断使用静脉静脉(V-V)模式治疗急性呼吸窘迫综合征的患者临床预后的工具[13]。Choi等[10]和Ro等[5]的研究也支持这一发现,同时他们还发现与心源性休克相比,脓毒性休克患者的乳酸水平更高。不仅如此,崔云等[14]的研究发现ECMO治疗的脓毒性休克患儿中,高乳酸血症或ECMO运转后高乳酸血症无明显改善的患儿预后较差,动态监测乳酸水平可以评估ECMO的治疗效果。既往研究显示,作为描述整体组织缺氧程度和持续时间的指标,连续测定乳酸水平随时间的变化或乳酸清除率在比乳酸绝对值更可靠[15],可以用于败血症至创伤等不同病理状态下的风险分层,未来的研究可以对此指标在ECMO治疗的脓毒性休克患者中的作用进行验证。
尽管作为高级生命支持手段的ECMO没有绝对的禁忌证[16],目前公认的不适宜采用ECMO治疗的合并症有播散性恶性肿瘤、高龄、移植物抗宿主病(graft-versus-host disease,GVHD)、重度脑损伤和持续时间较长的心脏骤停[17]。经过Meta分析后显示出有心脏骤停史及经历过较长的CPR术的患者预后更差,因此临床医生应该基于每个患者的不同情况合并既往的使用经验评估是否采用ECMO,以避免过度医疗和经济损失。
Lei等[9]发现休克至使用ECMO时间可以用于预测患者的病死率,Park等[6]报道,在脓毒性休克发生后超过30.5 h开始ECMO的患者均未存活。由于目前研究较少,对ECMO治疗脓毒性休克的时机尚无权威指南,无法得出一个相对正确的使用ECMO的时机[11]。Lee等[7]建议当患者存在组织器官灌注不足,不能维持平均动脉压在 > 65 mmHg(1 mmHg=0.133 kPa)的水平,并且输注大量儿茶酚胺后病情未见明显改善时,在排除其他因素后应该考虑尽早使用ECMO治疗。
本研究结果显示出V-A模式是患者死亡的危险因素,而既往共识中一般建议伴有严重血流动力学障碍的患者使用V-A模式,但也有专家指出由肺炎引起的脓毒性休克或由脓毒症引起的急性呼吸窘迫综合征患者应首选V-V模式[18]。当然,ECMO治疗成人脓毒性休克的资料目前还比较少,暂时无法断言V-A模式就是绝对适合的。V-A模式的ECMO治疗儿童脓毒性休克效果较好,这可以解释为年龄较小的儿童侵袭性链球菌和葡萄球菌感染的发生率较高,而使用VA-ECMO挽救的危及生命的葡萄球菌和链球菌感染与诱导脓毒性心肌病的数量始终超过非发酵革兰阴性菌和真菌感染[8]。因此,未来的研究要进一步研究VA-ECMO治疗脓毒性心肌病的结果与微生物学和病理生理学是否相关。使用ECMO治疗脓毒性休克的主要目的是改善组织灌注,而脓毒症是一个复杂且临床异质性较大的疾病,在使用过程中具体选择何种模式应该基于患者的病情进展、血流动力学以及氧合情况及时调整治疗方案。
本研究的局限性:①纳入Meta分析的文献均为回顾性病例对照研究,总体文献质量一般;②尽管实验室指标的采血时间点均为ECMO使用前24 h内,但脓毒性休克患者病情复杂、变化迅速,采血的具体时间和检验条件不统一可能造成一定程度上的偏倚;③脓毒性休克患者是否使用ECMO以及使用的时机是根据医生的临床经验或其他经济社会因素所决定,而非随机分组,可能影响结果的真实有效性;④目前世界范围内使用ECMO治疗脓毒性休克的研究较少,并且纳入分析的个别研究样本量较少,可能存在混杂因素的影响。因此本研究得出的结论仍需大型、多中心的随机对照试验进行验证。
综上所述,尽管本研究具有一定的局限性,但是可以提出潜在的研究方向。经过整合分析后发现乳酸水平、心脏骤停史、心肺复苏时间、休克至ECMO时间以及V-A模式与患者死亡密切相关,尤其是乳酸水平能够作为预测患者死亡的独立预测指标,在临床工作中具有一定的指导意义。在部分儿童的研究中已经发现ECMO与具体病原体相关,在深入研究后也许可以找出适合ECMO治疗的脓毒性休克患者。目前我国对于成人脓毒性休克患者采用ECMO治疗的研究较少,危险因素和预后都尚不明确,在不违背伦理学的情况下可以进行这一领域的临床研究。
利益冲突 所有作者均声明不存在利益冲突
| [1] | Davis AL, Carcillo JA, Aneja RK, et al. The American college of critical care medicine clinical practice parameters for hemodynamic support of pediatric and neonatal septic shock: Executive Summary[J]. Pediatr Crit Care Med, 2017, 45(6): 1061-1093. DOI:10.1097/PCC.0000000000001259 |
| [2] | Solé A, Jordan I, Bobillo S, et al. Venoarterial extracorporeal membrane oxygenation support for neonatal and pediatric refractory septic shock: more than 15 years of learning[J]. Eur J Pediatr, 2018, 177(8): 1191-1200. DOI:10.1007/s00431-018-3174-2 |
| [3] | 兰超, 许能媛, 吕青, 等. 体外膜肺氧合对非肺部原发性急诊危重症患者预后影响的Meta分析[J]. 中华急诊医学杂志, 2018, 27(9): 1019-1025. DOI:10.3760/cma.j.issn.1671-0282.2018.09.013 |
| [4] | Kim HS, Cheon DY, Ha SO, et al. Early changes in coagulation profiles and lactate levels in patients with septic shock undergoing extracorporeal membrane oxygenation[J]. J Thorac Dis, 2018, 10(3): 1418-1430. DOI:10.21037/jtd.2018.02.28 |
| [5] | Ro SK, Kim WK, Lim JY, et al. Extracorporeal life support for adults with refractory septic shock[J]. J Thorac Cardiovasc Surg, 2018, 156(3): 1104-1109. DOI:10.1016/j.jtcvs.2018.03.123 |
| [6] | Park TK, Yang JH, Jeon K, et al. Extracorporeal membrane oxygenation for refractory septic shock in adults[J]. Eur J Cardio - Thorac Surg, 2015, 47(2): e68-e74. DOI:10.1093/ejcts/ezu462 |
| [7] | Lee KW, Cho CW, Lee N, et al. Extracorporeal membrane oxygenation support for refractory septic shock in liver transplantation recipients[J]. Ann Surg Treat Res, 2017, 93(3): 152-158. DOI:10.4174/astr.2017.93.3.152 |
| [8] | Cheng A, Sun HY, Tsai MS, et al. Predictors of survival in adults undergoing extracorporeal membrane oxygenation with severe infections[J]. J Thorac Cardiovasc Surg, 2016, 152(6): 1526-1536. DOI:10.1016/j.jtcvs.2016.08.038 |
| [9] | Han L, Zhang Y, Zhang YH, et al. Risk factors for refractory septic shock treated with VA ECMO[J]. Ann Transl Med, 2019, 7(18): 476. DOI:10.21037/atm.2019.08.07 |
| [10] | Choi MJ, Ha SO, Kim HS, et al. The simplified acute physiology score Ⅱ as a predictor of mortality in patients who underwent extracorporeal membrane oxygenation for septic shock[J]. Ann Thorac Surg, 2017, 103(4): 1246-1253. DOI:10.1016/j.athoracsur.2016.07.069 |
| [11] | 崔云, 张育才. 儿童难治脓毒性休克, ECMO挽救性治疗的难点与探索[J]. 中华急诊医学杂志, 2019, 28(6): 669-672. DOI:10.3760/cma.j.issn.1671-0282.2019.06.003 |
| [12] | Gabel E, Gudzenko V, Cruz D, et al. Successful use of extracorporeal membrane oxygenation in an adult patient with toxic shock-induced heart failure[J]. J Intensive Care Med, 2015, 30(2): 115-118. DOI:10.1177/0885066613517069 |
| [13] | Bonizzoli M, Lazzeri C, Cianchi G, et al. Serial lactate measurements as a prognostic tool in venovenous extracorporeal membrane oxygenation support[J]. Ann Thorac Surg, 2017, 103(3): 812-818. DOI:10.1016/j.athoracsur.2016.06.087 |
| [14] | 崔云, 王斐, 任玉倩, 等. 静脉-动脉型体外膜肺氧合治疗儿童难治脓毒性休克的临床疗效观察[J]. 中华急诊医学杂志, 2019, 28(6): 697-701. DOI:10.3760/cma.j.issn.1671-0282.2019.06.008 |
| [15] | Riveiro DFM, de Oliveira VM, Braunner JS, et al. Evaluation of serum lactate, central venous saturation, and venous-arterial carbon dioxide difference in the prediction of mortality in postcardiac arrest syndrome[J]. J Intensive Care Med, 2016, 31(8): 544-552. DOI:10.1177/0885066615592865 |
| [16] | Ventetuolo CE, Muratore CS. Extracorporeal life support in critically ill adults[J]. Am J Respir Crit Care Med, 2014, 190(5): 497-508. DOI:10.1164/rccm.201404-0736CI |
| [17] | Marasco SF, Lukas G, McDonald M, et al. Review of ECMO (extra corporeal membrane oxygenation) support in critically ill adult patients[J]. Heart Lung Circ, 2008, 17(Suppl 4): S41-S47. DOI:10.1016/j.hlc.2008.08.009 |
| [18] | Bréchot N, Luyt CE, Schmidt M, et al. Venoarterial extracorporeal membrane oxygenation support for refractory cardiovascular dysfunction during severe bacterial septic shock[J]. Crit Care Med, 2013, 41(7): 1616-1626. DOI:10.1097/ccm.0b013e31828a2370 |
 2021, Vol. 30
2021, Vol. 30




