急性心力衰竭(acute heart failure,AHF)是在原有心脏结构或功能异常基础上出现的以急性呼吸困难及外周水肿为主要表现的急危重症,包括急性起病和慢性心力衰竭急性失代偿,其预后极差,住院病死率及5年病死率分别为3%、60%,6个月急诊就诊与急诊再住院率达50%[1-2]。虽然目前已有一些评估预后的指标及方法,比如血清可溶性ST2[3]、血浆利钠肽水平、超声心动图、心功能分级,但其应用各有其局限性。近一半的AHF患者入院时血糖水平升高,研究发现应激性高血糖、合并糖尿病者的血糖水平急剧变化是危重症患者死亡的独立危险因素[4-5]。入院即刻血糖水平和AHF患者预后有关[4, 6-7],但结论并不完全一致。Capes等[8]发现心肌梗死患者应激性血糖升高的预后作用与基础血糖水平相关,其在非糖尿病心肌梗死患者中可以预测心力衰竭的发生,这提示急性期血糖水平评估预后时应校正基线血糖水平。2015年Roberts等[9]首次提出了评估应激状态血糖的新参数,即应激性血糖升高比值(stress hyperglycemia ratio,SHR),是由入院即刻血糖和糖化血红蛋白(glycosylated hemoglobin,HbA1c)通过数学模型计算所得的数值。SHR校正了基线血糖水平,用于评估应激时血糖相对升高的比例,其在预测疾病危重程度时比单纯血糖水平更有价值。但目前关于SHR的研究仅在急性心肌梗死、急诊冠状动脉支架植入术及脑卒中取栓术后患者中[10-12],对AHF患者鲜有研究,本文初步探讨其与AHF患者预后的关系。
1 资料与方法 1.1 纳入及排除标准回顾性纳入2016年12月至2019年1月在上海交通大学附属第六人民医院急诊科住院的AHF患者。纳入标准:⑴根据《中国心力衰竭诊断和治疗指南2018》[1]及《中国急性心力衰竭急诊临床实践指南2017》[13]诊断为AHF,诊断依据如下:患者有基础心血管疾病史,此次入院表现为劳力性呼吸困难或阵发性夜间呼吸困难或端坐呼吸或咳粉红色泡沫痰,查体可及肺部湿啰音或哮鸣音、舒张早期或中期奔马律、颈静脉充盈或肝颈静脉反流、下肢水肿,实验室检查可见B型钠尿肽或N末端B型利钠肽原(N-terminal prohormone of brain natriuretic peptide,NT-proBNP)升高,胸片及超声心动图可见心脏扩大、胸腔积液,心电图可有各种异常表现;⑵年龄≥18岁。排除标准:⑴入院首次血肌酐 > 180 mmol/L或既往接受血液透析或腹膜透析或肾脏移植患者;⑵入院首次血红蛋白 < 100 g/L;⑶合并重症肺炎、脓毒症、感染性休克、晚期恶性肿瘤;⑷年龄 > 100岁或 < 18岁。
1.2 一般资料由同一组医生详细采集病史,收集相关资料,主要包括:⑴一般信息:姓名、年龄、性别、糖尿病史;⑵原发疾病:是否有高血压、冠状动脉粥样硬化心脏病(简称冠心病)、慢性阻塞性肺疾病、结构性心脏病包括先天性心脏病、心脏瓣膜病、心肌病[14];⑶此次发病诱因(感染、心律失常、电解质紊乱、补液速度过快或脱水等)、症状、体征及辅助检查结果;⑷既往心血管疾病用药情况、入院心功能纽约(New York Heart Association,NYHA)分级、住院天数及出院病情转归等。
1.3 检测及计算方法所有检验均由本院检验中心检测,入院即刻血糖由入院后即刻肘静脉血经酶法测定,入院次晨空腹肘静脉血酶法测定血肌酐,比色法测定血红蛋白,化学发光法测定血浆NT-proBNP,离子交换层析高压液相分离法测定HbA1c,所有试剂盒均由相应检测仪器公司提供,均达到上海市临床检验质量控制要求。入院1周内由同一组经验丰富的心脏超声医师行心脏超声检查,采用西门子公司的Sequoia 512彩色多普勒超声仪,用Simpson双平面法测定左心室射血分数(left ventricular ejection fraction,LVEF)。SHR=入院即刻血糖(mmol/L)/[(1.59×HbA1c)-2.59]。本研究经上海交通大学附属第六人民医院伦理委员会审查通过,审批编号为:2020-KY-021(K)。
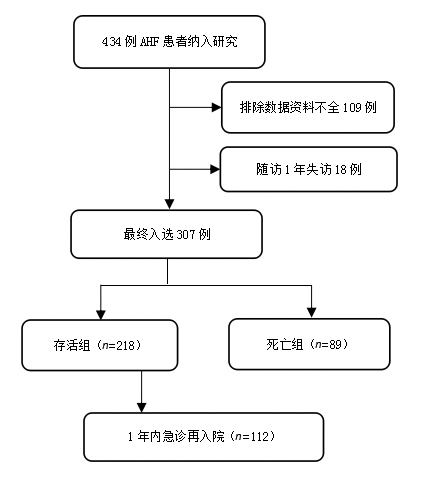
1.4 观察结局采用电话随访,随访时间为入院当日起1年,主要观察指标:死亡(其中在院死亡定义为1年内死亡);次要观察指标:因心血管疾病急诊就诊或者急诊再住院,简称为急诊再入院,主要观察指标和次要观察指标统称为总体事件。研究流程见图 1。
|
| 图 1 研究流程图 Fig 1 Research process |
|
|
采用SPSS 23.0统计软件对实验数据进行统计学分析。定量资料进行正态性检验,符合正态分布的定量资料以均数±标准差(Mean±SD)表示,组间比较采用独立样本t检验;不符合正态分布的定量资料以中位数(四分位数)[M(QL, QU)]表示,组间比较采用非参数检验。定性资料以频数(百分比)表示,组间比较采用χ2检验。将单因素分析有意义的指标纳入多因素Logistic回归分析筛选影响患者预后的独立危险因素。以1年内死亡为终点事件,采用Kaplan-Meier法绘制生存曲线,log-rank法比较组间生存曲线是否有差异。以P < 0.05为差异有统计学意义。
2 结果 2.1 基线数据及人口学特点本研究收集符合要求的AHF患者307例,男性153例(47.1%),年龄(79.58±10.94)岁。结构性心脏病包括风湿性心脏病5例(29.4%)、二尖瓣脱垂2例(11.7%)、主动脉缩窄1例(5.9%)、扩张型心肌病6例(35.3%)、肥厚型心肌病3例(17.7%)。发病诱因中其他包括外科手术3例(18.7%)、糖尿病酮症酸中毒5例(31.3%)、甲状腺功能亢进2例(12.5%)、酒精中毒4例(25.0%)、负性肌力药物2例(12.5%)。存活组和死亡组基线资料的比较见表 1。
| 指标 | 总人数 (n=307) |
存活组 (n=218) |
死亡组 (n=89) |
P值 |
| 年龄(岁) a | 83(74, 87) | 82(72, 86) | 84(78, 88) | 0.011 |
| 男性(例, %) | 153(47.1) | 110(50.5) | 34(38.2) | 0.051 |
| 体质量指数(kg/m2) a | 23.44 (21.76, 24.97) |
23.44 (21.76, 24.91) |
23.36 (21.23, 26.04) |
0.536 |
| 糖尿病(例, %) | 129(39.7) | 92(42.2) | 31(34.8) | 0.232 |
| 原发疾病(例, %) | ||||
| 冠心病 | 142(43.7) | 96(44.0) | 37(41.6) | 0.693 |
| 慢性阻塞性肺疾病 | 50(15.4) | 35(16.1) | 13(14.6) | 0.751 |
| 高血压 | 216(66.5) | 146(67.0) | 58(65.2) | 0.761 |
| 结构性心脏病 | 17(5.2) | 9(4.1) | 7(7.9) | 0.181 |
| 发病诱因(例, %) | ||||
| 感染 | 225(68.8) | 152(69.7) | 63(70.8) | 0.854 |
| 心律失常 | 122(37.3) | 82(37.6) | 33(37.1) | 0.930 |
| 血容量急剧变化及电解质紊乱 | 82(25.2) | 59(27.1) | 23(25.8) | 0.826 |
| 急性心肌梗死 | 11(3.4) | 6(2.8) | 5(5.6) | 0.220 |
| 其他 | 16(4.9) | 10(4.6) | 6(6.7) | 0.441 |
| 入院前用药情况(例, %) | ||||
| 阿司匹林 | 278(85.5) | 188(86.2) | 74(83.1) | 0.487 |
| 口服洋地黄 | 57(17.5) | 35(16.1) | 17(19.1) | 0.519 |
| ACEI/ARB | 299(92.0) | 204(93.6) | 81(91.0) | 0.429 |
| 利尿剂 | 308(94.8) | 210(96.3) | 87(97.8) | 0.524 |
| β受体阻滞剂 | 172(52.9) | 113(51.8) | 44(49.4) | 0.703 |
| 入院血流动力学情况 | ||||
| 心率(次/min) a | 81(75, 95) | 80(76, 93) | 85(74, 96) | 0.317 |
| 收缩压(mmHg) a | 137(120, 149) | 135(118, 147) | 140(131, 152) | 0.412 |
| LVEF (%) a | 55(42, 63) | 58(44, 64) | 53(45, 57) | 0.046 |
| LVEF < 40%(例, %) | 69(21.2) | 51(23.4) | 16(18.0) | 0.297 |
| 入院心功能分级(例, %) | ||||
| NYHA Ⅰ级 | 24(7.4) | 12(5.5) | 4(4.5) | 0.718 |
| NYHA Ⅱ级 | 118(36.3) | 80(36.7) | 32(36.0) | 0.902 |
| NYHA Ⅲ级 | 113(34.8) | 79(36.2) | 32(36.0) | 0.903 |
| NYHA Ⅳ级 | 70(21.5) | 47(21.6) | 21(23.6) | 0.697 |
| 入院实验室指标 | ||||
| SHRa | 1.04(0.87, 1.29) | 1.02(0.86, 1.27) | 1.11(0.91, 1.51) | 0.011 |
| 血糖(mmol/L) a | 7.4(6.2, 11.3) | 7.4(6.3, 10.8) | 7.6(6.2, 12.2) | 0.570 |
| 血红蛋白(g/L) a | 125(111, 136) | 126(111, 137) | 121(111, 132) | 0.237 |
| 肌酐(μ mol/L) a | 90(69, 119) | 90(66, 118) | 93(76, 125) | 0.188 |
| NT-proBNP (μ g/L) a | 4 293 (2 173, 8 273) | 4 243 (2 294, 7 565) | 5 351 (2 098, 14 039) | 0.043 |
| 注:a为M(QL,QU);P值表示存活组与死亡组间基本资料比较;ACEI为血管紧张素转化酶抑制剂,ARB为血管紧张素受体阻滞剂,LVEF为左心室射血分数,NYHA为入院心功能纽约分级;SHR为入院即刻血糖;NT-proBNP为N末端B型利钠肽原 | ||||
以AHF患者1年内死亡事件为因变量,将在单因素分析中具有统计意义的指标纳入协变量,包括年龄、SHR水平、NT-proBNP、LVEF,发现SHR(OR=2.397,95%CI:1.285~4.47,P < 0.05)是患者1年内死亡的独立危险因素,回归系数为0.874。LVEF(OR=0.070,95%CI:0.044~0.996,P < 0.05)为保护性因素,见表 2。
| 因素 | β | S.E. | OR | 95%CI | P值 |
| 年龄 | 0.028 | 0.015 | 1.028 | 0.998~1.060 | 0.070 |
| SHR | 0.874 | 0.318 | 2.397 | 1.285~4.471 | 0.006 |
| NT-proBNP | 0.000 | 0.000 | 1.000 | 1.000~1.000 | < 0.01 |
| LVEF | -0.029 | 0.013 | 0.070 | 0.044~0.996 | 0.021 |
| 注:SHR为入院即刻血糖;NT-proBNP为N末端B型利钠肽原;LVEF为左心室射血分数 | |||||
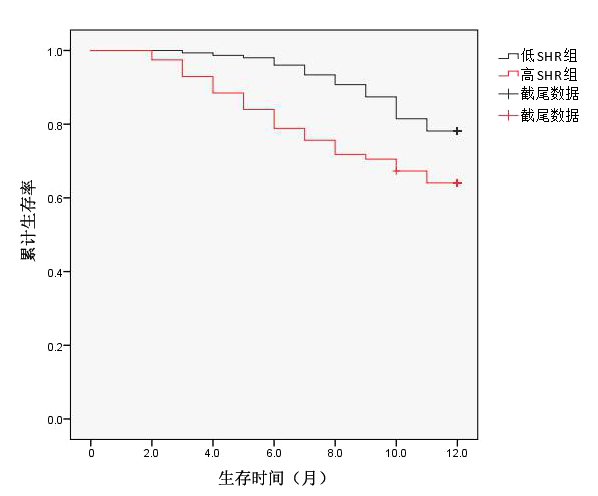
根据SHR中位数将患者分为低SHR组(SHR≤1.04)和高SHR组(SHR > 1.04),绘制Kaplan-Meier生存曲线,高SHR组生存率低于低SHR组,差异有统计学意义,见图 2。低SHR组及高SHR组间患者总体事件及死亡事件差异有统计学意义(P < 0.05),急诊再入院组间差异无统计学意义(P > 0.05)。
|
| log-rank,P=0.002,χ2=9.461 图 2 SHR中位数分组生存曲线 Fig 2 SHR median grouping Kaplan-Meier survival curve |
|
|
本研究探讨SHR对AHF患者1年内死亡事件的预测价值,发现SHR能预测危重的AHF患者,是AHF患者1年内死亡的独立危险因素。
人体受到应激时会产生皮质醇激素,如肾上腺素和儿茶酚胺等,这些激素均为升糖激素,使血糖短时间内急剧升高,且创伤及应激程度越大,激素分泌水平越高,血糖水平也越高。应激性血糖升高的目的是对机体起保护作用,但事实上过度的高血糖产生大量游离脂肪酸加剧氧化应激及细胞内皮损伤,并通过破坏钙稳态、激活内源性凝血途径、升高胰高血糖素水平、心肌再灌注损伤、细胞内酸中毒等途径对心肌产生毒害作用,并同时反过来使皮质醇激素水平升高,再次升高血糖[15-20]。
入院即刻血糖水平和AHF的预后关系已有报道,但是入院即刻血糖水平对疾病的预后价值与基础血糖水平有关[8],既往关于AHF的研究忽略了基础血糖水平对结果的影响。入院时的高血糖可能是应激性的,也可能是糖尿病长期血糖未控制的结果。一项纳入50 532例患者的随访时间为1年的回顾性研究中发现入院即刻血糖水平升高与老年AHF患者预后不相关[7],该研究排除了65岁以下的人群,平均年龄为79.4岁。另外一项多中心的研究中亚洲及非洲人种的入院即刻血糖水平升高与30 d病死率无明显相关性[5]。本研究中研究对象年龄(79.58±10.94)岁,结果提示SHR是AHF患者不良预后的独立危险因素。SHR调整了基线血糖水平对入院即刻血糖的影响,反映了真正的应激性高血糖对疾病的预后价值。本研究根据中位数水平分组进行生存分析,结果显示SHR水平 > 1.04时患者1年内累积生存率高于SHR水平≤1.04组,差异有统计学意义,但本研究是单中心研究,SHR评估AHF患者预后的临界值仍需进一步随机对照试验反复验证。
AHF患者预后的预测指标较多,包括患者的年龄和性别、LVEF、是否合并结构性心脏病、入院时心功能NYHA分级、血浆利钠肽水平及基础治疗情况等。心力衰竭与糖尿病互为危险因素,本研究中39.7%的AHF患者合并糖尿病,尚有一部分为诊断的糖尿病或糖耐量异常患者混杂在内。一项中位随访时间为895 d的日本研究发现AHF患者再入院率在90 d内最高,并且90 d再入院事件组生存率低于90 d无再入院事件组,组间Kaplan-Meier曲线分析差异有统计学意义(log-rank, P < 0.01)[21]。本研究发现SHR是AHF患者1年内死亡的独立危险因素,这可能是由于患者交感神经更容易兴奋,引发了一系列机体应激性反应,其中一项即是血糖升高,其衡量指标可能为SHR。应激反应过激通过一系列机制,包扩交感系统、肾素-血管紧张素-醛固酮系统、炎症系统等破坏内环境稳态,部分应激反应强烈的患者反复急诊入院,最终影响1年内生存率,但具体机制仍需进一步研究。
综上所述,SHR由HbA1c和入院即刻血糖计算而来,此指标简单易得且能快速检测,是能对AHF患者进行早期危险度分层的预警指标。血糖是一个临床上比较容易干预的指标,但尚不清楚如何从触发机制干预使高危的AHF患者从中受益,因此有待进一步研究。
利益冲突 所有作者均声明不存在利益冲突
| [1] | 中华医学会心血管病学分会心力衰竭学组, 中国医师协会心力衰竭专业委员会, 中华心血管病杂志编辑委员会. 中国心力衰竭诊断和治疗指南2018[J]. 中华心血管病杂志, 2018, 46(10): 760-789. DOI:10.3760/cma.j.issn.0253-3758.2018.10.004 |
| [2] | Olchanski N, Vest AR, Cohen JT, et al. Two-year outcomes and cost for heart failure patients following discharge from the hospital after an acute heart failure admission[J]. Int J Cardiol, 2020, 307: 109-113. DOI:10.1016/j.ijcard.2019.10.033 |
| [3] | 胡振, 张新超, 张堃, 等. 血清可溶性ST2评价老年急性心力衰竭患者病情与预后的研究[J]. 中华急诊医学杂志, 2016, 25(8): 1035-1040. DOI:10.3760/cma.j.issn.1671-0282.2016.08.014 |
| [4] | Targher G, Dauriz M, Laroche C, et al. In-hospital and 1-year mortality associated with diabetes in patients with acute heart failure: results from the ESC-HFA Heart Failure Long-Term Registry[J]. Eur J Heart Fail, 2017, 19(1): 54-65. DOI:10.1002/ejhf.679 |
| [5] | Mebazaa A, Gayat E, Lassus J, et al. Association between elevated blood glucose and outcome in acute heart failure: results from an international observational cohort[J]. J Am Coll Cardiol, 2013, 61(8): 820-829. DOI:10.1016/j.jacc.2012.11.054 |
| [6] | Chen YY, Chen Y, Liang SM, et al. Prognostic impact of fasting plasma glucose on mortality and Re-hospitalization in patients with acute heart failure[J]. Chin Med J (Engl), 2018, 131(17): 2032-2040. DOI:10.4103/0366-6999.239310 |
| [7] | Kosiborod M, Inzucchi SE, Spertus JA, et al. Elevated admission glucose and mortality in elderly patients hospitalized with heart failure[J]. Circulation, 2009, 119(14): 1899-1907. DOI:10.1161/circulationaha.108.821843 |
| [8] | Capes SE, Hunt D, Malmberg K, et al. Stress hyperglycaemia and increased risk of death after myocardial infarction in patients with and without diabetes: a systematic overview[J]. Lancet, 2000, 355(9206): 773-778. DOI:10.1016/S0140-6736(99)08415-9 |
| [9] | Roberts GW, Quinn SJ, Valentine N, et al. Relative hyperglycemia, a marker of critical illness: introducing the stress hyperglycemia ratio[J]. J Clin Endocrinol Metab, 2015, 100(12): 4490-4497. DOI:10.1210/jc.2015-2660 |
| [10] | 夏智丽, 高程洁, 高亚洁, 等. 应激性血糖升高比值对急性心肌梗死患者预后的评估价值[J]. 上海交通大学学报(医学版), 2019, 39(3): 309-315. DOI:10.3969/j.issn.1674-8115.2019.03.016 |
| [11] | Chen X, Liu Z, Miao J, et al. High stress hyperglycemia ratio predicts poor outcome after mechanical thrombectomy for ischemic stroke[J]. J Stroke Cerebrovasc Dis, 2019, 28(6): 1668-1673. DOI:10.1016/j.jstrokecerebrovasdis.2019.02.022 |
| [12] | Yang Y, Kim TH, Yoon KH, et al. The stress hyperglycemia ratio, an index of relative hyperglycemia, as a predictor of clinical outcomes after percutaneous coronary intervention[J]. Int J Cardiol, 2017, 241: 57-63. DOI:10.1016/j.ijcard.2017.02.065 |
| [13] | 中国医师协会急诊医师分会, 中国心胸血管麻醉学会急救与复苏分会. 中国急性心力衰竭急诊临床实践指南(2017)[J]. 中华急诊医学杂志, 2017, 26(12): 1347-1357. DOI:10.3760/cma.j.issn.1671-0282.2017.12.003 |
| [14] | 朱鲜阳, 肖家旺. 结构性心脏病认识与进展[J]. 中国实用内科杂志, 2013, 33(4): 256-258. |
| [15] | Ceriello A, Giacomello R, Stel G, et al. Hyperglycemia-induced thrombin formation in diabetes. The possible role of oxidative stress[J]. Diabetes, 1995, 44(8): 924-928. DOI:10.2337/diab.44.8.924 |
| [16] | Zhang JW, Zhou YJ, Cao SJ, et al. Impact of stress hyperglycemia on in-hospital stent thrombosis and prognosis in nondiabetic patients with ST-segment elevation myocardial infarction undergoing a primary percutaneous coronary intervention[J]. Coron Artery Dis, 2013, 24(5): 352-356. DOI:10.1097/MCA.0b013e328361a942 |
| [17] | Harp JB, Yancopoulos GD, Gromada J. Glucagon orchestrates stress-induced hyperglycaemia[J]. Diabetes Obes Metab, 2016, 18(7): 648-653. DOI:10.1111/dom.12668 |
| [18] | Mifsud S, Schembri EL, Gruppetta M. Stress-induced hyperglycaemia[J]. Br J Hosp Med (Lond), 2018, 79(11): 634-639. DOI:10.12968/hmed.2018.79.11.634 |
| [19] | Luitse MJ, Biessels GJ, Rutten GE, et al. Diabetes, hyperglycaemia, and acute ischaemic stroke[J]. Lancet Neurol, 2012, 11(3): 261-271. DOI:10.1016/s1474-4422(12)70005-4 |
| [20] | Capes SE, Hunt D, Malmberg K, et al. Stress hyperglycemia and prognosis of stroke in nondiabetic and diabetic patients: a systematic overview[J]. Stroke, 2001, 32(10): 2426-2432. DOI:10.1161/hs1001.096194 |
| [21] | Ishihara S, Kawakami R, Nogi M, et al. Incidence and clinical significance of 30-day and 90-day rehospitalization for heart failure among patients with acute decompensated heart failure in Japan- From the NARA-HF Study[J]. Circ J, 2019, 84(2): 194-202. DOI:10.1253/circj.CJ-19-0620 |
 2021, Vol. 30
2021, Vol. 30




