相对于神经损伤,急性一氧化碳中毒(acute carbon monoxide poisoning,ACOP)心肌损伤因其隐匿性,且大多呈可逆性过程等特点而被忽视[1],但临床中时常遇到ACOP出现新发严重心律失常、急性心力衰竭、心肌梗死甚至猝死等心血管不良事件[2],故探寻可早期预测ACOP心肌损伤患者院内心血管不良事件的指标具有临床意义。早期研究显示,ACOP的心血管系统损伤呈两个高峰,第一个为中毒即刻,一氧化碳(CO)对心肌的直接和或间接毒性作用,第二个为中毒后3 d,与再灌注损伤有关[3]。后续病理生理研究表明[4],早期中毒缺氧及后续“缺血-再灌注”过程均可激活炎症细胞,从而引起炎症性损伤。中性粒细胞/淋巴细胞比值(neutrophil/lymphocyte ratio,NLR)是近年研究较多的反映炎症的标志物,多项研究证实NLR可作为预测心血管事件的潜在生物标志物[5-6];可溶性生长刺激表达基因2蛋白(soluble growth stimulating expression gene 2 protein,sST2)作为可同时反映炎症、纤维化和心肌应激的标志物被广泛研究,对急性冠脉综合征、心力衰竭、脓毒症等不良预后预测价值肯定[7-9]。本研究旨在通过前瞻性观察性研究探究sST2联合NLR在预测ACOP心肌损伤患者发生院内心血管不良事件的价值,进而对ACOP心肌损害的早期监测和干预提供一定帮助。
1 资料与方法 1.1 一般资料采用前瞻性队列研究方法,选择2017年1月至2019年12月于河北医科大学哈励逊国际和平医院急诊病房及EICU收治的ACOP合并心肌损伤的患者。纳入标准:急性中重度CO中毒诊断符合GBZ23-2002《职业性急性一氧化碳中毒诊断标准》[10],ACOP心肌损伤诊断参照GBZ74-2002《职业性急性化学物中毒性心脏病诊断标准》,(1)有明确的CO接触史;(2)出现昏迷症状;⑶入院3 h cTnl阳性;⑷发病24 h内入院。排除标准:(1)年龄 < 18岁;⑵于就诊时即存在急性肺水肿、心源性休克、心房颤动、阵发性室上性心动过速、室性心动过速、房室传导阻滞、室颤等心血管不良事件;⑶存在类风湿性关节炎、系统性红斑狼疮、强直性脊柱炎等自身免疫性疾病,3个月内应用过免疫抑制药物治疗;⑷冠心病、心肌病、慢性心功能不全;⑸存在支气管哮喘、慢性阻塞性肺疾病、肺间质纤维化;(6)存在血液系统疾病;⑺入院时合并严重感染;⑻恶性肿瘤。
1.2 研究分组方法以患者入院作为研究起点,以院内心血管不良事件为临床观察终点。根据是否发生心血管不良事件,分为事件组和无事件组。院内心血管不良事件定义为:严重心律失常、心力衰竭、心绞痛及心肌梗死样改变、心源性休克、心搏骤停、全因死亡,其中严重心律失常定义为:入院后新出现的包括心电监护仪或心电图记录到的房颤、阵发性室上性心动过速、室速、室颤、房室传导阻滞;同时或相继发生两种或以上事件者不重复记录。本研究符合医学伦理学标准,经本院伦理委员会审查批准(2017-1-008),所有检测及治疗均获得患者或家属的知情同意。
1.3 治疗方法所有患者均给予心电监测、吸氧、高压氧治疗,不能行高压氧治疗者给予间断呼吸机辅助纯氧吸入,防治脑水肿、营养心肌等综合治疗。
1.4 样本采集与检测入院时抽取静脉血,查血常规检测中性粒细胞计数、淋巴细胞计数,计算NLR=中性粒细胞/淋巴细胞;于入院时、入院3 d时抽2 mL肘静脉血于促凝管内,送中心实验室应用酶联免疫吸附法(ELISA)检测sST2,采用上海瑞缔生物科技有限公司检测试剂盒,可精确检测 > 1.8 ng/mL范围sST2水平。对于夜间标本不能及时送检者,置于冰箱冷藏室保存。
1.5 观察指标采集患者性别、年龄、昏迷时间,高血压、糖尿病等既往病史资料,是否行气管插管,入院时急性生理与慢性健康状况评分(APACHEⅡ评分),抽静脉血3 mL送生化室检测入院时乳酸(Lac)、肌钙蛋白Ⅰ(cTNI)、肌酸激酶同工酶(CK-MB)、肌酸激酶(CK)、N末端脑钠肽前体(NT-proBNP)水平。
1.6 统计学方法采用SPSS 21.0软件进行统计学分析。采用非参数Kolmogorov-Smirnov检验进行正态性评价,计量资料以均数±标准差(Mean±SD)表示,组间比较采用t检验;计数资料采用χ2检验;采用二元logistic回归分析院内心血管不良事件的危险因素;对心血管不良事件预测价值的评价使用受试者工作曲线(ROC曲线),最佳临界值的选择由约登指数计算得出。以P < 0.05为差异有统计学意义。
2 结果 2.1 事件组与无事件组基本资料比较255例ACOP心肌损伤患者被纳入最终分析,男性146例,女性109例,年龄35~85岁,(62.25±11.29)岁;事件组29例,发生率11.37%,其中新发生心房颤动6例且均需药物干预,室性心动过速2例,心力衰竭11例,猝死6例,多脏器功能衰竭致死亡2例,胸痛发作症状伴心肌梗死样心电图改变2例。事件组昏迷时间长于无事件组(P < 0.05)、APACHEⅡ评分显著高于无事件组(P < 0.01);两组性别、年龄、气管插管率、高血压、基础糖尿病差异无统计学意义(均P > 0.05),见表 1。
| 指标 | 无事件组 (n=226) |
事件组 (n=29) |
t/χ2值 | P值 |
| 年龄(岁, Mean±SD) | 62.17±11.39 | 62.86±10.63 | 0.309 | 0.758 |
| 男性(例,%) | 127(56.2) | 19(65.5) | 0.913 | 0.226 |
| 昏迷时间(h, Mean±SD) | 9.21±8.92 | 12.97±9.60 | 2.115 | 0.035 |
| APACHEⅡ评分(Mean±SD) | 13.19±4.56 | 15.55±3.54 | 2.682 | 0.008 |
| 气管插管(例,%) | 24(10.6) | 3(10.3) | 0.002 | 0.631 |
| 高血压(例,%) | 92(40.7) | 17(58.6) | 3.370 | 0.075 |
| 糖尿病(例,%) | 54(23.9) | 9(31.0) | 0.705 | 0.265 |
两组cTNI、NLR、Lac、T3dsST2差异有统计学意义(P < 0.05),T0sST2、CK、CK-MB、NT-proBNP差异无统计学意义(P > 0.05),见表 2。
| 指标 | 无事件组 (n=226) |
事件组 (n=29) |
t值 | P值 |
| cTNI (ng/mL) | 0.46±0.24 | 0.84±0.36 | 2.440 | 0.015 |
| CK (U/L) | 2 774.40±505.7 | 4 038.07±695.64 | 1.205 | 0.229 |
| CK-MB (U/L) | 73.33±9.73 | 101.62±10.31 | 1.464 | 0.144 |
| NT-proBNP (pg/mL) | 1 885.55±319.06 | 2 323.52±289.07 | 0.703 | 0.483 |
| Lac (mmol/L) | 2.41±1.36 | 2.94±1.31 | 1.978 | 0.049 |
| NLR | 9.57±4.22 | 13.38±4.33 | 4.569 | < 0.01 |
| T0sST2 (ng/mL) | 242.43±93.09 | 265.34±89.95 | 0.969 | 0.333 |
| T3dsST2 (ng/mL) | 40.52±13.14 | 61.59±22.67 | 7.363 | < 0.01 |
| 注:cTNI,肌钙蛋白Ⅰ;CK,肌酸激酶;CK-MB,肌酸激酶同工酶;NT-proBNP,N末端脑钠肽前体;Lac,乳酸;NLR,中性粒细胞/ 淋巴细胞比值;T0sST2,入院时可溶性生长刺激表达基因2蛋白;T3dsST2,入院3天时可溶性生长刺激表达基因2蛋白 | ||||
将单因素分析中P < 0.2的变量纳入二元logistics回归分析中结果显示,T3dsST2和NLR是影响ACOP心肌损伤患者院内心血管不良事件的独立危险因素,见表 3。
| 因素 | β值 | S.E | Wald | P值 | OR值 | 95%CI |
| T3d sST2 | 0.079 | 0.015 | 29.129 | < 0.01 | 1.082 | 1.052~1.114 |
| NLR | 0.239 | 0.062 | 14.891 | < 0.01 | 1.270 | 1.125~1.434 |
| APACHEⅡ评分 | 0.122 | 0.055 | 4.823 | 0.028 | 1.130 | 1.013~1.260 |
| 常量 | -10.464 | 1.608 | 42.373 | < 0.01 | 0.000 |
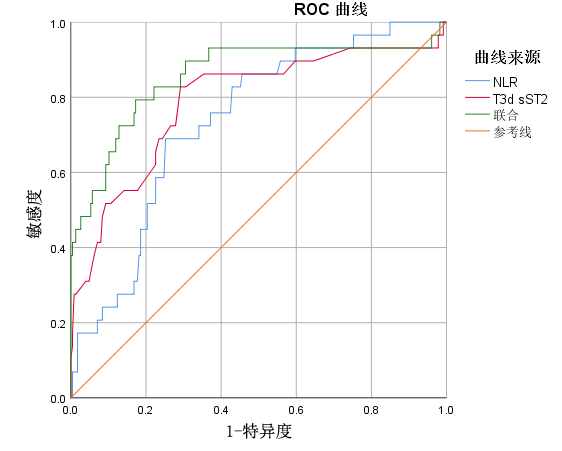
经ROC曲线分析,以NLR > 12.08预测ACOP患者院内不良心血管事件的敏感度为69%,特异度为74.8%(AUC=0.737);以T3dsST2 > 44.5 ng/mL预测ACOP患者院内心血管不良事件的敏感度为82.8%,特异度为70.8%(AUC=0.788);T3dsST2与NLR联合应用预测ACOP患者院内心血管不良事件的敏感度为79.3%,特异度为82.7%(AUC=0.857),见表 4、图 1。
| 指标 | AUC | 约登指数 | 95%CI | P值 | 最佳临界值 | 敏感度(%) | 特异度(%) |
| NLR | 0.737 | 0.438 | 0.651~0.824 | < 0.01 | 12.08 | 69 | 74.8 |
| T 3d sST2 | 0.788 | 0.536 | 0.687~0.889 | < 0.01 | 44.5 ng/mL | 82.8 | 70.8 |
| 联合诊断 | 0.857 | 0.620 | 0.765~0.949 | < 0.01 | 0.11 | 79.3 | 82.7 |
|
| 图 1 NLR、T3d sST2及联合预测ACOP心肌损伤患者院内心血管不良事件的ROC曲线 Fig 1 ROC curve of NLR, T3d sST2 and combined prediction of hospital cardiovascular adverse events in ACOP patients with myocardial injury |
|
|
ACOP可导致广泛的心肌损伤,并与近期不良预后有关[11]。虽然Henry等[12]曾呼吁对于ACOP心肌损伤患者要给予关注并进行心血管危险分层,然而遗憾的是,近十余年关于ACOP心肌损伤的研究较少,以至于临床中对心肌损伤预后的观察与评估匮乏。
ACOP对心血管的效应极为复杂,主要有如下方面:(1)ACOP导致的氧输送减少,可由心脏输出量增加,氧摄取增加等机制增加代偿,当失代偿时则可能出现心血管不良事件的发生。(2)多种因素导致全身炎症反应,炎症导致广泛内皮功能障碍及进一步心功能抑制[13]。(3)线粒体氧化磷酸化受损,即使供氧充足,一氧化碳导致的线粒体功能障碍仍可引起心肌顿抑,出现心功能受损、心律失常、心绞痛甚至急性心肌梗死[14]。(4)交感神经兴奋,循环中的儿茶酚胺引起的微血管痉挛或功能障碍,导致心肌顿抑,或引起直接的儿茶酚胺相关心肌毒性[13]。本研究中ACOP心肌损害患者中院内心血管不良事件总发生率11.37%,尚无相关数据报道,但由该数据来看ACOP心肌损伤患者院内不良事件应该引起重视。
cTnI是心肌损伤的特异性标志物之一,当心肌细胞受损时,cTnI迅速从细胞质内释放入血,且其浓度可反映心肌细胞损伤程度[15],故本研究中以cTnI升高作为入选标准,本研究中事件组与无事件组cTnI水平差异有统计学意义(P=0.015),但经二元logistics回归分析,cTnI并未纳入预测模型,可见cTnI虽然是心肌损伤的可靠指标,但并非ACOP心肌损伤患者院内心血管不良事件的独立预测指标。分析其原因可能与中重度一氧化碳中毒患者大部分因被他人发现意识不清入院,其具体发病时间不明,故临床实际中很难在cTnI峰浓度时间测定有关。
已有多项研究表明[5-6],入院时NLR升高是急性冠脉综合征患者院内不良心血管事件的危险因素。且NLR获取简单、检测成本低廉,可推广性强。本研究前期工作亦发现,入院时NLR水平增高对ACOP出现心肌损伤有一定预测价值[16],与郑爱华等[17]的研究结论一致。本研究中,不良事件组较无事件组入院时NLR明显增高(P < 0.01),其原因考虑如下:炎症学说是目前公认的ACOP心肌损伤的重要机理;中性粒细胞增加反映了系统炎症的恶化,淋巴细胞减少反映了机体免疫调节能力下降和应激增加,故NLR明显增高反映了炎症失衡,最终诱发院内心血管不良事件。但NLR预测院内心血管不良事件的敏感性较低。
单一的病理生理途径不能完全解释心肌损伤的复杂发生发展过程,sST2作为一种能兼具反映心肌牵张、纤维化以及机体炎症的新型生物标志物[18],已有较多临床研究证实其可预测心肌梗死患者院内、院外心血管不良事件的发生[7-8]。sST2可参与多种炎症过程,并在此过程中发挥免疫调节作用,可在心肌细胞发生缺血、缺氧,或受到机械应力时大量表达。本研究人群中入院时sST2(T0sST2)水平均明显升高,但在事件组与无事件组并无明显差异,而第3天sST2(T3dsST2)水平差异明显(P < 0.01),经二元logistics回归分析,第3天sST2水平是预测院内心血管不良事件的独立危险因素。这与Weinberg等[19]在PRAISE-2研究中对于心功能Ⅲ/Ⅳ级的慢性心力衰竭患者的研究sST2浓度变化而非基线sST2浓度是心力衰竭患者90 d死亡的预测因素的结论具有一致性,蔡娟和周陵[20]的研究亦发现AMI患者第4天时血清sST2水平可以作为短期不良预后的预测指标。关于sST2的释放形式,Eggers等[21]在403例非ST段抬高心肌梗死(NSTEMI)患者中发现sST2在机体发病后2~4 h增高,在6~17 h达到峰值,之后逐渐降至稳态。而其在风湿免疫性疾病、肺间质纤维化等其他疾病中的表达特点未见详细阐述。本研究前期研究发现ACOP心肌损伤患者入院时随机sST2水平明显升高,第3天时即迅速下降,故本研究中将入院时和第3天作为sST2的检测时间节点。经ROC曲线分析,T3dsST2预测AOPP患者院内不良心血管事件的AUC为0.788,敏感度为82.8%,特异度为70.8%。
除此之外值得思考的是,ACOP心肌损伤患者sST2高表达是否存在心肌重塑及冠状动脉病变的因素?有动物研究显示,健康大鼠暴露在中等浓度一氧化碳环境下4周会促进心肌重塑,但在急性中毒中,未观测到心肌重塑及冠状动脉密度改变[22]。
经ROC曲线分析显示对于ACOP心肌损伤患者院内心血管不良事件的预测,第3天sST2的最佳截断值为44.5 ng/mL,NLR的最佳截断值为12.08,二者联合时灵敏度79.3%,特异度82.7%,可见对于NLR > 12.08,T3dsST2 > 44.5 ng/mL的ACOP心肌损伤患者需加强监测防范院内心血管不良事件。
本研究为单中心观察性研究,样本数相对较少,在一定程度上影响研究结果的准确性。仅监测了入院时及发病3 d sST2水平,可能造成结论的局限性,进一步研究尚需进行多时刻监测。研究排除了既往冠心病人群,而这部分患者是急性一氧化碳中毒后发生心血管不良事件的高危人群,一定程度上造成样本选择的偏倚。
利益冲突 所有作者均声明不存在利益冲突
| [1] | Garg J, Krishnamoorthy P, Palaniswamy C, et al. Cardiovascular abnormalities in carbon monoxide poisoning[J]. Am J Ther, 2018, 25(3): e339-e348. DOI:10.1097/mjt.0000000000000016 |
| [2] | 孙中吉, 杨朝斌, 王辉, 等. 左旋肉碱对一氧化碳中毒后血清心肌损伤标志物水平的影响[J]. 中国危重病急救医学, 2011, 23(12): 739-742. DOI:10.3760/cma.j.issn.1003-0603.2011.12.009 |
| [3] | 李佳, 李雅琴, 孔繁拓, 等. 参附注射液治疗急性重度一氧化碳中毒所致心肌损伤的临床疗效探讨[J]. 中国中西医结合急救杂志, 2015, 22(6): 652-653. DOI:10.3969/j.issn.1008-9691.2015.06.025 |
| [4] | Moon JM, Chun BJ, Cho YS. The predictive value of scores based on peripheral complete blood cell count for long-term neurological outcome in acute carbon monoxide intoxication[J]. Basic Clin Pharmacol Toxicol, 2019, 124(4): 500-510. DOI:10.1111/bcpt.13157 |
| [5] | Ghaffari S, Nadiri M, Pourafkari L, et al. The predictive value of total neutrophil count and neutrophil/lymphocyte ratio in predicting in-hospital mortality and complications after STEMI[J]. J Cardiovasc Thorac Res, 2014, 6(1): 35-41. DOI:10.5681/jcvtr.2014.007 |
| [6] | 贺威, 范继红, 靳志涛, 等. 急性ST段抬高型心肌梗死患者入院早期中性粒细胞/淋巴细胞比值与院内主要不良心血管事件的相关性[J]. 中国循环杂志, 2016, 31(1): 36-39. DOI:10.3969/j.issn.1000-3614.2016.01.008 |
| [7] | Dhillon OS, Narayan HK, Quinn PA, et al. Interleukin 33 and ST2 in non-ST-elevation myocardial infarction: comparison with Global Registry of Acute Coronary Events Risk Scoring and NT-proBNP[J]. Am Heart J, 2011, 161(6): 1163-1170. DOI:10.1016/j.ahj.2011.03.025 |
| [8] | 何蕾, 彭剑, 郑璇, 等. 血清可溶性致癌抑制因子2水平与急性ST段抬高型心肌梗死患者近期临床预后的相关性研究[J]. 中国循环杂志, 2017, 32(1): 41-45. DOI:10.3969/j.issn.1000-3614.2017.01.010 |
| [9] | 孔夏, 张新超. 血清可溶性ST2对脓毒症预后的判断价值研究[J]. 中华急诊医学杂志, 2018, 27(4): 394-398. DOI:10.3760/cma.j.issn.1671-0282.2018.04.012 |
| [10] | 王维展, 马国营, 赵玲俊, 等. 血乳酸清除率与急性一氧化碳中毒迟发性脑病的相关性研究[J]. 中华危重病急救医学, 2013, 25(10): 622-626. DOI:10.3760/cma.j.issn.2095-4352.2013.10.011 |
| [11] | Kao HK, Lien TC, Kou YR, et al. Assessment of myocardial injury in the emergency department independently predicts the short-term poor outcome in patients with severe carbon monoxide poisoning receiving mechanical ventilation and hyperbaric oxygen therapy[J]. Pulm Pharmacol Ther, 2009, 22(6): 473-477. DOI:10.1016/j.pupt.2009.04.006 |
| [12] | Henry CR, Satran D, Lindgren B, et al. Myocardial injury and long-term mortality following moderate to severe carbon monoxide poisoning[J]. JAMA, 2006, 295(4): 398-402. DOI:10.1001/jama.295.4.398 |
| [13] | Cha YS, Kim H, Lee Y, et al. Evaluation of relationship between coronary artery status evaluated by coronary computed tomography angiography and development of cardiomyopathy in carbon monoxide poisoned patients with myocardial injury: a prospective observational study[J]. Clin Toxicol (Phila), 2018, 56(1): 30-36. DOI:10.1080/15563650.2017.1337910 |
| [14] | 戴淑芳, 孙艺平, 傅雷, 等. 高压氧对急性一氧化碳中毒大鼠心肌超微结构及心电图的影响[J]. 大连医科大学学报, 2018, 40(1): 22-26. DOI:10.11724/jdmu.2018.01.04 |
| [15] | Boeddinghaus J, Nestelberger T, Twerenbold R, et al. Direct comparison of the ESC 0/3h-algorithm with four very early rule-out strategies for acute myocardial infarction using high-sensitivity cardiac troponin I[J]. Eur Heart J, 2017, 38(suppl 1): 7-8. DOI:10.1093/eurheartj/ehx501.54 |
| [16] | 韩永燕, 王岩, 赵国强, 等. 中性粒细胞与淋巴细胞比值和急性一氧化碳中毒心肌损伤的关系[J]. 中华劳动卫生职业病杂志, 2018, 36(5): 362-364. DOI:10.3760/cma.j.issn.1001-9391.2018.05.010 |
| [17] | 郑爱华, 才立云, 王克宇. 早期NT-proBNP、NLR及PLR对急性一氧化碳中毒心肌损伤的预测价值[J]. 现代预防医学, 2019, 46(15): 2824-2825. |
| [18] | 刘晓婷, 王磊, 陈静, 等. 超敏肌钙蛋白Ⅰ和可溶性致癌抑制因子2在急性有机磷农药中毒的作用[J]. 中华急诊医学杂志, 2019, 28(3): 298-302. DOI:10.3760/cma.j.issn.1671-0282.2019.03.005 |
| [19] | Weinberg EO, Shimpo M, Hurwitz S, et al. Identification of serum soluble ST2 receptor as a novel heart failure biomarker[J]. Circulation, 2003, 107(5): 721-726. DOI:10.1161/01.cir.0000047274.66749.fe |
| [20] | 蔡娟, 周陵. 急性心肌梗死4天时血清可溶性生长刺激表达基因2蛋白水平与6个月内心原性死亡关系的研究[J]. 中国循环杂志, 2019, 34(5): 467-471. DOI:10.3969/j.issn.1000-3614.2019.05.008 |
| [21] | Eggers KM, Armstrong PW, Califf RM, et al. ST2 and mortality in non-ST-segment elevation acute coronary syndrome[J]. Am Heart J, 2010, 159(5): 788-794. DOI:10.1016/j.ahj.2010.02.022 |
| [22] | Kalay N, Ozdogru I, Cetinkaya Y, et al. Cardiovascular effects of carbon monoxide poisoning[J]. Am J Cardiol, 2007, 99(3): 322-324. DOI:10.1016/j.amjcard.2006.08.030 |
 2021, Vol. 30
2021, Vol. 30




