高原性肺水肿(HAPE)是高原地区特发病。高原空气稀薄,大气压和氧分压低,由于人体不能适应低气压、低氧环境,诱发组织缺氧[1],缺氧刺激血管内皮生长因子(VEGF)的表达上调、肺血管痉挛[2-3],肌型细动脉平滑肌增厚,肺循环阻力升高,肺毛细血管静脉压明显升高,毛细血管通透性增加,血浆渗出产生肺水肿[4]。机体缺氧后即可发生急性高原性肺水肿、高原性脑水肿等一系列高原疾病,是快速上升到高海拔地区的常见后果,也是高海拔地区的主要死因[5]。高原性肺水肿的特征是呼吸急促,咳粉红色泡沫痰,高原性脑水肿特点是共济失调和意识下降,导致脑疝和昏迷,如不及时治疗将致命[6-7]。本院2019年7月8日收治一例高海拔地区运用ECMO技术联合航空转运救治高原性肺水肿所致呼吸心搏骤停患者,经过综合治疗,患者最终痊愈出院,CPC评分1分。现将诊疗经过报道如下,以期为高原地区危重症救援、高原地区ECMO开展运用以及ECMO联合航空转运提供新的思路。
1 发病经过患者女性,37岁,于2019年7月5日出差到四川省甘孜州白玉县某镇(海拔3 900 m),于7月6日10 AM左右出现头晕、胸闷,吸氧后症状无缓解,病情逐渐加重,继而全身无力、呼吸困难、意识模糊,考虑高原性肺水肿被紧急送往当地县医院,在转运途中出现咳粉红色泡沫痰,意识障碍加深逐渐昏迷。本研究所涉及临床资料均通过医院伦理委员会批准。
2 救治过程 2.1 治疗经过患者于当日14:00被送达甘孜县人民医院(海拔3 500 m),入院时意识昏迷,全身湿冷,濒死状态,立即给予气管插管,抢救过程中出现心率下降、心搏骤停,给予徒手心肺复苏术,约2 min恢复ROSC,病程中出现反复抽搐。治疗给予呼吸机正压通气,予右锁骨下深静脉置管,持续泵入血管活性药物维持血压; 咪达唑仑控制抽搐; 地塞米松、呋塞米纠正肺水肿。结合病史及临床表现,诊断考虑:急性高原性肺水肿、急性肺源性心脏病、急性全心衰、心源性休克、呼吸心搏骤停、心肺复苏术后、缺血缺氧性脑病、高原性脑水肿、继发性癫痫。
病情反馈至四川省人民医院,医院立即组织多学科(MDT)远程会诊,同时派出专业救援队包括急危重症医学科、呼吸科、心内科成员携带相关医疗设备和药品赶赴甘孜县人民医院。
救援队于7月7日6:00抵达,查看患者生命体征:SPO2 90%(呼吸机条件:PEEP 15 cmH2O,FiO2 100%),HR 120次/min,BP 100/60 mmHg[去甲肾上腺素1.1 μg/(kg·min),多巴胺15 μg/(kg·min),肾上腺素0.03 μg/(kg·min)],重度昏迷,双瞳0.2 cm, 等大等圆,光反射消失,气道内不断涌出大量粉红色泡沫痰,无尿3 h。咪达唑仑8 mg/h泵入仍持续全身抽搐。当地无血气分析仪,无血气资料。受限于当地医疗条件并考虑到高原性肺水肿治疗首要是降低海拔高度,综合评估后决定将患者转运至低海拔地区。
因患者严重心肺功能衰竭,无法承受长途转运。救援队决定实施ECMO辅助下转运。救援队出发前已根据病情做出预判,派出人员中包含急危重症医学科ECMO小组成员,携带包括ECMO机器、膜式氧合器、穿刺包及穿刺针等所需设备。
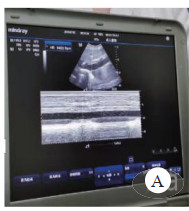
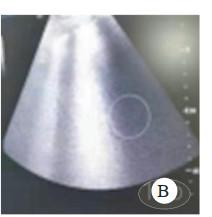
启动ECMO之前完善床旁心脏超声及CT检查。超声提示下腔静脉宽且恒定(图 1),右心增大明显呈D字征,左心EF < 30%。肺部超声提示双侧大量B线(图 2)
|
| 图 1 下腔静脉宽恒定 Fig 1 Constant width of inferior vena cava |
|
|
|
| 图 2 肺部超声大量B线 Fig 2 Large B-line of lung ultrasound |
|
|
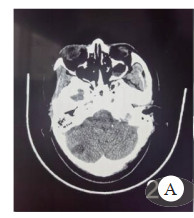
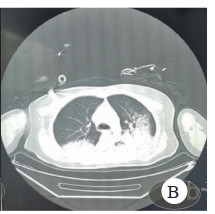
头胸部CT(图 3、图 4),分别提示右侧小脑半球、右侧枕叶片状低密度影,局灶性脑水肿以及双肺多叶段片状模糊影及磨玻璃影。
|
| 图 3 头颅CT Fig 3 Head CT |
|
|
|
| 图 4 胸部CT Fig 4 Chest CT |
|
|
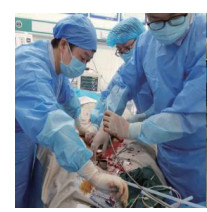
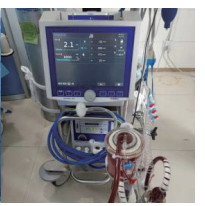
10 :00 ECMO启动,ECMO机器型号:MEDOS DELTA STREAMSⅢ,膜式氧合器型号:hilite 7000 LT,穿刺管:美敦力17 Fr动脉管及及22 Fr静脉管,选择模式:静脉-动脉体外膜肺氧合(VA-ECMO),插管部位:右侧股静脉及左侧股动脉(图 5),首次肝素负荷剂量2 000 U(体质量60 kg),并以5 U/(kg·h)持续泵入。因条件有限,未予安置左下肢股浅动脉侧枝循环。上机时ECMO转数5 700 r/min,流量2.1 L/min(图 6)。患者氧合循环逐渐好转,SPO2上升至98%,吸机参数下调至:FiO2 35%, VT 360 mL(6 mL/kg), PEEP 8 cmH2O,F10次/min。患者HR 94次/min,BP 116/89 mmHg,血管活性药物用量下调,停用多巴胺及肾上腺素,去甲肾上腺素减量至0.3 μg/(kg·min),小便100 mL/h。ECMO运转2 h后患者出现多尿,尿量高达800~1 200 mL/h,ECMO流量不稳, 转数7 000转/min,流量1.8 L/min,频繁抖管,考虑血容量不足,中枢性尿崩症所致,当地无去氨加压素类药物,给予加快输液速度(1 000 mL/h)以保证ECMO流量。输入全血4U(当地无储血库,由部队驻军现场献血),20%人血白蛋白200 mL、人工胶体等。患者迫切需要转移到低海拔地区接受治疗。
|
| 图 5 ECMO小组启动 Fig 5 ECMO team startup diagram |
|
|
|
| 图 6 ECMO上机时转速及流量 Fig 6 Speed and flow on ECMO |
|
|
(1) 救护车:转运至就近且海拔相对较低的甘孜州人民医院(海拔2 000 m),车程需要8-10 h,且需翻越高山,又遇下雨,风险极大。(2)直升机:转运至甘孜州人民医院约1.5~2 h,但正值雨季,雷暴较多,航行空窗时间短。经四川省应急办与西部战区陆航旅协调后当日15:00~18:00有航行条件。救援队最终选择航空转运(图 7)。

|
| 图 7 机场转运 Fig 7 Airport transfer |
|
|
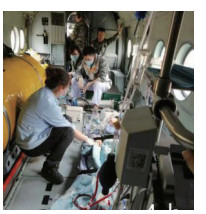
直升机于15:10分起飞,最高飞行高度5 500米,飞行途中患者多次出现肺水肿加重,气道内涌出大量粉红色泡沫痰,予吗啡5 mg静推可缓解。飞行中ECMO流量稳定,转速6 800转/min,流量3.0 L/min,小便量仍然多900 mL/h,HR 117次/min,BP 125/55 mmHg,MAP75 mmHg,SPO2 100%(图 8)。直升机上无电源,ECMO自身携带两枚电池可供使用6 h,转运呼吸机蓄电池可供使用2~4 h。最终于16:30顺利抵达甘孜州人民医院所在的康定机场,飞行时间80 min。
|
| 图 8 机舱内情况 Fig 8 Situation in the cabin |
|
|
到达甘孜州人民医院(海拔2 000 m)后患者尿崩症状自行消失,ECMO流量稳定,粉红色泡沫痰显著减少。意识有改善,轻微躁动。ECMO参数调整:转数7 000 r/min,流量3.1 L/min,氧饱和度维持在99%~100%,尿量1~2 mL/(kg·min)。
陆地转运:当夜在州人民医院进一步稳定病情后,第2天即7月8日14:18出发,经救护车陆地转运265 km,于18:00到达四川省人民医院急救中心EICU(海拔600 m)。转运过程ECMO及呼吸机参数见表 1.ECMO上机前后肝肾功比较,见表 2。
| 位点 | 参数 | ||||||
| 海拔 | ECMO | 呼吸机 | |||||
| 高度 (km) |
转速 (转/min) |
流量 (L/min) |
VT (mL/kg) |
PEEP (cmH2O) | FiO2 (%) | F (次/min) |
|
| 甘孜县医院 | 3900 | 5700 | 2.1 | 6 | 8 | 35 | 10 |
| 直升机上 | 2000-5000 | 6800 | 3 | 6 | 10 | 80 | 14 |
| 甘孜州医院 | 2000 | 7000 | 3.1 | 6 | 8 | 40 | 10 |
| 救护车上 | 600-2000 | 6600 | 2.8 | 6 | 8 | 40 | 10 |
| 检验值 | 时间/海拔 | ||
| ECMO前/ 3 700 m |
ECMO后/ 3 700 m |
航空转运后/ 2 000 m |
|
| CR(μmol/L) | 199 | 66.08 | 100 |
| BUN(mmol/L) | 9.16 | 7.2 | 7.1 |
| ALT(U/L) | 317 | 888 | 712 |
| AST(U/L) | 412 | 565 | 842 |
| CK(U/L) | 2026 | ~ | ~ |
| CK-MB(ng/mL) | 130.2 | ~ | ~ |
| 备注:表中~表示数据缺失 | |||
四川省人民医院EICU入科时查体:T36.6℃,P86次/min,BP101/89 mmHg [去甲肾上腺素0.5μg/(kg·min)持续泵入],SPO2 100%,ECMO参数:转速6 600,流量2.8 L/min,呼吸机参数:模式SIMV(PC),f 10次/min,FiO2 40%,PEEP 8 cmH2O,PS 8 cmH2O,镇静状态,咪达唑仑2 mg/h泵入,双侧瞳孔2 mm,对光反射灵敏,右侧肢体不自主运动。双肺闻及散在湿啰音,心率86次/min,闻及早搏。右侧股静脉及左侧股动脉ECMO穿刺置管在位,双侧足背动脉正常,双下肢皮温正常。
治疗:继续VA-ECMO辅助,ACT维持在140~160 s,全身无出血倾向,膜肺无血栓,持续有创呼吸机辅助,新活素0.007 μg/(kg·min)、白蛋白+托拉塞米、甘露醇利尿改善肺水肿、脑水肿,心功能逐步恢复,ECMO流量逐步减小。减流量过程中加用多巴酚丁胺2 μg/(kg·min)强心,咪达唑仑联合丙戊酸钠、左乙拉西坦控制癫痫发作。因未安置左下肢股浅动脉远端灌注管。每天监测患者左下肢皮温及左足背动脉搏动正常。
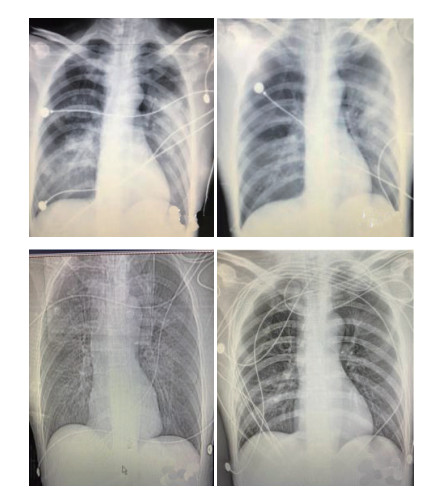
随着精细化治疗,患者病情逐渐好转,7月10日胸片心影形态正常,片絮影吸收(图 9),心脏超声:左心EF上升至45%(表 3)。停用血管活性药物,尿量及乳酸正常,在ECMO辅助72 h后顺利撤机,当天即外出行高压氧治疗。患者神志逐渐清醒,于7月12日脱离呼吸机拔出气管插管,于7月15日顺利转出EICU。未留下神经系统后遗症,CPC评分1分。
|
| A-C依次为7月8日至7月11日胸片 图 9 患者胸片 Fig 9 Chest CT of the patient |
|
|
| 心超 | 时间 | ||||
| 7月7日 | 7月8日 | 7月9日 | 7月10日 | 7月11日 | |
| LV(D) | 未测 | 53 | 51 | 49 | 43 |
| EF | < 0.3 | 0.33 | 0.35 | 0.45 | 0.49 |
急性高原病由高原低氧应激所致,低氧导致肺动脉收缩,平均肺动脉压(PA)升高超过35~40 mmHg,且肺血管收缩不均衡。这种不均衡的血管收缩和区域性过度灌注导致肺泡-毛细血管屏障破坏及斑片状肺水肿。高相对分子质量蛋白、细胞和液体漏入肺泡腔。最终,内皮细胞及上皮细胞基底膜被破坏,导致肺泡出血[8]。高原肺水肿的一个显著特征是下到低海拔地区或吸氧可迅速逆转。到低海拔地区后,肺血管阻力在数日内可恢复正常。其发生风险取决于个体易感性、海拔高度、海拔上升的速度和在高原停留的时间。发病率增加的相关因素包括男性、环境温度较低、预先存在呼吸道感染以及剧烈运动[9]。在预防方面,目前控制上升速率是预防的最佳途径[10]。成功治疗的关键原则是迅速降低PA压。方法包括限制体力活动和限制寒冷暴露、供氧、撤离至较低海拔、用高压氧疗模拟降低海拔,以及给予适当的药物。降低海拔及补氧常常能单独起效,优于任何药物治疗[11-12]。
ECMO应用于临床各种急危重症患者的抢救,并取得良好疗效[13-14]。因心搏骤停、严重心源性休克或心脏术后接受ECMO治疗的患者中,生存率为20%~50%[15-16],成人难治性院外心搏骤停研究显示,在复苏期间接受ECMO治疗的833例患者中有22%存活,其中半数患者的神经系统功能恢复良好[17]。针对本例高原性肺水肿合并心源性休克、呼吸心搏骤停的患者,ECMO发挥了巨大作用,选择VA模式,同时辅助循环和呼吸,其不仅能够提高生存率及获得良好神经学预后[18],也为患者转入低海拔地区救治赢得宝贵时间,同时也为高海拔地区航空转运提供安全保障。
笔者观察到ECMO流量和患者所处的海拔高度无关。本例发现在高海拔、直升机上,中度海拔,低海拔地区ECMO流量均稳定,只有在尿量增加尿崩时ECMO流量下降,经快速补液后流量也快速稳定。ECMO流量与血容量及管路位置,管路打折等有关,故在高海拔地区开展ECMO是可行的。另外,在本例患者中,高原环境下ECMO转流2 h后出现尿量过多,尿崩症表现,导致ECMO流量不能维持,频繁抖管,进入低海拔地区后(海拔2 000 m)尿崩自行停止,考虑是由于高原性脑水肿引起缺氧性脑病进而导致ADH释放减少[18]有关。
在航空转运过程中其海拔最高升至5 500 m,患者心肺功能存在极大挑战,也是本例患者飞行途中多次出现大量粉红色泡沫痰的原因。航空转运的挑战不仅在于设备的局限性,具有挑战的环境,还在于难以开发用于研究和数据收集的方法[19]。
利益冲突 所有作者均声明不存在利益冲突
| [1] | Li Y, Zhang Y, Zhang Y. Research advances in pathogenesis and prophylactic measures of acute high altitude illness[J]. Respir Med, 2018, 145: 145-152. DOI:10.1016/j.rmed.2018.11.004 |
| [2] | Pavlicek V, Marti H H, Grad S, et al. Effects of hypobaric hypoxia on vascular endothelial growth factor and the acute phase response in subjects who are susceptible to high-altitude pulmonary oedema[J]. Eur J Appl Physiol, 2000, 81(6): 497-503. DOI:10.1007/s004210050074 |
| [3] | Tsai SH, Huang PH, Tsai HY, et al. Roles of the hypoximir microRNA-424/322 in acute hypoxia and hypoxia-induced pulmonary vascular leakage[J]. FASEB J, 2019, 33(11): 12565-12575. DOI:10.1096/fj.201900564RR |
| [4] | 夏鹏, 郎珈馨, 文煜冰, 等. 肾小管周毛细血管损伤与原发高血压恶性肾硬化患者临床及长期预后的关系[J]. 中华肾脏病杂志, 2017, 33(9): 641-648. DOI:10.3760/cma.j.issn.1001-7097.2017.09.001 |
| [5] | Mulchrone A, Moulton H, Eldridge MW, et al. Susceptibility to high-altitude pulmonary edema is associated with increased pulmonary arterial stiffness during exercise[J]. J Appl Physiol (1985), 2020, 128(3): 514-522. DOI:10.1152/japplphysiol.00153.2019 |
| [6] | Basnyat B, Hofmeyr R, Tölken G, et al. Acute high-altitude illness[J]. S Afr Med J, 2017, 107(12): 1047-1048. DOI:10.7196/SAMJ.2017.v107i12.12863 |
| [7] | 张卫善, 卓嘎拉姆, 王斐, 等. 基于胸部X线的定量分析在高原肺水肿治疗前后中的对比研究[J]. 实用放射学杂志, 2019, 35(12): 1918-1921. DOI:10.3969/j.issn.1002-1671.2019.12.008 |
| [8] | Swenson ER. Early hours in the development of high-altitude pulmonary edema: time course and mechanisms[J]. J Appl Physiol, 2020, 128(6): 1539-1546. DOI:10.1152/japplphysiol.00824.2019 |
| [9] | Li YH, Tana WR, Bai ZZ, et al. Transcriptomic profiling reveals gene expression kinetics in patients with hypoxia and high altitude pulmonary edema[J]. Gene, 2018, 651: 200-205. DOI:10.1016/j.gene.2018.01.052 |
| [10] | Swenson ER, Bärtsch P. The search for a model of high-altitude pulmonary oedema must continue[J]. Acta Physiol, 2020: e13485. DOI:10.1111/apha.13485 |
| [11] | Ahmadipour B, Sharifi M, Khajali F. Pulmonary hypertensive response of broiler chickens to arginine and guanidinoacetic acid under high-altitude hypoxia[J]. Acta Vet Hung, 2018, 66(1): 116-124. DOI:10.1556/004.2018.011 |
| [12] | Luks AM, McIntosh SE, Grissom CK, et al. Wilderness Medical Society practice guidelines for the prevention and treatment of acute altitude illness: 2014 update[J]. Wilderness Environ Med, 2014, 25(4 Suppl): S4-S14. DOI:10.1016/j.wem.2014.06.017 |
| [13] | 吴颖, 张励庭, 冯力, 等. 体外膜肺氧合联合急诊经皮冠状动脉介入治疗抢救急性心肌梗死后心脏骤停患者的临床疗效及其影响因素分析[J]. 中国循环杂志, 2018, 33(6): 561-566. DOI:10.3969/j.issn.1000-3614.2018.06.009 |
| [14] | 廉波, 陈彧, 赵舟, 等. 插管策略对静-动脉体外膜式氧合相关并发症的影响——单中心回顾性研究[J]. 中国循环杂志, 2018, 33(4): 380-384. DOI:10.3969/j.issn.1000-3614.2018.04.016 |
| [15] | Henderson MA, Gyorki D, Burmeister BH, et al. Inguinal and ilio-inguinal lymphadenectomy in management of palpable melanoma lymph node metastasis: a long-term prospective evaluation of morbidity and quality of life[J]. Ann Surg Oncol, 2019, 26(13): 4663-4672. DOI:10.1245/s10434-019-07810-0 |
| [16] | Mariscalco G, Fiore A, Ragnarsson S, et al. Venoarterial extracorporeal membrane oxygenation after surgical repair of type A aortic dissection[J]. Am J Cardiol, 2020, 125(12): 1901-1905. DOI:10.1016/j.amjcard.2020.03.012 |
| [17] | Ortega-Deballon I, Hornby L, Shemie SD, et al. Extracorporeal resuscitation for refractory out-of-hospital cardiac arrest in adults: A systematic review of international practices and outcomes[J]. Resuscitation, 2016, 101: 12-20. DOI:10.1016/j.resuscitation.2016.01.018 |
| [18] | Sun T, Guy A, Sidhu A, et al. Veno-arterial extracorporeal membrane oxygenation (VA-ECMO) for emergency cardiac support[J]. J Crit Care, 2018, 44: 31-38. DOI:10.1016/j.jcrc.2017.10.011 |
| [19] | Kouliev T, Richardson A, Glushak C. Intracranial hemorrhage during aeromedical transport and correlation with high altitude adaptations in the brain[J]. Open Access Emerg Med, 2012, 4: 93-95. DOI:10.2147/OAEM.S34171 |
 2020, Vol. 29
2020, Vol. 29




