非创伤性急腹症(Non-traumatic acute abdomen, NTAA)是指腹腔内、腹壁、胸部或全身性疾病引起的急性腹痛,发病时间短于1周,可能需要手术等紧急干预[1]。
急诊科收治患者中约5%~10%以急性腹痛为主诉,在年龄超过65岁的人群中这一比例甚至高于20%[2-3]。NTAA的常见病因包括急性阑尾炎、急性胰腺炎、憩室炎、胃炎、盆腔炎、胆石症、输尿管结石、消化性溃疡穿孔、肠梗阻等。除上述常见的病因外,近些年因血管性疾病导致的NTAA明显增多,如腹主动脉瘤、肠系膜动脉缺血、主动脉夹层破裂等。这些患者中,1/2至2/3需要入院治疗,且1/3需要外科手术干预。NTAA的不良预后因素包括:高龄,呼吸循环功能障碍,类固醇药物的使用,器官衰竭等。此类患者往往起病急、疼痛程度重,及时镇痛的需求强烈。
疼痛是组织损伤或潜在组织损伤所引起的不愉快感觉和情感体验,或是具有感觉、情绪、认知和社会层面的痛苦体验。World Society of Pain Clinicians(WSPC)认为,疼痛是人的第五大生命体征。急性腹痛会使患者心率增快、血管收缩、心肌耗氧量和心脏负荷增加,从而增加心肌缺血及心肌梗死的风险。急性腹痛还会引起交感神经系统的兴奋性增加,导致全身组织的耗氧增加、胃肠蠕动减弱影响其功能、尿道及膀胱肌肉动力减弱引起尿潴留,以及促发深静脉血栓形成甚至造成肺栓塞。此外,还会造成患者情绪焦虑、无助、沮丧,以及家属的恐慌等。
镇痛剂(analgesic)是指可部分或完全缓解疼痛的药物。传统观点认为NTAA患者在未明确诊断之前不能使用镇痛剂,以避免因使用镇痛剂掩盖病情、改变体征,影响对病情的准确判断,甚至导致误诊、误治[4]。但随着循证医学的发展,越来越多的研究表明,早期、正确地使用镇痛剂不仅可以明显减轻NTAA患者的疼痛、改善患者的感受,而且不影响诊断的准确率[5]。还有一些研究提示,NTAA患者早期使用镇痛剂后的诊断准确率高于不使用镇痛剂的患者[6-7]。
虽然越来越多的证据支持在NTAA早期使用镇痛剂,但是目前国内、国外目前仍缺乏NTAA早期镇痛相关的指南或规范。本共识专家组基于现有研究证据并结合临床实践,探讨了成人NTAA早期镇痛的依据、原则、方法及注意事项等并达成共识,为临床工作提供科学、规范的建议。
1 NTAA早期镇痛的概念及观念演变推荐意见1:急腹症患者评估疼痛情况之后,要尽早使用镇痛剂。早期使用镇痛剂可以提高患者的配合度,从而提高诊断的准确性。
NTAA早期镇痛(non-traumatic acute abdomen early analgesia, NTAAA)是指有毒麻药品处方资质的医生对NTAA患者进行初步问诊、查体后,在病因尚未明确前给予镇痛剂的处理。
传统的观点认为急腹症明确诊断前不能给予镇痛药物。1921年,Cope首先提出急腹症患者不能给予早期镇痛的观点[8]并记录在由他主编的《Early Diagnosis of the Acute Abdomen》一书中[9],但此观点的提出没有明确的循证医学证据支持。50余年后的1979年,Fraser对急腹症患者不宜早期使用镇痛剂的观点提出了异议[10]。1986年,Zohie等在研究中发现,急腹症患者早期应用镇痛剂不仅不影响诊断的准确性,而且使用镇痛剂后有助于提高触诊定位的准确性[11]。1992年,Attard等在研究中发现,早期使用镇痛剂既减轻患者疼痛程度,又不影响诊断的准确性,而且使用镇痛剂后,更有助于患者配合各项检查,因此诊断的准确性得到了提高[12]。1996年,Pace等[13]的研究提示,急腹症患者早期使用吗啡可以有效缓解疼痛,且不影响诊断和处理的准确性。2000年,Mahadevan等[14]的研究提示,急腹症患者使用曲马多后患者疼痛明显下降,腹部触痛、反跳痛、叩痛等体征未消失,没有影响诊断的准确性。2004年Wolfe等的研究提示,急诊阑尾炎患者早期使用吗啡后疼痛明显下降,而体征没有发生改变[15]。2012年,Oguzturk等发现曲马多和对乙酰氨基酚可明显减轻腹痛程度,而且不影响诊断的准确率[16]。
上述研究表明,镇痛剂虽然使疼痛程度减轻,但疾病表现出的体征和影像学特征并没有变化,其检验学结果也不受镇痛剂影响,因此不会因使用镇痛剂掩盖腹部体征或者引起死亡率或致残率升高[5]。而且,剧烈疼痛时,患者常难以配合查体或辅助检查,早期使用镇痛剂可以提高患者的配合度,从而提高诊断的准确性[17]。
在一系列循证医学证据的支持下,NTAA患者不宜早期镇痛的观点被扭转。1996年,Silen提出有资格的医生在经过询问病史和系统的体格检查后可以使用镇痛剂[18]。1996年版的《Early Diagnosis of the Acute Abdomen》中修改了关于急腹症早期镇痛的表述,指出有毒麻药品处方资质的医生在对NTAA患者进行初步问诊、查体后可以使用镇痛剂[19-20]。2000年,美国急诊医学院(American College of Emergency Physicians)提出急腹症患者在经过初步评估后可以使用镇痛剂[21]。2015年日本腹部急救医学学会与日本放射学会、日本初级保健协会、日本妇产科协会、日本血管外科协会共同编撰的《急腹症管理指南》中提出急腹症评估疼痛情况之后,要尽早使用止痛剂[1]。
2 NTAA患者的疼痛评估具有毒麻药品处方资质的医生在完成问诊、体格检查的同时,需要对疼痛性质及程度进行评估,应根据疼痛性质及程度给予相应镇痛剂,应用镇痛剂30 min后对镇痛效果进行复评并评估不良反应,根据复评结果指导进一步镇痛措施。
2.1 疼痛性质评估推荐意见2:急腹症疼痛性质评估重点是区分腹痛是否为绞痛,绞痛患者给予镇痛的同时可辅助性给予解痉药。
NTAA患者腹痛性质包括刀割样痛、烧灼样痛、隐痛、绞痛等。在疼痛性质评估中,重点是区分患者腹痛是否为绞痛。通常,阵发性发作或阵发性加重的疼痛多为绞痛。绞痛常见病因包括肠梗阻、肾结石、输尿管结石、胆结石等。绞痛患者在给予镇痛剂的同时可辅助性地给予解痉药。
2.2 疼痛程度评估推荐意见3:根据NTAA接诊的特点,交流正常患者使用疼痛数字评价量表(numerical rating scale, NRS)评估腹痛程度,对交流困难患者可使用Wong-Baker面部表情量表法评估腹痛程度。
(1)交流正常患者使用疼痛数字评价量表(NRS)[22]:用0~10数字的刻度标示出不同程度的疼痛强度等级,0表示“无痛”,10表示“最剧烈的疼痛”(图 1)。由患者选择符合其疼痛感受的分值来量化疼痛程度,评分越高疼痛程度越重。临床评定以1~3分为“轻度疼痛”,4~5分为“中度疼痛”,6~7分为“重度疼痛”,8~10分为“极重度疼痛”。NRS具有快速、方便、可靠性高等特点。

|
| 图 1 数字评价量表 |
|
|
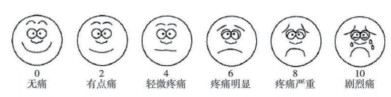
(2)交流困难的人群,如儿童、老年人、意识不清或不能用言语准确表达的患者,可使用Wong-Baker面部表情量表(Wong-Baker face pain rating scale)[22]:由6张从微笑或幸福直至流泪的不同面部表情图组成(图 2)。但这种方法易受情绪、文化、教育程度、环境等因素的影响,应结合具体情况使用。Wong-Baker面部表情量表的临床评定同NRS法。
|
| 图 2 Wong-Baker面部表情量表 |
|
|
推荐意见4:镇痛效果评估使用尼莫地平法计算公式,根据疗效指数调整镇痛方案。
应用镇痛剂30 min后应再次评价镇痛效果,使用NRS的尼莫地平法计算公式评估镇痛效果(见表 1)。Wong-Baker面部表情量表法的镇痛效果评估参照NRS法的效果评估。
NRS的尼莫地平法计算公式:疗效指数=(A-B)/A×100% (A=镇痛前NRS评分、B=镇痛后NRS评分)。疗效指数≥50%,镇痛效果为疼痛可控制,不需要调整镇痛方案;疗效指数 < 50%,镇痛效果为疼痛不可控制,需调整用药剂量或使用更强效药物。
2.4 镇痛剂不良反应评估推荐意见5:镇痛剂不良反应的评估,包括恶心评分、呕吐评分、镇静评分;当恶心评分≥6分、呕吐评分≥6分、镇静评分≥2分,三者有其一为不良反应不能耐受,需要调整镇痛方案。
镇痛剂不良反应的评估主要评估药物的短期不良反应,包括恶心评分、呕吐评分、镇静评分。恶心评分、呕吐评分,分别参照上述NRS法,以无恶心、呕吐为0分,最剧烈的恶心、呕吐为10分进行评分。镇静评分:清醒为0分,呼之睁眼为1分,摇晃身体能睁眼为2分,不能唤醒为3分。当恶心评分≥6分、呕吐评分≥6分、镇静评分≥2分,三者有其一为不良反应不能耐受,需要调整镇痛方案。NTAAA疗效评估表(见表 2)。
 |
用药前评估 | 用药30 min后评估 | 效果评估 | |
| 疼痛评分 | ||||
| 不良反应 | 恶心评分 | |||
| 呕吐评分 | ||||
| 镇静评分 | ||||
| 注:恶心、呕吐评分:以NRS法评为0~10分,1~4分为轻度,5~6分为中度,7~10分为重度;镇静评分:0分=清醒,1分=呼之睁眼,2分=摇能睁眼,3分=不能唤醒 | ||||
NTAAA常用镇痛剂包括对乙酰氨基酚、非甾体抗炎药(nonsteroidal anti-inflammatory drugs,NSAIDs)、曲马多(tramadol)、阿片类药物等。
使用镇痛剂前,应熟知该药物的药理作用、给药途径、安全剂量、禁忌证、不良反应等。应告知患者及家属用药后的注意事项,尤其是疼痛缓解后不应轻视NTAA的病情严重性,应按照医师的建议继续诊疗。在用药30 min后,应再次评估,出现不良反应及副作用时及时处理。
(1)对乙酰氨基酚:对乙酰氨基酚通过抑制中枢神经系统合成前列腺素而产生镇痛作用。对轻至中度疼痛可单独应用。对严重疼痛患者,可与NSAIDs药物、曲马多或阿片类联合应用,产生镇痛相加或协同效应。口服给药常用剂量为每6小时6~10 mg/kg,最大剂量不超过3 000 mg/d;静脉输注常用剂量为每6小时1 000 mg或每4小时650 mg,可以单次或重复给药,最大剂量不超过4000 mg/d。联合给药或复方制剂不超过1500 mg/d,否则可能引起肝脏损伤和急性肾小管坏死。
推荐意见6:对乙酰氨基酚对NTAA轻至中度疼痛可单独应用;对严重疼痛患者,可与NSAIDs药物、曲马多或阿片类联合应用。
(2)NSAIDs:主要是通过抑制环氧化酶(cyclooxygenase, COX)减少前列腺素的生成,产生抗炎、镇痛、解热的作用。对轻至中度疼痛可单独应用。对严重疼痛患者,可与曲马多或阿片类联合应用,产生协同效应。
NSAIDs分为非选择性NSAIDs和选择性COX-2抑制剂两大类。非选择性NSAIDs不良反应主要为血小板功能抑制、消化道损伤、变态反应致哮喘发作和心血管副作用等。选择性COX-2抑制剂的血小板功能抑制和消化道损伤作用较非选择性NSAIDs减轻、哮喘症状少见,但心血管副作用同非选择性NSAIDs。因此,对有心血管高危因素的患者(尤其是心脏搭桥术后患者、有心绞痛症状的患者)、曾有过中风或近期有过一过性脑缺血病史的患者、肾功能损伤的患者,NSAIDs应视为相对或绝对禁忌[24]。
临床常用的口服非选择性NSAIDs包括布洛芬、双氯芬酸、氯诺昔康等,注射用非选择性NSAIDs包括氯诺昔康、酮咯酸、氟比洛芬酯等。临床常用的选择性COX-2抑制剂包括美洛昔康、塞来昔布、帕瑞昔布等。常用注射用NSAIDs用法和用量见表 3。
| 药物 | 剂量范围(mg) | 静注起效时间(min) | 维持时间(h) | 用法和用量 |
| 氟比洛芬酯 | 50~250 | 15 | 8 | IV:50 mg/次,日剂量不超过250 mg |
| 帕瑞昔布 | 40~80 | 13 | 12 | IM/IV:首次剂量40 mg,以后40 mg/12 h,连续用药物不超过3 d |
| 酮咯酸 | 30~120 | 50 | 4~6 | IM/IV:首次剂量30 mg,以后15~30 mg/6 h,最大剂量120 mg/d,连续用药不超2 d |
| 氯诺昔康 | 8~24 | 20 | 3~6 | IV:8 mg/次,2~3次/d,日剂量不超过24 mg |
推荐意见7:NSAIDs对NTAA轻至中度疼痛可单独应用。对严重疼痛患者,可与曲马多或阿片类联合应用,产生协同效应。
(3)曲马多:多为中枢性镇痛药,与阿片受体有较弱的亲和力,通过抑制神经元突触对去甲肾上腺素的再摄取并增加神经元外5-羟色胺浓度影响痛觉传递而产生镇痛作用,需要有毒麻药品处方资质的医师开具。
曲马多的镇痛作用强度为吗啡的1/10~1/8,和等剂量哌替啶作用几乎相当。对中度疼痛可单独应用。对严重疼痛患者,可与乙酰氨基酚、NSAIDs或阿片类联合应用,产生协同效应。
常见的不良反应包括出汗、眩晕、恶心、呕吐、食欲减退及排尿困难等,少见不良反应包括心悸、心动过缓或直立性低血压,偶见胸闷、口干、疲劳、瘙痒、皮疹等。已知或怀疑胃肠道梗阻患者,急性或严重支气管哮喘患者和呼吸抑制患者禁用。曲马多的不良反应及程度与用药方式、剂量、使用时间及过敏体质有一定的相关性。
推荐口服剂量为50~100 mg/次;肌内注射剂量为50~100 mg/次;静脉注射剂量为100 mg/次,缓慢注射或稀释后滴注。24 h总量不宜超过400 mg。
推荐意见8:曲马多对NTAA中度疼痛可单独应用。对严重疼痛患者,可与乙酰氨基酚、NSAIDs或阿片类联合应用,产生协同效应。
(4)阿片类药物:即麻醉性镇痛药,通过激动外周和中枢神经系统阿片受体发挥镇痛作用,是治疗中、重度急、慢性疼痛的最常用药物,需要有毒麻药品处方资质的医师开具。
根据镇痛强度的不同可分为弱阿片类和强阿片类。弱阿片类有可待因、双氢可待因等,主要用于中度疼痛镇痛。强阿片类药物包括吗啡、芬太尼、哌替啶、舒芬太尼、羟考酮和氢吗啡酮等,主要用于中、重度疼痛镇痛。
阿片类药物镇痛作用强,无器官毒性,无封顶效应。常见不良反应包括恶心、呕吐、呼吸抑制、瘙痒、肌肉僵直、肌阵挛和惊厥、认知功能障碍、缩瞳、体温下降等。联合用药以减少阿片类用量可以一定程度地避免阿片类的不良反应。不良反应的处理原则是停药、对症治疗,必要时使用阿片类拮抗剂纳洛酮。
推荐意见9:阿片类药物主要用于中、重度疼痛镇痛,是治疗中、重度急、慢性疼痛最常用的药物。联合用药以减少阿片类用量可以一定程度地避免阿片类的不良反应。
(5)联合用药:中、重度疼痛镇痛可使用联合用药,联合用药的优点包括:①可以发挥不同类别药物的协同作用,增强镇痛效果;②可减少其中某一类类药物的用量,减少用药产生的副作用及不良反应。
镇痛剂的联合用药主要包括:①对乙酰氨基酚与曲马多或阿片类药物联合使用[25],联合应用可在达到同等镇痛效果的前提下减少阿片类药物用量达20%~40%;②对乙酰氨基酚与NSAIDs联合使用[25-27],可发挥镇痛相加或协同作用,提高镇痛效果。③NSAIDs与曲马多或阿片类联合使用,使用常规剂量的NSAIDs可减少阿片类药物用量达20%~50%[28-29]。必要时可联合使用3种作用机制不同的药物实施多靶点镇痛[30-32]。
推荐意见10:中、重度疼痛镇痛联合用药优势明显,不仅可增强镇痛效果,也可减少用药产生的副作用及不良反应。
3.2 常用镇痛剂给药方法推荐意见11:镇痛剂给药方法中皮下注射或肌肉注射为急诊环境下的首选给药方法;静脉注射为第二推荐的给药方法;不推荐口服给药作为NTAAA的常规给药途径。
(1)皮下注射或肌肉注射:为急诊环境下的首选给药方法。当患者存在皮下给药的禁忌证(如外周水肿、凝血功能障碍、末梢循环差等),肌肉注射给药的禁忌证(如注射部位有硬结、感染等),以及用药剂量较大时,应考虑静脉注射给药。酮咯酸、帕瑞昔布等NSAIDs药物、曲马多和吗啡、哌替啶等阿片类药物可通过皮下或肌肉注射给药,具体参见药品说明书。
(2)静脉注射:在急诊环境下作为第二推荐的给药方法。静脉注射起效快,可避免皮下注射、肌肉注射的反复多次穿刺操作,但相对于其他给药方式操作略复杂。大剂量、持续用药时需考虑静脉注射。对乙酰氨基酚、曲马多、大部分NSAIDs药物、吗啡等阿片类药物可通过静脉注射给药,具体参见药品说明书。
(3)直肠给药:无刺激的药物可以经直肠给药。直肠给药适用于口服、输液存在困难且存在皮下注射禁忌证的病人。曲马多、对乙酰氨基酚、吲哚美辛栓等栓剂可经直肠给药,具体参见药品说明书。
(4)口服:由于部分NTAA患者明确诊断后需急诊手术,术前需要禁食水,所以不推荐口服给药作为NTAAA的常规给药途径。口服给药使用方便,但起效慢、吸收率不高,只限于不需要急诊手术且神志清醒、胃肠道功能良好患者的轻、中度疼痛的控制。重度恶心、呕吐、吞咽功能障碍、鼻饲患者和便秘者慎用。禁用于肠梗阻患者。
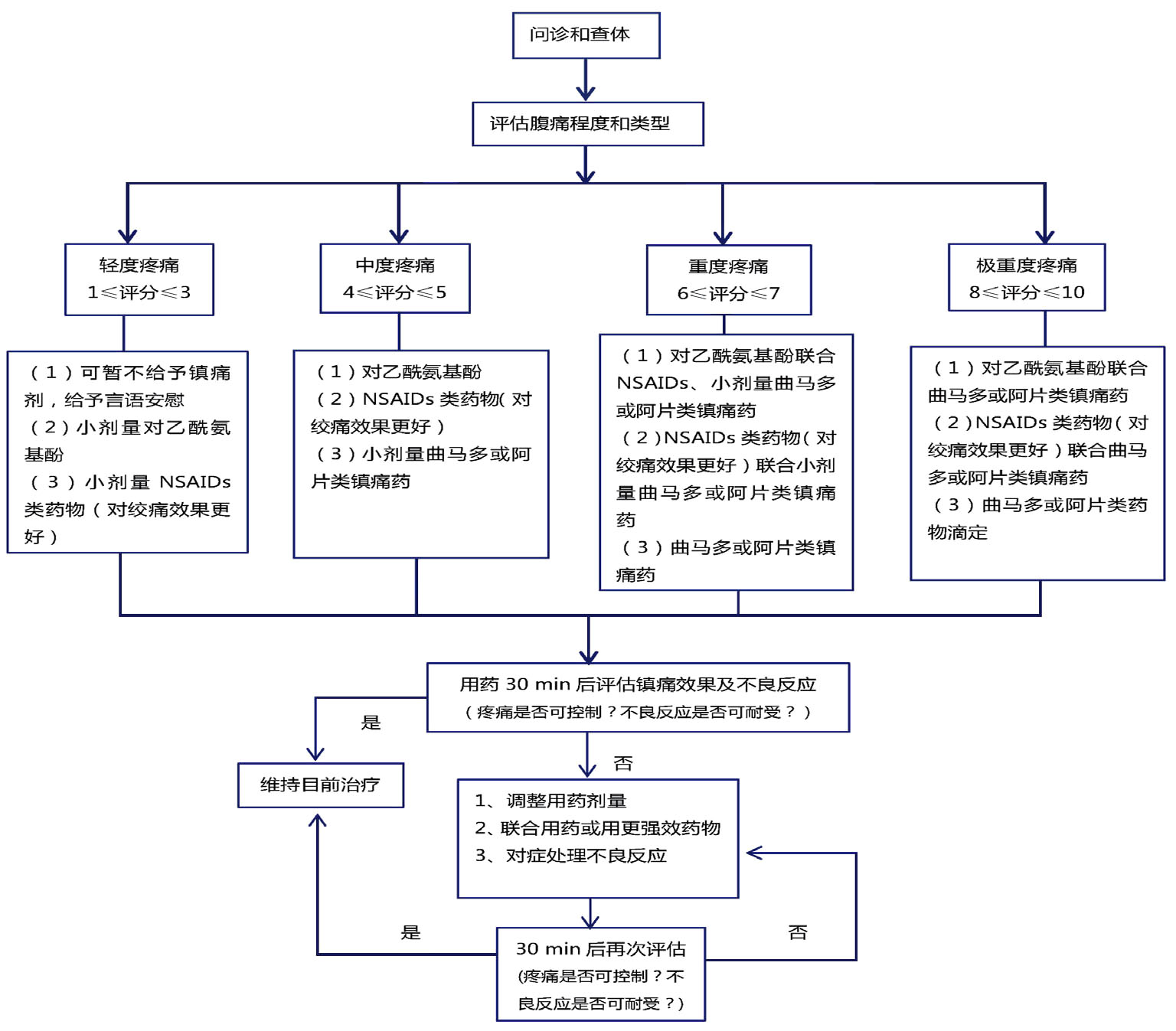
4 NTAAA方案推荐本共识在2015年日本腹部急救医学学会与其他4个医疗团体(日本放射学会、日本初级保健协会、日本妇产科协会、日本血管外科协会)共同编撰的《急腹症管理指南》[33]及2019年美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)编撰的《成人癌症疼痛管理方法》[34]基础上结合多中心的临床实践,制定以下成人NTAAA流程图(图 3)。
|
| 图 3 NTAAA流程图 |
|
|
推荐意见12:镇痛前,应告知患者及家属用药后的注意事项,尤其是疼痛缓解后不应轻视NTAA的病情严重性,应按照医师的建议继续诊疗。
镇痛前,应告知患者及家属用药后的注意事项,应用镇痛剂后要注意对患者进一步观察和检查, 不可随意放走患者,患者疼痛程度的减轻可能会导致医患双方对病情严重程度的轻视。镇痛只是NTAA诊疗过程的一部分,应用镇痛剂后应尽快继续查明病因,采取针对病因的干预措施或手术治疗。避免因疼痛缓解而延误原发病的诊治。
推荐意见13:诊治过程中每隔30 min需对患者进行评估,包括疼痛程度、镇痛效果、不良反应等。
接诊医生在完成问诊后即进行初次体格检查、疼痛程度评估,给止痛剂后每隔30 min需对患者进行评估。为了将患者的疼痛程度控制在其可接受的水平,有必要多次进行常规疼痛评估,包括记录疼痛程度(最重要)、镇痛效果、是否发生不良反应、患者满意度的评估等[35]。有研究指出这种系统性疼痛评估可以改善治疗结局,减少围手术期的风险,降低住院时间[36-37]。
推荐意见14:对于疑诊胆管炎、胰腺炎的患者,NTAAA时慎用阿片类药物,可给予NSAIDs镇痛同时可辅助性给予解痉药。
一项研究发现包括杜冷丁、吗啡在内的所有阿片类药物均会不同程度的引起Oddi’s括约肌收缩,从而可能导致胆道压力升高、加重胆管炎、胰腺炎病情[38]。NSAIDs对胆管炎、胰腺炎的镇痛效果和阿片类药物相近,如无禁忌,可作为首选,同时可辅助性给予解痉药。
一些辅助药物可增加镇痛剂的效果,从而减少镇痛剂的使用剂量。这些药物包括解痉药、皮质类固醇激素、抗抑郁药、抗惊厥药等。
(1)解痉药:如山莨菪碱、间苯三酚等,可作为缓解绞痛的辅助用药。
(2)皮质类固醇激素:如地塞米松和强的松等,可以减轻周围神经水肿和压迫神经引起的疼痛。
(3)抗抑郁药:如阿米替林、多虑平、美舒郁、百忧解等,可镇痛、镇静、改善情绪和心情。
(4)抗惊厥药:如卡马西平、苯妥英钠等,可减轻神经源性疼痛和放化疗引起的肌肉痉挛性疼痛。
执笔人:马义祥、刘斯(北京大学第一医院急诊科)
共识专家组成员(以姓氏拼音为序):范昭(北京大学深圳医院急诊科) 高雨松(北京大学第一医院急诊科) 李硕(北京大学第三医院急诊科) 刘秀芬(北京大学第一医院疼痛科) 马青变(北京大学第三医院急诊科) 秦宇红(北京大学国际医院急诊科) 周启棣(北京大学深圳医院急诊科) 王传林(北京大学人民医院急诊科) 王武超(北京大学人民医院急诊科) 王聪(北京积水潭医院急诊科) 王东信(北京大学第一医院麻醉科) 王真(北京世纪坛医院急诊科) 汪欣(北京大学第一医院普外科) 王旭东(航天中心医院急诊科) 温伟(北京医院急诊科) 熊辉(北京大学第一医院急诊科) 闫圣涛(中日友好医院急诊科) 张新超(北京医院急诊科) 张国强(中日友好医院急诊科) 祝振忠(北京大学首钢医院急诊科) 赵斌(北京积水潭医院急诊科) 朱继红(北京大学人民医院急诊科) 张利华(北京大学滨海医院急诊科)
致谢: 本共识在起草、讨论与定稿过程中凝聚了北京大学医学部急诊医学学系20余位专家的心血。
利益冲突 所有作者均声明不存在利益冲突。
| [1] | Mayumi T, Yoshida M, Tazuma S, et al. The practice guidelines for primary care of acute abdomen 2015[J]. Jpn J Radiol, 2016, 34(1): 80-115. DOI:10.1007/s11604-015-0489-z |
| [2] | Hustey FM, Meldon SW, Banet GA, et al. The use of abdominal computed tomography in older ED patients with acute abdominal pain[J]. Am J Emerg Med, 2005, 23(3): 259-265. DOI:10.1016/j.ajem.2005.02.021 |
| [3] | Lewis LM, Banet GA, Blanda M, et al. Etiology and clinical course of abdominal pain in senior patients: a prospective, multicenter study[J]. J Gerontol A Biol Sci Med Sci, 2005, 60(8): 1071-1076. DOI:10.1093/gerona/60.8.1071 |
| [4] | Silen W. Cope's early diagnosis of the acute abdomen18th ed [M]. Oxford University press, 1991. |
| [5] | Ranji SR, Goldman LE, Simel DL, et al. Do opiates affect the clinical evaluation of patients with acute abdominal pain?[J]. JAMA, 2006, 296(14): 1764. DOI:10.1001/jama.296.14.1764 |
| [6] | Thomas SH, Silen W, Cheema F, et al. Effects of morphine analgesia on diagnostic accuracy in Emergency Department patients with abdominal pain: a prospective, randomized trial[J]. J Am Coll Surg, 2003, 196(1): 18-31. DOI:10.1016/s1072-7515(02)01480-1 |
| [7] | 宋飞, 蔡清萍, 李扬, 等. 早期使用止痛剂对急腹症体格检查及诊断影响研究[J]. 中国实用外科杂志, 2007, 27(9): 716-719. |
| [8] | Stuart IM. Cope's early diagnosis of the acute abdomen, 19th ed[J]. J Vasc Surg, 1997, 26(4): 724-725. |
| [9] | Early Diagnosis of the Acute Abdomen (ed 14). Cope Z : New York, Oxford University Press, 1972. |
| [10] | Fraser ID. Analgesia and the acute abdomen[J]. Br Med J, 1979, 2(6201): 1363. DOI:10.1136/bmj.2.6201.1363-b |
| [11] | Zoltie N. Analgesia in the acute abdomen[M]. Ann R Coll Surg Engl, 1986: 209-10. |
| [12] | Attard AR, Corlett MJ, Kidner NJ, et al. Safety of early pain relief for acute abdominal pain[J]. BMJ, 1992, 305(6853): 554-556. DOI:10.1136/bmj.305.6853.554 |
| [13] | Pace S, Burke TF. Intravenous morphine for early pain relief in patients with acute abdominal pain[J]. Acad Emerg Med, 1996, 3(12): 1086-1092. DOI:10.1111/j.1553-2712.1996.tb03365.x |
| [14] | Mahadevan M, Graff L. Prospective randomized study of analgesic use for ED patients with right lower quadrant abdominal pain[J]. Am J Emerg Med, 2000, 18(7): 753-756. DOI:10.1053/ajem.2000.16315 |
| [15] | Wolfe JM, Smithline HA, Phipen S, et al. Does morphine change the physical examination in patients with acute appendicitis?[J]. Am J Emerg Med, 2004, 22(4): 280-285. DOI:10.1016/j.ajem.2004.02.015 |
| [16] | Oguzturk H, Ozgur D, Turtay MG, et al. Tramadol or paracetamol do not effect the diagnostic accuracy of acute abdominal pain with significant pain relief - a prospective, randomized, placebo controlled double blind study[J]. Eur Rev Med Pharmacol Sci, 2012, 16(14): 1983-1988. |
| [17] | Attard AR, Corlett MJ, Kidner NJ, et al. Safety of early pain relief for acute abdominal pain[J]. BMJ, 1992, 305(6853): 554-556. DOI:10.1136/bmj.305.6853.554 |
| [18] | Brandt MM. Cope's early diagnosis of the acute abdomen, 20th edition. Written by William silen, MD. 296 pages, illustrated. $29.95. New york: Oxford university press, 2000[J]. J Am Coll Surg, 2000, 191(4): 476. DOI:10.1016/S1072-7515(00)00722-5 |
| [19] | Early Diagnosis of the Acute Abdomen. Silen W : New York, Oxford University Press, 1996. |
| [20] | LoVecchio F, Oster N, Sturmann K, et al. The use of analgesics in patients with acute abdominal pain[J]. J Emerg Med, 1997, 15(6): 775-779. DOI:10.1016/s0736-4679(97)00183-2 |
| [21] | Clinical policy: critical issues for the initial evaluation and management of patients presenting with a chief complaint of nontraumatic acute abdominal pain[J]. Ann Emerg Med, 2000, 36(4): 406-415. DOI: 10.1067/mem.2000.109446. |
| [22] | Gagliese L, Weizblit N, Ellis W, et al. The measurement of postoperative pain: a comparison of intensity scales in younger and older surgical patients[J]. Pain, 2005, 117(3): 412-420. DOI:10.1016/j.pain.2005.07.004 |
| [23] | Wong DL, Baker CM. Pain in Children: Comparison of Assessment Scales[J]. Pediatric Nursing, 1988, 14(1): 9. |
| [24] | Bozimowski G. A review of nonsteroidal anti-inflammatory drugs[J]. AANA J, 2015, 83(6): 425-433. |
| [25] | McNicol ED, Tzortzopoulou A, Cepeda MS, et al. Single-dose intravenous paracetamol or propacetamol for prevention or treatment of postoperative pain: a systematic review and meta-analysis[J]. Br J Anaesth, 2011, 106(6): 764-775. DOI:10.1093/bja/aer107 |
| [26] | Grundmann U, Wörnle C, Biedler A, et al. The efficacy of the non-opioid analgesics parecoxib, paracetamol and metamizol for postoperative pain relief after lumbar microdiscectomy[J]. Anesth Analg, 2006, 103(1): 217-222. DOI:10.1213/01.ane.0000221438.08990.06 |
| [27] | Ong CK, Seymour RA, Lirk P, et al. Combining paracetamol (acetaminophen) with nonsteroidal antiinflammatory drugs: a qualitative systematic review of analgesic efficacy for acute postoperative pain[J]. Anesth Analg, 2010, 110(4): 1170-1179. DOI:10.1213/ANE.0b013e3181cf9281 |
| [28] | Webb A, Leong S. The combination of tramadol and morphine may b recommended for postoperative analges[J]. Anesth Analg, 2005, 101(6): 1884-1885. DOI:10.1213/01.ANE.0000180271.88987.5B |
| [29] | Ozalevli M, Unlügenç H, Tuncer U, et al. Comparison of morphine and tramadol by patient-controlled analgesia for postoperative analgesia after tonsillectomy in children[J]. Paediatr Anaesth, 2005, 15(11): 979-984. DOI:10.1111/j.1460-9592.2005.01591.x |
| [30] | Laskowski K, Stirling A, McKay WP, et al. A systematic review of intravenous ketamine for postoperative analgesia[J]. J Can D'anesthesie, 2011, 58(10): 911-923. DOI:10.1007/s12630-011-9560-0 |
| [31] | Zhang J, Ho KY, Wang Y. Efficacy of pregabalin in acute postoperative pain: a meta-analysis[J]. Br J Anaesth, 2011, 106(4): 454-462. DOI:10.1093/bja/aer027 |
| [32] | Engelman E, Marsala C. Efficacy of adding clonidine to intrathecal morphine in acute postoperative pain: meta-analysis[J]. Br J Anaesth, 2013, 110(1): 21-27. DOI:10.1093/bja/aes344 |
| [33] | Mayumi T, Yoshida M, Tazuma S, et al. The practice guidelines for primary care of acute abdomen 2015[J]. Jpn J Radiol, 2016, 34(1): 80-115. DOI:10.1007/s11604-015-0489-z |
| [34] | Swarm RA, Paice JA, Anghelescu DL, et al. Adult cancer pain, version 3.2019, NCCN clinical practice guidelines in oncology[J]. J Natl Compr Canc Netw, 2019, 17(8): 977-1007. DOI:10.6004/jnccn.2019.0038 |
| [35] | Devlin JW, Skrobik Y, Gélinas C, et al. Clinical practice guidelines for the prevention and management of pain, agitation/sedation, delirium, immobility, and sleep disruption in adult patients in the ICU[J]. Crit Care Med, 2018, 46(9): e825-e873. DOI:10.1097/CCM.0000000000003299 |
| [36] | Payen JF, Bosson JL, Chanques G, et al. Pain assessment is associated with decreased duration of mechanical ventilation in the intensive care unit: a post Hoc analysis of the DOLOREA study[J]. Anesthesiology, 2009, 111(6): 1308-1316. DOI:10.1097/ALN.0b013e3181c0d4f0 |
| [37] | Chou R, Gordon DB, de Leon-Casasola OA, et al. Management of postoperative pain: a clinical practice guideline from the American pain society, the American society of regional anesthesia and pain medicine, and the American society of anesthesiologists' committee on regional anesthesia, executive committee, and administrative council[J]. J Pain, 2016, 17(2): 131-157. DOI:10.1016/j.jpain.2015.12.008 |
| [38] | Elta GH, Barnett JL. Meperidine need not be proscribed during sphincter of Oddi manometry[J]. Gastrointest Endosc, 1994, 40(1): 7-9. DOI:10.1016/s0016-5107(94)70002-8 |
 2020, Vol. 29
2020, Vol. 29




