近些年来,机器损伤、车祸、坠落伤等造成的创伤导致患者死亡的人数逐年呈上升趋势[1],严重创伤患者常合并创伤失血性休克,是造成严重创伤患者早期死亡最常见原因之一,如果缺乏及时有效的治疗,患者随时可能会出现呼吸及心搏骤停[2-3]。液体复苏是创伤失血性休克患者最主要的治疗措施。现阶段提倡在创伤失血性休克早期,即出血未控制时采用限制性复苏,而关于复苏液体的选择一直都存在争议。目前晶体液是临床常用的复苏液体[4],包括生理盐水、乳酸钠林格液和醋酸林格液等,但临床应用中都存在各自的不足之处。碳酸氢钠林格液是新一代的晶体液,由多种电解质(含钠、钾、镁、钙离子)成份组成的复方制剂,对于循环血流量和组织间液减少时细胞外液的补充校正,以及代谢性酸中毒的纠正[5]有较好的临床效果,但目前关于其应用于创伤失血性休克的复苏效果的研究较少。本研究以创伤性失血性休克兔为研究模型,通过采用不同晶体液进行液体复苏,观察碳酸氢钠林格液对兔子的心率、平均动脉压(mean arterial pressure,MAP)、动脉血气及生存率等的影响,为临床治疗创伤失血性休克提供新思路。
1 材料与方法 1.1 实验动物与分组健康级日本长耳大白兔30只5~7月龄,雌雄各半,体质量约2.3 kg,由安徽医科大学实验动物中心提供,随机(随机数字法)分成3组:正常对照组(NC组)10只,乳酸钠林格液复苏组(LRS组)10只,碳酸氢钠林格液复苏组(BRS组)10只。动物在实验前禁食12 h,禁水8 h。本研究经安徽医科大学实验动物伦理委员会批准,研究中所有操作程序均符合安徽医科大学动物伦理委员会相关规定。
1.2 主要实验器材及试剂高速低温离心机Eppendorf(德国);BL420E+生物功能实验系统(成都泰能仪器有限公司);i-STAT便携式血气分析仪及电子模拟器;戊巴比妥钠(上海制药厂);肝素钠(赛诺);乳酸钠林格注射液(天津天安);碳酸氢钠林格液(江苏恒瑞)。
1.3 模型制备及给药方法用Lamson's法建立创伤性休克动物模型[6]。3%戊巴比妥钠溶液30 mg/kg经耳缘静脉注射麻醉后,将兔仰卧并固定于小动物手术台,行右侧颈动脉、股动脉插管术,经耳缘静脉注射肝素(6 mg/kg)将兔全身肝素化,股动脉导管接换能器与BL420E+生物功能实验系统连接,监测MAP及心率(heart rate,HR);颈动脉插管用于放血和采取血液标本。上述手术完成后,用3 kg铁锤在0.5 m高处垂直下落,击打兔股骨中段,致粉碎性骨折;再经右颈动脉快速放血(约10 min)使MAP降至35~45 mmHg(1 mmHg=0.133 kPa),并维持45 min[7]。然后,对兔子进行包扎止血、外固定进入复苏期。LRS组经耳缘静脉回输全部失血及等量乳酸钠林格液;BRS组回输全部失血及等量碳酸氢钠林格液进行复苏,复苏时间约需60 min。NC组动物仅做颈动脉、股动脉插管及全身肝素化,未行击打及放血。
1.4 检测指标BL420E+生物功能实验系统检测记录NC组、LRS组及BRS组休克前即基础期(T1)、休克后(T2)、复苏期后(T3)、复苏期后2 h(T4)各时间点兔子的血压和心率,并采动脉血进行血气分析。分别于制备模型后12、24、36、48 h记录各组实验动物死亡数量,计算存活率,存活率=某一时间点某组存活的日本长耳大白兔/同组日本长耳大白兔数×100%。
1.5 统计学方法使用SPSS 22.0统计软件进行分析,定量数据以均数±标准差(Mean±SD)表示,组内比较采用重复测量设计的方差分析,组间比较采用单因素方差分析,多重比较用LSD法,各组生存时间的比较采用Kaplan生存分析。以P < 0.05为差异有统计学意义。
2 结果 2.1 实验前各组兔子基础情况比较三组兔子基本情况、月龄、体质量、基础血压比较,差异无统计学意义(P>0.05),见表 1。
| 组别 | 月龄(个月) | 体质量(kg) | 血压(mmHg) |
| NC组 | 5.94±0.61 | 2.33±0.36 | 97.02±2.86 |
| LRS组 | 5.76±0.71 | 2.28±0.28 | 94.38±4.60 |
| BRS组 | 6.12±0.65 | 2.24±0.32 | 95.64±3.36 |
| F值 | 0.748 | 0.197 | 1.287 |
| P值 | 0.483 | 0.823 | 0.292 |
| 注:NC组为正常对照组,LRS组为乳酸钠林格液组,BRS组为碳酸氢钠林格液组;1 mmHg=0.133 kPa | |||
休克前基础期(T1时间点),各组间MAP比较差异无统计学意义(P>0.05);休克后(T2时间点)实验组(LRS组和BRS组)相对于对照组(NS组),MAP下降,差异有统计学意义(P < 0.05);不同液体复苏后(T3时间点),BRS组与LRS组相比,MAP升高,差异有统计学意义(P < 0.05);复苏后2 h(T4时间点),BRS组相比LRS组MAP升高,差异有统计学意义(P < 0.05)。NC组各不同时间点指标差异无统计学意义(P>0.05),见表 2。
| 组别 | T1 | T2 | T3 | T4 |
| NC组 | 97.02±2.86 | 95.38±3.53 | 96.42±4.61 | 94.29±2.19 |
| LRS组 | 94.38±4.60 | 43.27±3.61a | 70.69±5.34a | 79.24±3.81a |
| BRS组 | 95.64±3.36 | 41.76±3.28a | 77.34±3.83ab | 87.79±2.94ab |
| F值 | 1.287 | 771.396 | 83.051 | 61.142 |
| P值 | 0.292 | < 0.01 | < 0.01 | < 0.01 |
| 注:NC组为正常对照组,LRS组为乳酸钠林格液组,BRS组为碳酸氢钠林格液组;T1为基础期、T2为休克后、T3为复苏期后、T4为复苏后2 h;与NC组比较,aP < 0.05;与LRS组比较,bP < 0.05 | ||||
休克前T1时间点,各组间HR比较差异无统计学意义(P>0.05);休克后T2时间点实验组相对于对照组,HR下降,差异有统计学意义(P < 0.05);不同液体复苏后T3时间点,BRS组与LRS组相比,HR下降,差异有统计学意义(P < 0.05);T4时间点,BRS组相比LRS组HR下降,差异有统计学意义(P < 0.05)。NC组各不同时间点指标差异无统计学意义(P>0.05),见表 3。
| 组别 | T1 | T2 | T3 | T4 |
| NC组 | 276.3±23.6 | 283.4±18.9 | 274.3±16.4 | 268.5±26.7 |
| LRS组 | 268.3±26.4 | 223.4±18.6a | 220.1±14.2a | 211.3±15.6a |
| BRS组 | 282.6±17.8 | 231.7±17.6a | 205.4±12.7ab | 191.9±16.8ab |
| F值 | 0.981 | 31.304 | 56.299 | 30.867 |
| P值 | 0.388 | < 0.01 | < 0.01 | < 0.01 |
| 注:NC组为正常对照组,LRS组为乳酸钠林格液组,BRS组为碳酸氢钠林格液组;T1为基础期、T2为休克后、T3为复苏期后、T4为复苏后2 h;与NC组比较,aP < 0.05;与LRS组比较,bP < 0.05 | ||||
休克前T1时间点,各组间pH比较差异无统计学意义(P>0.05);休克后T2时间点,实验组相对于对照组,pH下降,差异有统计学意义(P < 0.05);不同液体复苏后T3时间点,BRS组与LRS组相比pH升高,差异有统计学意义(P < 0.05);T4时间点BRS组相比LRS组pH升高,差异有统计学意义(P < 0.05)。NC组各不同时间点指标差异无统计学意义(P>0.05),见表 4。
| 组别 | T1 | T2 | T3 | T4 |
| NC组 | 7.42±0.04 | 7.41±0.03 | 7.39±0.02 | 7.44±0.03 |
| LRS组 | 7.41±0.04 | 7.03±0.061a | 7.13±0.03a | 7.21±0.04a |
| BRS组 | 7.40±0.02 | 7.05±0.03a | 7.26±0.05ab | 7.31±0.04ab |
| F值 | 0.833 | 254.074 | 133.421 | 97.317 |
| P值 | 0.455 | < 0.01 | < 0.01 | < 0.01 |
| 注:NC组为正常对照组,LRS组为乳酸钠林格液组,BRS组为碳酸氢钠林格液组;T1为基础期、T2为休克后、T3为复苏期后、T4为复苏后2 h;与NC组比较,aP < 0.05;与LRS组比较,bP < 0.05 | ||||
休克前T1时间点,各组间Lac比较差异无统计学意义(P>0.05);休克后T2时间点,实验组相对于对照组Lac升高,差异有统计学意义(P < 0.05);不同液体复苏后T3时间点,BRS组与LRS组相比Lac降低,差异有统计学意义(P < 0.05);T4时间点,BRS组相比LRS组Lac降低,差异有统计学意义(P < 0.05)。NC组各不同时间点指标差异无统计学意义(P>0.05),见表 5。
| 组别 | T1 | T2 | T3 | T4 |
| NC组 | 2.34±0.67 | 2.38±0.71 | 2.58±0.84 | 2.63±0.78 |
| LRS组 | 2.27±0.56 | 10.67±1.98a | 9.32±2.34a | 7.89±2.47a |
| BRS组 | 1.94±0.68 | 11.33±2.51a | 7.13±2.53ab | 6.09±1.94ab |
| F值 | 1.118 | 69.589 | 28.185 | 20.472 |
| P值 | 0.342 | < 0.01 | < 0.01 | < 0.01 |
| 注:NC组为正常对照组,LRS组为乳酸钠林格液组,BRS组为碳酸氢钠林格液组;T1为基础期、T2为休克后、T3为复苏期后、T4为复苏后2 h;与NC组比较,aP < 0.05;与LRS组比较,bP < 0.05 | ||||
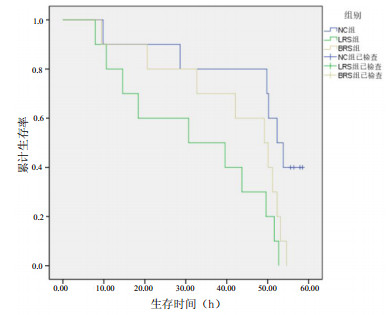
各组创伤性失血性休克兔12、24、36、48 h生存率见表 6。NC组因仅作插管各时点生存率最高;BRS组各时点生存率比LRS组高,差异有统计学意义(P < 0.05)。Kaplan生存分析显示BRS组比LRS组存活时间长(P < 0.05),见图 1。
|
| NC组为正常对照组,LRS组为乳酸钠林格液组,BRS组为碳酸氢钠林格液组 图 1 各组动物Kaplan生存曲线 Fig 1 Kaplan survival curve for each group |
|
|
| 组别 | 存活率 | |||
| 12 h | 24 h | 36 h | 48 h | |
| NC组 | 9/10 | 9/10 | 8/10 | 8/10 |
| LRS组 | 8/10a | 6/10a | 5/10a | 3/10a |
| BRS组 | 9/10b | 8/10ab | 7/10ab | 6/10ab |
| 注:NC组为正常对照组,LRS组为乳酸钠林格液组,BRS组为碳酸氢钠林格液组。与NC组比较,aP < 0.05;与LRS组比较,bP < 0.05 | ||||
创伤性失血性休克时有效循环血量严重不足,可导致组织灌注不足、细胞缺氧、组织损伤和死亡,液体复苏是创伤性失血性休克早期急救的重要手段之一,它直接影响患者的预后情况[8-9]。碳酸氢钠林格液作为新一代的晶体液,在创伤及围手术期补液中具有其一定的优势。2005年,Satoh等[10]研究表明,在狗出血性休克模型中碳酸氢钠林格液比醋酸钠林格液能更快更显著地改善BE值,碳酸氢钠林格液的碱化效果优于醋酸钠林格液,相对其他林格液,碳酸氢钠林格液对Mg2+浓度稳定性更好。Sasano等[11]研究指出接受胃切除术的MELAS综合征(线粒体肌病脑病伴乳酸中毒及中风样发作)患者,术中使用生理浓度的碳酸氢钠林格液,血清乳酸水平无明显升高,手术开始至术后3 h未发生代谢性酸中毒。日本学者在对接受开胸手术的婴儿和儿童的研究中发现,碳酸氢钠林格液组与醋酸林格液组间在各时点的pH、HCO3-、碱过量和乳酸值均差异无统计学意义,但碳酸氢钠林格液组术中给予碳酸氢钠的量明显小于醋酸林格液组[12]。
本研究的目的是确定和比较使用乳酸钠林格液和碳酸氢钠林格液对创伤失血性休克兔的血液动力学、动脉血气及生存率的影响。本研究对三个实验组兔进行基本月龄,体质量和血压评估,差异无统计学意义,因此,这些因素的干扰基本被排除。本研究结果提示,BRS组和LRS组MAP及HR在休克补液后差异有统计学意义,输注碳酸氢钠林格液的创伤失血性休克兔具有更好的血流动力学稳定性。另外,相关的血液检测指标也表明,输注碳酸氢钠林格液后,血乳酸水平明显下降,动脉血pH值也得到明显改善,且创伤失血性休克兔的存活率也明显升高,与LRS组相比,差异有统计学意义,表明碳酸氢钠林格液能够明显降低血乳酸水平,更有助于维持创伤失血性休克兔体内的酸碱平衡,并提高创伤失血性休克兔的存活率。乳酸是组织、器官灌注不足或组织、器官损伤氧利用的障碍,无氧酵解取代有氧代谢,产生大量酸性物质酮体、乳酸等有害物质[13]。更有学者认为,早期乳酸水平的监测更有临床意义,可作为预测休克及循环衰竭的危险因子之一[14]。一些基础研究及临床研究对乳酸钠林格液的复苏效果产生质疑[15-16],认为其能造成乳酸堆积,引起细胞内乳酸酸中毒,加重器官水肿,并能引起氧化应激、激活炎症因子,加重机体损伤。而本实验证明在使用碳酸氢钠林格液后,相对于乳酸钠林格液能够明显降低血乳酸水平,改善血pH值,维持机体的酸碱平衡稳定,这主要与碳酸氢钠林格液中含有独有的HCO3-缓冲体系有关。
综上所述,在创伤失血性休克兔的液体复苏中,与乳酸钠林格液相比,碳酸氢钠林格液能够明显降低血乳酸水平,并维持机体酸碱平衡及循环稳定,有望成为创伤失血性休克救治中的有效晶体液。本研究的主体为创伤失血性休克兔模型,对于临床中创伤失血性休克患者是否有同样的效果,尚需进一步的研究。
利益冲突 所有作者均声明不存在利益冲突
| [1] | Gando S, Otomo Y. Local hemostasis, immunothrombosis, and systemic disseminated intravascular coagulation in trauma and traumatic shock[J]. Crit Care, 2015, 19(1): 72. DOI:10.1186/s13054-015-0735-x |
| [2] | Tremoleda JL, Watts SA, Reynolds PS, et al. Modeling acute traumatic hemorrhagic shock injury[J]. Shock, 2017, 48(6): 610-623. DOI:10.1097/shk.0000000000000901 |
| [3] | Hutchings SD, Naumann DN, Hopkins P, et al. Microcirculatory impairment is associated with multiple organ dysfunction following traumatic hemorrhagic shock[J]. Crit Care Med, 2018, 46(9): e889-e896. DOI:10.1097/ccm.0000000000003275 |
| [4] | 刘国辉. 创伤失血性休克液体复苏策略[J]. 中华急诊医学杂志, 2018, 27(5): 473-475. DOI:10.3760/cma.j.issn.1671-0282.2018.05.003 |
| [5] | Heidari S, Hashemi S, Yaraghi A, et al. Acid-base and hemodynamic status of patients with intraoperative hemorrhage using two solution types:Crystalloid Ringer lactate and 1.3% sodium bicarbonate in half-normal saline solution[J]. Adv Biomed Res, 2016, 5(1): 190. DOI:10.4103/2277-9175.191000 |
| [6] | Fishman EK, Horton KM, Urban BA. Multidetector CT angiography in the evaluation of pancreatic carcinoma:preliminary observations[J]. J Comput Assist Tomogr, 2000, 24(6): 849-853. DOI:10.1097/00004728-200011000-00005 |
| [7] | Nielsen VG. Endogenous heparin decreases the thrombotic response to hemorrhagic shock in rabbits[J]. J Crit Care, 2001, 16(2): 64-68. DOI:10.1053/jcrc.2001.26292 |
| [8] | Jacob M, Kumar P. The challenge in management of hemorrhagic shock in trauma[J]. Med J Armed Forces India, 2014, 70(2): 163-169. DOI:10.1016/j.mjafi.2014.03.001 |
| [9] | Chang R, Holcomb JB. Optimal fluid therapy for traumatic hemorrhagic shock[J]. Crit Care Clin, 2017, 33(1): 15-36. DOI:10.1016/j.ccc.2016.08.007 |
| [10] | Satoh K, Ohtawa M, Okamura E, et al. Pharmacological study of BRS, a new bicarbonated Ringer's solution, in partially hepatectomized rabbits[J]. Eur J Anaesthesiol, 2005, 22(8): 624-629. DOI:10.1017/s0265021505001043 |
| [11] | Sasano N, Fujita Y, So M, et al. Anesthetic management of a patient with mitochondrial myopathy, encephalopathy, lactic acidosis, and stroke-like episodes (MELAS) during laparotomy[J]. J Anesth, 2007, 21(1): 72-75. DOI:10.1007/s00540-006-0449-y |
| [12] | Asano M, Doi Y, Soen M, et al. Effects of bicarbonated Ringer's solution for infants and children undergoing open-heart surgery[J]. Masui, 2009(58): 897-902. |
| [13] | 颜海鹏, 卢秀兰, 仇君, 等. 血乳酸在脓毒症患儿病情及预后评价中的意义[J]. 中国当代儿科杂志, 2016, 18(6): 506-510. DOI:10.7499/j.issn.1008-8830.2016.06.008 |
| [14] | Bakker J, Jansen TC. Don't take vitals, take a lactate[J]. Intensive Care Med, 2007, 33(11): 1863-1865. DOI:10.1007/s00134-007-0679-y |
| [15] | Hussmann B, Lendemans S, de Groot H, et al. Volume replacement with Ringer-lactate is detrimental in severe hemorrhagic shock but protective in moderate hemorrhagic shock:studies in a rat model[J]. Crit Care, 2014, 18(1): R5. DOI:10.1186/cc13182 |
| [16] | Rohrig R, Rönn T, Lendemans S, et al. Adverse effects of resuscitation with lactated ringer compared with ringer solution after severe hemorrhagic shock in rats[J]. Shock, 2012, 38(2): 137-145. DOI:10.1097/shk.0b013e31825b4ed9 |
 2020, Vol. 29
2020, Vol. 29




