2 天津医科大学总医院医院急诊科,300052
2 Department of Emergency Medicine, General Hospital Affiliated to Tianjin Medical University, Tianjin 300052, China
胸痛是急诊科常见的就诊症状,以急性胸痛就诊的患者占急诊内科疾病的5%~20%[1]。引起胸痛的病因涉及到多种疾病,主要为胸部疾病引起,少数为其他疾病所致,理论上各种物理、化学因素及刺激因子均可刺激胸部感觉神经纤维产生痛觉冲动,传至大脑皮层的痛觉中枢即引起胸痛。胸痛性疾病容易导致猝死,致命性胸痛除急性冠脉综合征,还包括主动脉夹层、肺栓塞、张力性气胸和心包填塞等,除ST段抬高型急性心肌梗死患者通过心电图即可获得初步诊断,大部分患者都不能立即明确诊断而需要进一步检查、留观。因此,在临床实践中目前普遍做法是建议不能除外高危胸痛的患者急诊留观6~12 h,而最后大约只有15%~25%的患者确诊为高危胸痛,其中主要为急性冠脉综合征。这必然导致本就紧张拥挤的急诊科更加拥挤不堪。以美国为例,每年因胸痛和心肌缺血而就诊的急诊患者大概有600万[2],其中包括大约300万最后未发现严重疾病的胸痛患者,急诊的花费大概为(30~40)亿美元[3-4],这些患者在急诊均有不同程度的留观。中国目前未见准确的数据,但是按照人口规模以及更加拥挤的急诊现状,应该不会低于美国。
胸痛快速危险分层方案是对急性胸痛患者进行快速评估,高效安全排除高危胸痛尤其是急性心肌梗死的一套方法。目前的研究集中在英国、新西兰、美国等发达国家。国内对这些方案的研究较少,评分之间进行比较的研究更加稀少,因此有必要对其进行研究。本研究探讨TRUST加速诊断路径、EDACS加速诊断路径、温哥华胸痛诊断流程等3个0~2 h快速危险分层方案快速评估急诊胸痛患者的能力。以期改善目前胸痛患者留观时间长,患者反复抽血化验浪费医疗资源的问题,保证低危患者早期安全离院。
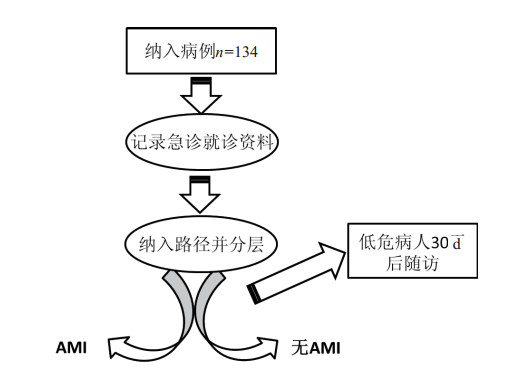
1 资料与方法收集2017年1月1日0时至2017年2月1日0时就诊于天津医科大学总医院急诊的疑似急性冠脉综合征的胸痛患者,患者年龄≥18岁,主诉必须包括前胸或侧胸疼痛,并签署随访同意书。急诊诊治期间记录患者的性别、年龄、基础疾病及危险因素、胸痛性质及伴随症状、生命体征、查体、初始心电图及2~h心电图、入院心肺功能五项及hs-cTnI结果、2~h心肌损伤三项结果、6~h hs-cTnI结果及初步诊断。对患者分别按TRUST加速诊断路径、EDACS加速诊断路径及温哥华胸痛诊断流程进行危险分层。随访记录患者30 d内发生急性心肌梗死的人数。使用SPSS软件进行数据统计,分析评估各流程对疑似急性冠状动脉综合征胸痛患者危险分层的性能并进行比较。该项研究获得医院伦理委员会审批,并取得患者或家属知情同意。流程图如图 1。
|
| 图 1 本研究的流程 Fig 1 The flow chart of the research process |
|
|
0~h和2~h:使用美国博适Alere Triage心肺功能五项及心肌损伤三项床旁快速检测仪,检测原理为双抗体夹心免疫荧光法。患者在诊室就诊后床旁完成抽血,检验同时在诊室进行,15 min输出结果。心肺功能五项包括肌红蛋白、肌酸激酶同工酶-2、心肌肌钙蛋白Ⅰ、脑利钠肽、D-二聚体,心肌损伤三项为肌红蛋白、肌酸激酶同工酶-2和心肌肌钙蛋白Ⅰ。各个标志物检测范围见表 1。
| 标志物 | 检测范围(ng/mL) | 临界值(ng/mL) |
| CK-MB | 1~80 | 4.3 |
| MYO | 5~500 | 107 |
| TNI | 0.05~30 | 0.4 |
| BNP | 5~5000 | 100 |
| DDIM | 100~5000 | 600 |
0~h和6~h:采用日本三菱PATHFAST床旁超敏肌钙蛋白Ⅰ(hs-cTnI)快速检测平台,床旁抽血15 min完成检测。检测原理为化学发光酶联免疫技术(CLEIA)和Magtration专利技术,hs-cTnI检测范围0.001~50 ng/mL,第99百分位值0.02 ng/mL。
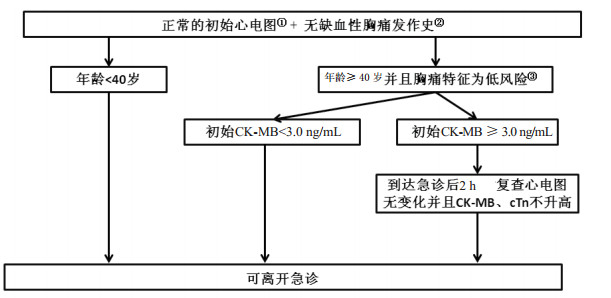
1.2 诊断路径说明温哥华胸痛诊断流程(图 2);TRUST加速诊断路径(表 2)和EDACS加速诊断路径(表 3)。
|
| ①T波低平可认为是正常心电图;②缺血性胸痛定义为既往有明确诊断的心肌梗死或心绞痛病史,有劳力性心绞痛发作史,而且曾服用硝酸酯类药物;③低风险胸痛的特征:胸痛不伴放射痛(如放射至手臂、颈部、下颌);深呼吸时胸痛加重;胸壁触诊可诱发胸痛。特别注意:怀疑肺栓塞、主动脉夹层、气胸、食管破裂等其他高危胸痛时应该分别按相关指南进行处理 图 2 温哥华胸痛诊断流程 Fig 2 Vancouver chest pain rule |
|
|
| 以下指标得分相加(即改良Goldman评分)为总分 |
| 1.静息状态下新发胸痛 |
| 2.胸痛性质与既往心肌梗死相似 |
| 3.使用硝酸甘油15 min内胸痛未见缓解 |
| 4.疼痛 > 60 min |
| 5.疼痛频次较前增加 |
| 6.低血压(收缩压 < 100 mmHg) |
| 7.急性呼吸困难 |
| 8.胸痛发生于心肌梗死或血管重建后6周内 |
| 以上每项均为1分 |
| TRUST加速诊断路径: |
| 低危:改良Goldman总评分≤1分,ECG无缺血改变,hs-cTnI≤26.2 ng/L,可以离院 |
| 非低危:改良Goldman总评分 > 1分,ECG缺血改变,hs-cTnI > 26.2ng/L |
| EDACS项目 | 分值 |
| 年龄(岁) | |
| 18~45 | +2 |
| 46~50 | +4 |
| 51~55 | +6 |
| 56~60 | +8 |
| 61~65 | +10 |
| 66~70 | +12 |
| 71~75 | +14 |
| 76~80 | +16 |
| 81~85 | +18 |
| 86+ | +20 |
| 男性 | +6 |
| 年龄18~50岁并且以下包含一项 | +4 |
| (ⅰ)冠心病(既往心梗、CABG、PCI史) | |
| (ⅱ)≥ 3个危险因素(早发冠心病家族史、血脂异常、糖尿病、高血压、正在吸烟) | |
| 症状和体征 | |
| 出汗 | +3 |
| 胸痛放射至手臂或肩部 | +5 |
| 吸气时胸痛或吸气加重 | -4 |
| 胸痛为触诊导致的疼痛 | -6 |
| EDACS加速诊断路径: | |
| 低危:EDACS < 16;心电图无新发缺血性改变;0~h及2~h肌钙蛋白均正常。(注:患者生命体征不稳定或胸痛持续不缓解、胸痛进行性加重不能认定为低危) | |
| 高危:EDACS ≥ 16;心电图新发缺血性改变;0~h或2~h肌钙蛋白异常。 |
胸痛指必须包含有锁骨以下,肋弓以上,双侧腋后线之前发生的疼痛,包括压榨样痛、针刺样痛、钝痛、烧灼痛、闷痛、胀痛等所有性质的疼痛。
1.4 急性心肌梗死诊断标准[5]按照2012急性心肌梗死全球统一定义,指血清心肌标志物(主要指心肌肌钙蛋白)升高(超过99%参考值上限)且伴有以下至少一项临床指标:心肌缺血症状;新出现的心电图缺血性改变(新出现的心电图ST-T改变或左束支传导阻滞或心电图病理性Q波形成);影像学上出现新的心肌活性丧失或新发的局部室壁运动异常;冠脉造影或尸检证实冠状动脉内有血栓。
1.5 所用指标说明参考经典文献,敏感度≥98%[6];阴性预测值≥99.5%[7];低危患者占比 > 30%[8]。
1.6 排除标准明确为急性ST段抬高型心肌梗死或新发左束支传导阻滞,心律失常(新发房颤或房扑,持续性室上速,二度或完全性房室传导阻滞,持续性或周期性室性心律),心包积液,明确为其他高危胸痛(例如肺栓塞、主动脉夹层、气胸),妊娠,需要透析的肾衰患者,拒绝抽血化验的患者,离院后不能随访(失访)患者。
1.7 统计学方法应用SPSS 20.0统计软件进行统计学分析。采用2×2表格形式并用χ2检验计算敏感度,特异度,阴性预测值,阳性预测值,阳性似然比,阴性似然比。以P < 0.05为有统计学意义。
2 结果 2.1 入组患者临床特征按照纳入标准及排除标准,本研究最终共入组134例患者,入组患者临床特征见表 4。
| 一般情况 | 数值 |
| 性别(男%) | 82(53.7) |
| 年龄,[均数(SD),岁] | 52.3(13.5) |
| 危险因素 | |
| 糖尿病(%) | 21(15.7) |
| 高血压(%) | 63(47.0) |
| 高脂血症(%) | 55(41.0) |
| 早发CAD家族史 | 0 |
| 正在吸烟或既往吸烟(%) | 42(31.3) |
| 既往病史 | |
| 心绞痛(%) | 14(10.4) |
| 心绞痛6周内加重 | 0 |
| 冠脉造影狭窄≥50%史(%) | 3(2.2) |
| 心肌梗死或PCI或CABG史 | 0 |
| 心衰史 | 0 |
| 脑卒中史(%) | 6(4.5) |
| 慢性肺病史(%) | 18(13.4) |
| 1周内使用阿司匹林(%) | 9(6.7) |
| 现病史 | |
| 劳力性心绞痛(%) | 24(17.9) |
| 放射痛 | 0 |
| 近24 h胸痛持续最长时间(h) | 15 |
| 深呼吸胸痛加重(%) | 15(11.2) |
| 胸壁触诊诱发胸痛(%) | 13(9.7) |
| 伴出汗(%) | 3(2.2) |
| 入院前曾服用硝酸酯类并可缓解胸痛(%) | 5(3.7) |
| 体格检查 | |
| 入院心率,均数(SD),次/min | 82(20.9) |
| 入院血压,(均数,mmHg) | 131/81 |
| 入院呼吸, 均数(SD),次/min | 18(2.6) |
| 入院SPO2,均数(SD),% | 98(1.2) |
| 肺部湿啰音(%) | 6(4.5) |
| 呼吸音低(%) | 10(7.5) |
| 下肢水肿(单侧) | 0 |
| 下肢水肿(双侧)(%) | 1(0.7) |
| 化验结果 | |
| 0-h hs-cTnI, 均数(ng/L) | 15.9 |
| 入院心肺五项(Mean) | |
| cTnI(ng/mL)① | - |
| CK-MB(ng/mL)② | - |
| MYO(ng/mL) | 65.3 |
| D-Dimer(ng/mL) | 571.5 |
| BNP(pg/mL) | 45.5 |
| 2-h心肌损伤三项(Mean) | |
| cTnI(ng/mL)① | - |
| CK-MB(ng/mL)② | - |
| MYO(ng/mL) | 89.3 |
| 6-h hs-cTnI(ng/L) | 19.4 |
| 注:①超过半数患者cTnI显示为检测极限 < 0.05 ng/mL,无法计算均值;②超过半数患者CK-MB显示为检测极限 < 1 ng/mL,无法计算均值。 | |
TRUST加速诊断路径共筛选低危患者57例,30天内随访结果发现急性心肌梗死1例,鉴别低危胸痛的敏感度为83.3%,特异度43.8%,阴性预测值98.2%,阳性预测值6.3%,阳性似然比1.5,阴性似然比0.4;低危患者占比 > 30%,但敏感度 < 98%,阴性预测值< 99.5%。EDACS加速诊断路径共筛选低危患者51例,30 d内随访结果未发现急性心肌梗死病例,鉴别低危胸痛的敏感度为100%,特异度39.8%,阴性预测值100%,阳性预测值7.2%,阳性似然比1.7,阴性似然比0;低危患者占比 > 30%,敏感度 > 98%,阴性预测值> 99.5%。温哥华胸痛诊断流程共筛选低危患者24例,30天内随访结果未发现急性心肌梗死病例,鉴别低危胸痛的敏感度为100%,特异度18.8%,阴性预测值100%,阳性预测值5.5%,阳性似然比1.2,阴性似然比0;低危患者占比 < 30%,但敏感度 > 98%,阴性预测值> 99.5%。见表 5。
| 指标 | TRUST加速诊断路径 | EDACS加速诊断路径 | 温哥华胸痛诊断流程 |
| 敏感度(%) | 83.3 | 100 | 100 |
| 特异度(%) | 43.8 | 39.8 | 18.8 |
| 阴性预测值(%) | 98.2 | 100 | 100 |
| 阳性预测值(%) | 6.3 | 7.2 | 5.5 |
| 阳性似然比 | 1.5 | 1.7 | 1.2 |
| 阴性似然比 | 0.4 | 0 | 0 |
| 低危占比(%) | 42.5 | 38.1 | 17.9 |
| 30 d内发生急性心肌梗死(%) | 1/57(1.8) | 0/51(0) | 0/24(0) |
近年来,随着我国人口老龄化加快,急诊医学科在胸痛中心建设中的作用越来越突出[9-10]。胸痛患者在排除是否为高危胸痛之前往往需要长时间的留观甚至需收住院检查,这导致了医疗资源的浪费并大大增加了患者经济负担。与此同时,每年漏诊的急性冠脉综合征患者大约在2%~10%[11]。胸痛快速危险分层方案是对急性胸痛患者进行快速评估,达到尽可能早期安全排除高危胸痛的一套方法,可减少不必要的急诊留观和抽血化验,并减少不必要的住院,减轻患者的经济负担。本研究通过对比3种快速危险分层方案鉴别急性胸痛患者的能力,显示快速危险分层方案有利于急性胸痛患者早期安全离院。
3.1 TRUST加速诊断路径在急诊胸痛中的应用TRUST加速诊断路径(Triage Rule-out Using high-Sensitivity Troponin accelerated diagnostic protocol,表 2)由英国伯恩茅斯大学Carlton教授在2015年提出[8],路径主要基于改良Goldman评分及超敏肌钙蛋白检测。Carlton教授在其研究中共纳入867例患者,就诊时间2012年6月到2013年8月,平均年龄57.9岁,以30 d之内发生急性心肌梗死作为研究终点,TRUST加速诊断路径鉴别低危胸痛的敏感度为92.8%,阴性预测值98.7%,特异度47.4%。
本研究共纳入134例患者,TRUST加速诊断路径鉴别低危胸痛敏感度为83.3%,特异度43.8%,阴性预测值98.2%,阳性预测值6.3%,阳性似然比1.5,阴性似然比0.4。与Carlton教授研究相比较,经卡方检验证实鉴别低危胸痛的效能差异无统计学意义(P > 0.05)(表 6)。
| 组别 | 中高危 | 低危 | χ2值 | P值 |
| 本研究 | 77 | 57 | 0.164 | 0.685 |
| Carlton研究 | 482 | 385 |
EDACS加速诊断路径(Emergency Department Assessment of Chest pain Score accelerated diagnostic protocol)由新西兰学者Than等[12]在急诊室胸痛评估评分系统基础上加入心电图及0-2h肌钙蛋白后于2014年提出。Than教授在初始研究中纳入1974例患者,以30天内发生主要心脏不良事件(Major adverse cardiac event,MACE)人数作为终点事件,其鉴别低危胸痛敏感度为99.0%,特异度49.9%。Than的后期验证研究则证实其敏感度为100%,特异度59.0%,低危占比达51.3%。在2015年[13]美国的一项共282例患者的验证研究结果并不让人满意,鉴别低危胸痛敏感度仅88.2%。同年,加拿大的验证研究[14]纳入763例患者,鉴别低危胸痛的敏感度达到100%,特异度46.4%,阴性预测值100%,阳性预测值17.5%。
本研究EDACS加速诊断路径鉴别低危胸痛的敏感度为100%,低危患者占比 > 30%,与Than等的研究一致;特异度为39.8%,阴性预测值100%,阳性预测值7.2%,阳性似然比1.7,阴性似然比0,达到低危患者占比 > 30%,敏感度 > 98%,阴性预测值> 99.5%的目标,且是3种快速危险分层方案中唯一一个达到此目标的路径,期待更多的相关研究,以利临床的广泛应用。
3.3 温哥华胸痛诊断流程在胸痛中的应用温哥华胸痛诊断流程(Vancouver chest pain rule)由Christenson等[15]在2006年提出,流程包括危险因素、胸痛特征、体格检查、ECG及心肌标志物等数项内容,研究共纳入769例胸痛患者,鉴别低危胸痛的敏感度为98.8%,特异度32.5%,阴性预测值99.0%,低危患者占比25.7%。2012年Jalili等[16]验证其鉴别低危胸痛敏感度95.1%,特异度56.3%,阴性预测值98.6%。
本研究中温哥华胸痛诊断流程鉴别低危胸痛的敏感度为100%,特异度18.8%,阴性预测值100%,阳性预测值5.5%,阳性似然比1.2,阴性似然比0。与Christenson等[15]的研究比较,敏感度和阴性预测值均达到100%,但低危患者占比仍旧较低,为3种路径中最少的一个。
综上所述,随着急诊胸痛患者逐年增多,探讨快速危险分层方案早期鉴别低危患者具有可行性,值得进一步研究探讨。EDACS加速诊断路径可能有利于急性胸痛低危患者早期安全离院。
本研究的局限性:本研究30天主要心脏不良事件统一以发生急性心肌梗死代替,这可能使部分30 d内发生了心脏不良事件并可能最终发展为急性心肌梗死的患者因充分救治归为未发生终点事件,使研究终点阳性率有所降低。
利益冲突 所有作者均声明不存在利益冲突
| [1] | Lee T H, Goldman L. Evaluation of the patient with acute chest pain[J]. New England Journal of Medicine, 2000, 342(16): 1187. DOI:10.1056/NEJM200004203421607 |
| [2] | Bhuiya FA, Pitts SR, McCaig LF. Emergency department visits for chest pain and abdominal pain: United States, 1999-2008[J]. Nchs Data Brief, 2010, 43: 1. PMID: 20854746. |
| [3] | Bruce D. McCarthy, John B. Wong, Dr. Harry P. Selker. Detecting acute cardiac ischemia in the emergency department[J]. Journal of General Internal Medicine, 1990, 5(4): 365-373. DOI:10.1007/BF02600409 |
| [4] | Lambrew C T. Chest pain evaluation: through a glass darkly[J]. Annals of Emergency Medicine, 1997, 29(1): 163-4. PMID: 8998097. |
| [5] | Thygesen K, Alpert J S, Jaffe A S, et al. Third universal definition of myocardial infarction[J]. Revista Espanola De Cardiologia, 2012, 55(3): 275. DOI:10.1093/eurheartj/ehs184 |
| [6] | Kline J, Johnson C, Pollack CJ, et al. Pretest probability assessment derived from attribute matching[J]. BMC Med Inform Decis Mak, 2005, 5: 26. DOI:10.1186/1472-6947-5-26 |
| [7] | Than M, Herbert M, Flaws D, et al. What is an acceptable risk of major adverse cardiac event in chest pain patients soon after discharge from the emergency department? a clinical survey[J]. International Journal of Cardiology, 2012, 166: 752-754. DOI:10.1016/j.ijcard.2012.09.171 |
| [8] | Carlton E, Cullen L, Than M, et al. A novel diagnostic protocol to identify patients suitable for discharge after a single high-sensitivity troponin[J]. Heart, 2015, 101: 1041-1046. DOI:10.1136/heartjnl-2014-307288 |
| [9] | 中华医学会急诊医学分会, 中国医疗保健国际交流促进会胸痛分会. 急性胸痛急诊诊疗专家共识[J]. 中华急诊医学杂志, 2019, 28(4): 413-420. DOI:10.3760/cma.j.issn.1671-0282.2019.04.002 |
| [10] | 汪正权, 高金丹, 谢开娜, 张燕燕, 李子龙. 县级医院急诊医学科在胸痛中心建设中的地位与作为[J]. 中华急诊医学杂志, 2018, 27(10): 1080-1082. DOI:10.3760/cma.j.issn.1671-0282.2018.10.003 |
| [11] | McCarthy BD, Beshansky JR, D'Agostino RB, et al. Missed diagnoses of acute myocardial infarction in the emergency department: Results from a multicenter study[J]. Annals of Emergency Medicine, 1993, 22(3): 579-582. DOI:10.1016/s0196-0644(05)81945-6 |
| [12] | Than M, Flaws D, Sanders S, et al. Development and validation of the Emergency Department Assessment of Chest pain Score and 2 h accelerated diagnostic protocol[J]. Emergency Medicine Australasia, 2014, 26(1): 34-44. DOI:10.1111/1742-6723.12164 |
| [13] | Stopyra J P, Miller C D, Hiestand B C, et al. Performance of the EDACS-accelerated Diagnostic Pathway in a Cohort of US Patients with Acute Chest Pain[J]. Crit Pathw Cardiol, 2015, 14(4): 134-138. DOI:10.1097/HPC.0000000000000059 |
| [14] | Flaws D, Than M, Scheuermeyer F X, et al. External validation of the emergency department assessment of chest pain score accelerated diagnostic pathway (EDACS-ADP)[J]. Emergency Medicine Journal Emj, 2016, 33(9): emermed-2015-205028. DOI:10.1136/emermed-2015-205028 |
| [15] | Christenson J, Innes G, Mcknight D, et al. A clinical prediction rule for early discharge of patients with chest pain[J]. Annals of Emergency Medicine, 2006, 47(1): 1. DOI:10.1016/j.annemergmed.2005.08.007 |
| [16] | Jalili M, Hejripour Z, Honarmand A R, et al. Validation of the Vancouver Chest Pain Rule: a prospective cohort study[J]. Academic Emergency Medicine Official Journal of the Society for Academic Emergency Medicine, 2012, 19(7): 837. DOI:10.1111/j.1553-2712.2012.01399.x |
 2020, Vol. 29
2020, Vol. 29




