体外膜肺氧合(extracorporeal membrane oxygenation,ECMO)已经成为抢救急危重患者生命的最后一道防线[1]。急性肾损伤(Acute kidney injury,AKI)在ECMO患者的治疗过程中极为常见,发生率高达70%~85%,ECMO治疗对肾脏的直接损伤或者原发疾病造成的肾脏损伤都可能导致患者需要联合肾脏替代治疗(renal replacement therapy,RRT)[2-4]。血管活性药物评分(Vasoactive-inotropic score,VIS)是评估血管活性药物对循环系统支持作用的有效指标[5],长时间大量应用血管活性药物已被发现是肾功能损害的危险因素[6]。ECMO患者血管活性药物的应用情况,以及VIS对ECMO患者RRT和预后的影响目前尚不明确。此外,一直以来临床上RRT的应用标准及开始时机并无统一的推荐意见[7],是否同样适用于ECMO患者值得探讨。本文回顾性统计江苏省人民医院急诊中心2015年1月至2018年12月68位ECMO患者的临床资料,探索ECMO治疗下血管活性药物与RRT的应用情况,并分析ECMO患者是否需要RRT的预测因素。
1 资料与方法 1.1 一般资料以2015年1月至2018年12月江苏省人民医院急诊中心(以下简称“本中心”)68位接受ECMO治疗的患者为研究对象。ECMO治疗的建立标准:各种原因引起的心搏呼吸骤停,急性严重心功能衰竭,急性严重呼吸功能衰竭,各种严重威胁呼吸和循环功能的疾患。ECMO期间调整系统流量及血管活性药物剂量,以维持有效的组织灌注,当循环和呼吸功能改善,逐步减低辅助流量并撤离ECMO。RRT适应证包括急性肾损伤、容量超负荷、严重的代谢性酸中毒、电解质紊乱以及尿毒症等,特别是血流动力学不稳定的患者。
收集ECMO治疗患者的年龄、性别、体质量、疾病、血管活性药物使用剂量、ECMO前有无心搏骤停、ECMO模式、ECMO及RRT治疗时间、ECMO是否成功下机、最终预后等信息。部分患者因放弃治疗而停机,部分患者在脱离ECMO后因综合因素出现院内死亡,均视为ECMO死亡率。
1.2 血管活性药物评分使用系数将所有血管活性药物进行整合,并赋予相应权重,以整合后的数值作为血管活性药物评分(Vasoactive-inotropic score, VIS)。VIS=多巴胺[µg/(kg·min)]+多巴酚丁胺[µg/(kg·min)]+10×米力农[µg/(kg·min)]+100×肾上腺素[µg/(kg·min)+100×去甲肾上腺素[µg/(kg·min)]+10 000×垂体后叶素[U/(kg·min)][5]。统计ECMO治疗后第1个24 h的血管活性药物评分为24 h VIS,第2个24 h的血管活性药物评分为48 h VIS,第3个24 h的血管活性药物评分为72 h VIS。
1.3 统计学方法应用SPSS 20.0进行数据处理。计量资料采用均数±标准差(Mean±SD)表示,计数资料以率表示,组间比较采用成组t检验或卡方检验。用Logistic回归筛选ECMO患者是否需要RRT的相关预测因素,以ROC曲线下面积(AUROC)评价预测效果以P<0.05为差异有统计学意义。
2 结果 2.1 ECMO患者基本情况2015年1月至2018年12月本中心接受ECMO治疗的患者68人(男性40人,女性28人),平均年龄(44.7±2.2)岁[男性(45.0±3.0)岁,女性(44.1±3.3)岁],总死亡率58.8%(男性60.0%,女性57.1%),男女性的平均年龄及死亡率差异无统计学意义。ECMO治疗前发生心搏骤停的有35人(51.5%)。V-A模式ECMO患者58人,V-V模式ECMO患者10人。平均ECMO治疗时间(146.4±12.6) h,ECMO成功下机34人(50.0%)。ECMO治疗期间接受RRT的患者50人(73.5%),平均RRT治疗时间(201.1±21.2)h。
RRT组与非RRT组在性别、体质量、ECMO前有无心搏骤停、ECMO模式、ECMO治疗时间方面差异无统计学意义,而RRT组的平均年龄更高,差异有统计学意义(P<0.05)。RRT与ECMO能否成功下机及最终预后密切相关,RRT组ECMO下机的成功率为38.0%显著低于非RRT组的83.3%,而RRT组的死亡率为74.0%高于非RRT组的16.7%,差异有统计学意义(P<0.05)。见表 1。
| 基本信息 | RRT | P值 | |
| 是 | 否 | ||
| 平均年龄(岁) | 48.2±2.5 | 34.9±4.1 | 0.0075 |
| 性别(n) | 0.375 | ||
| 男 | 31 | 9 | |
| 女 | 19 | 9 | |
| 体质量(kg) | 67.7±1.9 | 60.9±2.5 | 0.06 |
| ECMO前有无心搏骤停(n) | 0.487 | ||
| 有 | 27(54.0%) | 8(44.4%) | |
| 无 | 23(46.0%) | 10(55.6%) | |
| ECMO模式(n) | 0.201 | ||
| V-A模式 | 41(82.0%) | 17(94.4%) | |
| V-V模式 | 9(18.0%) | 1(5.6%) | |
| ECMO治疗时间(h) | 152.8±16.1 | 128.6±15.9 | 0.4 |
| RRT治疗时间(h) | 201.1±21.2 | 0 | |
| ECMO是否成功下机(n) | 0.001 | ||
| 是 | 19(38.0%) | 15(83.3%) | |
| 否 | 31(62.0%) | 3(16.7%) | |
| 死亡(n) | 0.000 | ||
| 是 | 37(74.0%) | 3(16.7%) | |
| 否 | 13(26.0%) | 15(83.3%) | |
ECMO治疗期间RRT组的24 h VIS、48 h VIS、72 h VIS均显著高于非RRT组,即RRT组需要更高剂量的血管活性药物。其中24 h VIS在两组之间的差异具有统计学意义(P<0.05)。见表 2。
| 基本信息 | RRT | P值 | |
| 是 | 否 | ||
| 24 h VIS | 83.8±18.3 | 27.8±13.0 | 0.03 |
| 48 h VIS | 35.8±12.1 | 5.6±3.9 | 0.05 |
| 72 h VIS | 23.8±8.2 | 0.6±0.15 | 0.08 |
以年龄预测ECMO患者是否需要RRT的ROC曲线下面积(AUROC)为0.711,标准误为0.075,P=0.008,95%可信区间为0.564~0.857。根据最大约登指数(约登指数=0.44,灵敏度=0.72,特异度=0.72),年龄的临界值38.5岁。见表 3。
| 因素 | AUROC | 标准误 | P值 | 95%可信区间 | 截断值 | 约登指数 | 敏感度 (%) |
特异度 (%) |
|
| 下限值 | 上限值 | ||||||||
| 年龄 | 0.711 | 0.075 | 0.008 | 0.564 | 0.857 | 38.50 | 0.44 | 72.0 | 72.2 |
| VIS(24 h) | 0.725 | 0.078 | 0.043 | 0.54 | 0.845 | 33.75 | 0.42 | 50.0 | 92.3 |
| VIS(48 h) | 0.643 | 0.086 | 0.221 | 0.448 | 0.785 | ||||
| VIS(72 h) | 0.638 | 0.086 | 0.122 | 0.478 | 0.816 | ||||
根据年龄临界值38.5岁,将ECMO患者分为高年龄组(41人)和低年龄组(27人)。两组之间在性别、体质量、ECMO模式、ECMO和RRT时间、VIS、ECMO下机成功率和死亡率方面差异无统计学意义。而在是否接受RRT方面差异有统计学意义(P<0.05),高年龄组ECMO患者RRT使用率高达87.8%。见表 4。
| 项目 | 高年龄组 | 低年龄组 | P值 |
| 性别(n) | 0.657 | ||
| 男 | 25(61.0%) | 15(55.6%) | |
| 女 | 16(39.0%) | 12(44.4%) | |
| 体质量 | 68.0±1.9 | 62.8±2.8 | 0.11 |
| ECMO治疗时间 | 146.7±18.1 | 146.0±16.2 | 0.98 |
| ECMO前有无心搏骤停(n) | 0.042 | ||
| 有 | 17(41.5%) | 18(66.7%) | |
| 无 | 24(58.5%) | 9(33.3%) | |
| ECMO模式(n) | 0.497 | ||
| V-A模式 | 34(82.9%) | 24(88.9%) | |
| V-V模式 | 7(17.1%) | 3(11.1%) | |
| ECMO是否成功下机(n) | 0.083 | ||
| 是 | 17(41.5%) | 17(63.0%) | |
| 否 | 24(58.5%) | 10(37.0%) | |
| 死亡(n) | 0.147 | ||
| 是 | 27(65.9%) | 13(48.1%) | |
| 否 | 14(34.1%) | 14(51.9%) | |
| RRT时间 | 160.3±23.1 | 129.0±32.6 | 0.424 |
| 是否RRT(n) | 0.001 | ||
| 是 | 36(87.8%) | 14(51.9%) | |
| 否 | 5(12.2%) | 13(48.1%) | |
| 24 h VIS | 57.1±11.1 | 53.6±24.4 | 0.886 |
| 48 h VIS | 32.2±9.9 | 13.9±4.6 | 0.146 |
| 72 h VIS | 20.7±6.4 | 7.84±4.1 | 0.128 |
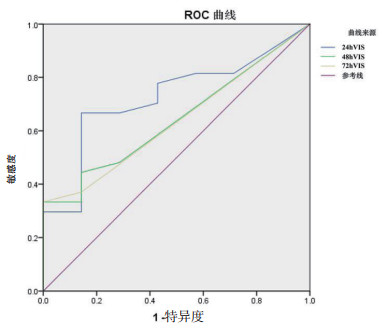
以24 h VIS、48 h VIS、72 h VIS预测ECMO患者是否需要RRT的ROC曲线下面积(AUROC)均大于0.5,其中24 h VIS的AUROC最大,且具有统计学差异(P<0.05)。见表 4。根据最大约登指数(约登指数=0.42,灵敏度=0.50,特异度=0.92),24 h VIS的临界值为33.75。见图 1和表 3。
|
| 图 1 VIS对ECMO患者是否需要RRT的预测价值 Fig 1 Predictive value of VIS for RRT in ECMO patients |
|
|
根据24 h VIS的临界值33.75,将68位ECMO患者分为高VIS组(30人)和低VIS组(38人)。两组之间在年龄、性别、体质量、ECMO治疗时间方面差异无统计学意义。与低VIS组相比,高VIS组的ECMO前心搏骤停率、V-A模式使用率、ECMO下机失败率、死亡率、RRT使用率均显著高于低VIS组,差异有统计学意义(P<0.05)。而低VIS组的RRT治疗时间显著长于高VIS组,差异有统计学意义(P<0.05)。见表 5。
| 项目 | 高VIS组 | 低VIS组 | P值 |
| 年龄 | 47.23±3.44 | 42.61±2.91 | 0.305 |
| 性别(n) | 0.502 | ||
| 男 | 19(63.3%) | 21(55.3%) | |
| 女 | 11(36.7%) | 17(44.7%) | |
| 体质量 | 64.2±2.0 | 67.11±2.3 | 0.353 |
| ECMO治疗时间 | 119.9±23.9 | 167.3±11.5 | 0.06 |
| ECMO模式(n) | 0.02 | ||
| V-A模式 | 29(96.7%) | 29(76.3%) | |
| V-V模式 | 1(3.3%) | 9(23.7%) | |
| ECMO前有无心搏骤停(n) | 0.007 | ||
| 有 | 21(70.0%) | 14(36.8%) | |
| 无 | 9(30.0%) | 24(63.2%) | |
| ECMO是否成功下机(n) | 0.000 | ||
| 是 | 6(20.0%) | 28(73.7%) | |
| 否 | 24(80.0%) | 10(26.3%) | |
| 死亡(n) | 0.000 | ||
| 是 | 27(90.0%) | 13(34.2%) | |
| 否 | 3(10.0%) | 25(65.8%) | |
| RRT时间 | 146.6±27.1 | 270.6±27.9 | 0.003 |
| 是否RRT(n) | 0.001 | ||
| 是 | 28(93.3%) | 22(57.9%) | |
| 否 | 2(6.7%) | 16(42.1%) |
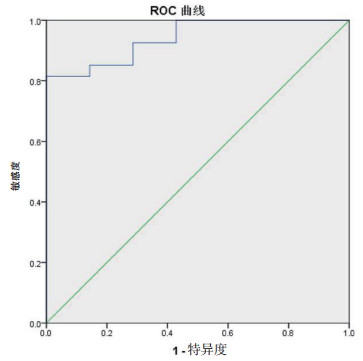
为明确哪些因素对ECMO患者是否需要RRT有影响,以年龄、性别、体质量、ECMO前有无心搏骤停、ECMO模式、ECMO治疗时间、24 h/48 h/72 h VIS的数据,建立Logistic回归模型。最终纳入年龄(OR 1.223)和24 h VIS(OR 1.033)两个变量,该Logistic回归模型认为这两个变量因素可以预测ECMO患者是否需要RRT,而其他因素没有预测价值。见表 6。根据年龄和24 h VIS两个因素可以计算每个ECMO患者是否需要RRT的Logit(P):Logit(P)= -6.746+0.201×年龄+0.032×24 h VIS。使用预测概率建立ROC曲线,该曲线下面积AUROC为0.942,标准误为0.04,P值<0.001,95%可信区间为0.864~1。见图 2。该曲线下面积大于仅由年龄和24 h VIS建立的ROC曲线下面积,可以更准确的预测ECMO患者是否需要RRT。
| 项目 | B | 标准误差 | 瓦尔德 | 自由度 | 显著性 | Exp(B) |
| 年龄 | 0.201 | 0.088 | 5.253 | 1 | 0.022 | 1.223 |
| 血管活性药物24 h评分 | 0.032 | 0.016 | 4.008 | 1 | 0.045 | 1.033 |
| 常量 | -6.746 | 3.02 | 4.989 | 1 | 0.026 | 0.001 |
|
| 图 2 24 h VIS和年龄对ECMO患者是否需要RRT的预测价值 Fig 2 Predictive value of age and 24 h VIS for RRT in ECMO patients |
|
|
ECMO治疗前缺氧、肾脏低灌注和炎性反应等原发因素以及ECMO期间缺血-再灌注、非搏动性血流、溶血、儿茶酚胺增加等继发因素对肾脏的直接或间接损伤导致ECMO患者容易发生AKI,常需要联合RRT。临床上RRT通常在缺乏持续性或进行性AKI标准的情况下启动。此外,ECMO患者常合并容量超负荷、严重内环境紊乱等其他因素需要启动RRT,而目前ECMO患者开始RRT的时机并无统一推荐意见[8-9]。
ECMO治疗是持续RRT的独立影响因素[10],本研究中RRT组ECMO下机的成功率为38.0%显著低于非RRT组的83.3%。同时,RRT也是ECMO患者不良预后的独立危险因素,本研究中RRT组的死亡率为74.0%显著高于非RRT组的16.7%,与既往研究相符。RRT对于ECMO患者能否成功下机和最终的预后密切相关,预测ECMO治疗患者是否需要RRT具有一定的临床意义。
年龄是预测ECMO患者是否需要RRT的影响因素之一。年龄对ECMO患者是否需要RRT的预测临界值为38.5岁,超过38.5岁的ECMO患者RRT使用率高达87.8%,可能与肾脏储备能力不足有关[11]。同时,最新研究显示年龄与ECMO患者死亡率的增加呈线性相关,每增加10岁,死亡率约增加14%[12]。24 h VIS对ECMO患者是否需要RRT也具有一定的预测价值,临界值为33.75。ECMO治疗的24 h内,若VIS超过33.75,接受RRT的比率高达93.3%。本研究中ECMO治疗的24 h内仍然需要高剂量血管活性药物(24 h VIS > 33.75)的患者死亡率高达90%。显然,同时结合年龄和24 h VIS两个因素相较于年龄或24 h VIS单一因素的ROC曲线下面积更高,可以更准确的预测ECMO患者是否需要RRT。
高年龄的ECMO患者(年龄 > 临界年龄38.5岁)的RRT使用率高达87.8%,ECMO治疗的24 h内需要应用高剂量血管活性药物(VIS >临界VIS 33.75)的患者RRT使用率和死亡率均超过90%。年龄(OR 1.223)和24 h VIS(OR 1.033)两个因素对ECMO患者是否需要RRT具有一定预测价值,且两者相结合的预测价值更大。
| [1] | Shekar K, Mullany DV, Thomson B, et al. Extracorporeal life support devices and strategies for management of acute cardiorespiratory failure in adult patients:a comprehensive review[J]. Crit Care, 2014, 18(3): 219. DOI:10.1186/cc13865 |
| [2] | Kilburn DJ, Shekar K, Fraser JF. The Complex Relationship of Extracorporeal Membrane Oxygenation and Acute Kidney Injury:Causation or Association?[J]. Biomed Res Int, 2016, 2016: 1094296. DOI:10.1155/2016/1094296 |
| [3] | Han SS, Kim HJ, Lee SJ, et al. Effects of Renal Replacement Therapy in Patients Receiving Extracorporeal Membrane Oxygenation:A Meta-Analysis[J]. Ann Thorac Surg, 2015, 100(4): 1485-1495. DOI:10.1016/j.athoracsur.2015.06.018 |
| [4] | Chen H, Yu RG, Yin NN, et al. Combination of extracorporeal membrane oxygenation and continuous renal replacement therapy in critically ill patients:a systematic review[J]. Crit Care, 2014, 18(6): 675. DOI:10.1186/s13054-014-0675-x |
| [5] | Yamazaki Y, Oba K, Matsui Y, et al. Vasoactive-inotropic score as a predictor of morbidity and mortality in adults after cardiac surgery with cardiopulmonary bypass[J]. J Anesth, 2018, 32(2): 167-173. DOI:10.1007/s00540-018-2447-2 |
| [6] | Choi SJ, Ha EJ, Jhang WK, et al. Factors Associated With Mortality in Continuous Renal Replacement Therapy for Pediatric Patients With Acute Kidney Injury[J]. Pediatr Crit Care Med, 2017, 18(2): e56-e61. DOI:10.1097/PCC.0000000000001024 |
| [7] | Tandukar S, Palevsky PM. Continuous Renal Replacement Therapy:Who, When, Why, and How[J]. Chest, 2019, 155(3): 626-638. DOI:10.1016/j.chest.2018.09.004 |
| [8] | Ostermann M, Connor M, J r. , Kashani K Continuous renal replacement therapy during extracorporeal membrane oxygenation:why, when and how?[J]. Curr Opin Crit Care, 2018, 24(6): 493-503. DOI:10.1097/MCC.0000000000000559 |
| [9] | Paek JH, Park S, Lee A, et al. Timing for initiation of sequential continuous renal replacement therapy in patients on extracorporeal membrane oxygenation[J]. Kidney Res Clin Pract, 2018, 37(3): 239-247. DOI:10.23876/j.krcp.2018.37.3.239 |
| [10] | Baek SD, Kang JY, Shin S, et al. Predictive Factors of Duration of Continuous Renal Replacement Therapy in Acute Kidney Injury Survivors[J]. Shock, 2019. DOI:10.1097/SHK.0000000000001328 |
| [11] | Cohen E, Nardi Y, Krause I, et al. A longitudinal assessment of the natural rate of decline in renal function with age[J]. J Nephrol, 2014, 27(6): 635-641. DOI:10.1007/s40620-014-0077-9 |
| [12] | Chung M, Zhao Y, Strom JB, et al. Extracorporeal Membrane Oxygenation Use in Cardiogenic Shock:Impact of Age on In-Hospital Mortality, Length of Stay, and Costs[J]. Crit Care Med, 2019, 47(3): e214-e21. DOI:10.1097/CCM.0000000000003631 |
 2020, Vol. 29
2020, Vol. 29




