危重患者常常因各种因素导致严重的内分泌功能紊乱,引发血糖大范围波动,发生应激性高血糖(stress-induced hyperglycemia, SIH)或低血糖。研究发现,SIH与低血糖是影响危重患者住院病死率和住院时间的独立危险因素[1-3]。血糖变异度(glucose variability, GV)作为血糖波动的指标,也是预测患者死亡的独立危险因素[4-6]。因此,严格的血糖监测与管理至关重要。经皮连续血糖监测系统(continuous glucose monitoring system, CGMS)每5 min提供一次血糖数值,便于严格管理危重患者血糖,减少血糖波动。研究发现,连续血糖数据便于分析GV,相比间断血糖监测更有利于控制GV[7],为患者预后的评估提供重要依据[8-10]。目前国内尚少见CGMS在危重患者中应用的相关报告,国外关于CGMS准确性的研究以动脉血气分析作为校准方法。本文拟应用末梢间断血糖监测法进行校准,研究CGMS在危重患者血糖监测中的准确性,及其在预后评估中的价值,为危重患者血糖管理提供参考依据。
1 资料与方法本观察性研究在浙江大学附属第二医院急诊重症监护室(emergency intensive care unit, EICU)进行。研究时间为2015年8月1日至2016年11月30日。研究通过医院伦理委员会的审批,审批号为:(2015年度)伦审研第(073)号。
1.1 纳入排除标准纳入标准:年龄≥18岁; 应用CGMS监测血糖的危重患者; 预计EICU住院时间≥48 h。排除标准:患者或家属拒绝使用CGMS监测血糖; 肿瘤或其他终末期患者; 因转出EICU至其他科室或自动出院、CGMS仪器故障导致的CGMS仪器监测不足48 h。
1.2 研究方法纳入研究的患者,经患者或家属签署知情同意后,应用经皮CGMS(GUARDIAN® REAL-TIME MONITOR; Medtronic, USA)与指端末梢微量法血糖监测方法(罗氏血糖仪,ACCU-CHEK® Performa; Roche, DEU)协同监测血糖,间断血糖检测法的测量频率根据患者病情制定(4~24次/d)。
一套CGMS装置包含一次性血糖皮下探针,循环使用的信号发射器和血糖监测仪。血糖探针运用发射埋于患者腹部皮下,固定后拔除枕芯并与信号发射器相连,连接后即可在血糖监测仪上实时显示血糖,CGMS每5 min获得一次血糖平均数并显示于监测仪上。根据CGMS说明书,使用末梢微量法血糖值每6 h对CGMS仪器进行校准。设置仪器的血糖监测报警上限为10.0 mmol/L,下限为7.78 mmol/L,控制血糖在该范围内。CGMS监测时间为72 h,监测完成后,可通过无线传输设备将检测仪中的连续血糖数据导入计算机配套软件中。
此外,每位患者每天常规测量2~3次动脉血气分析(罗氏血气电解质分析仪,cobas b 123 POC system; Roche, DEU),研究者或床旁护士按照1:1配对的形式记录相同时间点CGMS血糖读数。
EICU的危重患者常规血糖控制范围为7. 8~10.0 mmol/L[11-14]。如果任何方法测得血糖高于10.0 mmol/L,则开始应用静脉胰岛素治疗(40 mL生理盐水+20 U胰岛素),根据血糖调整胰岛素使用的速度,同时每30 min复测血糖。如血糖低于7.8 mmol/L,则暂停胰岛素治疗。如血糖低于4.44 mmol/L,则静脉应用葡萄糖并复测血糖。
1.3 数据收集收集入选患者的资料包括:性别、年龄、体质量指数(body mass index, BMI)、入院主要诊断、初始pH值、初始乳酸值、初始收缩压值、血管活性药物使用、机械通气、格拉斯哥昏迷评分(Glasgow coma scale,GCS)、急性生理与慢性健康评分(acute physiology and chronic health evaluation Ⅱ,APACHE Ⅱ)、序贯器官衰竭估计评分(sequential organ failure assessment,SOFA)、糖尿病病史、胰岛素使用、初始血糖值、动脉血气分析血糖值、指尖末梢微量法血糖值、EICU住院时间、总住院时间、机械通气时间和患者结局。
CGMS血糖数据导出后计算GV相关指标,包括:血糖平均数、血糖最高值、血糖最低值、血糖标准差(standard deviation, SD)、血糖不稳定指数(glucose lability index, GLI; 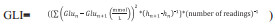
计量资料进行正态性检验,正态分布者以均数±标准差(Mean±SD)表示,非正态分布者以中位数(M)和四分位数(interquartile range, IQR)表示; 计数资料以比或率表示。两组正态分布的计量资料比较采用LSD-t检验,非正态分布的计量资料比较采用Mann-Whitney U检验; 率的比较采用χ2检验或Fisher确切概率检验。应用皮尔逊相关性系数和Bland-Altman一致性检验[15]检查配对血糖数据的相关性。分析存活组和死亡组之间各指标的差异,应用重复测量方差分析法分析重复测量数据,应用多因素Logistic回归分析影响死亡的独立危险因素,应用线性回归进行各危险因素间的共线性诊断。以上统计学分析和作图采用SPSS 23.0软件(SPSS Inc., Chicago, IL),以P<0.05为差异有统计学意义。
应用MATLAB软件(R2018a,MathWorks)进行误差网格分析[16-17]。结果被显示在不同区域:A区指临床上精确测量的值,可指导正确的临床治疗,偏离参考值20%之内,或当参考处于低血糖范围内时,被测值也处于低血糖范围(<70 mg/dL); B区指临床可接受范围内的误差值,偏离超过参考值20%;C区指对高血糖或低血糖的误判,可能导致不必要的过度治疗; D区和E区指对低血糖的高估和对高血糖的低估,可能导致危险的治疗。A区和B区内的值是临床上可接受的偏离值,而C~E区的值存在潜在的风险,并可能导致临床决策错误。
2 结果 2.1 患者的一般资料本研究共71例患者符合纳入标准,在获得患者或家属知情同意后予纳入研究,其中8例患者CGMS监测<48 h,1例患者遇到CGMS故障,最终62例患者纳入统计分析。男性45例(72.58%),女性17例(27.42%),年龄(51±17)岁。住院病死率为29.03%,其中死亡患者18例,死亡患者入院初始乳酸值显著高于存活组,分别为5.00(3.23~8.43)mmol/L,3.25(1.55~4.80)mmol/L,P=0.017。死亡患者APACHEⅡ评分、SOFA评分、GCS评分高于存活组(P=0.001、P=0.001、P=0.004),见表 1。
| 指标 | 存活组(n=44) | 死亡组(n=18) | 统计值 | P值 |
| 性别(例,%) | ||||
| 男 | 35(79.5) | 10(55.6) | 2.587 | 0.108 |
| 女 | 9(20.5) | 8(44.4) | ||
| 年龄(岁,Mean±SD) | 50±15 | 54±21 | -0.945 | 0.348 |
| BMI[kg/m2, M(IQR)] | 22.57(20.8, 20.0) | 24.13(22.3, 25.4) | 282.0 | 0.077 |
| 诊断(例,%) | ||||
| 神经系统疾病 | 2(4.5) | — | — | — |
| 呼吸系统疾病 | — | 1(6.7) | ||
| 心血管系统疾病 | 2(4.5) | 2(11.1) | ||
| 消化系统疾病 | 1(2.3) | — | ||
| 外科术后 | — | 2(11.1) | ||
| 创伤 | 31(70.5) | 11(61.1) | ||
| 呼吸心搏骤停 | 5(11.4) | 2(11.1) | ||
| 脓毒症 | 3(6.8) | — | ||
| 初始pH值(Mean±SD) | 7.37±0.09 | 7.31±0.17 | 1.277 | 0.215 |
| 初始乳酸[mmol/L, M(IQR)] | 3.25(1.55, 4.80) | 5.00(3.23, 8.43) | 242.5 | 0.017 |
| 收缩压(mmHg,Mean±SD) | 122±32 | 108±35 | 1.665 | 0.101 |
| 血管活性药物使用(例,%) | 22(50.0) | 13(72.2) | 2.566 | 0.109 |
| 机械通气(例,%) | 41(93.2) | 18(100.0) | — | 0.550a |
| GCS评分[M(IQR)] | 6(5, 10) | 5(3, 5) | 214.5 | 0.004 |
| APACHEⅡ评分[M(IQR)] | 18(13, 27) | 29(20, 35) | 188.0 | 0.001 |
| SOFA评分[M(IQR)] | 7(4, 10) | 12(8, 14) | 191.0 | 0.001 |
| 糖尿病病史(例,%) | 11(25.0) | 6(33.3) | 0.125 | 0.723 |
| 胰岛素使用(例,%) | 12(27.3) | 12(66.7) | 8.356 | 0.004 |
| 初始血糖值(mmol/L,Mean±SD) | 10.21±4.13 | 13.00±5.41 | -1.962 | 0.061 |
| 动脉血糖(mmol/L,Mean±SD) | 8.77±2.08 | 9.54±2.91 | -1.020 | 0.318 |
| 微量法血糖(mmol/L,Mean±SD) | 9.19±1.83 | 9.44±3.23 | -0.306 | 0.763 |
| CGMS血糖(mmol/L,Mean±SD) | 9.17±1.87 | 9.62±2.80 | -0.632 | 0.533 |
| CGMS最高值[mmol/L, M(IQR)] | 14.21(11.24, 17.98) | 14.60(10.07, 19.63) | 381.5 | 0.822 |
| CGMS最低值[mmol/L, M(IQR)] | 5.50(4.66, 6.44) | 5.28(3.86, 6.55) | 361.0 | 0.587 |
| 总住院时间[d, M(IQR)] | 34.0(25.0, 55.0) | 7.0(6.0, 14.0) | 68.5 | <0.01 |
| ICU住院时间[d, M(IQR)] | 13.5(8.0, 28.0) | 6.5(5.0, 11.0) | 192.0 | 0.002 |
| 机械通气时间[d, M(IQR)] | 9.0(5.0, 19.0) | 6.5(5.0, 11.0) | 305.5 | 0.159 |
| 注:a为Fisher确切概率检验; 1 mmHg=0.133 kPa | ||||
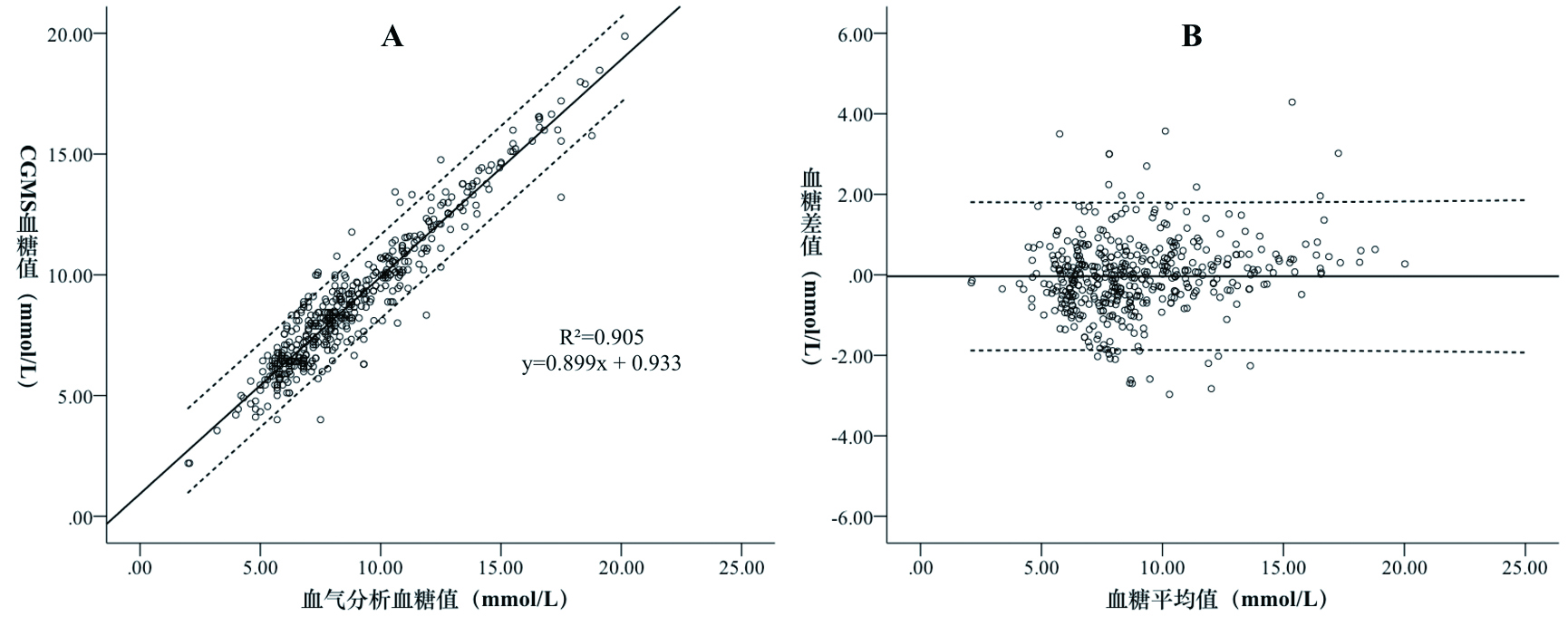
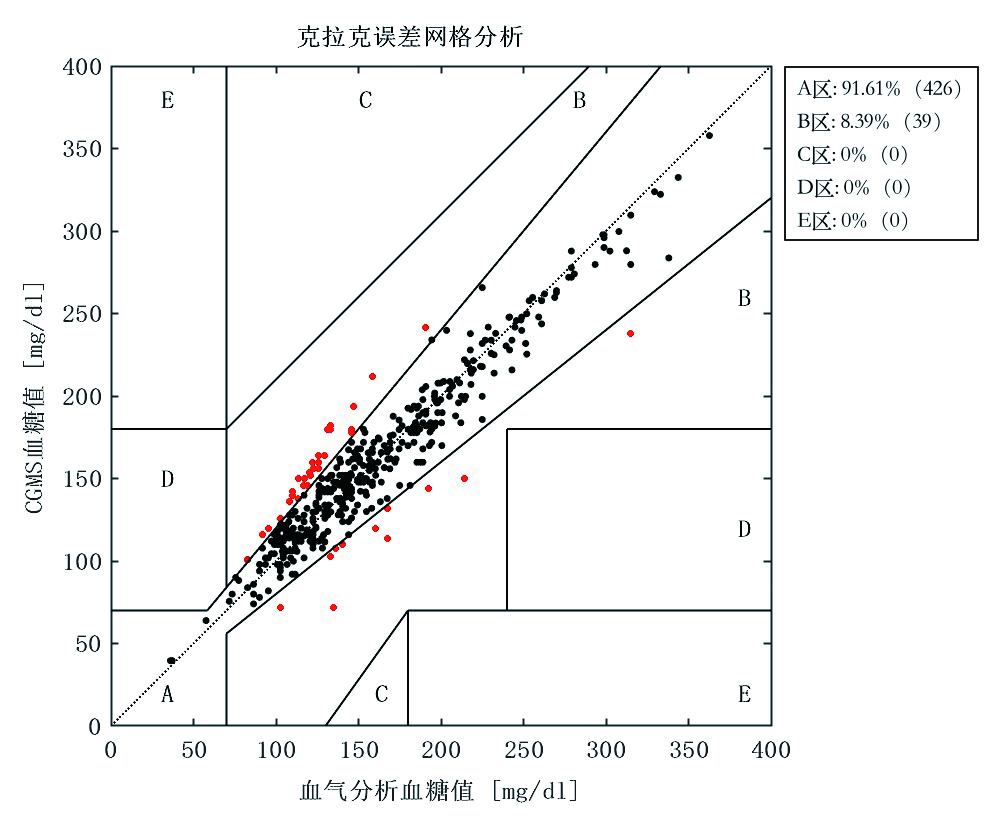
本研究按照1:1配对的方式,分别收集血气血糖值与CGMS血糖值各465例次,其血糖值分别为(8.86±3.01)mmol/L,(8.89±2.84)mmol/L。两者皮尔逊相关性系数(r)为0.951(R2=0.904,P<0.01),94.74%的血糖值位于95%置信区间内(图 1A)。CGMS血糖值与血气分析血糖值的Bland-Altman一致性检验显示,配对血糖差值的均数为-0.04 mmol/L,标准差为0.93 mmol/L,95%CI:-1.86~1.78 mmol/L,10.57%(28/265)的点在95%界限之外(图 1B)。克拉克误差网格分析显示所有的CGMS血糖值均位于A区和B区,其中91.61%位于A区,8.39%位于B区(图 2),由此可见CGMS血糖的准确性较好。
|
| 图 1 465对CGMS血糖值与血气分析血糖值的散点图(A)和Bland-Altman检验(B) |
|
|
|
| 图 2 465对CGMS血糖值与血气分析血糖值的克拉克误差网格分析 |
|
|
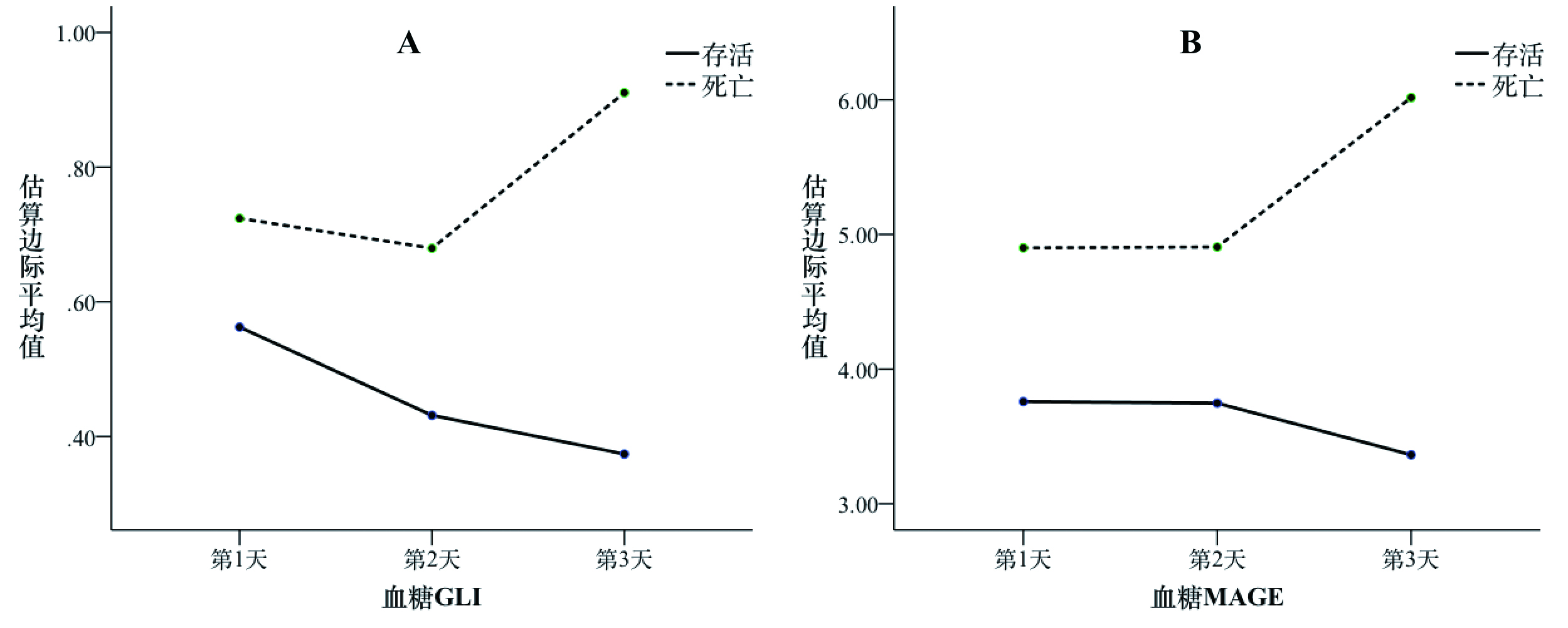
本研究共收集CGMS血糖数据52 626例次,存活组和死亡组CGMS血糖分别为(9.17±1.87)mmol/L,(9.62±2.80)mmol/L。CGMS血糖变异度相关指标(血糖最大差值、SD、CV、GLI、MAGE)及连续3 d的变化情况见表 2。死亡组GLI、MAGE显著高于存活组(P=0.029,P=0.036)。存活组与死亡组每日GLI、MAGE的重复测量方差分析结果显示,两组间每日GLI、MAGE差异有统计学意义(组间因素,P=0.005;P=0.009)。同时,GLI与MAGE在存活组呈下降趋势,死亡组呈上升趋势,两者随时间变化差异有统计学意义(交互作用,P=0.011,P=0.008)。此外,每日GLI、MAGE之间差异无统计学意义,见表 3、图 3。
| 因素 | 存活组(n=44) | 死亡组(n=18) | 统计量 | P值 |
| CGMS标准差 | 1.81(1.19, 2.76) | 2.13(1.12, 3.29) | 345.5 | 0.433 |
| 最大差值 | 9.72(5.72, 11.76) | 9.68(5.55, 13.38) | 362.0 | 0.598 |
| GLI | 0.41(0.23, 0.58) | 0.76(0.28, 1.06) | 255.0 | 0.029 |
| CV | 0.21(0.14, 0.27) | 0.20(0.16, 0.29) | 344.0 | 0.419 |
| MAGE | 3.37(2.02, 5.12) | 4.94(3.42, 7.16) | 260.5 | 0.036 |
| 第1天SD | 1.58(0.94, 2.97) | 1.87(1.02, 2.42) | 393.0 | 0.963 |
| 最大差值 | 6.78(3.94, 10.38) | 7.72(4.18, 10.02) | 383.5 | 0.846 |
| GLI | 0.46(0.22, 0.86) | 0.80(0.20, 1.04) | 333.0 | 0.328 |
| CV | 0.17(0.11, 0.26) | 0.17(0.14, 0.20) | 368.5 | 0.669 |
| MAGE | 3.25(2.00, 4.95) | 5.08(2.78, 6.07) | 277.5 | 0.066 |
| 第2天SD | 1.30(0.86, 1.84) | 1.58(1.00, 2.87) | 300.5 | 0.138 |
| 最大差值 | 5.72(3.53, 6.80) | 7.61(4.28, 10.92) | 291.0 | 0.103 |
| GLI | 0.39(0.16, 0.53) | 0.59(0.23, 1.04) | 253.5 | 0.027 |
| CV | 0.14(0.10, 0.21) | 0.17(0.13, 0.26) | 291.5 | 0.104 |
| MAGE | 2.80(1.97, 5.06) | 4.59(3.19, 6.69) | 270.5 | 0.052 |
| 第3天SD | 1.08(0.78, 1.54) | 1.39(0.86, 2.61) | 305.0 | 0.158 |
| 最大差值 | 4.83(2.89, 6.58) | 5.06(3.69, 11.02) | 317.0 | 0.220 |
| GLI | 0.21(0.15, 0.44) | 0.91(0.15, 1.40) | 226.0 | 0.008 |
| CV | 0.12(0.09, 0.17) | 0.17(0.09, 0.32) | 283.0 | 0.079 |
| MAGE | 2.78(1.85, 4.62) | 4.94(3.80, 7.04) | 196.5 | 0.002 |
| 注:SD,血糖标准差; GLI,血糖不稳定指数; MAGE,平均血糖波动幅度; CV,血糖变异系数 | ||||
| 因素 | 自由度 | 均方 | F值 | P值 |
| GLI | ||||
| 组间因素(预后分组) | 1 | 1.271 | 8.573 | 0.005 |
| 组内因素(每日GLI) | 1.514 | 0.171 | 1.423 | 0.245 |
| 交互作用 | 1.514 | 0.652 | 5.407 | 0.011 |
| MAGE | ||||
| 组间因素(预后分组) | 1 | 104.483 | 7.240 | 0.009 |
| 组内因素(每日GLI) | 1.727 | 2.575 | 1.279 | 0.280 |
| 交互作用 | 1.727 | 11.128 | 5.525 | 0.008 |
| 注:GLI,血糖不稳定指数; MAGE,平均血糖波动幅度 | ||||
|
| 图 3 每日GLI(A)、MAGE(B)与预后分组因素的交互轮廓图 |
|
|
根据单因素分析结果显示,存活组和死亡组GCS评分、APACHEⅡ评分、SOFA评分、初始乳酸值、胰岛素使用率、GLI、MAGE均差异有统计学意义。考虑自变量与结局之间的相关性并检验自变量的共线性之后,以预后(死亡/存活)作为因变量,以APACHEⅡ评分、SOFA评分、GLI、MAGE作为自变量进行Logistic回归分析,结果显示MAGE与SOFA评分是影响死亡的独立危险因素(-2对数似然值,55.521;Hosmer-Lemeshow检验,χ 2=8.988,P=0.343)。MAGE每增加1,死亡风险约增加1.43倍。该结果在控制糖尿病、胰岛素使用率、GCS评分后并没有发生变化,结果一致。见表 4。
| 危险因素 | β | 标准误差 | 瓦尔德 | 自由度 | OR | 95%CI | P值 |
| SOFA评分 | 0.297 | 0.099 | 9.076 | 1 | 1.346 | 1.109~1.633 | 0.003 |
| MAGE | 0.358 | 0.138 | 6.705 | 1 | 1.430 | 1.091~1.874 | 0.010 |
| APACHE Ⅱ评分 | 0.084 | 0.063 | 1.747 | 1 | 1.087 | 0.960~1.230 | 0.186 |
| GLI | 1.027 | 1.129 | 0.829 | 1 | 2.794 | 0.306~25.527 | 0.363 |
| 注:四个危险因素均为连续变量; GLI,血糖不稳定指数; MAGE,平均血糖波动幅度 | |||||||
危重患者的综合评估及救治有利于改善患者预后[18-19],而血糖管理是危重患者救治的重要环节,危重患者的内分泌功能紊乱引发血糖大范围波动,与预后密切相关[1-3, 20-21]。同时,血糖大范围波动导致的血糖变异度(GV)升高是预测患者死亡的独立危险因素[4-6]。研究发现,连续血糖监测系统(CGMS)相比间断血糖监测血糖法更有利于控制GV及避免低血糖事件的发生[7]。因此,CGMS在控制GV、改善预后方面具有明显优势。利用CGMS进行严格血糖监测和管理,可以更好地控制危重患者血糖,减少血糖波动及血糖变异度(GV),有助于改善危重患者的综合救治,改善临床结局。本研究对CGMS在危重患者中的准确性及预后评估价值进行了研究,入选了62例应用CGMS监测血糖的危重患者,通过比较1:1配对的465对血气分析血糖值和CGMS血糖值发现,两者相关较好(R2=0.951),克拉克误差网格分析法显示所有的CGMS血糖值均位于A区和B区,表明CGMS仪器准确性能高。同时比较存活患者与死亡患者GV相关指标发现,MAGE与危重患者预后密切相关,是影响死亡的独立危险因素(OR=1.430,P=0.010)。
根据CGMS仪器说明书,需要对CGMS仪器进行每日4次的校准(每6 h校准1次)。国外研究以动脉血气分析血糖值作为CGMS仪器校准方法[8-10],相同型号的CGMS血糖仪也采用血气分析进行校准,并证实其准确性较可靠[22-23]。本研究按照仪器说明书,采用指尖末梢微量法血糖值对仪器进行校准,因该法的准确性未知,故对其进行准确性的检验。1:1配对的465对血气分析血糖值和CGMS血糖值,皮尔逊相关分析、Bland-Altman一致性检验以及克拉克误差网格分析法均显示准确性较好。同时,国外研究入选的危重患者大多为内科重症患者,外科或创伤患者占比较少[8-10]。本研究所在EICU主要收治创伤危重患者,入选患者中包含42例(67.74%)创伤患者,可为CGMS在创伤患者中的应用提供重要依据。
本研究纳入的危重患者病死率为29.03%(15/62),创伤患者病死率为26.19%(8/42),该比例高于本EICU既往严重创伤患者病死率(12.1%)[24]。原因可能为:1)纳入标准中要求患者预计ICU住院时间>48 h,大多数病情较稳定的患者因此未纳入研究; 2)许多患者或其家属拒绝使用CGMS; 3)本研究将院内死亡和病情恶化的自动出院均归为死亡组。
本研究中,死亡患者APACHEⅡ评分、SOFA评分明显高于存活患者(均P =0.001)。血糖变异度(GV)相关指标中,死亡组GLI、MAGE显著高于存活组(P=0.029、P=0.036)。重复测量方差分析结果显示,存活组GLI与MAGE连续3 d呈下降趋势,死亡组呈上升趋势,两者随时间变化差异有统计学意义(P=0.011,P=0.008)。多项研究报道,GV与患者病死率密切相关[4-6]。血糖变异度不仅取决于患者原发病的严重度和糖尿病相关病史等内源性因素[6],还受到血糖监测,胰岛素使用以及肠内肠外营养的使用等外源性因素的影响。体外实验表明,血糖的剧烈波动可诱导内皮细胞损伤和凋亡[25]。Kurtz等[26]通过研究全身血糖变异度与蛛网膜下腔出血患者脑代谢水平及预后的关系发现,GV增高与脑代谢水平下降、住院病死率增高密切相关。他们认为GV是判断蛛网膜下腔出血患者预后的独立危险因素。一项有关脓毒症血糖管理的研究报道,GV越高患者预后就越差[27]。目前反映GV的指标包括血糖平均数、标准差(SD)、平均每日血糖最大差值、不稳定指数(GLI)、平均血糖波动幅度(MAGE)、变异系数(CV)等。目前并没有适合描述GV的金标准,现有研究多采用不同的描述指标,且每项研究至少一个指标与病死率相关[28]。根据各项指标的计算公式,血糖平均数、SD、CV易受到极端值的影响,而GLI、MAGE体现了单位时间内血糖变异情况,同时考虑了极端值的影响,能更好地体现血糖变异状况。本研究中,死亡组和存活组之间的血糖平均数、SD、CV差异无统计学意义。而死亡组GLI、MAGE均显著大于存活组。同时Logistic回归分析显示,MAGE是影响死亡的独立危险因素。
本研究也存在不足之处:第一,为观察性研究,虽有严格的纳入排除标准,但仍可能存在一定的选择偏倚,证据强度不及随机对照研究; 第二,为单中心研究,研究所在的EICU主要收治严重创伤患者,研究对象中创伤患者比例较高,研究结果可能与其他危重患者并不一定一致; 第三,研究纳入样本量较少,同样可能导致一定的偏倚。
综上所述,本研究通过单中心观察性研究,应用连续血糖监测系统监测EICU危重患者血糖,比较了配对的CGMS血糖值与血气分析血糖值的相关性,发现CGMS仪器准确性较好。同时CGMS可获得GV相关指标,通过比较存活患者与死亡患者GV相关指标发现,MAGE与危重患者预后密切相关,通过连续血糖数据计算GV,有助于间接了解患者预后,便于早期实施干预措施,为临床病情综合评估提供参考依据。
| [1] | Kerby JD, Griffin RL, MacLennan P, et al. Stress-induced hyperglycemia, not diabetic hyperglycemia, is associated with higher mortality in trauma[J]. Ann Surg, 2012, 256(3): 446-452. DOI:10.1097/SLA.0b013e3182654549 |
| [2] | Bosarge PL, Shoultz TH, Griffin RL, et al. Stress-induced hyperglycemia is associated with higher mortality in severe traumatic brain injury[J]. J Trauma Acute Care Surg, 2015, 79(2): 289-294. DOI:10.1097/ta.0000000000000716 |
| [3] | Krinsley J, Schultz MJ, Spronk PE, et al. Mild hypoglycemia is strongly associated with increased intensive care unit length of stay[J]. Ann Intensive Care, 2011, 1: 49. DOI:10.1186/2110-5820-1-49 |
| [4] | Krinsley JS. Glycemic variability: a strong independent predictor of mortality in critically ill patients[J]. Crit Care Med, 2008, 36(11): 3008-3013. DOI:10.1097/CCM.0b013e31818b38d2 |
| [5] | Lundelin K, Vigil L, Bua S, et al. Differences in complexity of glycemic profile in survivors and nonsurvivors in an intensive care unit: a pilot study[J]. Crit Care Med, 2010, 38(3): 849-854. DOI:10.1097/CCM.0b013e3181ce49cf |
| [6] | Krinsley JS. Glycemic variability and mortality in critically ill patients: the impact of diabetes[J]. J Diabetes Sci Technol, 2009, 3(6): 1292-1301. DOI:10.1177/193229680900300609 |
| [7] | Lu M, Zuo Y, Guo J, et al. Continuous glucose monitoring system can improve the quality of glucose control and glucose variability compared with point-of-care measurement in critically ill patients: A randomized controlled trial[J]. Medicine (Baltimore), 2018, 97(36): e12138. DOI:10.1097/md.0000000000012138 |
| [8] | Brunner R, Kitzberger R, Miehsler W, et al. Accuracy and reliability of a subcutaneous continuous glucose-monitoring system in critically ill patients[J]. Crit Care Med, 2011, 39(4): 659-664. DOI:10.1097/CCM.0b013e318206bf2e |
| [9] | Boom DT, Sechterberger MK, Rijkenberg S, et al. Insulin treatment guided by subcutaneous continuous glucose monitoring compared to frequent point-of-care measurement in critically ill patients: a randomized controlled trial[J]. Crit Care, 2014, 18(4): 453. DOI:10.1186/s13054-014-0453-9 |
| [10] | Corstjens AM, Ligtenberg JJ, van der Horst IC, et al. Accuracy and feasibility of point-of-care and continuous blood glucose analysis in critically ill ICU patients[J]. Crit Care, 2006, 10(5): R135. DOI:10.1186/cc5048 |
| [11] | Moghissi ES, Korytkowski MT, DiNardo M, et al. American Association of Clinical Endocrinologists and American Diabetes Association consensus statement on inpatient glycemic control[J]. Endocr Pract, 2009, 15(4): 353-369. DOI:10.4158/ep09102.ra |
| [12] | Bilotta F, Caramia R, Cernak I, et al. Intensive insulin therapy after severe traumatic brain injury: a randomized clinical trial[J]. Neurocrit Care, 2008, 9(2): 159-166. DOI:10.1007/s12028-008-9084-9 |
| [13] | Kutcher ME, Pepper MB, Morabito D, et al. Finding the sweet spot: identification of optimal glucose levels in critically injured patients[J]. J Trauma, 2011, 71(5): 1108-1114. DOI:10.1097/TA.0b013e318232e35b |
| [14] | Inzucchi SE, Bergenstal RM, Buse JB, et al. Management of hyperglycemia in type 2 diabetes: a patient-centered approach: position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD)[J]. Diabetes Care, 2012, 35(6): 1364-1379. DOI:10.2337/dc12-0413 |
| [15] | Bland JM, Altman DG. Statistical methods for assessing agreement between two methods of clinical measurement[J]. Lancet, 1986, 1(8476): 307-310. DOI:10.1016/s0140-6736(86)90837-8 |
| [16] | Kovatchev BP, Gonder-Frederick LA, Cox DJ, et al. Evaluating the accuracy of continuous glucose-monitoring sensors: continuous glucose-error grid analysis illustrated by TheraSense Freestyle Navigator data[J]. Diabetes Care, 2004, 27(8): 1922-1928. DOI:10.2337/diacare.27.8.1922 |
| [17] | Maran A, Crepaldi C, Tiengo A, et al. Continuous subcutaneous glucose monitoring in diabetic patients: a multicenter analysis[J]. Diabetes Care, 2002, 25(2): 347-352. DOI:10.2337/diacare.25.2.347 |
| [18] | 季兵, 朱建良, 马丽梅, 等. 早期集束化治疗对脓毒症及脓毒性休克患者预后的影响[J]. 中华急诊医学杂志, 2019, 28(2): 170-174. DOI:10.3760/cma.j.issn.1671-0282.2019.02.008 |
| [19] | Mahmood S, Mahmood O, El-Menyar A, et al. Predisposing factors, clinical assessment, management and outcomes of agitation in the trauma intensive care unit[J]. World J Emerg Med, 2018, 9(2): 105-112. DOI:10.5847/wjem.j.1920-8642.2018.02.004 |
| [20] | 贾育梅, 李春盛. 血糖对严重脓毒症合并2型糖尿病患者程序性死亡因子-1表达的影响[J]. 中华急诊医学杂志, 2017, 26(12): 1432-1437. DOI:10.3760/cma.j.issn.1671-0282.2017.12.020 |
| [21] | 柳学, 林晓军, 何楷然, 等. 重症脓毒症患者血糖控制与炎症因子变化及临床意义[J]. 中华急诊医学杂志, 2017, 26(12): 1438-1441. DOI:10.3760/cma.j.issn.1671-0282.2017.12.021 |
| [22] | Holzinger U, Warszawska J, Kitzberger R, et al. Real-time continuous glucose monitoring in critically ill patients: a prospective randomized trial[J]. Diabetes Care, 2010, 33(3): 467-472. DOI:10.2337/dc09-1352 |
| [23] | Brunner R, Adelsmayr G, Herkner H, et al. Glycemic variability and glucose complexity in critically ill patients: a retrospective analysis of continuous glucose monitoring data[J]. Crit Care, 2012, 16(5): R175. DOI:10.1186/cc11657 |
| [24] | Ba L, Zhang M, Su L, et al. Nine-year change of mortality and discharge against medical advice among major trauma patients in a Chinese Intensive Care Unit[J]. Eur J Trauma Emerg Surg, 2016, 42(1): 47-53. DOI:10.1007/s00068-015-0511-2 |
| [25] | Risso A, Mercuri F, Quagliaro L, et al. Intermittent high glucose enhances apoptosis in human umbilical vein endothelial cells in culture[J]. Am J Physiol Endocrinol Metab, 2001, 281(5): E924-930. DOI:10.1152/ajpendo.2001.281.5.E924 |
| [26] | Kurtz P, Claassen J, Helbok R, et al. Systemic glucose variability predicts cerebral metabolic distress and mortality after subarachnoid hemorrhage: a retrospective observational study[J]. Crit Care, 2014, 18(3): R89. DOI:10.1186/cc13857 |
| [27] | Waeschle RM, Moerer O, Hilgers R, et al. The impact of the severity of sepsis on the risk of hypoglycaemia and glycaemic variability[J]. Crit Care, 2008, 12(5): R129. DOI:10.1186/cc7097 |
| [28] | Eslami S, Taherzadeh Z, Schultz MJ, et al. Glucose variability measures and their effect on mortality: a systematic review[J]. Intensive Care Med, 2011, 37(4): 583-593. DOI:10.1007/s00134-010-2129-5 |
 2019, Vol. 28
2019, Vol. 28




