急性肺损伤(acute lung injury,ALI)是急性重症胰腺炎(acute necrotizing pancreatitis,ANP)的最常见早期并发症之一,由肺损伤持续加重导致且进一步可发展为急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)甚至危及生命,然而其确切发生机制尚不完全清晰,可能与ANP时大量炎症因子释放有关[1]。由于调控这些炎症因子产生的信号通路主要为Toll受体家族(toll-like receptor,TLRs)介导的核转录因子(nuclear factor kappa-B,NF-κB)等信号通路[2],而脂氧素A(lipoxin A,LXA)具有抑制白细胞游走、抑制黏附分子表达、拮抗白三烯等功能,脂氧素A4类似物(Lipoxin A4,LXA4)是体内炎症反应的重要抑制因子[3],因此,本研究分析了Toll样受体4(toll-like receptor 4,TLR4)/NF-KB信号通路在急性重症胰腺炎相关肺损伤中的作用,并探讨了LXA4的干预结果,旨在为临床急性重症胰腺炎相关肺损伤的治疗提供参考依据。
1 材料与方法 1.1 材料牛磺胆酸钠购自美国Sigma-Aldrich公司。采用全自动生化分析仪检测血清淀粉酶含量(检测试剂盒购于Sigma公司)。应用ELISA法检测血清中TNF-α、IL-1β、IL-6含量(检测试剂盒购于北京中杉金桥生物有限公司)。应用微生物快速动态监测系统检测血清内毒素含量(检测试剂盒购于天津一瑞生物工程有限公司)。
1.2 实验动物及分组清洁级健康雄性SD大鼠(SCXK(陕)2018-001)45只,体质量200~300 g,购于本校实验动物中心,在安静、温暖(18~25℃)、避强光、昼夜光照节律的实验室饲养1周后供本研究实验所用,自由饮水和摄食。为每只SD大鼠编号,按照随机数字表法分为假手术组、实验组、干预组,每组15只。本研究经西安交通大学动物实验伦理审批(XJTULAC2019-1150)。
1.3 方法 1.3.1 ANP动物模型制备实验组:动物于术前12 h禁食,不禁水[4]。术前腹腔内注射10%水合氯醛3~4 mL/kg麻醉[5],达到满意麻醉状态后腹部备皮,剑突下腹正中开腹,找到十二指肠及胆胰管,阻断胆总管出肝门处,静脉留置针穿刺胆胰管开口处的十二指肠对侧壁,进入十二指肠肠腔,退出针芯,进入套管,按1 mL/kg体质量的剂量缓慢(0.1 mL/min)注射4%牛磺胆酸钠10 min[6];注射完毕应用血管钳夹闭胆总管入十二指肠处5 min[5],肉眼可见充血、水肿时提示造模成功,随后缝合、关腹; 所有实验操作在无菌操作下完成。
假手术组:胆胰管内不注入牛磺胆酸钠,其余操作同实验组。干预组:于造模后30 min经尾静脉注射LXA4,具体剂量参考文献[7]标准(87.5μg/kg)。假手术组和实验组均于造模后30 min经尾静脉注射等量生理盐水。
1.3.2 标本采集将各组15只大鼠随机分为3组,每组5只,分别于术后6 h、12 h、24 h采用腹主动脉抽血法处死。采集血液后抗凝、离心,采集血清; 取胰腺和肺组织。
(1)大鼠术后血清淀粉酶、肿瘤坏死因子-α(TNF-α)、白介素-1β(IL-1β)、白介素-6(IL-6)、内毒素水平检测
(2)大鼠术后肺损伤学评分、肺湿/干质量比值取右肺上叶进行常规病理检查,参考Osman肺脏组织学评分[8]标准进行肺损伤评分,从“肺组织水肿”,“肺泡组织中性粒细胞、肺间质单核细胞浸润”,“肺组织出血”三个层面进行评分,评分范围0~9分,分数越高表明肺组织损伤程度越严重。
取左肺称质量,电热干燥箱烘烤(60℃,48 h),称干质量。计算肺组织湿/干质量比值[9]=(肺湿质量-肺干质量)/肺干质量。
(3)大鼠术后肺组织中TLR4、NF-κB p65蛋白表达检测取10 g右肺中叶,匀浆,常规进行Western-blot检测。TLR4、NF-κB p65蛋白一抗及二抗均购于美国Sigma公司,实验结束后经图像分析软件进行分析,以平均灰度值表示TLR4、NF-κB p65蛋白的相对含量。
1.4 统计学方法实验数据应用SPSS 21.0软件分析,计量资料用均数±标准差(Mean±SD)表示,采用单因素方差分析及LSD-t检验进行统计学分析,以P<0.05为差异有统计学意义。
2 结果 2.1 各组大鼠术后血清淀粉酶、TNF-α、IL-1β、IL-6、内毒素水平比较统计结果显示,实验组、干预组术后6 h、12 h、24 h的血清淀粉酶、TNF-α、IL-1β、IL-6、内毒素水平均明显高于假手术组,差异有统计学意义(P<0.05); 干预组术后6 h、12 h、24 h的血清淀粉酶、TNF-α、IL-1β、IL-6、内毒素水平均明显低于实验组,差异有统计学意义(P<0.05)。见表 1。
| 指标 | n | 术后6 h | 术后12 h | 术后24 h | F值 | P值 |
| 淀粉酶(U/L) | ||||||
| 假手术组 | 5 | 246.53±9.42 | 242.28±10.57 | 249.46±14.82 | 0.465 | 0.639 |
| 实验组 | 5 | 831.80±18.24c | 1765.47±71.86ac | 2314.45±52.65abc | 1019.334 | <0.001 |
| 干预组 | 5 | 520.70±32.31cd | 1144.52±55.91acd | 1908.19±64.70abcd | 866.872 | <0.001 |
| F值 | 877.671 | 1047.350 | 2501.024 | |||
| P值 | <0.001 | <0.001 | <0.001 | |||
| TNF-α(pg/mL) | ||||||
| 假手术组 | 5 | 15.93±0.70 | 16.22±1.39 | 16.01±2.52 | 0.040 | 0.961 |
| 实验组 | 5 | 377.64±24.02c | 762.74±40.88ac | 985.84±53.29abc | 279.085 | <0.001 |
| 干预组 | 5 | 82.08±11.13cd | 156.66±10.05acd | 291.62±45.13abcd | 74.827 | <0.001 |
| F值 | 793.569 | 1330.650 | 767.241 | |||
| P值 | <0.001 | <0.001 | <0.001 | |||
| IL-1β(pg/mL) | ||||||
| 假手术组 | 5 | 43.97±10.15 | 45.37±9.40 | 48.00±12.46 | 0.181 | 0.837 |
| 实验组 | 5 | 94.74±10.21c | 193.13±20.51ac | 347.76±26.80abc | 196.275 | <0.001 |
| 干预组 | 5 | 79.04±11.80cd | 98.94±14.13cd | 157.82±18.33abcd | 37.327 | <0.001 |
| F值 | 29.259 | 118.421 | 285.213 | |||
| P值 | <0.001 | <0.001 | <0.001 | |||
| IL-6(pg/mL) | ||||||
| 假手术组 | 5 | 33.58±11.11 | 35.54±9.60 | 32.89±4.03 | 0.122 | 0.886 |
| 实验组 | 5 | 98.49±13.90c | 164.18±20.50ac | 196.41±21.66abc | 34.510 | <0.001 |
| 干预组 | 5 | 78.00±6.63cd | 139.76±15.51acd | 122.74±7.27abcd | 45.234 | <0.001 |
| F值 | 45.823 | 92.961 | 186.929 | |||
| P值 | <0.001 | <0.001 | <0.001 | |||
| 内毒素(pg/L) | ||||||
| 假手术组 | 5 | 7.71±0.74 | 7.90±0.75 | 7.90±0.97 | 0.084 | 0.920 |
| 实验组 | 5 | 86.80±10.30c | 256.69±21.87ac | 429.68±22.53abc | 403.647 | <0.001 |
| 干预组 | 5 | 54.95±8.46cd | 183.07±11.05acd | 212.16±12.95abcd | 290.431 | <0.001 |
| F值 | 133.343 | 407.491 | 986.692 | |||
| P值 | <0.001 | <0.001 | <0.001 | |||
| 注:与术后6 h比较,aP<0.05;与术后12 h比较,bP<0.05;与假手术组比较,cP<0.05;与实验组比较,dP<0.05 | ||||||
实验组术后6 h、12 h、24 h的肺损伤学评分、肺湿/干质量比值均明显高于假手术组,差异有统计学意义(P<0.05); 干预组术后6h肺损伤学评分与假手术组比较差异无统计学意义(P>0.05),但术后6 h肺湿/干质量比值以及12 h、24 h的肺损伤学评分、肺湿/干质量比值均明显高于假手术组,差异有统计学意义(P<0.05); 干预组术后6 h、12 h、24 h的肺损伤学评分、肺湿/干质量比值均明显低于实验组,差异有统计学意义(P<0.05)。且肺损伤学评分,实验组术后12 h与6 h比较差异无统计学意义(P>0.05),术后24 h与术后12h比较差异无统计学意义(P>0.05)。见表 2。
| 指标 | n | 术后6 h | 术后12 h | 术后24 h | F值 | P值 | |
| 肺损伤学评分 | |||||||
| 假手术组 | 5 | 0.20±0.45 | 0.20±0.45 | 0.20±0.45 | 0.000 | 1.000 | |
| 实验组 | 5 | 3.40±1.95c | 4.60±1.14c | 6.40±1.14ac | 5.344 | 0.022 | |
| 干预组 | 5 | 1.00±0.00d | 2.00±0.71acd | 3.00±0.00abcd | 30.000 | <0.001 | |
| F值 | 10.400 | 36.700 | 96.400 | ||||
| P值 | 0.002 | <0.001 | <0.001 | ||||
| 肺湿/干质量比值 | |||||||
| 假手术组 | 5 | 2.57±0.37 | 2.68±0.11 | 2.65±0.37 | 0.148 | 0.864 | |
| 实验组 | 5 | 4.03±0.19c | 4.54±0.42ac | 5.18±0.38abc | 14.232 | 0.001 | |
| 干预组 | 5 | 3.29±0.32cd | 4.02±0.29acd | 4.25±0.28acd | 14.419 | 0.001 | |
| F值 | 29.539 | 51.742 | 69.733 | ||||
| P值 | <0.001 | <0.001 | <0.001 | ||||
| 注:与术后6 h比较,aP<0.05;与术后12 h比较,bP<0.05;与假手术组比较,cP<0.05;与实验组比较,dP<0.05 | |||||||
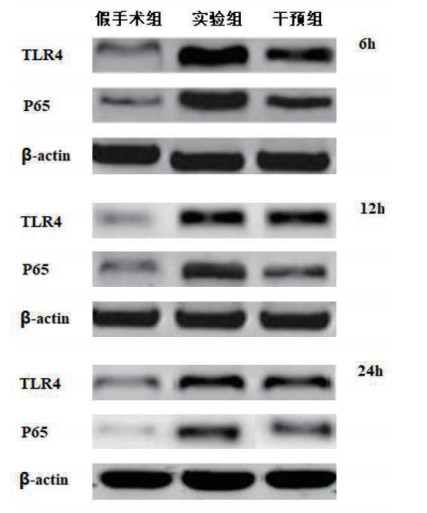
实验组、干预组术后6 h、12 h、24 h的肺组织中TLR4、NF-κB p65表达水平均明显高于假手术组,差异有统计学意义(P<0.05); 干预组术后6 h、12 h、24 h的肺组织中TLR4、NF-κB p65表达水平均明显低于实验组,差异有统计学意义(P<0.05)。见表 3,图 1。
| 指标 | n | 术后6 h | 术后12 h | 术后24 h | F值 | P值 |
| TLR4 | ||||||
| 假手术组 | 5 | 894.31±103.87 | 885.46±97.64 | 889.32±49.54 | 0.013 | 0.987 |
| 实验组 | 5 | 1683.55±69.32c | 2089.77±83.77ac | 2349.02±65.75abc | 104.529 | <0.001 |
| 干预组 | 5 | 1252.14±55.89cd | 1458.05±104.44acd | 1613.91±76.31abcd | 24.878 | <0.001 |
| F值 | 125.154 | 198.244 | 634.110 | |||
| P值 | <0.001 | <0.001 | <0.001 | |||
| NF-κB p65 | ||||||
| 假手术组 | 5 | 642.32±58.72 | 664.51±34.26 | 633.67±67.00 | 0.416 | 0.669 |
| 实验组 | 5 | 1687.16±197.79c | 1950.38±139.21ac | 2314.30±124.66abc | 20.091 | <0.001 |
| 干预组 | 5 | 1074.35±64.14cd | 1331.89±109.47acd | 1600.24±70.64abcd | 49.191 | <0.001 |
| F值 | 88.569 | 190.664 | 426.541 | |||
| P值 | <0.001 | <0.001 | <0.001 | |||
| 注:与术后6 h比较,Pa<0.05;与术后12 h比较,bP<0.05;与假手术组比较,cP<0.05;与实验组比较,dP<0.05 | ||||||
|
| 图 1 术后不同时间点肺组织中TLR4、NF-κB p65蛋白的表达 Fig 1 Expression of TLR4 and p65 proteins in lung tissues at different time points after operation |
|
|
ANP的最常见早期并发症是ALI,其发病率约15%~60%,可由肺损伤持续加重导致,且进一步可发展为ARDS。有统计结果显示,60%~80%发病后1周内死亡的ANP患者均与ALI和(或)ARDS有关[10-12]。目前,ANP相关肺损伤的确切发生机制尚不完全清晰,得到证实的是TLRs家族的TLR4与其主要配体内毒素结合后被激活,致使ANP发生,同时可导致NF-κB活化,而激活的NF-κB信号通路可触发炎症介质瀑布样级联反应并导致大量炎症因子释放[13-15],进而参与胰外脏器损伤的发生发展过程。其中TNF-α、IL-6等促炎因子不仅在ANP的发病中发挥了核心作用,也是诱发最终多器官功能障碍的重要[16]因素。
本研究采用牛磺胆酸钠进行胆胰管逆行注射法造模,是目前最常用且最稳定的ANP造模方法[17-20]。目前国内广泛采用的是Zhang等[4]的方案,即采用3.5%牛磺胆酸钠进行造模,但是,袁琳等[21]研究发现,采用5%牛磺胆酸钠进行造模优于3.5%浓度,而Zhang等[6]采用4%浓度也获得了稳定的模型,因此,笔者进行预实验,采用4%牛磺胆酸钠胆胰管逆行注射法造模,随后通过对胰腺组织的观察、判断以及病理学检查、Schimidt评分[22]并结合淀粉酶等指标,发现采用4%牛磺胆酸钠进行胆胰管逆行注射法造模,可以稳定制造ANP模型,且符合ANP的生理、病理表现。因此,本研究采用该方案造模,随后观察各组大鼠术后不同时间点血中炎性细胞因子、内毒素的水平变化情况。结果显示,实验组、干预组术后6 h、12 h、24 h的TNF-α、IL-1β、IL-6、内毒素水平均明显高于假手术组。说明TNF-α、IL-1β、IL-6等炎性细胞因子参与了ANP相关肺损伤过程,可能与高水平的内毒素与TLR4的结合从而活化NF-κB信号传导通路有关。干预组术后6 h、12 h、24 h的TNF-α、IL-1β、IL-6、内毒素水平均明显低于实验组。说明经过LXA4的干预,能够对ANP发生时体内炎症反应等病理过程发挥一定的抑制作用,LXA4可能为体内重要的内源性促炎症消退介质。
脂氧素是二十烷家族的代谢产物,具有抑制白细胞游走、黏附分子表达、拮抗白三烯等功能,LXA4是体内炎症反应的重要刹车信号[23],已有研究结果证实,在减轻肺损伤、血管内皮细胞损伤、缺血-再灌注损伤等病理过程中,LXA4均发挥重要的保护作用[24-26]。进一步研究各组大鼠肺损伤的情况,结果表明实验组术后6 h、12 h、24 h,以及干预组术后12 h、24 h的肺损伤学评分、肺湿/干质量比值均明显高于假手术组; 干预组术后6 h、12 h、24 h的肺损伤学评分、肺湿/干质量比值均明显低于实验组,且术后6 h肺损伤学评分与假手术组比较差异无统计学意义,证实了经过LXA4的干预能够明显的减轻ANP相关肺损伤的程度。实验还发现,实验组术后12 h肺损伤学评分与6 h比较差异无统计学意义,术后24 h与术后12 h比较差异无统计学意义,说明应用LXA4可以延缓肺损伤的进展,进一步证实了LXA4对ANP相关肺损伤的潜在治疗作用。
为了进一步分析NF-κB信号传导通路在ANP相关肺损伤中的表达和LXA4的干预效果,经Western-blot实验检测了各组大鼠术后不同时间点肺组织中TLR4、NF-κB p65的蛋白表达情况,结果证实:TLR4、NF-κB p65的蛋白表达与TNF-α、IL-1β、IL-6、内毒素的变化具有类似趋势,进一步证实了TLR4、NF-κB参与了ANP相关肺损伤的发病过程以及LXA4的积极干预效果。
| [1] | Störmann P, Lustenberger T, Relja B, et al. Role of biomarkers in acute traumatic lung injury[J]. Injury, 2017, 48(11): 2400-2406. DOI:10.1016/j.injury.2017.08.041 |
| [2] | Zhu ZY, Sun L, Hao R, et al. Nedd8 modification of Cullin-5 regulates lipopolysaccharide-induced acute lung injury[J]. Am J Physiol Lung Cell Mol Physiol, 2017, 313(1): L104-L114. DOI:10.1152/ajplung.00410.2016 |
| [3] | Peng CK, Wu CP, Lin JY, et al. Gas6/Axl signaling attenuates alveolar inflammation in ischemia-reperfusion-induced acute lung injury by up-regulating SOCS3-mediated pathway[J]. PLoS One, 2019, 14(7): e0219788. DOI:10.1371/journal.pone.0219788 |
| [4] | Zhang XP, Ye Q, Jiang XG, et al. Preparation method of an ideal model of multiple organ injury of rat with severe acute pancreatitis[J]. World Journal of Gastroenterology, 2007, 13(34): 4566-4573. DOI:10.3748/wjg.v13.i34.4566 |
| [5] | 李欢.重症急性胰腺炎大鼠肺损伤的病理生理变化及机制[D].河北医科大学, 2009. DOI: 10.7666/d.y1636673. http://cdmd.cnki.com.cn/Article/CDMD-11919-2009139301.htm |
| [6] | Zhang DQ, Feng H, Chen WC. Effects of Hydrogen-Rich Saline on Taurocholate-Induced Acute Pancreatitis in Rat[J]. Evidence-Based Complementary and Alternative Medicine, 2013(2013): 1-6. DOI:10.1155/2013/731932 |
| [7] | 周春华, 呼闯营, 王少峰, 等. 脂氧素A4类似物对急性胰腺炎肺损伤大鼠的保护作用[J]. 中华实验外科杂志, 2012, 29(9): 1784-1787. DOI:10.3760/cma.j.issn.1001-9030.2012.09.051 |
| [8] | Kiyonari Y, Nishina K, Mikawa K, et al. Lidocaine attenuates acute lung injury induced by a combination of phospholipase A2 and trypsin[J]. Crit Care Med, 2000, 28(2): 484-489. DOI:10.1097/00003246-200002000-00033 |
| [9] | Collins JC, Newman JH, Wickersham NE, et al. Relation of blood-free to blood-inclusive postmortem lung water measurements in sheep[J]. Journal of Applied Physiology, 1985, 59(2): 592. DOI:10.1152/jappl.1985.59.2.592 |
| [10] | Shields CJ, Winter DC, Redmond HP. Lung injury in acute pancreatitis: mechanisms, prevention, and therapy[J]. Current Opinion in Critical Care, 2002, 8(2): 158-163. DOI:10.1097/00075198-200204000-00012 |
| [11] | 陈秋星, 吕德超, 曹斌, 等. 重症急性胰腺炎并发急性肺损伤危险因素的临床研究[J]. 肝胆胰外科杂志, 2012, 24(6): 451-454, 458. DOI:10.3969/j.issn.1007-1954.2012.06.004 |
| [12] | Li QQ, Sun MH, Wan ZR, et al. Bee pollen extracts modulate serum metabolism in lipopolysaccharide-induced acute lung injury mice with anti-inflammatory effects[J]. J Agric Food Chem, 2019, 67(28): 7855-7868. DOI:10.1021/acs.jafc.9b03082 |
| [13] | Pan LF, Yu L, Wang LM, et al. Augmenter of liver regeneration (ALR) regulates acute pancreatitis via inhibiting HMGB1/TLR4/NF-kappa B signaling pathway[J]. Am J Transl Res, 2018, 10(2): 402-410. |
| [14] | Pan LF, Yu L, Wang LM, et al. Inflammatory stimuli promote oxidative stress in pancreatic acinar cells via Toll-like receptor 4/nuclear factor-κB pathway[J]. International Journal of Molecular Medicine, 2018, 42(6): 3582-3590. DOI:10.3892/ijmm.2018.3906 |
| [15] | Jiang QH, Wang SJ, Shi Y. Posttreatment With LYRM03 Protects Rats From Acute Lung Inflammation Induced by Lipopolysaccharide via Suppressing the NF-κB/MyD88/TLR4 Axis[J]. J Surg Res, 2019, 27(243): 316-324. DOI:10.1016/j.jss.2019.05.036 |
| [16] | Wang J, Fan SM, Zhang J. Epigallocatechin-3-gallate ameliorates lipopolysaccharide-induced acute lung injury by suppression of TLR4/NF-κB signaling activation[J]. Braz J Med Biol Res, 2019, 52(7): e8092. DOI:10.1590/1414-431x20198092 |
| [17] | Aho H J, Koskensalo S M, Nevalainen TJ. Experimental pancreatitis in the rat: Sodium taurocholate-induced acute haemorrhagic pancreatitis[J]. Scand J Gastroenterol, 1980, 15(4): 411-416. DOI:10.3109/00365528009181493 |
| [18] | Zhao Q, Zhang H, Huang JH, et al. Melatonin attenuates the inflammatory response via inhibiting the C/EBP homologous protein-mediated pathway in taurocholate-induced acute pancreatitis[J]. International Journal of Molecular Medicine, 2018, 42(6): 3513-3521. DOI:10.3892/ijmm.2018.3920 |
| [19] | Silva-Vaz P, Abrantes AM, Castelo-Branco M, et al. Murine Models of Acute Pancreatitis: A Critical Appraisal of Clinical Relevance[J]. Int J Mol Sci, 2019, 20(11): 2794. DOI:10.3390/ijms20112794 |
| [20] | Banks PA, Bollen TL, Dervenis C, et al. Classification of acute pancreatitis—2012: revision of the Atlanta classification and definitions by international consensus[J]. Gut, 2013, 62(1): 102-111. DOI:10.1136/gutjnl-2012-302779 |
| [21] | 袁琳, 周秉舵, 王晓素, 等. 三种不同严重程度大鼠重症胰腺炎模型比较研究[J]. 中国比较医学杂志, 2015, 25(05): 20-23. DOI:10.3969/j.issn.1671.7856.2015.005.005 |
| [22] | Schmidt J, Rattner DW, Lewandrowski K, et al. A Better Model of Acute Pancreatitis for Evaluating Therapy[J]. Annals of Surgery, 1992, 215(1): 44-56. DOI:10.1097/00000658-199201000-00007 |
| [23] | 葛思堂, 赵群, 王姗, 等. 脂氧素A4对重症急性胰腺炎模型小鼠肾损伤的保护性作用[J]. 齐齐哈尔医学院学报, 2018, 39(20): 2361-2363. DOI:10.3969/j.issn.1002-1256.2018.20.002 |
| [24] | Liu HZ, Zhou KF, Liao LK, et al. Lipoxin A4 receptor agonist BML-111 induces autophagy in alveolar macrophages and protects from acute lung injury by activating MAPK signaling[J]. Respir Res, 2018, 19(1): 243. DOI:10.1186/s12931-018-0937-2 |
| [25] | Liu ZH, Qu M, Yang Q, et al. Lipoxin A4 ameliorates renal ischaemia-reperfusion-induced acute lung injury in rats[J]. Clin Exp Pharmacol Physiol, 2019, 46(1): 65-74. DOI:10.1111/1440-1681.13023 |
| [26] | Pádua TA, Torres ND, Candéa ALP, et al. Therapeutic effect of Lipoxin A4 in malaria-induced acute lung injury[J]. J Leukoc Biol, 2018, 103(4): 657-670. DOI:10.1002/JLB.3A1016-435RRR |
 2019, Vol. 28
2019, Vol. 28




