2 首都医科大学附属北京友谊医院急危重症中心 100050
2 Emergency and Intensive Care Medicine Center, Beijing Friendship Hospital, Capital Medical University, Beijing 100050, China
目前病原体培养仍是鉴别脓毒症病原学的重要方法,但病原体培养所需的时间较长,阳性率不高,从而使有针对性的抗感染治疗变得十分困难[1]。降钙素原(procalcitonin, PCT)和C-反应蛋白(C-reactive protein, CRP)是诊断脓毒症常用的生物标志物,已广泛应用于临床[2-7]。可溶性CD14亚型(sCD14-ST,即Presepsin)作为诊断脓毒症的新型生物标志物,在脓毒症早期诊断方面具有较高的敏感度和特异度[8-15]。本研究旨在比较Presepsin、PCT和CRP对脓毒症患者不同病原菌感染的鉴别价值,为临床上早期选择恰当的抗生素提供思路。
1 资料与方法 1.1 一般资料收集2016年7月至2018年1月入住大连医科大学附属第一医院急诊ICU的脓毒症患者为脓毒症组(n=322),其中男性179例,女性143例,年龄(63.04±16.12)岁。纳入标准:符合“脓毒症3.0”的诊断标准[16];血培养结果至少一次为阳性;进行血培养前未应用抗生素。排除标准:血培养结果怀疑为污染的患者;合并严重急慢性肝肾功能不全或血液病的患者;免疫系统疾病患者;正使用糖皮质激素和(或)免疫抑制剂治疗患者;有恶性肿瘤病史者;临床资料不全者。选择健康志愿者作为对照组(n=45),其中男性26例,女性19例,年龄(61.93±13.24)岁。本研究方案经大连医科大学附属第一医院伦理委员会批准,并获患者或家属知情同意。
1.2 检测方法入院第1天无菌条件下采集脓毒症患者外周静脉血10 mL,注入血培养瓶(8 mL)和真空采血管(2 mL),分别做血培养(Bactec FX200全自动血培养仪,美国BD公司)、细菌鉴定(MicroScan96全自动细菌鉴定仪,德国西门子公司)和检测Presepsin(PATHFAST化学发光免疫测定分析仪,日本三菱化学医药公司)、PCT(Cobas e411电化学发光仪,美国罗氏公司)及CRP(BN-Ⅱ特种蛋白仪,德国西门子公司);所用测定试剂均选用原厂家仪器配套试剂。
1.3 统计学方法采用SPSS 20.0统计软件进行统计分析。符合正态分布的计量资料用均数±标准差(Mean±SD)表示,非正态分布的计量资料用中位数(四分位数)[M(P25, P75)]表示,多组间比较采用单因素方差分析,组间两两比较采用SNK-q检验或Mann-Whitney U检验。计数资料比较采用χ2检验或Fisher精确概率法。绘制受试者工作特征曲线(ROC),计算ROC曲线下面积(AUC)来确定Presepsin及PCT对脓毒症患者的诊断价值以及对不同病原菌感染的鉴别诊断价值,并确定最佳截断点。以P < 0.05为差异有统计学意义。
2 结果 2.1 研究对象一般情况入选的322例脓毒症患者中血培养阳性和阴性的患者与对照组之间年龄与性别差异无统计学意义(P > 0.05,表 1)。血培养阳性中G+球菌、G-杆菌、真菌组和混合菌感染的患者之间年龄与性别差异无统计学意义(P > 0.05,表 1)。
| 组别 | 例数 | 年龄 (岁,Mean±SD) |
男性(例, %) | P值 |
| 血培养阳性 | 114 | 64.6±15.8 | 71(62.3) | > 0.05 |
| G+球菌 | 47 | 64.6±17.9 | 29(61.7) | > 0.05 |
| G-杆菌 | 52 | 63.2±14.7 | 33(63.5) | > 0.05 |
| 真菌 | 12 | 70.8±12.9 | 7(58.3) | > 0.05 |
| 混合菌 | 3 | 66.0±5.0 | 2(66.7) | > 0.05 |
| 血培养阴性 | 208 | 62.2±16.2 | 108(51.9) | > 0.05 |
| 对照组 | 45 | 61.9±13.2 | 26(57.8) | > 0.05 |
血培养阳性和阴性患者Presepsin、PCT和CRP均显著高于对照组(均P < 0.05,表 2);血培养阳性患者Presepsin和PCT均显著高于血培养阴性患者(均P < 0.05),而CRP差异无统计学意义(P > 0.05)。
| 指标 | 对照组 | 脓毒症组 | |
| 血培养阴性 | 血培养阳性 | ||
| Presepsin(pg/mL) | 156±63 | 511(354, 807)a | 708(556, 1007)b |
| PCT(ng/mL) | 0.04±0.02 | 0.99(0.38, 2.85)a | 1.63(0.53, 8.93)b |
| CRP(mg/L) | 4.2(3.2, 6.5) | 87.7(46.3, 128.0) | 87.9(58.6, 114.0) |
| 注:与对照组比较,aP < 0.05;与血培养阴性比较,bP < 0.05 | |||
114例血培养阳性的ICU脓毒症患者病原菌分布及相应的Presepsin、PCT和CRP值见表 3。
| 病原菌类型 | 例数 | Presepsin (pg/mL) |
PCT (ng/mL) |
CRP (mg/L) |
| 革兰阳性球菌 | 47 | |||
| 表皮葡萄球菌 | 5 | 685.8±284.9 | 0.20(0.08, 6.59) | 87.7±55.7 |
| 屎肠球菌 | 7 | 988.8±508.4 | 0.26(0.07, 2.76) | 114(76.4, 132) |
| s金黄色葡萄球菌 | 18 | 663.5(503.3, 1 027) | 1.11(0.28, 2.97) | 107.6±55.3 |
| 人葡萄球菌 | 4 | 585.9±160.1 | 0.70(0.25, 1.16) | 91.2±40.7 |
| 其他 | 13 | 883.5±518.3 | 1.05(0.58, 2.30) | 85.5±48.1 |
| 革兰阴性杆菌 | 52 | |||
| 大肠埃希菌 | 15 | 649(592, 1 405) | 2.35(0.31, 9.49) | 84.3±53.3 |
| 鲍曼不动杆菌 | 6 | 926.8±422.1 | 6.13(2.33, 20.85) | 108.0±20.7 |
| 肺炎克雷伯杆菌 | 13 | 761.6±294.3 | 13.36(5.16, 34.89) | 86.3(64.9, 110) |
| 铜绿假单胞菌 | 4 | 1 213.8±842.8 | 8.55(2.38, 16.31) | 80.4±35.0 |
| 其他 | 14 | 1 014.7±544.6 | 4.69(0.54, 16.13) | 103.3±57.7 |
| 真菌 | 12 | |||
| 白色假丝酵母菌 | 5 | 800.4±236.6 | 1.05(0.78, 4.31) | 61.2±26.1 |
| 近平滑假丝酵母菌 | 3 | 734.6±178.2 | 0.72±0.51 | 108.7±23.7 |
| 念珠菌 | 4 | 966.5±85.6 | 1.08±0.30 | 64.6±19.6 |
| 混合菌 | 3 | |||
| 大肠+屎肠球菌 | 1 | 672 | 29.27 | 87.8 |
| 鲍曼+屎肠球菌 | 1 | 973 | 4.72 | 78.5 |
| 铜绿+金葡 | 1 | 867 | 10.28 | 52.7 |
| 注:CRP,C-反应蛋白;PCT,降钙素原;Presepsin,可溶性CD14亚型;大肠,大肠埃希菌;铜绿,铜绿假单胞菌;金葡,金黄色葡萄球菌;鲍曼,鲍曼不动杆菌 | ||||
G+球菌、G-杆菌、真菌组和混合菌感染患者血Presepsin和CRP的差异均无统计学意义(均P > 0.05,表 4)。G-杆菌和混合菌感染患者血PCT均显著高于G+球菌或真菌感染患者(均P < 0.05),而G-杆菌和混合菌感染以及G+球菌和真菌感染之间的PCT差异均无统计学意义(均P > 0.05)。
| 指标 | G+球菌 | G-杆菌 | 真菌 | 混合菌 |
| Presepsin(pg/mL) | 790.5±419.3 | 712.0(592.0, 1 178.0) | 800. 7±198.9 | 910.8±152.7 |
| PCT(ng/mL) | 1.04(0.26, 2.53) | 5.48(0.86, 17.48)ab | 0.95(0.53, 1.46) | 14.76±12.87ab |
| CRP(mg/L) | 95.7±57.8 | 95.6±56.1 | 81.5±32.6 | 73.0±18.2 |
| 注:CRP,C-反应蛋白;PCT,降钙素原;Presepsin,可溶性CD14亚型。与G+球菌感染比较,aP < 0.05;与真菌感染比较,bP < 0.05 | ||||
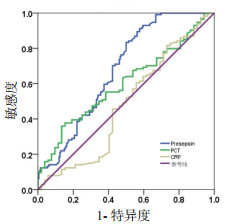
Presepsin、PCT和CRP预测脓毒症患者血培养阳性的ROC曲线见图 1。Presepsin的曲线下面积(AUC)高于PCT(0.680 vs 0.599,P < 0.05)或CRP(0.680 vs 0.479,P < 0.05)。当Presepsin截断值为451 pg/mL时,预测脓毒症患者血培养阳性的灵敏度为91.2%,特异度为42.3%。
|
| CRP,C-反应蛋白;PCT,降钙素原;Presepsin,可溶性CD14亚型 图 1 Presepsin、PCT和CRP预测脓毒症患者血培养阳性的ROC曲线 Fig 1 The ROC curve of Presepsin, PCT and CRP in patients with sepsis for prediction of positive blood culture |
|
|
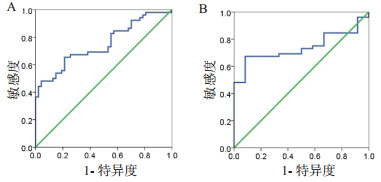
当PCT截断值为2.75 ng/mL时,区分G-杆菌与G+球菌感染的AUC为0.749(95%CI: 0.654~0.845),灵敏度为65.4%,特异性为78.7%(图 2A)。当PCT截断值为2.18 ng/mL时,区分G-杆菌与真菌感染的AUC为0.739(95%CI: 0.619~0.859),灵敏度为67.3%,特异度为91.7%(图 2B)。
|
| 图 2 PCT鉴别G-杆菌与G+球菌(A)、G-杆菌与真菌(B)感染的ROC曲线 Fig 2 The ROC curve of PCT for identification of G- bacillus and G+ cocci (A), G- bacillus and fungus (B) infections |
|
|
本研究发现无论血培养阳性还是阴性的脓毒症患者血Presepsin、PCT和CRP均显著升高,但血培养阳性的脓毒症患者血Presepsin和PCT均显著高于血培养阴性的;Presepsin在血培养出G-杆菌、G+球菌、混合菌和真菌的脓毒症患者间的差异无统计学意义;G-杆菌和混合菌感染者的PCT均显著高于G+球菌及真菌感染者;Presepsin预测血培养阳性的ROC曲线下面积大于PCT,提示Presepsin对早期预测脓毒症患者血培养阳性具有更高的价值。
脓毒症为机体对感染的反应失调而导致危及生命的器官功能障碍[16]。早期有针对性的抗感染治疗对于脓毒症的成功救治非常关键。PCT和CRP是诊断脓毒症常用的生物标志物,且已广泛应用于临床,目前已有研究表明PCT对不同病原菌所致感染有鉴别诊断意义[3, 7, 17],与本研究结果类似。但PCT也有其局限性,一些非感染情况(如创伤)也可引起其升高。Presepsin是sCD14被组织蛋白酶D水解的N端片段构成的亚型[12]。健康志愿者血Presepsin为55~184 pg/mL[10, 13, 18],本研究结果(155.6±62.8)pg/mL与以前报道类似。目前,Presepsin作为脓毒症新型标志物,已被证实在脓毒症患者的血中会显著升高,升高程度与脓毒症的严重程度呈正相关[11, 14, 19-20],并且Presepsin在脓毒症的诊断、病情严重性和预后评估方面均优于PCT和CRP[8],但Presepsin对脓毒症不同病原菌的鉴别诊断却未见报道。本研究发现Presepsin预测脓毒症患者血培养阳性的ROC曲线下面积大于PCT和CRP,提示Presepsin对早期预测脓毒症患者血培养阳性的诊断价值高于PCT和CRP,这可能是由于脓毒症患者血Presepsin的产生与细菌被吞噬过程有关,而与细菌的脂多糖(LPS)和炎症介质无关[21]。然而,Presepsin水平受肾功能影响,在肾功能不全的非感染性疾病患者中,Presepsin水平也会有不同程度地升高[22],因此本研究剔除了合并有肾功能不全的患者,以减少对Presepsin水平的影响。
本研究中,G-杆菌或混合菌感染的脓毒症患者血PCT显著高于G+球菌或真菌感染者,而四个亚组(G+球菌、G-杆菌、真菌和混合菌感染者)Presepsin及CRP差异均无统计学意义。这提示PCT对G-杆菌与G+球菌、G-杆菌与真菌、混合菌与G+球菌、混合菌与真菌感染可能具有鉴别诊断意义;而PCT对G-杆菌感染与混合菌感染,G+球菌感染与真菌感染均无鉴别意义;Presepsin对脓毒症不同病原菌感染无鉴别价值。CD14作为G-杆菌LPS的特异性受体,应该特异性地反映G-杆菌的感染,而本研究中Presepsin在脓毒症患者G-杆菌、G+球菌、混合菌和真菌感染者中的差异均无统计学意义,可能与Presepsin是在病原菌感染后被吞噬过程中所产生的有关;且病原菌感染上调了CD14转录和组织蛋白的表达,增加了sCD14的合成[23-24]。
综上所述,血Presepsin对于脓毒症患者血培养阳性的早期预测价值高于PCT,但仅PCT对脓毒症血培养阳性患者不同病原菌感染有鉴别价值,提示在临床实践中两者联合检测可能更有意义。然而,本研究所纳入的样本量偏少,尤其是混合菌和真菌所致的脓毒症患者较少,且试验受采血时间与发病时间等因素影响,研究结果存在一定的偏倚,因此,有待继续收集大样本资料进一步验证。
| [1] | Moore MS, McCarroll MG, McCann CD, et al. Direct screening of blood by PCR and pyrosequencing for a 16S rRNA gene target from emergency department and intensive care unit patients being evaluated for bloodstream infection[J]. J Clin Microbiol, 2016, 54(1): 99-105. DOI:10.1128/jcm.02394-15 |
| [2] | 唐洪影, 岳娜, 田彬, 等. 降钙素原在念珠菌血流感染中的辅助诊断价值[J]. 中华急诊医学杂志, 2018, 27(3): 254-258. DOI:10.3760/cma.j.issn.1671-0282.2018.03.006 |
| [3] | 闫圣涛, 贾红兵, 杨建萍, 等. 降钙素原在革兰阴性菌感染脓毒症诊断中的临床价值[J]. 中华急诊医学杂志, 2017, 26(3): 291-296. DOI:10.3760/cma.j.issn.1671-0282.2017.03.011 |
| [4] | 赵倩, 谢月群, 张涛, 等. 降钙素原对脓毒症患者病情及预后的临床价值[J]. 中华急诊医学杂志, 2016, 25(7): 937-943. DOI:10.3760/cma.j.issn.1671-0282.2016.07.019 |
| [5] | Liu HH, Zhang MW, Guo JB, et al. Procalcitonin and C-reactive protein in early diagnosis of sepsis caused by either Gram-negative or Gram-positive bacteria[J]. Ir J Med Sci, 2017, 186(1): 207-212. DOI:10.1007/s11845-016-1457-z |
| [6] | Leli C, Ferranti M, Moretti A, et al. Procalcitonin levels in gram-positive, gram-negative, and fungal bloodstream infections[J]. Dis Markers, 2015, 2015: 701480. DOI:10.1155/2015/701480 |
| [7] | Watanabe Y, Oikawa N, Hariu M, et al. Ability of procalcitonin to diagnose bacterial infection and bacteria types compared with blood culture findings[J]. Int J Gen Med, 2016, 9: 325-331. DOI:10.2147/IJGM.S115277 |
| [8] | Yaegashi Y, Shirakawa K, Sato N, et al. Evaluation of a newly identified soluble CD14 subtype as a marker for sepsis[J]. J Infect Chemother, 2005, 11(5): 234-238. DOI:10.1007/s10156-005-0400-4 |
| [9] | Ali FT, Ali MA, Elnakeeb MM, et al. Presepsin is an early monitoring biomarker for predicting clinical outcome in patients with sepsis[J]. Clin Chim Acta, 2016, 460: 93-101. DOI:10.1016/j.cca.2016.06.030 |
| [10] | Giavarina D, Carta M. Determination of reference interval for presepsin, an early marker for sepsis[J]. Biochem Med (Zagreb), 2015, 25(1): 64-68. DOI:10.11613/BM.2015.007 |
| [11] | Sargentini V, Ceccarelli G, D' Alessandro M, et al. Presepsin as a potential marker for bacterial infection relapse in critical care patients. A preliminary study[J]. Clin Chem Lab Med, 2015, 53(4): 567-573. DOI:10.1515/cclm-2014-0119 |
| [12] | Shirakawa K, Naitou K, Hirose J, et al. The new sepsis marker, sCD14-ST, induction mechanism in the rabbit sepsis models[J]. Crit Care, 2010, 14(Suppl 2): P19. DOI:10.1186/cc9122 |
| [13] | Vodnik T, Kaljevic G, Tadic T, et al. Presepsin (sCD14-ST) in preoperative diagnosis of abdominal sepsis[J]. Clin Chem Lab Med, 2013, 51(10): 2053-2062. DOI:10.1515/cclm-2013-0061 |
| [14] | 李真玉, 赵华杰, 赵君, 等. 血清presepsin(sCD14-ST)对脓毒症早期诊断价值及预后意义[J]. 中华急诊医学杂志, 2016, 25(7): 896-902. DOI:10.3760/cma.j.issn.1671-0282.2016.07.011 |
| [15] | 全锦花, 杨鲁, 张新超. 血清presepsin(sCD14-ST)联合NEWS评分评估脓毒症预后的价值[J]. 中华急诊医学杂志, 2017, 26(8): 948-952. DOI:10.3760/cma.j.issn.1671-0282.2017.08.024 |
| [16] | Singer M, Deutschman CS, Seymour CW, et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3)[J]. JAMA, 2016, 315(8): 801-810. DOI:10.1001/jama.2016.0287 |
| [17] | Li S, Rong H, Guo Q, et al. Serum procalcitonin levels distinguish Gram-negative bacterial sepsis from Gram-positive bacterial and fungal sepsis[J]. J Res Med Sci, 2016, 21(1): 39. DOI:10.4103/1735-1995.183996 |
| [18] | Okamura Y, Yokoi H. Development of a point-of-care assay system for measurement of presepsin (sCD14-ST)[J]. Clin Chim Acta, 2011, 412(23/24): 2157-2161. DOI:10.1016/j.cca.2011.07.024 |
| [19] | Stubljar D, Skvarc M. Effective strategies for diagnosis of systemic inflammatory response syndrome (SIRS) due to bacterial infection in surgical patients[J]. Infect Disord Drug Targets, 2015, 15(1): 53-56. DOI:10.2174/1871526515666150320161804 |
| [20] | Endo S, Suzuki Y, Takahashi G, et al. Usefulness of presepsin in the diagnosis of sepsis in a multicenter prospective study[J]. J Infect Chemother, 2012, 18(6): 891-897. DOI:10.1007/s10156-012-0435-2 |
| [21] | Arai Y, Mizugishi K, Nonomura K, et al. Phagocytosis by human monocytes is required for the secretion of presepsin[J]. J Infect Chemother, 2015, 21(8): 564-569. DOI:10.1016/j.jiac.2015.04.011 |
| [22] | Nagata T, Yasuda Y, Ando M, et al. Clinical impact of kidney function on presepsin levels[J]. PLoS One, 2015, 10(6): e0129159. DOI:10.1371/journal.pone.0129159 |
| [23] | Pan Z, Zhou L, Hetherington CJ, et al. Hepatocytes contribute to soluble CD14 production, and CD14 expression is differentially regulated in hepatocytes and monocytes[J]. J Biol Chem, 2000, 275(46): 36430-36435. DOI:10.1074/jbc.M003192200 |
| [24] | Liu S, Khemlani LS, Shapiro RA, et al. Expression of CD14 by hepatocytes: upregulation by cytokines during endotoxemia[J]. Infect Immun, 1998, 66(11): 5089-5098. DOI:10.1007/BF02770849 |
 2019, Vol. 28
2019, Vol. 28




