脓毒症是指宿主对感染的反应失调而致的危及生命的器官功能障碍[1],若病情进一步进展,可发展为多器官功能障碍综合征。该病是重症监护病房发病率和病死率的主要原因之一。有数据显示其约占ICU中急危重症总患病率的11 %,且以每年8 % ~13 %的速度递增[2]。调查显示,国内外科重症监护病房的脓毒症发病率为8.68%,住院期间病死率为48.7%[3]。心脏损伤是脓毒症中严重并发症之一[4],大约有40%~50%的脓毒症患者出现心功能不全,其中出现心力衰竭者占7%[5],脓毒症一旦合并心肌损伤可加重疾病的演变过程,增加多脏器衰竭及死亡风险[6]。本研究以脓毒症患者作为研究对象,前瞻性分析脓毒症并发心肌损伤患者的临床特征,探讨脓毒症患者发生心肌损伤的危险因素,为脓毒症合并心肌损伤患者的诊治提供临床依据。
1 资料与方法 1.1 一般资料前瞻性收集北京市友谊医院急诊科2016年4月至2017年12月住院的160例脓毒症患者。入选标准均符合2016年美国重症医学会与欧洲重症医学会联合发布的脓毒症3.0定义及诊断标准:脓毒症相关的序贯器官功能衰竭评分(sequential organ failure assessment,SOFA)急性改变≥2分,即“脓毒症=感染+SOFA≥2分[1]。排除标准:既往基础心脏病史(冠心病史、心肌病史、瓣膜性心脏病史、先天性心脏病史、心律失常病史)、急性冠脉综合征、严重心力衰竭、心胸外科手术、胸外按压、除颤、直流电复律、肝肾功能不全、肿瘤或自身免疫性疾病、妊娠。入院诊断包括急性胆管炎、急性胰腺炎、胆囊炎、肺炎、慢性阻塞性肺疾病、肝脓肿、泌尿系统感染等基础疾病合并脓毒症。
1.2 分组根据是否存在心肌损伤分为非心肌损伤组和心肌损伤组。心肌损伤定义为采用PATHFAST化学发光免疫分析检测的血清肌钙蛋白Ⅰ(cTnI)高于正常(≥ 0.04 ng/mL)[7-8]。
1.3 监测指标及方法(1)记录入选患者性别、年龄、呼吸、心率、血压。(2)入院第1天、第3天及第7天进行血清cTNT(AQT90,FLEX免疫分析仪)、cTNI(PATHFAST化学发光免疫分析仪)、NT-proBNP(雅培i2000全自动免疫分析仪)全定量检测。(3)入院72 h内完成超声心动图检查(飞利浦iE33),测定左室舒张末内径(EDD)、左室收缩末内径(ESD)、左室舒张末期容积(EDV)、左室收缩末期容积(ESV)、每搏输出量(SV)、左室射血分数(LVEF)、左心室短轴缩短指数(FS)、室间隔(IVS)厚度、IVS振幅、舒张末期左室后壁(LVPW)厚度、LVPW振幅、右室(RV)内径、二尖瓣口舒张早期最大流速与心房收缩期最大流速比值(E/A)等指标。
1.4 统计学方法采用SPSS16.0统计分析软件,两组间计数资料的比较应用χ2检验;两组间计量资料以均数±标准差(Mean±SD)表示,若为正态分布变量应用成组t检验,若为非正态分布变量,应用非参数检验中的秩和检验。组间随时间动态变化比较采用重复测量方差分析。应用二元Logistic回归分析脓毒症并发心肌损伤的独立危险因素。所有检验的显著性均为双侧并以P值表示,以P < 0.05为差异有统计学意义。
2 结果 2.1 脓毒症非心肌损伤与心肌损伤患者临床资料比较纳入160例脓毒症患者,其中心肌损伤患者75例(46.9%),非心肌损伤患者85例(53.1%)。男性97例,女性63例,年龄(68±15)岁。心肌损伤组年龄高于非心肌损伤组(P=0.001)。相较于非心肌损伤组,心肌损伤者多合并既往高血压病史(P=0.015)。28 d死亡3例(1.9%)。见表 1。
| 指标 | 非心肌损伤组 (n=75) |
心肌损伤组 (n=85) |
t/χ2值 | P值 |
| 年龄(岁) | 64±15 | 72±13 | -3.603 | < 0.01 |
| 性别[例%)] | 0.227 | 0.634 | ||
| 男 | 53(62.4) | 44(58.7) | ||
| 女 | 32(37.6) | 31(41.3) | ||
| 高血压病史[例(%)] | 38(44.7) | 48(64) | 5.967 | 0.015 |
| 死亡[例(%)] | 0(0) | 3(4) | 0.101 |
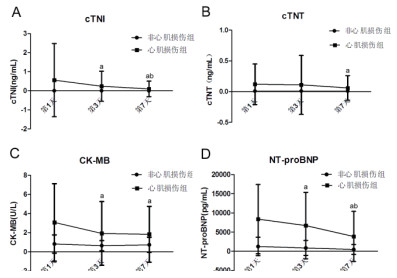
与非心肌损伤组相比,心肌损伤组cTNT[(0.01±0.023) ng/mL vs (0.10±0.025) ng/mL, F=10.300, P=0.002)、cTNI[(0.005±0.07) ng/mL vs (0.30±0.08) ng/mL, F=7.708, P=0.006]、CK-MB[(0.745±0.251)U/L vs (2.286±0.265) U/L, F=68.781, P < 0.01]、NT-ProBNP[(851.370±799.831) pg/mL vs (6 318±840.874) pg/mL, F=38.161, P=0.000]明显升高,并随时间逐渐减低(图 1)。
|
| 与第1天比较,aP < 0.05;与第3天比较,bP < 0.05 图 1 脓毒症时两组cTNT、cTNI、NTproBNP随时间变化 Fig 1 Changes of cTNT, cTNI and NTproBNP with time in two groups in sepsis |
|
|
脓毒症患者心功能障碍以舒张功能障碍为主:160例脓毒症患者,心功能障碍者113例(86.9%),其中舒张功能障碍者106例(84.1%),收缩功能障碍6例(4.3%),室壁运动异常者24例(17.3%)。与非心肌损伤组相比,心肌损伤组更易出现室壁运动异常(9.6% vs 25.8%, P=0.012)、IVS振幅[(0.87±0.16) cm vs (0.80±0.21) cm, P=0.03]、LVPW振幅更低[(1.03±0.21) cm vs (0.96±0.18) cm, P=0.034]、FS更低(P=0.033)。心肌损伤组SV可能低于非心肌损伤组(P=0.054)。两组间EDD、ESD、EDV、ESV、SV、IVS厚度、LVPW厚度、RV、LA、EF、E/A差异无统计学意义。Logistic回归分析显示FS(P=0.015)和SV(P=0.035)为心肌损伤的独立危险因素。
2.4 脓毒症并发心肌损伤的独立危险因素s将上述两组间有统计学意义的指标:年龄、既往高血压病史、FS、SV纳入Logistic回归模型,分析显示年龄大、FS减低为脓毒症并发心肌损伤的独立危险因素(P < 0.05), 见表 2。
| 指标 | B值 | RR值 | 95%可信区间 | P值 |
| 年龄 | 0.032 | 1.033 | 1.006-1.061 | 0.018 |
| 既往高血压 | 0.451 | 1.570 | 0.737-3.344 | 0.243 |
| FS | -9.131 | 0.000 | 0.000-0.309 | 0.024 |
| SV | -0.025 | 0.975 | 0.949-1.001 | 0.061 |
| 注:左心室短轴缩短指数(FS);每搏输出量(SV) | ||||
cTnI浓度增高,不仅可反映缺血性心脏疾病,而且可反映脓毒症等非心源性疾病心肌功能障碍[9]。在内毒素感染后1 h就可出现cTnI升高的现象,提示脓毒症早期就可存在心肌损伤[10-11]。研究发现1 124例脓毒症患者中,673例患者(60%)在脓毒症第1天hs-cTnI浓度升高,755例(67%)患者在脓毒症发生4 d内升高[12]。Cox回归分析显示hs-cTnI浓度升高与脓毒症14 d病死率升高密切相关。此外hs-cTnI浓度升高与200例生存者的心血管事件的发生密切相关。因此,心肌损伤发生于多数脓毒症患者中,并与早期病死率而非晚期病死率独立相关,并与出院后心血管事件的发生率显著相关。故本研究以cTnI浓度升高作为脓毒症早期心肌损伤的标志物,发现脓毒症患者中发生心肌损伤者占46.9%,与Frencken等[12]研究结果相似。本研究脓毒症患者28 d病死率较低,原因可能是①排除了所有影响TNI升高的基础疾病和合并症,如排除了既往基础心脏病史(冠心病史、心肌病史、瓣膜性心脏病史、先天性心脏病史、心律失常病史)、急性冠脉综合征、严重心力衰竭、肝肾功能不全等。②本研究纳入脓毒症患者病因中以急性化脓性胆管炎最多,本院因开通急诊内镜逆行胰胆管造影+内镜下鼻胆汁引流术,可及时解除胆道梗阻,故脓毒症病死率明显减低。
脓毒症可导致可逆性心肌功能障碍,这一现象在临床上称脓毒性心肌病[13]。Parker等[14]首次发现脓毒症患者中发生了可逆性心肌功能障碍。主要有3个特点:(1)射血分数降低,大多数临床研究以LVEF≤0.50作为诊断标准;(2)左心室扩张;(3)可在疾病控制早期恢复正常,存在可逆性。然而,近年来,随着血流动力学监测和心脏超声技术的发展,研究者发现脓毒症心肌损伤可表现为不同类型的心功能障碍,如左室舒张功能障碍、左室收缩功能障碍和右室功能障碍,且不同类型的心功能障碍可互相并存[15-16]。Pulido等[17]在106例严重脓毒症或脓毒性休克患者中,采用经胸壁心脏超声评价不同心功能障碍对病死率影响,结果发现68例(64%)患者存在心功能不全,其中,存在左室舒张功能不全、左室收缩功能不全和右室功能不全的患者分别为39例(37%)、29例(27%)和33例(31%),提示左室舒张功能障碍所占比例最高。相比较收缩功能障碍患者,脓毒症心脏舒张功能障碍患者对液体治疗反应性差,其病死率增加。本研究与Pulido等研究结果一致,脓毒症患者中86.9%出现心功能障碍,其中以舒张功能障碍为主,占84.1%,收缩功能障碍者占4.3%,室壁运动异常者占17.3%。但此处是对本实验脓毒症患者心功能的描述性资料,并未对脓毒症与非脓毒症患者的心功能进行统计分析,受年龄、既往高血压病等多种因素影响,故本研究以cTnI高于正常(≥ 0.04 ng/ml)界定脓毒症心肌损伤[7-8]。FS是目前临床常用的评价心脏收缩功能的超声指标。韩斌等[18]研究显示脓毒症组、严重脓毒症组、脓毒性休克组患者FS减低,患者FS与APACHEⅡ评分、BNP及cTnI水平呈负相关。提示FS减低与脓毒症严重度及心肌损伤程度明显相关。刘安雷等[19]动物实验显示,与对照组比较,脓毒症小鼠每搏输出量明显下降、心肌细胞发生凋亡。张娈娈等[20]研究亦发现,与脓毒症心功能正常患者比较,心功能障碍患者SV明显减低。本研究显示,与脓毒症非心肌损伤患者相比,Logistic回归分析显示年龄和FS减低为脓毒症心肌损伤的独立危险因素。
综上所述,脓毒症时以舒张功能障碍为主,同时存在收缩功能障碍。脓毒症合并心肌损伤患者多为年龄大者、既往合并高血压者,超声心动图表现为SV和FS减低。
| [1] | Singer M, Deutschman CS, Seymour CW, et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3)[J]. JAMA, 2016, 315(8): 801-810. DOI:10.1001/jama.2016.0287 |
| [2] | Deutschman CS, Tracey KJ. Sepsis:current dogma and new perspectives[J]. Immunity, 2014, 40: 463-475. DOI:10.1016/j.immuni.2014.04.001 |
| [3] | Levy MM, Dellinger RP, Townsend SR, et al. The Surviving Sepsis Campaign:results of an international guidelinebased performance improvement program targeting severe sepsis[J]. Intensive Care Med, 2010, 36(2): 222-231. DOI:10.1007/s00134-009-1738-3 |
| [4] | Rudiger A, Singer M. Mechanisms of sepsis induced cardiac dysfunction[J]. Crit Care Med, 2007, 35(6): 1599-1608. DOI:10.1097/01.CCM.0000266683.64081.02 |
| [5] | Esper AM, Martin GS. Extending international sepsis epidemiology:the impact of organ dysfunction[J]. Crit Care, 2009, 13(1): 120. DOI:10.1186/cc7704 |
| [6] | 彭娜, 向定成, 苏磊. 活性氧与脓毒症心肌损伤[J]. 中华急诊医学杂志, 2010, 19(3): 329-331. DOI:10.3760/cma.j.issn.1671-0282.2010.03.037 |
| [7] | 胡雪珍, 卢中秋, 李志涛, 等. 黄芪注射液对脓毒症患者心肌损伤干预作用的观察[J]. 中国中西医结合急救杂志, 2010, 17(6): 346-348. DOI:10.3969/j.issn.1008-9691.2010.06.009 |
| [8] | Huang S, Peng WP, Yang N, et al. Myocardial injury in elderly patients after abdominal surgery[J]. Aging Clin Exp Res, 2018, 30(10): 1217-1223. DOI:10.1007/s40520-018-0908-y |
| [9] | Favory R, Neviere R. Bench-to-bedside review:Significance and interpretation of elevated tmponin in septic patients[J]. Crit Care, 2006, 10(4): 1-6. DOI:10.1186/cc4991 |
| [10] | 邝巧芬. 小儿脓毒症心肌损伤的临床治疗分析[J]. 中国医药指南, 2013, 11(2): 163-164. DOI:10.3969/j.issn.1671-8194.2013.02.127 |
| [11] | 潘小进, 孙华. 兔脓毒症早期心肌功能的变化[J]. 中国危重病急救医学, 2004, 16(6): 355-357. DOI:10.3760/j.issn:1003-0603.2004.06.009 |
| [12] | Frencken JF, Donker DW, Spitoni C, et al. Myocardial injury in patients with sepsis and its association with long-term outcome[J]. Circ Cardiovasc Qual Outcomes, 2018, 11(2): e004040. DOI:10.1161/CIRCOUTCOMES.117.004040 |
| [13] | Sato R, Nasu M. A review of sepsis-induced cardiomyopathy[J]. J Intensive Care, 2015, 3(1): 48. DOI:10.1186/s40560-015-0112-5 |
| [14] | Parker MM. Profound but reversible myocardial depression in patients with septic shock[J]. Ann Intern Med, 1984, 100(4): 483-490. DOI:10.7326/0003-4819-100-4-483 |
| [15] | Zaky A, Deem S, Bendjelid K, et al. Characterization of cardiac dysfunction in sepsis:An ongoing challenge[J]. Shock, 2014, 41(1): 12-24. DOI:10.1097/SHK.0000000000000065 |
| [16] | Antonucci E, Fiaccadori E, Donadello K, et al. Myocardial depression in sepsis:From pathogenesis to clinical manifestations and treatment[J]. J Crit Care, 2014, 29(4): 500-511. DOI:10.1016/j.jcrc.2014.03.028 |
| [17] | Pulido JN, Afessa B, Masaki M, et al. Clinical spectrum, frequency, and significance of myocardial dysfunction in severe sepsis and septic shock[J]. Mayo Clin Proc, 2012, 87(7): 620-628. DOI:10.1016/j.mayocp.2012.01.018 |
| [18] | 韩斌, 郑文香, 曹新河, 等. 超声心动图联合HbA1c和MOP检测对脓毒症心肌损伤风险的评估价值[J]. 河北医药, 2017, 39(21): 3239-3243. DOI:10.3969/j.issn.1002-7386.2017.21.010 |
| [19] | 刘安雷, 刘洁, 张天鹏, 等. 血管再生在小鼠脓毒症心肌损伤中的作用[J]. 中华急诊医学杂志, 2011, 20(12): 1295-1299. DOI:10.3760/cma.j.issn.1671-0282.2011.12.018 |
| [20] | 张娈娈, 王奇坤, 陈德, 等. 脓毒症患者血浆可溶性晚期糖基化终末产物受体水平与心功能的关系[J]. 中国循环杂志, 2016, 31(1): 73-76. DOI:10.3969/j.issn.1000-3614.2016.01.016 |
 2019, Vol. 28
2019, Vol. 28




