2 北京市心肺脑复苏重点实验室
2
脓毒症在重症监护病房(ICU)和急诊科极为常见,因其发病率、死亡率高且呈上逐年升趋势,被认为是重症医学所面临的棘手难题,快速、早期诊断、治疗尤为重要[1-2]。脓毒症主要侵犯血管内皮系统,微血管内皮是脓毒症的主要靶点,特点是血管微循环功能障碍。脓毒症的病理生理过程可分为血管内皮细胞功能障碍和高凝状态导致的血栓形成两部分,病程的进展可以用内皮细胞的损伤、微血栓形成的程度间接反映,内皮细胞在脓毒症及其导致的多脏器功能障碍综合征(multiple organ dysfunction syndrome, MODS)中担任了重要的角色。因此探讨血管内皮标记物对脓毒症危险分层及病情评估有重要意义[3]。
人内皮细胞特异性分子-1[3-4](endothelial cell specific molecule-1,endocan)、血管性血友病因子[5-7](von Willebrand factor, vWF)、含Ⅰ型血小板结合蛋白基序的解聚蛋白样金属蛋白酶[6-9](A disintegrin-like and metalloprotease with thrombospondin type 1 motif,ADAMTS-13)均是血管内皮细胞受损和功能障碍的标记物。本研究通过急诊抢救室脓毒症患者循环endocan,vWF,ADAMTS-13及vWF/ADAMTS-13水平的研究,明确这些指标与脓毒症疾病严重程度的关系,进一步阐明内皮细胞标记物作为脓毒症生物标记物的应用价值。
1 资料与方法 1.1 一般资料入选标准:北京朝阳医院急诊抢救室自2014年10月到2015年10月符合2001年华盛顿脓毒症定义会议制定的标准[10]的SIRS或脓毒症诊断患者301例。根据诊断标准分为SIRS组,脓毒症组,严重脓毒症组和脓毒症休克组。选择同期在北京朝阳医院体检中心的健康体检者40例作为健康对照组。
排除标准包括:年龄不满18周岁,患者或家属不同意参与研究,患有精神疾病者,肿瘤患者,脏器移植术后或长期服用免疫抑制剂者,存在过敏反应者,在此次发病前已明确有两个或两个以上脏器功能不全者。本研究通过北京朝阳医院伦理委员会的批准,所有参与者(或其亲属)均签署知情同意书。
1.2 检测方法在病例入选即刻及入选第5天各抽取肘静脉血4 mL,置于不含添加剂的血清管中,使用微量高速离心机在4 000 r/min的速度下离心5 min,以一次性移液吸管取出血清,置于1.5 mL普通离心管中,在-80℃低温保存箱冷冻保存备检测。使用ELISA试剂盒应用双抗体夹心法测定:endocan(美国Cloud-Clone Corp,SEC463Hu)、vWF(美国Cloud-Clone Corp,CEA833Hu)、ADAMTS-13(美国Cloud-Clone Corp,SEA950Hu)。PCT使用美国Mini VIDAS全自动免疫分析仪(Block Scientific,Inc.美国纽约)检测。记录患者的既往病史,生命体征,常规化验及影像学检查等。使用入选时数据进行APACHEⅡ评分[11]、MEDS评分[12]和SOFA评分[13]。以患者入选第28天的转归情况作为研究终点。在随访时间点患者因各种原因死亡的定义为死亡病例,未死亡者转归定义为存活病例。
1.3 数据处理和统计分析方法所有数据使用SPSS 19.0统计软件处理,正态数据采用均值±标准差(Mean±SD)表示,非正态数据采用中位数(25%~75%分位数)表示。两组以上正态分布的计量资料的均值比较使用单因素方差分析(One-way ANOVA),组间两两比较采用LSD方法。非正态分布的计量资料的均值比较采用非参数检验的Kruskal-Wallis方法,组间两两比较采用非参数检验的Mann-Whitney U方法,计数资料的比较采用χ2检验,以P < 0.05为差异有统计学意义。
2 结果 2.1 入选病例一般情况入选病例的年龄、性别比例、既往疾病以及感染部位在各组患者之间差异无统计学意义。28 d病死率、PCT、MEDS评分、APACHEⅡ评分、SOFA评分在脓毒症、严重脓毒症、脓毒症休克患者逐级增高,各组间的差异有统计学意义(P < 0.01)。见表 1。
| 指标 | 对照组 | SIRS | 脓毒症 | 严重脓毒症 | 脓毒症休克 | P值 |
| 病例数 | 40 | 40 | 77 | 132 | 52 | |
| 年龄(岁) | 66.5 (26~82) | 65(14~85) | 65(20~93) | 69(26~90) | 67(23~94) | 0.602 |
| 男性(%) | 55.0 | 63.6 | 55.8 | 61.4 | 65.4 | 0.758 |
| 入院时主要感染部位(例,%) | ||||||
| 肺 | 54(70.1) | 88(66.7) | 36(69.2) | 0.860 | ||
| 腹腔 | 3(3.9) | 6(4.5) | 4(7.7) | 0.650 | ||
| 泌尿系统 | 1(1.3) | 7(5.3) | 2(3.8) | 0.430 | ||
| 胃肠道 | 7(9.1) | 7(5.3) | 2(3.8) | 0.486 | ||
| 皮肤软组织 | 2(2.6) | 5(3.8) | 3(5.8) | 0.635 | ||
| 中枢系统 | 3(3.9) | 5(3.8) | 1(1.9) | 0.911 | ||
| 肝胆系统 | 7(9.1) | 14(10.6) | 4(7.7) | 0.821 | ||
| 既往史(例,%) | ||||||
| COPD | 12(30.0) | 27(35.1) | 51(38.6) | 16(30.8) | 0.658 | |
| 心血管疾病 | 13(32.5) | 29(37.7) | 53(40.2) | 17(32.7) | 0.659 | |
| 脑血管疾病 | 9(22.5) | 19(24.7) | 39(29.6) | 20(38.4) | 0.283 | |
| 糖尿病 | 11(27.5) | 27(35.1) | 49(37.1) | 21(40.4) | 0.617 | |
| 其他 | 4(10.0) | 12(15.6) | 25(18.9) | 10(19.2) | 0.564 | |
| 28天病死率(%) | 2.5 | 20.8 | 32.6 | 69.2 | < 0.01 | |
| PCT(ng/L) | 0.05(0.05~0.43) | 2.59(0.41~5.09) | 3.97(1.04~8.06) | 9.27(6.84~13.30) | < 0.01 | |
| MEDS评分 | 8.0(5.5~10.5) | 9.0(7.0-11.0) | 11.0(8.0-14.0) | 14.5(12.0~16.0) | < 0.01 | |
| APACHEⅡ评分 | 9.1±3.6 | 12.0±5.2 | 16.2±6.6 | 22.9±6.7 | < 0.01 | |
| SOFA评分 | 2.0(1.0~2.5) | 3.0(2.0~6.0) | 7.5(5.0~9.0) | 11.0(10.0~14.0) | < 0.01 | |
| 注:COPD,慢性阻塞性肺疾病;PCT,降钙素原;MEDS,急诊脓毒症死亡风险;APACHEⅡ,急性生理学和慢性健康状况;SOFA,序贯性器官功能衰竭评估 | ||||||
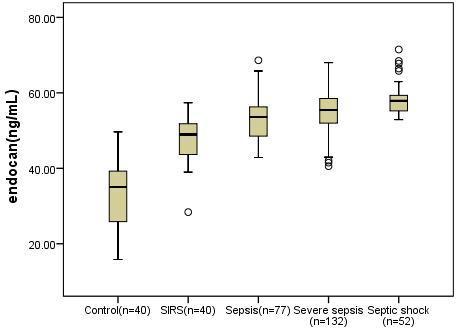
endocan,vWF,vWF/ADAMTS-13入院即刻的平均水平在健康对照组、SIRS、脓毒症、严重脓毒症和脓毒症休克的患者中呈逐渐增高的趋势,ADAMTS-13则呈逐渐降低趋势,各组间的差异具有统计学意义(P < 0.05),见表 2,图 1~4。
|
| 图 1 endocan的中位数水平在各组间的比较 Fig 1 Comparison of median levels of endocan among groups |
|
|
|
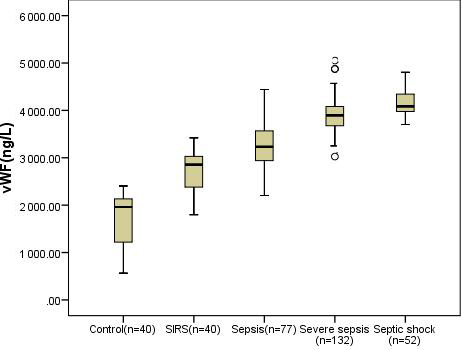
| 图 2 vWF的中位数水平在各组间的比较 Fig 2 Comparison of median levels of vWF among groups |
|
|
|
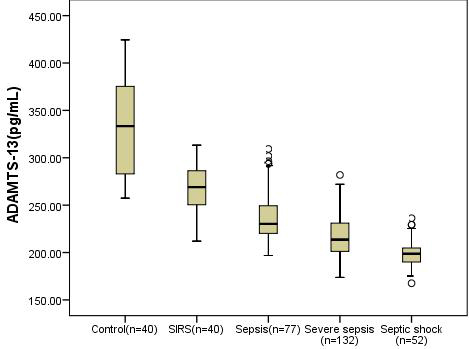
| 图 3 ADAMTS-13的中位数水平在各组间的比较 Fig 3 Comparison of median levels of ADAMTS-13 among groups |
|
|
|
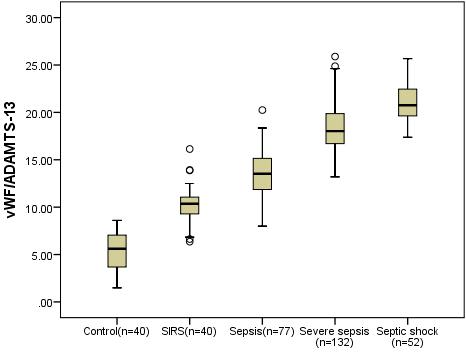
| 图 4 vWF/ADAMTS-13的中位数水平在各组间的比较 Fig 4 Comparison of median levels of vWF/ADAMTS-13 among groups |
|
|
| 指标 | 对照组 | SIRS | 脓毒症 | 严重脓毒症 | 脓毒症休克 | P值 |
| 病例数(n) | 40 | 40 | 77 | 132 | 52 | |
| endocan | ||||||
| (ng/mL) | 32.53±9.13 | 47.31±6.11 | 52.86±5.17 | 54.99±5.28a | 58.25±4.08 | < 0.001 |
| vWF(ng/L) | 1 729.49±565.60 | 2 736.22±436.98 | 3 199.17±425.61 | 3 909.27±334.02 | 4 161.97±275.65 | < 0.001 |
| ADAMTS-13 | ||||||
| (pg/mL) | 328.06±49.22 | 268.33±24.64 | 238.38±25.96 | 215.44±21.89 | 199.10±14.66 | < 0.001 |
| vWF/ADAMTS13 | 5.43±2.06 | 10.32±2.14 | 13.59±2.40 | 18.34±2.54 | 21.01±2.01 | < 0.001 |
| 注:与脓毒症组比较,aP < 0.05;endocan,人内皮细胞特异性分子-1;vWF,血管性血友病因子;ADAMTS-13,含Ⅰ型血小板结合蛋白基序的解聚蛋白样金属蛋白酶 | ||||||
endocan、vWF、vWF/ADAMTS-13在SIRS、脓毒症、严重脓毒症组,第5天水平较第1天明显下降(P < 0.05),在脓毒症休克组第5天水平较第1天明显升高(P < 0.05)。ADAMTS-13在SIRS、脓毒症、严重脓毒症组,第5天水平较第1天明显升高(P < 0.01),在脓毒症休克组第5天水平较第1天显著下降(P < 0.01),见表 3。
| 指标 | 第1天 | 第5天 | P值 |
| endocan (ng/mL) | |||
| SIRS组 | 47.31±6.11 | 42.96±5.67 | < 0.01 |
| 脓毒症组 | 52.86±5.17 | 45.74±6.65 | < 0.01 |
| 严重脓毒症组 | 54.99±5.28 | 49.02±6.53 | < 0.01 |
| 脓毒症休克组 | 58.25±4.08 | 63.41±5.44 | < 0.01 |
| vWF (ng/L) | |||
| SIRS组 | 2 736.22±436.98 | 2 643.86±395.78 | 0.012 |
| 脓毒症组 | 3 199.17±425.61 | 3 106.88±461.60 | 0.01 |
| 严重脓毒症组 | 3 909.27±334.02 | 3 744.34±388.40 | < 0.01 |
| 脓毒症休克组 | 4 161.97±275.65 | 4 248.11±368.07 | 0.02 |
| ADAMTS-13 (pg/mL) | |||
| SIRS组 | 268.33±24.64 | 280.05±24.01 | 0.007 |
| 脓毒症组 | 238.38±25.96 | 254.29±35.60 | < 0.01 |
| 严重脓毒症组 | 215.44±21.89 | 222.64±23.39 | < 0.01 |
| 脓毒症休克组 | 199.10±14.66 | 191.50±18.47 | 0.03 |
| vWF/ADAMTS-13 | |||
| SIRS组 | 10.32±2.14 | 9.53±1.74 | < 0.01 |
| 脓毒症组 | 13.59±2.40 | 12.55±3.08 | < 0.01 |
| 严重脓毒症组 | 18.34±2.54 | 17.04±2.87 | < 0.01 |
| 脓毒症休克组 | 21.01±2.01 | 22.45±3.34 | < 0.01 |
| 注:endocan,人内皮细胞特异性分子-1;vWF,血管性血友病因子;ADAMTS-13,含Ⅰ型血小板结合蛋白基序的解聚蛋白样金属蛋白酶;SIRS,全身炎症反应综合征 | |||
按入院时是否出现MODS分为MODS组及非MODS组;按入院时是否MEDS评分≥13分为两组。endocan、vWF、vWF/ADAMTS-13第1天、第5天水平在MODS组较非MODS组明显升高(P < 0.01),在MEDS≥13组较MEDS < 13组明显升高(P < 0.01),而ADAMTS-13在上述两组比较中呈明显减低趋势(P < 0.01)。endocan、vWF、vWF/ADAMTS-13在非MODS及MEDS < 13组第5天较第1天显著降低(P < 0.01),ADAMTS-13则显著升高(P < 0.01)。而在MODS组及MEDS≥13组,各指标第1天和第5天比较差异无统计学意义(P > 0.05),见表 4、5。
| 指标 | 非MODS组 | MODS组 | P值 |
| 病例数(n) | n=192 | n=109 | |
| endocan (ng/mL) | |||
| 第1天 | 52.89±6.21 | 56.49±4.63 | < 0.01 |
| 第5天 | 46.17±6.66 | 57.17±8.55 | < 0.01 |
| P值 | < 0.01 | 0.405 | |
| vWF (ng/L) | |||
| 第1天 | 3 409.88±585.76 | 4 056.23±326.51 | < 0.01 |
| 第5天 | 3 286.11±581.84 | 4 019.26±444.10 | < 0.01 |
| P值 | < 0.001 | 0.216 | |
| ADAMTS-13 (pg/mL) | |||
| 第1天 | 233.52±30.48 | 207.75±21.25 | < 0.01 |
| 第5天 | 245.56±35.42 | 206.47±27.01 | < 0.01 |
| P值 | < 0.01 | 0.532 | |
| vWF/ADAMTS-13 | |||
| 第1天 | 15.01±3.86 | 19.74±2.66 | < 0.01 |
| 第5天 | 13.86±3.92 | 19.92±4.08 | < 0.01 |
| P值 | < 0.01 | 0.530 | |
| 注:endocan,人内皮细胞特异性分子-1;vWF,血管性血友病因子;ADAMTS-13,含Ⅰ型血小板结合蛋白基序的解聚蛋白样金属蛋白酶;MODS,多脏器功能障碍综合征 | |||
| 指标 | MEDS < 13 | MEDS ≥13 | P |
| 病例数(n) | n=207 | n=94 | |
| endocan (ng/mL) | |||
| 第1天 | 53.34±6.37 | 55.87±4.49 | < 0.01 |
| 第5天 | 46.63±6.81 | 57.25±9.02 | < 0.01 |
| P值 | < 0.01 | 0.075 | |
| vWF (ng/L) | |||
| 第1天 | 3 490.82±573.84 | 3 945.89±521.06 | < 0.01 |
| 第5天 | 3 361.74±575.56 | 3 928.54±604.12 | < 0.01 |
| P值 | < 0.01 | 0.558 | |
| ADAMTS-13 (pg/mL) | |||
| 第1天 | 230.48±30.96 | 211.77±24.08 | < 0.01 |
| 第5天 | 242.63±35.41 | 208.97±31.63 | < 0.01 |
| P值 | < 0.01 | 0.208 | |
| vWF/ADAMTS-13 | |||
| 第1天 | 15.59±3.92 | 18.97±3.67 | < 0.01 |
| 第5天 | 14.35±3.98 | 19.45±4.93 | < 0.01 |
| P值 | < 0.01 | 0.099 | |
| 注:endocan,人内皮细胞特异性分子-1;vWF,血管性血友病因子;ADAMTS-13,含Ⅰ型血小板结合蛋白基序的解聚蛋白样金属蛋白酶;MED评分,急诊脓毒症死亡风险 | |||
endocan、vWF、vWF/ ADAMTS-13第1天及第5天死亡患者显著高于存活患者(P < 0.01),ADAMTS-13第1天及第5天则死亡患者较存活患者明显降低,组间差异有统计学意义(P < 0.01)。endocan、vWF、vWF/ADAMTS-13水平在存活组第5天较第1天显著降低(P < 0.01),ADAMTS-13则显著升高(P < 0.01)。而死亡组endocan、vWF、vWF/ADAMTS-13水平第5天较第1天显著升高(P < 0.05),ADAMTS-13则显著降低(P < 0.01)。见表 6。
| 指标 | 存活组 | 死亡组 | P值 |
| 病例数(n) | n=205 | n=96 | |
| endocan (ng/mL) | |||
| 第1天 | 53.14±6.55 | 56.22±3.71 | < 0.01 |
| 第5天 | 46.29±6.84 | 57.73±8.16 | < 0.01 |
| P值 | < 0.01 | 0.049 | |
| vWF (ng/L) | |||
| 第1天 | 3 476.83±586.27 | 3965.26±468.88 | < 0.01 |
| 第5天 | 3 296.10±557.98 | 4052.11±482.55 | < 0.01 |
| P值 | < 0.01 | 0.002 | |
| ADAMTS-13 (pg/mL) | |||
| 第1天 | 233.05±31.03 | 206.86±18.64 | < 0.01 |
| 第5天 | 247.32±33.91 | 199.99±21.45 | < 0.01 |
| P值 | < 0.01 | < 0.01 | |
| vWF/ADAMTS-13 | |||
| 第1天 | 15.35±3.90 | 19.39±3.22 | < 0.01 |
| 第5天 | 13.73±3.60 | 20.61±3.93 | < 0.01 |
| P值 | < 0.01 | < 0.01 | |
| 注:endocan,人内皮细胞特异性分子-1;vWF,血管性血友病因子;ADAMTS-13,含Ⅰ型血小板结合蛋白基序的解聚蛋白样金属蛋白酶 | |||
endocan、vWF、vWF/ADAMTS-13与MEDS评分、APACHEⅡ评分和SOFA评分之间均具有显著的正相关(P < 0.01),ADAMTS-13与各评分系统之间具有显著的负相关(P < 0.01)。相关系数见表 7。
| 指标 | endocan | vWF | vWF/ADAMTS-13 | ADAMTS-13 |
| MEDS | 0.264 | 0.378 | 0.403 | -0.332 |
| APACHEⅡ | 0.330 | 0.445 | 0.489 | -0.407 |
| SOFA | 0.400 | 0.642 | 0.675 | -0.548 |
| 注:endocan,人内皮细胞特异性分子-1;vWF,血管性血友病因子;ADAMTS-13,含Ⅰ型血小板结合蛋白基序的解聚蛋白样金属蛋白酶;MEDS,急诊脓毒症死亡风险;APACHE,急性生理学和慢性健康状况;SOFA,序贯性器官功能衰竭评估 | ||||
脓毒症是危重症患者的重要死因之一,已有的研究表明严重脓毒症和脓毒症休克患者病死率高达20%~54%[11, 14-17],每年脓毒症患者的死亡率仍在增加,且每当延迟1 h适当的抗生素治疗,病死率即增加5%~10%[18-19],因此脓毒症的早期诊断和早期治疗尤为重要。生物学标记物可以增加判断感染存在的准确性,并且有利于监测感染进程,在缺乏典型临床症状的情况下,能客观地反应疾病的严重程度,并可监测疾病的病理生理过程及对治疗干预的反应[20]。
脓毒症发生发展过程中全身血管内皮系统受到损伤,为主要靶点。内皮细胞的损伤及微血栓形成的程度能够间接反映机体循环衰竭程度。因此本研究选择endocan、vWF、ADAMTS-13这三个反映内皮细胞功能的生物标记物,并引入vWF/ADAMTS-13的比值,深入探讨其对脓毒症患者病情评估的重要价值。它们通过静脉血检测在临床工作中能够简单、快捷地获取,可多次反复检测并根据数值变化趋势以预测病情发展。能够直接体现内皮功能变化进而反映循环功能变化。
目前在临床上还有较多指标可用于脓毒症微循环障碍的评估, 如动脉血乳酸,虽能够反映组织缺氧和无氧代谢水平,但受到局部及全身缺氧状况、机体代谢乳酸的能力及线粒体功能的影响,并不能直接反映微循环障碍。此外通过混合静脉血氧饱和度、中心静脉血氧饱和度、胃肠道PCO2检测等间接反映微循环状况的方法,由于其操作复杂,未能在临床上广泛使用。因此,选择endocan、vWF、ADAMTS-13这三个直接体现内皮功能的指标进行研究可能更为有效。
本研究数据表明,endocan、vWF、vWF/ADAMTS-13的水平在健康对照组、SIRS组、脓毒症组、严重脓毒症组、脓毒症休克组呈逐级增高的趋势,ADAMTS-13则在各组呈逐级降低趋势,且差异有统计学意义,表明其具有一定的危险分层意义。即病情越重,endocan、vWF、vWF/ADAMTS-13水平越高,ADAMTS-13水平越低。随着脓毒症严重程度的增高,血管内皮损伤增重,内皮功能越加活跃,既而出现MODS,因此各标记物不但是疾病严重程度的标志,也是器官功能障碍和预后不良的独立指标[21]。
第1天与第5天均值比较,endocan、vWF、vWF/ADAMTS-13在SIRS、脓毒症、严重脓毒症组,第5天水平较第1天明显下降,在脓毒症休克组第5天水平较第1天明显升高。ADAMTS-13在SIRS、脓毒症、严重脓毒症组,第5天水平较第1天明显升高,在脓毒症休克组第5天水平较第1天显著下降。可以看出在病情较轻或病情可逆程度较大的分组,经过4 d治疗,endocan、vWF、vWF/ADAMTS-13水平较第1天有下降趋势,ADAMTS-13有增高趋势,即病情可能趋于好转。而在病情危重的脓毒症休克组,第5天endocan、vWF、vWF/ ADAMTS-13水平较第1天继续升高,ADAMTS-13水平较第1天则更低,即病情可能趋于加重。
MODS组较非MODS组病情危重;MEDS评分≥13组为脓毒症高、极高死亡风险组,较MEDS评分 < 13组病情危重。研究表明,endocan、vWF、vWF/ADAMTS-13水平在MODS组较非MODS组明显升高,在MEDS评分≥13组较MEDS评分 < 13组明显升高,而ADAMTS-13在上述两组比较中呈明显减低趋势。说明病情越重,endocan、vWF、vWF/ADAMTS-13水平越高,ADAMTS-13水平越低,这与危险分层结论是一致的。endocan、vWF、vWF/ADAMTS-13在非MODS及MEDS评分 < 13组第5天较第1天显著降低,ADAMTS-13则显著升高。而在MODS组及MEDS评分≥13组,各指标第1天和第5天比较无显著差异,说明在病情较轻的分组中endocan、vWF、vWF/ADAMTS-13在治疗后有降低趋势,ADAMTS-13有增高趋势,病情可能趋于好转。而在病情危重的MODS组及MEDS评分≥13组,经过4 d的治疗,上述指标并没有好转趋势。
按最终预后分析,endocan、vWF、vWF/ADAMTS-13死亡组显著高于存活组,ADAMTS-13死亡组较存活组明显降低。endocan、vWF、vWF/ADAMTS-13存活组第5天较第1天显著降低,ADAMTS-13则显著升高。而死亡组endocan、vWF、vWF/ADAMTS-13第5天较第1天显著升高,ADAMTS-13则显著降低。死亡组较存活组病情危重,endocan、vWF、vWF/ADAMTS-13死亡组较存活组高,ADAMTS-13死亡组则更低。存活组经过4 d治疗,endocan、vWF、vWF/ADAMTS-13水平较第1天降低,ADAMTS-13较第1天升高,说明病情趋于好转。死亡组则相反。
本研究发现endocan、vWF、vWF/ADAMTS-13与APACHEⅡ评分、MEDS评分和SOFA评分均具有显著的正相关关系,ADAMTS-13与上述评分系统呈显著的负相关。其中以vWF/ADAMTS-13与各项评分的相关系数最高。
本研究证实了endocan、vWF、ADAMTS-13、vWF/ADAMTS-13的水平对于急诊抢救室脓毒症患者具有一定的危险分层价值,尤其是vWF/ADAMTS-13,高水平的vWF/ADAMTS-13是脓毒症病情危重的标志。
综上所述,上述生物标记物在脓毒症的危险分层、病情评估均有一定的临床价值,可以作为新型的脓毒症生物标记物应用于临床。
| [1] | Lever A, Mackenzie I. Sepsis:definition, epidemiology, and diagnosis[J]. BMJ, 2007, 335(7625): 879-883. DOI:10.1136/bmj.39346.495880.AE |
| [2] | Zambon M, Ceola M, Almeida-de-Castro R, et al. Implementation of the Surviving Sepsis Campaign guidelines for severe sepsis and septic shock:we could go faster[J]. Crit Care, 2008, 23(4): 455-460. DOI:10.1016/j.jcrc.2007.08.003 |
| [3] | Pierrakos C, Vincent JL. Sepsis biomarkers: a review[J].Crit Care, 2010, 14: R15. DOI: 10.1186/cc8872.[Epub2010Feb9.] |
| [4] | Scherpereel A, Depontieu F, Grigoriu B, et al. Endocan, a new endothelial marker in human sepsis[J]. Crit Care Med, 2006, 34(2): 532-537. DOI:10.1097/01.CCM.0000198525.82124.74 |
| [5] | Vallet B. Bench-to-bedside review: endothelial cell dysfunction in severe sepsis: a role in organ dysfunction?[J]. Crit Care, 2003, 7(2): 130-138. DOI:10.1186/cc1864 |
| [6] | Sadler JE. Biochemistry and genetics of von Willebrand factor[J]. Annu Rev Biochem, 1998, 67: 395-424. DOI:10.1146/annurev.biochem.67.1.395 |
| [7] | van Mourik JA, Boertjes R, Huisveld IA, et al. Von Willebrand factor propeptide in vascular disorders: a tool to distinguish between acute and chronic endothelial cell perturbation[J]. Blood, 1999, 94(1): 179-185. |
| [8] | Dong JF, Moake JL, Nolasco L, et al. ADAMTS-13 rapidly cleaves newly secreted ultralarge von Willebrand factor multimers on the endothelial surface under flowing conditions[J]. Blood, 2002, 100(12): 4033-4039. DOI:10.1182/blood-2002-05-1401 |
| [9] | Ley K, Laudanna C, Cybulsky MI, et al. Getting to the site of inflammation, the leukocyte adhesion cascade updated[J]. Nat RevImmunol, 2007, 7(9): 678-689. DOI:10.1038/nri2156 |
| [10] | Levy MM, Fink MP, Marshall JC, et al. 2001 SCCM/ESICM/ACCP/ATS/SIS International Sepsis Definitions Conference[J]. Intensive Care Med, 2003, 29(4): 530-538. DOI:10.1007/s00134-003-1662-x |
| [11] | Knaus WA, Draper EA, Wagner DP. APACHE Ⅱ: a severity of disease classification system[J]. Crit Care Med, 1985, 13: 818-29. DOI:10.1097/00003246-198510000-00009 |
| [12] | Shapiro NI, Wolfe RE, Moore RB, et al. Mortality in Emergency Department Sepsis (MEDS) score: a prospectively derived and validated clinical prediction rule[J]. Crit Care Med, 2003, 31(3): 670-675. DOI:10.1097/01.CCM.0000054867.01688.D1 |
| [13] | Vincent JL, Moreno R, Takala J, et al. The SOFA (Sepsis-related Organ Failure Assessment) score to describe organ dysfunction/failure. On behalf of the Working Group on Sepsis-Related Problems of the European Society of Intensive Care Medicine[J]. Intensive Care Med, 1962, 22(7): 707-710. |
| [14] | Shirakawa K, Naitou K, Hirose J, Takahashi T, Furusako S. Presepsin (sCD14-ST): Development and evaluation of one-step ELISA with a new standard this is similar to the form of presepsin in septic patients[J]. Clin Chem Lab Med, 2011, 49: 937-939. DOI:10.1515/CCLM.2011.145 |
| [15] | Alberti C, Brun-Buisson C, Burchardi H, et al. Epidemiology of sepsis and infection in ICU patients from an international multicentre cohort study[J]. Intensive Care Med, 2002, 28: 108-121. DOI:10.1007/s00134-001-1143-z |
| [16] | Vincent JL, Sakr Y, Sprung CL, Ranieri VM, et al. Sepsis in European intensive care units: results of the SOAP study[J]. Crit Care Med, 2006, 34: 344-353. DOI:10.1097/01.CCM.0000194725.48928.3A |
| [17] | Esteban A, Frutos-Vivar F, Ferguson ND, et al. Sepsis incidence and outcome: contrasting the intensive care unit with the hospital ward[J]. Crit Care Med, 2007, 35: 1284-1289. DOI:10.1097/01.CCM.0000260960.94300.DE |
| [18] | Gonsalves MD, Sakr Y. Early identification of sepsis[J]. Curr Infect Dis Rep, 2010, 12: 329-335. DOI:10.1007/s11908-010-0122-3 |
| [19] | Bauer M, Reinhart K. Molecular diagnostics of sepsis-where are we today?[J]. Int J Med Microbiol, 2010, 300: 411-413. DOI:10.1016/j.ijmm.2010.04.006 |
| [20] | Levy MM. Preface biomarkers in critical illness[J]. Crit Care Clin, 2011, 27: xⅡi-xv. DOI:10.1016/j.ccc.2011.01.001 |
| [21] | Bongers TN, de Maat MP, van Goor ML, et al. High von Willebrand factor levels increase the risk of first ischemic stroke: influence of ADAMTS13, inflammation, and genetic variability[J]. Stroke, 2006, 37(11): 2672-2677. DOI:10.1161/01.STR.0000244767.39962.f7 |
 2019, Vol. 28
2019, Vol. 28




