大动脉炎(Takayasu arteritis,TA)是一种与免疫相关,累及大血管慢性非特异性肉芽肿性血管炎,多发于年轻女性,东南亚和中东地区常见,以受累血管狭窄、闭塞或扩张为特征,受累血管广泛。TA累及肺动脉并不少见,但既往对TA相关肺动脉高压(TA associated pulmonary hypertension,TA-PH)的研究较少。本研究对13例TA-PH患者的临床特点、肺血管病变特征、治疗与随访情况进行全面分析,以提高对该病的认识。
1 资料与方法 1.1 一般资料回顾性分析2008年至2017年上海市肺科医院肺循环科确诊13例TA-PH患者。TA诊断依据1990年美国风湿病学会标准[1]:①发病年龄≤40岁;②肢体间歇性运动障碍;③肱动脉搏动减弱;④血压差 > 10 mmHg(1 mmHg=0.133 kPa);⑤锁骨下动脉或主动脉杂音;⑥血管造影异常,并除外动脉粥样硬化、纤维肌发育不良等其他原因。满足3项或以上可诊断。肺动脉高压(PH)入选标准:静息状态右心导管测肺平均动脉压(mean pulmonary arterial pressure,mPAP)≥25 mmHg,且除外先天性心脏病、左心疾病、肺部疾病、血栓等其他疾病所致PH[2]。
TA临床分型[1]:根据病变部位,①头臂动脉型,累及主动脉弓及分支;②胸腹主动脉型,累及降主和腹腔动脉;③广泛性,具有上述两型;④肺动脉型。
病情活动性标准:Kerr评分[3],①全身症状,如发热、骨骼、肌肉症状;②血沉增高;③血管缺血或炎症,如间歇性跛行、脉弱或无脉、血管杂音等;④血管造影异常。四项中新出现或加重≥2项提示病情活动。
本研究获得上海市肺科医院伦理委员会的批准(K16-293)。
1.2 方法临床资料收集:①基本信息、症状、体征、既往史等(特别是肺动脉高压发病因素,如减肥药,先天性心脏病,结缔组织病、心脏瓣膜病、慢性肺病、血栓性疾病),并对患者进行电话或门诊随访,随访截至2017年12月。②超声心动图。常规测量右心结构和功能相关参数。③肺功能。包括体容、肺泡通气、残气和肺泡弥散等指标。④WHO功能分级(WHO FC)和6 min步行距离。依照我国肺动脉高压诊断治疗专家共识[4]。⑤右心导管。常规左前臂静脉或右颈内静脉入路,置入Swan-Ganz漂浮导管(131HF7或774HF75,Edwards Lifescience Co. Ltd,美国)测量上腔静脉、右心房、右心室、肺动脉和肺小动脉楔压,使用热稀释法测量心输出量[5]。9例用伊洛前列素(拜耳,德国)行急性肺血管扩张试验。⑥肺动脉CT血管造影(computed tomographic pulmonary angiography,CTPA)和DSA血管造影。所有患者均行CTPA,肺动脉或主动脉造影检查。
治疗:除吸氧、强心、利尿等传统治疗,确诊后给予PH靶向治疗。风湿专科医师根据风湿活动度给予激素、细胞毒性药物等。
1.3 统计学方法采用SPSS 22.0统计软件,计量资料以均数±标准差(x±s)表示,计数资料以百分率表示。采用Kaplan-Meier法计算生存率。以P < 0.05为差异有统计学意义。
2 结果 2.1 一般临床资料13例TA-PH患者中女性10例,男女比例1:3.3;确诊年龄(39±11)岁,(21~56)岁,女性(39±13)岁,男性(41±7)岁。3例合并高血压,2例肺结核,1例糖尿病,1例Graves病。10例以活动后气促首发症状,3例以晕厥首发。首发症状到确诊TA时间1个月~30年,平均7.0年;到确诊TA-PH时间2个月~50年,平均9.0年。10例TA和PH同时诊断,另外3例分别于TA确诊1个月、6年和20年后诊断PH。1例曾误诊为慢性血栓栓塞性肺高压(chronic thromboembolic pulmonary hypertension,CTEPH)。确诊TA-PH时6例患者WHO FC Ⅱ级,7例Ⅲ级。2例无法完成6 min步行试验,其余11例6 min步行距离250~605 m,平均444 m。
临床表现活动后气促(12例)、胸闷胸痛(8例)、心悸(6例)、咯血(4例)、头晕头痛(4例)、晕厥(3例)、发绀(3例)、胸背部疼痛(3例)、视物模糊(2例)、黑朦(2例)、发热(1例)和关节痛(1例)。8例听诊到血管杂音,6例血压不对称,4例无脉症,4例心包积液,2例足背动脉搏动不对称。7例血沉快,7例C反应蛋白升高。根据Kerr评分[3]8例在病情活动期。
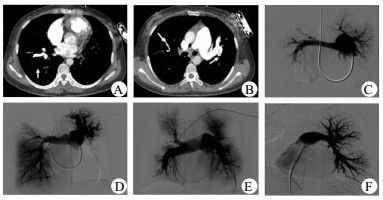
2.2 影像学和动脉受累情况CTPA和动脉造影示所有患者均肺动脉受累,且均累及双侧肺动脉。8例主肺动脉扩张,其中2例呈瘤样扩张。双侧肺动脉主干可同时受累,也可单个受累。受累血管多表现为狭窄或扩张。2例右肺动脉主干完全闭塞。每个患者均多个叶、段以及亚段肺动脉受累,表现为不同程度血管狭窄、血管壁增厚,管腔纤细、扩张、粗细不等,或动脉瘤,且DSA肺动脉造影见血管走形扭曲、僵硬,远端灌注稀疏或消失(图 1)。
|
| A:右中下叶肺动脉扩张,部分分支局限性狭窄,左下肺动脉未显影,提示血管完全闭塞;B:主肺动脉增宽,左侧肺动脉近段扩张、扭曲,右上肺动脉纤细,血管影稀疏;C:主肺动脉增宽,左肺动脉及分支纤细,远端灌注稀疏甚至缺失,右肺动脉远端动脉瘤,右上、中叶肺动脉僵硬,远端灌注稀疏,右下肺动脉缺如;D:肺动脉主干明显增粗,右上叶及左下叶肺动脉缺如,左上肺动脉瘤样扩张、扭曲,灌注略稀疏,右中下肺动脉近端多处狭窄,未见明显充盈缺损,远端灌注良好;E:主肺动脉和左右肺动脉增粗,右上叶前段肺动脉狭窄后闭塞,尖后段血管僵硬,远端灌注稀疏,右下叶肺动脉扩张,段肺动脉远端纤细、闭塞,灌注稀疏;左侧叶段肺动脉管腔通畅,远端灌注稍稀疏;F:左肺动脉及左侧各叶段肺动脉连续性扩张-狭窄-扩张样表现,即串珠样表现,血管僵硬,远端灌注稀疏 图 1 大动脉炎肺部累及的影像学表现 Figure 1 Images of pulmonary artery involvement in TA |
|
|
体循环受累:锁骨下动脉6例,头臂动脉5例,颈总动脉4例,肾动脉2例,胸主动脉3例,腹主动脉1例。分型:头臂动脉型6例,胸腹主动脉型1例,广泛型2例。所有患者均为肺动脉型,其中单纯肺动脉受累4例。
2.3 肺功能检查11例患者存在肺功能受累。7例轻度弥散功能减退,1例重度弥散功能减退。4例轻度限制性通气功能障碍,3例轻中度阻塞性通气功能障碍。
2.4 右心导管血流动力学表现TA-PH患者肺动脉压显著升高,肺动脉收缩压和mPAP分别为60~146 (89.5±23.2) mmHg,28~72(48.0±14.0)mmHg;肺血管阻力升高[3.63~16.53(7.59±4.21)Wood U,表 1]。7号和9号患者肺小动脉楔压 > 15 mmHg,为毛细血管后PH。其中病例#7舒张压差10 mmHg,肺血管阻力7.94 Wood U,提示为混合型毛细血管后PH;病例#9舒张压差1 mmHg,肺血管阻力3.63 Wood U,倾向单纯毛细血管后PH。其余11例均为毛细血管前PH。急性肺血管扩张试验均阴性。
| 病例 | PASP(mmHg) | mPAP(mmHg) | PAWP(mmHg) | CI[L/(min·m2)] | PVR(Wood U) | SVR(Wood U) | SvO2(%) | 急性肺血管扩张试验 |
| #1 | 95 | 44 | 10 | 5.07 | 4.66 | 12.88 | 72.7 | 阴性 |
| #2 | 146 | 72 | 13 | 2.27 | 16.53 | 18.49 | 61.8 | 阴性 |
| #3 | 61 | 61 | 5 | 2.97 | 5.3 | 12.44 | 60.6 | 阴性 |
| #4 | 97 | 42 | 12 | 2.08 | 9.38 | 15 | 48 | 阴性 |
| #5 | 106 | 62 | 5 | 2.32 | 16.29 | 15.71 | 57.1 | 阴性 |
| #6 | 117 | 64 | / | 2.77 | / | 19.38 | 68.9 | / |
| #7 | 84 | 65 | 38 | 2.7 | 7.94 | 27.65 | 57.7 | 阴性 |
| #8 | 67 | 39 | 4 | 3.68 | 4.47 | 14.05 | 72.9 | / |
| #9 | 68 | 36 | 16 | 3.23 | 3.63 | 6.37 | 67.9 | 阴性 |
| #10 | 86 | 36 | 5 | 2.63 | 5.57 | 17.56 | 48.7 | 阴性 |
| #11 | 90 | 41 | 12 | 3.24 | 5.21 | 25.89 | 74 | 阴性 |
| #12 | 87 | 34 | 7 | 2.96 | 6.43 | 19.05 | 62.9 | / |
| #13 | 60 | 28 | 9 | 2.13 | 5.69 | 28.14 | 69.7 | / |
| 注:PASP,肺动脉收缩压;mPAP,肺动脉平均压;PAWP,肺小动脉楔压;CI,心指数;PVR,肺血管阻力;SVR,体循环阻力;SvO2,混合静脉氧饱和度;/表示未测 | ||||||||
8例在活动期,7例用糖皮质激素,其中4例用糖皮质激素联合免疫抑制剂。所有患者均尝试PH靶向药物:4例单用5型磷酸二酯酶抑制剂,3例单用内皮素受体拮抗剂,3例联合5型磷酸二酯酶抑制剂和前列环素类似物,2例联合5型磷酸二酯酶抑制剂和内皮素受体拮抗剂,1例联合前列环素类似物和内皮素受体拮抗剂。5例叶级肺动脉显著狭窄行肺动脉球囊扩张和支架植入术,1例术后一年出现支架处再狭窄。1例行3次球囊扩张(表 2)。
| 病例 | 靶向药物 | 抗风湿药物 | 抗凝治疗 | 抗血小板 | 介入治疗 | 随访时间(月) | 结局 | 末次随访WHO FC |
| #1 | 伐地那非 | 强的松 | 否 | 是 | 支架置入术 | 84 | 存活 | Ⅰ |
| #2 | 波生坦 | 强的松+环磷酰胺 | 是 | 否 | 否 | 18 | 死亡 | - |
| #3 | 西地那非+贝前列素钠 | 无 | 是 | 否 | 支架置入术 | 100 | 存活 | Ⅱ |
| #4 | 波生坦+贝前列素钠 | 无 | 是 | 否 | 否 | 55 | 死亡 | - |
| #5 | 西地那非 | 泼尼松 | 否 | 否 | 否 | 1 | 失访 | Ⅳ |
| #6 | 西地那非+波生坦 | 无 | 否 | 否 | 支架置入术 | 78 | 存活 | Ⅱ |
| #7 | 波生坦 | 无 | 否 | 是 | 血管旁路手术 | 14 | 死亡 | - |
| #8 | 他达拉非 | 强的松+甲氨蝶呤 | 否 | 是 | 否 | 32 | 存活 | Ⅱ |
| #9 | 波生坦 | 环磷酰胺+强的松 | 是 | 否 | 否 | 42 | 存活 | Ⅰ |
| #10 | 西地那非+波生坦 | 无 | 是 | 否 | 球囊扩张术 | 126 | 存活 | Ⅰ |
| #11 | 西地那非+贝前列素钠 | 强的松 | 是 | 否 | 支架置入术 | 22 | 失访 | Ⅱ |
| #12 | 西地那非 | 强的松+环磷酰胺+羟氯喹 | 否 | 是 | 否 | 4 | 存活 | Ⅲ |
| #13 | 西地那非+贝前列素钠 | 无 | 是 | 无 | 支架置入术 | 110 | 存活 | Ⅱ |
| 注:#1,#3,#6,#11,#13行单支叶级肺动脉球囊扩张和支架置入术,#10行3次单纯叶级肺动脉球囊扩张术,#7首次确诊TA后行腹主动脉和肾动脉人造血管旁路术 | ||||||||
随访中3例分别在确诊后14、18和55个月因重症右心衰竭死亡。2例失访,失访前WHO FC分别为Ⅳ级和Ⅱ级。目前仍有8例随访,5例WHO FC稳定在Ⅰ~Ⅱ级,且随访超过5年。2例分别随访32和42个月,WHO FC稳定在Ⅰ~Ⅱ级。1例用西地那非、强的松、环磷酰胺和羟氯喹治疗,随访4个月,WHO FC稳定在Ⅲ级。若假定所有失访者均存活,估测TA-PH患者5年生存率为68.2%。
3 讨论TA中PH确切发病率尚不清楚,但既往小样本研究示约8.8%~68.9%的TA患者肺动脉受累[6-7],其中TA-PH患病率为6.3%~12.0%[8-10]。TA起病隐匿,本组患者中10例因发现PH而确诊TA,仅有2例是TA诊断数年后出现PH,提示PH可能并非均发生在TA晚期[9],也可能是TA首发表现,应引起重视。
本研究患者多为育龄期女性,多以活动后气促为首发症状,伴随胸闷胸痛、心悸等,合并视物模糊、血管杂音、血压不对称、脉弱/无脉等症状或体征。与既往研究相似[11-12],患者少有发热。TA发病经历非特异性炎症期,血管炎症期和静止期三阶段,PH可能发生在后两阶段,故以血管狭窄或闭塞所致症状为主要表现。
本研究患者均有肺动脉受累,累及双侧肺动脉,主干、叶、段、亚段,及远端肺动脉均有受累。CTPA表现为血管壁增厚,管腔狭窄、闭塞或扩张。肺动脉造影表现为血管迂曲、管腔僵硬、串珠样狭窄等。TA-PH与CTEPH在肺部影像学上比较相似,两者均少见,临床可能会导致误诊[11],病史和体检是两者鉴别的基本方法。CTEPH常有静脉血栓栓塞症病史,以及静脉曲张、下肢色素沉着等表现,CTPA见附壁型或中心型充盈缺损,肺动脉造影可有充盈缺损、截断征。光学相干断层成像和血管内超声等新兴技术[13]可观察血管壁形态结构,有助于两者鉴别。
本研究11例为毛细血管前PH,2例为毛细血管后PH,提示TA可通过多种机制引起PH。TA累及主肺动脉,导致动脉狭窄闭塞,导致第四大类PH;自身免疫和炎症促肺动脉内皮和平滑肌细胞增殖,致肺血管重构,引起第一大类PH;TA累及主动脉及分支、心脏瓣膜或心肌[14],导致舒张/收缩性心功能不全,引起第2大类PH[9]。此外,45%的TA患者有抗磷脂抗体综合征[15],且免疫和炎症是血栓形成危险因素[16],故TA有诱发血栓[17],引起CTEPH的风险。但本研究13例患者抗磷脂抗体均阴性,全球无此类TA-PH个案报道[8],提示这非TA-PH常见原因。
疑诊TA-PH患者建议至专科诊治,因多数医院不具备右心导管检查和肺动脉造影的条件,但前者是PH诊断金标准,后者是观察TA肺血管受累重要方法。两者均为有创操作,术者水平直接影响并发症发生率。专科中心经前臂静脉路径检查,操作简便,并发症少,舒适度高[5]。CTPA和超声心动图简单经济,是TA-PH筛查和随访的重要方法。血管超声可显示体表动脉结构、管壁水肿、血管阻力和血流速度等,且简单快捷,是TA诊断与鉴别的重要影像学手段。
TA治疗方案多源于观察性研究和专家推荐。活动期应用糖皮质激素或联合免疫抑制剂。肿瘤坏死因子α受体拮抗剂、白细胞介素6受体拮抗剂等生物制剂应用于TA患者也有一定疗效[18]。既往认为TA-PH机制与其他结缔组织病不同,不宜用PH靶向药物[9]。近期Wang等[19]用波生坦或西地那非治疗7例重症TA-PH患者(mPAP > 60 mmHg),结果症状显著改善。本研究对13例患者均单独或联合应用靶向药物, 多数患者心功能改善或维持稳定,提示靶向药物治疗有效。
与药物相比,经皮肺动脉球囊成形术和支架置入术创伤小,恢复快,是治疗稳定期TA-PH动脉重度狭窄闭塞,安全有效重建肺动脉血运的重要方法[20]。李庆雪等[21]介入治疗10例TA至肺动脉狭窄患者,术后肺动脉压显著下降,但介入后血管可能会出现再狭窄、血栓、出血等并发症。并发症与血沉、C反应蛋白和纤维蛋白原水平密切相关。介入后仍需积极控制原发病。外科手术是另一种常用血运重建治疗,常用于体循环动脉狭窄及闭塞性病变。肺动脉分支多,穿行于肺组织内,血管无法充分游离显露,外科手术治疗肺动脉狭窄限制极大,故目前仅有少量肺主动脉受累患者手术治疗个案报道[22]。
TA患者预后良好,5年生存率达94%[23]。TA-PH患者预后情况目前尚无报道,本研究估测TA-PH患者5年生存率明显偏低,提示PH仍是TA患者的严重并发症,可显著降低患者生存率。
TA累及肺动脉延误诊治会使肺动脉压力进行性升高,影响患者活动能力,严重影响预后。加强临床医师对该病认识,尽可能减少误诊误治,尽早诊断和治疗,可改善患者预后。
| [1] | 中华医学会风湿病学分会. 大动脉炎诊断及治疗指南[J]. 中华风湿病学杂志, 2011, 15(2): 119-120. DOI:10.3760/cma.j.issn.1007-7480.2011.02.013 |
| [2] | Simonneau G, Gatzoulis MA, Adatia I, et al. Updated clinical classification of pulmonary hypertension[J]. J Am Coll Cardiol, 2013, 62(25 Suppl): D34-41. DOI:10.1016/j.jacc.2013.10.029 |
| [3] | Kerr GS, Hallahan CW, Giordano J, et al. Takayasu arteritis[J]. Ann Intern Med, 1994, 120(11): 919-929. DOI:10.7326/0003-4819-120-11-199406010-00004 |
| [4] | 中华医学会心血管病学分会, 中华心血管病杂志编辑委员会. 肺动脉高压筛查诊断与治疗专家共识[J]. 中华心血管病杂志, 2007, 35(11): 979-987. DOI:10.3760/j.issn.0253-3758.2007.11.002 |
| [5] | 荆志成, 徐希奇, 蒋鑫, 等. 经前臂静脉径路行右心导管检查和肺动脉造影的可行性研究[J]. 中华心血管病杂志, 2009, 37(2): 142-144. DOI:10.3760/cma.j.issn.0253-3758.2009.02.013 |
| [6] | Zheng D, Fan D, Liu L. Takayasu arteritis in China: a report of 530 cases[J]. Heart Vessels Suppl, 1992, 7: 32-36. DOI:10.1007/BF01744541 |
| [7] | Li J, Sun F, Chen Z, et al. The clinical characteristics of Chinese Takayasu' s arteritis patients: a retrospective study of 411 patients over 24 years[J]. Arthritis Res Ther, 2017, 19(1): 107. DOI:10.1186/s13075-017-1307-z |
| [8] | 赖晋智, 徐东, 李梦涛, 等. 大动脉炎合并肺动脉高压患者的临床分析[J]. 中华风湿病学杂志, 2009, 13(9): 612-615. DOI:10.3760/cma.j.issn.1007-7480.2009.09.008 |
| [9] | 万瑾, 王天, 潘丽丽, 等. 多发性大动脉炎合并肺动脉高压临床特点分析[J]. 中国医药, 2015, 10(10): 1435-1438. DOI:10.3760/cma.j.issn.1673-4777.2015.10.007 |
| [10] | Bicakcigil M, Aksu K, Kamali S, et al. Takayasu' s arteritis in Turkey - clinical and angiographic features of 248 patients[J]. Clin Exp Rheumatol, 2009, 27(1 Suppl 52): S59-64. |
| [11] | 窦静波, 龚娟妮, 马展鸿, 等. 大动脉炎累及肺动脉的临床分析[J]. 中华结核和呼吸杂志, 2016, 39(8): 603-607. DOI:10.3760/cma.j.issn.1001-0939.2016.08.011 |
| [12] | 曾绮娴, 柳志红, 何建国, 等. 多发性大动脉炎累及肺动脉所致肺动脉高压患者的临床特征[J]. 中华医学杂志, 2016, 96(16): 1252-1255. DOI:10.3760/cma.j.issn.0376-2491.2016.16.006 |
| [13] | Jiang X, Peng FH, Liu QQ, et al. Optical coherence tomography for hypertensive pulmonary vasculature[J]. Int J Cardiol, 2016, 222: 494-498. DOI:10.1016/j.ijcard.2016.07.215 |
| [14] | 张晓群, 陈鑫, 王启闻, 等. 多发性大动脉炎合并冠状动脉闭塞病变介入治疗成功一例[J]. 中华急诊医学杂志, 2017, 26(9): 1086-1088. DOI:10.3760/cma.j.issn.1671-0282.2017.09.024 |
| [15] | Misra R, Aggarwal A, Chag M, et al. Raised anticardiolipin antibodies in Takayasu' s arteritis[J]. Lancet, 1994, 343(8913): 1644-1645. |
| [16] | Wang H, Lai B, Wu X, et al. Late diagnosis of Takayasu' s arteritis with repeated attacks of heart failure and uncontrolled hypertension due to abdominal aortic thrombosis: case report and review of the literature[J]. Blood Press, 2015, 24(6): 333-339. DOI:10.3109/08037051.2015.1049423 |
| [17] | 申磊, 夏豪, 江洪, 等. 混合型大动脉炎致急性肱动脉、冠状动脉、肺动脉血栓形成一例[J]. 中华急诊医学杂志, 2009, 18(7): 710. DOI:10.3760/cma.j.issn.1671-0282.2009.07.011 |
| [18] | 孔秀芳, 姜林娣. 大动脉炎诊断治疗的研究进展[J]. 中华医学杂志, 2016, 96(27): 2203-2205. DOI:10.3760/cma.j.issn.0376-2491.2016.027.022 |
| [19] | Wang X, Dang A, Chen B, et al. Takayasu arteritis-associated pulmonary hypertension[J]. J Rheumatol, 2015, 42(3): 495-503. DOI:10.3899/jrheum.140436 |
| [20] | 刘新文, 蒋雄京, 王建安, 等. 双侧肾动脉重度狭窄血管内介入治疗疗效分析[J]. 中华急诊医学杂志, 2012, 21(4): 415-418. DOI:10.3760/cma.j.issn.1671-0282.2012.04.019 |
| [21] | 李庆雪, 蒋雄京, 倪新海, 等. 经皮介入治疗大动脉炎所致肺动脉狭窄[J]. 中国分子心脏病学杂志, 2012, 12(1): 5-8. DOI:10.3969/j.issn.1671-6272.2012.01.002 |
| [22] | Fujita K, Nakashima K, Kanai H, et al. A successful surgical repair of pulmonary stenosis caused by isolated pulmonary Takayasu' s arteritis[J]. Heart Vessels, 2013, 28(2): 264-267. DOI:10.1007/s00380-012-0262-5 |
| [23] | Yang L, Zhang H, Jiang X, et al. Clinical manifestations and longterm outcome for patients with Takayasu arteritis in China[J]. J Rheumatol, 2014, 41(12): 2439-2446. DOI:10.3899/jrheum.140664 |
 2018, Vol. 27
2018, Vol. 27




