心源性休克(cardiogenic shock, CS)是造成急性ST段抬高型心肌梗死(ST segment elevation myocardial infarction, STEMI)院内死亡最主要的原因。尽管近年来诊疗技术有所进步,但即使在经急诊冠脉介入治疗(percutaneous intervention, PCI)后,病死率仍高达50%以上[1-2]。伴发CS的STEMI患者病情危重,临床表现复杂。急诊快速的危险分层有助于医疗决策及进一步预后判断。IABP SHOCK Ⅱ危险评分是针对急性心肌梗死伴发CS患者危险分层的评估工具[3]。本文回顾性分析2011年8月至2013年8月间伴发CS的STEMI入院经IABP机械辅助并行急诊PCI治疗的患者临床资料,比较不同危险分层患者入院一般情况、药物及介入治疗情况、IABP辅助情况等临床特点,评价IABP SHOCK Ⅱ危险评分对经急诊PCI血运重建并有IABP机械辅助的STEMI伴CS患者行住院死亡的预测价值,以期提高对危重STEMI的警觉,并指导临床治疗。
1 资料与方法 1.1 一般资料收录北京安贞医院心内科2011年8月至2013年8月期间置入IABP机械辅助并完成急诊PCI治疗的伴发CS的STEMI患者89例。纳入标准:(1)发病至入院时间少于72 h;(2)均符合中华医学会心脏病分会指定的急性STEMI及心源性休克的诊断标准[1];排除在院前出现心搏骤停、进行心肺复苏患者。(3)所有患者均经过STEMI急诊PCI及规范化药物治疗。临床资料从本院病历数据库中获得。
1.2 研究方法分组方法:以患者入院及急诊PCI资料计算IABP SHOCK Ⅱ评分,按照危险分层[2],分为低风险组(IABP SHOCK Ⅱ评分0~2分,n=71);中风险组(IABP SHOCK Ⅱ评分3~4分,n=13);高风险组(IABP SHOCK Ⅱ评分5~9分,n=5)。因中风险组及高风险组患者数量较少,将其合并为中高风险组(IABP SHOCK Ⅱ评分3~9分,n=18)。
比较2组患者一般资料(包括年龄、性别、既往病史)、入院时临床相关指标、急诊PCI治疗、住院诊治情况和IABP辅助情况。比较置入IABP前后2组生命体征(收缩压、舒张压、心率)。心肌标志物、血清肌酐在患者进入急诊室或心内科病房后即刻收集。入院后6 h内行床旁超声心动图以Simpson公式计算射血分数),其余的辅助检查及化验在入院后24 h内收集。
IABP的置入方法及使用参数:根据患者身高选择30 mL或40 mL球囊导管,在局麻下用Seldinger法经右或左股动脉穿刺送入导丝,局部预扩后置入IABP导管,导管尖端至左锁骨下动脉开口下方2~3 cm处(胸骨角水平),近端在肾动脉开口上方。导管尖端位置由导管室行透视或经拍摄胸片确定。选择合适患者的模式触发(心电触发或压力触发),以1:1或1:2比例反搏。
1.3 相关定义心源性休克:由于心功能受损导致收缩压 < 90 mmHg(1 mmHg=0.133 kPa)长于30 min,或在没有低血容量的情况下必须使用血管收缩剂维持血压,并出现周围器官低灌注的临床表现,如少尿、烦躁、肢端冰冷等。
肾功能不全[3]:eGFR < 60 mL/(min·1.73 m2),入院时估算肾小球滤过率(estimated glomerular filtration rate,eGFR)通过简化MDRD公式(the modification of diet in renal disease equation)计算。
IABP拔除指征:主动拔除根据血压、心率及心功能情况,由主管医生判断是否停用IABP治疗。被动拔除:①严重的并发症。严重的血小板减少(PLT < 40×109/L)、出血、血肿、股动脉假性动脉瘤、严重的下肢末梢循环不良、动脉闭塞、主动脉并发症。②IABP导管损坏,如打折或球囊破裂。
IABP SHOCK Ⅱ评分[2]:由多中心、随机对照的IABP-SHOCK Ⅱ试验数据分析得出。包含年龄大于73岁(1分),既往卒中病史(2分),入院血糖大于10.6 mmol/L(1分),血肌酐大于132.6 μmol/L(1分),血乳酸大于5 mmol/L(2分)及PCI后TIMI冠脉血流小于3级(2分)6个变量组成。0~2分为低风险组,3~4分为中风险组,5~9分为高风险组。
1.4 统计学方法采用SPSS 20.0软件分析数据,计数资料以例数(%)表示,用χ2检验或Fisher确切概率法计算。计量资料首先进行正态性分析,符合正态分布者以均数±标准差(x±s)表示,计量变量采用成组t检验比较,采用双侧检验。比较IABP置入前后生命体征(收缩压、舒张压、心率)采用配对t检验。偏态分布者以M(QR)表示,使用秩和检验分析。通过计算受试者工作特征(ROC)曲线下面积(AUC)评价IABP-SHOCK Ⅱ评分的预测能力。以P < 0.05为差异有统计学意义。
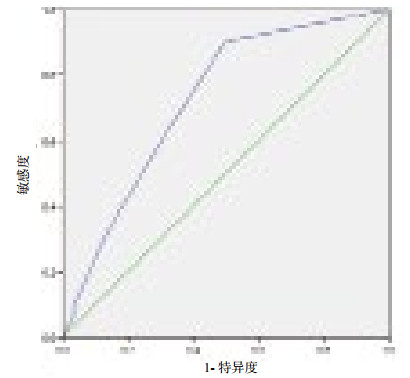
2 结果 2.1 IABP SHOCK Ⅱ评分对伴发CS的STEMI患者院内死亡预测价值IABP SHOCK Ⅱ评分对院内死亡预测的ROC曲线的AUC为0.723,P=0.001,95%CI: 0.616~0.830,见图 1。危险分层:低风险组(评分0~2分),住院病死率29.6%(21/71);中风险组(评分3~4分),住院病死率53.8%(7/13);高风险组(评分5~9分),5例中3例死亡。
|
| 图 1 IABP Ⅱ评分对院内死亡预测的ROC曲线分析 Figure 1 ROC analysis of IABP SHOCK Ⅱ Risk Scorefor predicting in-hospital mortality |
|
|
与低风险组比较,中高风险组患者年龄更高,更多患者有糖尿病史、脑血管病史及中度以上肾功能不全,入院时血清乳酸及血糖水平更高,见表 1。
| 指标 | 低风险组(n=71) | 中高风险组(n=18) | P值 |
| 年龄(岁,x±s) | 60.2±10.9 | 68.8±8.3 | 0.002 |
| 女性(例,%) | 14(19.7) | 3(16.7) | 0.769 |
| 危险因素(例,%) | |||
| 吸烟 | 50(70.4) | 10(55.6) | 0.229 |
| 高血压史 | 38(53.5) | 12(66.7) | 0.315 |
| 糖尿病史 | 19(26.8) | 11(61.1) | 0.006 |
| 肾功能不全 | 20(28.2) | 9(50.0) | 0.078 |
| 脑血管病史 | 3(4.2) | 5(27.8) | 0.002 |
| 冠心病家族史 | 4(5.7) | 0(0) | 0.299 |
| 冠心病史(例,%) | |||
| 陈旧性心梗 | 11(15.5) | 2(11.1) | 0.638 |
| PCI史 | 12(16.9) | 2(11.1) | 0.547 |
| CABG史 | 0(0) | 0(0) | - |
| 入院情况[M(QR)] | |||
| 发病至入院时间(h) | 5(3, 7) | 6(4, 9) | 0.12 |
| 收缩压(mmHg) | 81(70, 90) | 82.5(80, 110) | 0.370 |
| 舒张压(mmHg) | 56(44, 60) | 50(44, 64) | 0.589 |
| 心率(次/min) | 92(70, 110) | 90(80, 107) | 0.755 |
| 前壁心肌梗死(例,%) | 46(64.8) | 11(61.1) | 0.772 |
| 检验检查[M(QR)] | |||
| 血红蛋白(g/L) | 142(130, 156) | 130(123, 152) | 0.199 |
| 中性粒细胞比(%) | 83.8(74.5, 88.4) | 86.9(82.2, 89.0) | 0.188 |
| 肌钙蛋白Ⅰ(ng/mL) | 12.3(0.25, 102.7) | 8.7(1.6, 95.8) | 0.652 |
| 乳酸(mmol/L) | 2.4(1.0, 4.2) | 5.6(4.2, 11.5) | 0.004 |
| 血糖(mmol/L) | 7.4(5.9, 8.6) | 8.3(7.1, 11.6) | 0.041 |
| 血肌酐(μmol/L) | 100.4(80.6, 120.1) | 103.5(82.0, 147.3) | 0.287 |
| 低密度脂蛋白(mmol/L) | 2.7(2.1, 3.4) | 2.5(1.7, 3.3) | 0.482 |
| 左室射血分数(%) | 40(36, 50) | 38(27, 48) | 0.247 |
与低风险组相比,中高风险组急诊PCI后犯罪血管TIMI血流 < 3的患者比例明显较多。见表 2。
| 指标 | 低风险组(n=71) | 中高风险组(n=18) | P值 |
| 犯罪血管 | |||
| LM及LAD近端 | 39(54.9) | 11(61.1) | 0.637 |
| LCX | 0(0) | 0(0) | - |
| RCA | 32(45.1) | 7(38.9) | 0.637 |
| 多支血管病变 | 27(38.0) | 7(38.9) | 0.946 |
| 术后犯罪血管TIMI血流 < 3 | 9(12.7) | 11(61.1) | < 0.01 |
低风险组与中高风险组应用静脉利尿剂、血管活性药物及使用持续肾脏替代治疗的患者比例差异无统计学意义,见表 3。
| 指标 | 低风险组(n=71) | 中高风险组(n=18) | P值 |
| 静脉利尿剂 | 37(52.1) | 10(55.6) | 0.794 |
| 血管活性药物 | 67(94.4) | 18(100) | 0.303 |
| CRRT | 7(10.4) | 1(5.6) | 0.528 |
| 注:CRRT,持续肾脏替代治疗 | |||
低风险组与中高风险组在置入IABP后收缩压、舒张压均较置入前有所改善(P < 0.05)。但置入IABP后中高风险组较置入前相比心率改善不明显(P=0.919),见表 4。
| 指标 | 低风险组(n=71) | 中高风险组(n=18) |
| 收缩压(mmHg) | ||
| 置入前 | 78.3±18.3a | 74.2±12.3a |
| 置入后 | 99.0±20.8a | 100.7±30.0a |
| 舒张压(mmHg) | ||
| 置入前 | 49.6±11.7a | 45.1±9.2a |
| 置入后 | 56.7±14.3a | 59.8±18.0a |
| 心率(次/min) | ||
| 置入前 | 95.0±34.9a | 88.4±21.1 |
| 置入后 | 91.5±17.4a | 80.5±24.1 |
| 注:低风险组与中高风险组比较,aP < 0.05;置入前后比较,bP < 0.05 | ||
STEMI是心内科的重症疾病,特别是合并CS后,尽管治疗策略不断进展,伴发CS的STEMI住院病死率仍高达50%以上[4-5]。迅速、有效、简单的评分有助于医疗决策及进一步预后判断。目前评价急性心肌梗死风险的临床评分很多,如心肌梗死溶栓治疗临床试验评分(TIMI危险评分)、GRACE评分等。但此类评分涉及项目多,临床实施复杂,且并不针对已伴发CS的STEMI患者,临床指导意义有限。虽然早期有一些对于心源性休克的风险评分[6-8],但这些研究规模较小,且多数患者未能进行急诊PCI。而急诊PCI血运重建可使CS患者明显获益[9-10],所以这些研究存在着多种偏倚。IABP-SHOCK Ⅱ风险评分经多中心、随机对照的IABP-SHOCK Ⅱ试验数据分析得出。由年龄、既往卒中病史、入院血糖、血肌酐、血乳酸水平及PCI后冠脉血流情况6个变量组成,用于预测急性心肌梗死伴发心源性休克人群短期死亡风险[2, 11]。而IABP-SHOCK Ⅱ评分对于伴发CS的STEMI患者短期死亡预测,特别是经IABP机械辅助的伴有CS的STEMI患者的预测能力需要进一步评价及分析。本研究探讨了IABP-SHOCK Ⅱ评分对伴发CS的STEMI临床预测意义。本研究入选的患者均为经急诊PCI血运重建后STEMI伴发CS病情危重需联合IABP辅助的患者。ROC曲线分析后,AUC为0.723,P=0.001,95%CI为0.616~0.830。因此从统计学角度考虑,IABP-SHOCK Ⅱ评分对伴发CS的STEMI患者院内死亡有预测价值。
本研究中,中高风险组患者一般资料与低风险组相比,中高风险组患者年龄更高,更多患者有糖尿病史、脑血管病史及中度以上肾功能不全(P < 0.05)。提示中高风险组的患者基础血管条件更不理想。两组的患者入院生命体征均不稳定,血压低、心率快,心功能差,LVEF低,伴发CS的STEMI患者冠状动脉病变严重、心脏贮备功能差。而中高风险组患者入院血糖及血乳酸水平明显更高。说明中高风险组心肌梗死及休克状态对循环状态及机体代谢的影响比低风险组更严重,导致患者病死率明显升高。与ROC曲线的预测结果一致。本研究中,中高风险组急诊PCI术后犯罪血管血流情况明显不如低风险组。实际手术中,因为生命体征不稳定、循环状态不良且冠状动脉病变严重,急诊PCI处理病变操作可能更加困难。而急诊冠状动脉旁路移植术在临床上实施困难。
IABP辅助对两组患者而言,辅助后血流动力学均有所改善。低风险组在置入IABP后能观察到收缩压、舒张压均有上升而心率下降,反映了IABP在血流动力学支持方面的有效作用。但中高风险组置入IABP后心率并没有明显下降。既往有文献支持合适的血压可以保证急性心肌梗死患者冠脉灌注,而有效控制急性心肌梗死患者心率可以减少心肌耗氧,改善近期预后[12-14]。辅助后血压、心率的改善迅速提示IABP辅助较为有效,这类患者预后较好,而IABP辅助后血压及心率等血流动力学指标改善程度有限的患者预后不良。患者血流动力学较难纠正。置入IABP后并没有明显改善预后。尽管治疗策略不断进展,但循环崩溃时,IABP机械辅助的疗效欠佳[15-17]。
但是本研究为回顾性研究,IABP-SHOCK Ⅱ评分仅由入院状态及急诊PCI情况评估,仅能反映患者当时的情况。如果能动态观察,患者的评分也许有所改变,可能会提高对患者预后判断的准确性。且为单中心研究,仅纳入89例患者,可能存在一定的选择偏倚。因此,对于IABP-SHOCK Ⅱ评分对伴发CS的STEMI患者人群院内死亡的预测,以及对急诊PCI及机械辅助装置的治疗时机有待进一步研究。
综上所述,伴发CS的STEMI患者人群中,IABP-SHOCK Ⅱ评分是一项简单、实用的危险分层评估工具。当IABP-SHOCK Ⅱ评分≥3时,即使经急诊PCI血运重建及IABP机械辅助,患者的院内死亡风险明显升高,需提高警惕。
| [1] | 中华医学会心血管病学分会, 中华心血管病杂志编辑委员会. 急性ST段抬高型心肌梗死诊断和治疗指南[J]. 中华心血管病杂志, 2015, 43(5): 380-393. DOI:10.3760/cma.j.issn.0253-3758.2015.05.003 |
| [2] | Poss J, Koster J, Fuernau G, et al. Risk stratification for patients in cardiogenic shock after acute myocardial infarction[J]. J Am Coll Cardiol, 2017, 69(15): 1913-1920. DOI:10.1016/j.jacc.2017.02.027 |
| [3] | Stevens LA, Coresh J, Greene T, et al. Assessing kidney function--measured and estimated glomerular filtration rate[J]. N Engl J Med, 2006, 354(23): 2473-2483. DOI:10.1056/NEJMra054415 |
| [4] | Goldberg RJ, Spencer FA, Gore JM, et al. Thirty-year trends (1975 to 2005) in the magnitude of, management of, and hospital death rates associated with cardiogenic shock in patients with acute myocardial infarction: a population-based perspective[J]. Circulation, 2009, 119(9): 1211-1219. DOI:10.1161/CIRCULATIONAHA.108.814947 |
| [5] | Nguyen HL, Yarzebski J, Lessard D, et al. Ten-Year (2001-2011) trends in the incidence rates and short-term outcomes of early versus late onset cardiogenic shock after hospitalization for acute myocardial infarction[J]. J Am Heart Assoc, 2017, 6(6): e005566. DOI:10.1161/JAHA.117.005566 |
| [6] | Klein LW, Shaw RE, Krone RJ, et al. Mortality after emergent percutaneous coronary intervention in cardiogenic shock secondary to acute myocardial infarction and usefulness of a mortality prediction model[J]. Am J Cardiol, 2005, 96(1): 35-41. DOI:10.1016/j.amjcard.2005.02.040 |
| [7] | Harjola VP, Lassus J, Sionis A, et al. Clinical picture and risk prediction of short-term mortality in cardiogenic shock[J]. Eur J Heart Fail, 2015, 17(5): 501-509. DOI:10.1002/ejhf.260 |
| [8] | Sleeper LA, Reynolds HR, White HD, et al. A severity scoring system for risk assessment of patients with cardiogenic shock: a report from the SHOCK Trial and Registry[J]. Am Heart J, 2010, 160(3): 443-450. DOI:10.1016/j.ahj.2010.06.024 |
| [9] | Sjauw KD, Engstrom AE, Vis MM, et al. A systematic review and meta-analysis of intra-aortic balloon pump therapy in ST-elevation myocardial infarction: should we change the guidelines[J]. Eur Heart J, 2009, 30(4): 459-468. DOI:10.1093/eurheartj/ehn602 |
| [10] | van Domburg RT, Sonnenschein K, Nieuwlaat R, et al. Sustained benefit 20 years after reperfusion therapy in acute myocardial infarction[J]. J Am Coll Cardiol, 2005, 46(1): 15-20. DOI:10.1016/j.jacc.2005.03.047 |
| [11] | Thiele H, Schuler G, Neumann FJ, et al. Intraaortic balloon counterpulsation in acute myocardial infarction complicated by cardiogenic shock: design and rationale of the Intraaortic Balloon Pump in Cardiogenic Shock Ⅱ (IABP-SHOCK Ⅱ) trial[J]. Am Heart J, 2012, 163(6): 938-945. DOI:10.1016/j.ahj.2012.03.012 |
| [12] | 王春梅, 吴学思, 韩智红, 等. 心率对急性心肌梗死患者住院期间病死率的影响[J]. 中华心血管病杂志, 2008, 36(7): 594-597. DOI:10.3321/j.issn.0253-3758.2008.07.005 |
| [13] | Fox KA, Dabbous OH, Goldberg RJ, et al. Prediction of risk of death and myocardial infarction in the six months after presentation with acute coronary syndrome: prospective multinational observational study (GRACE)[J]. BMJ, 2006, 333(7578): 1091. DOI:10.1136/bmj.38985.646481.55 |
| [14] | Boersma E, Pieper KS, Steyerberg EW, et al. Predictors of outcome in patients with acute coronary syndromes without persistent ST-segment elevation. Results from an international trial of 9461 patients. The PURSUIT Investigators[J]. Circulation, 2000, 101(22): 2557-2567. DOI:10.1161/01.CIR.101.22.2557 |
| [15] | Cao J, Liu W, Zhu J, et al. Risk factors and clinical characteristics of in-hospital death in acute myocardial infarction with IABP support[J]. Int J Clin Exp Med, 2015, 8(5): 8032-8041. |
| [16] | 盛瑾, 刘文娴, 曹佳宁. 主动脉内球囊反搏辅助的急性心肌梗死院内死亡患者临床特征分析[J]. 心肺血管病杂志, 2016, 35(3): 175-179. DOI:10.3969/j.issn.1007-5062.2016.03.004 |
| [17] | 高志伟, 赵红梅, 黄英姿, 等. 主动脉内球囊反搏对急性心肌梗死患者短期和远期预后影响的荟萃分析[J]. 中华急诊医学杂志, 2017, 26(1): 102-107. DOI:10.3760/cma.j.issn.1671-0282.2017.01.020 |
 2018, Vol. 27
2018, Vol. 27




