再通治疗, 包括静脉溶栓和血管内介入治疗, 是脑梗死早期非常重要的治疗措施, 可有效减少此类患者的致残率[1-4]。不过即使在有效时间窗内,再通治疗的效果也有很大的不确定性,约40%的脑梗死患者神经功能由此明显改善,而其余患者并无获益,甚至有6%的症状性脑出血风险[5]。患者的个体差异可以影响再通治疗的效果,本课题组曾对阿替普酶(recombinant tissue plasminogen activator, rt-PA)溶栓的脑梗死患者进行回顾性分析, 发现侧支代偿良好患者神经功能恢复更好, 病死率更低[6]。以往也有研究曾分别指出,年龄、再通治疗时间等可能是此类患者预后转归的影响因素[7-8]。有鉴于此,本研究收集在南京医科大学第一附属医院接受再通治疗的脑梗死患者病例资料,根据患者基础状况、病情、治疗等不同特点,以多元回归模型分析影响患者近期(30 d)预后的危险因素,为此类患者的预后评估提供资料。
1 资料与方法 1.1 一般资料本研究回顾性分析2014年10月至2016年8月期间在南京医科大学第一附属医院急诊科就诊的脑梗死再通治疗患者病例。参考《重组组织型纤溶酶原激活剂静脉溶栓治疗缺血性卒中中国专家共识(2012版)》[2],开展急性脑梗死再通治疗绿色通道,该通道的进入标准为:①年龄≥18岁;②突发言语不清、单侧肢体肌力下降等症状,且美国国立卫生研究院卒中量表(National Institute of Health Stroke Scale, NIHSS)评分4~25分;③再通治疗时间窗以内:静脉溶栓4.5 h,血管内介入取栓6 h。排除标准为:①近3个月有颅脑手术、严重颅脑外伤或脑梗死病史;②既往有颅内肿瘤、脑动脉瘤或脑出血病史;③身体存在活动性出血;④出血倾向,血小板 < 100×109/L;口服抗凝剂者,PT > 15 s或INR > 1.7;⑤妊娠;⑥收缩压大于180 mmHg,或舒张压 > 100 mmHg(1 mmHg=0.133 kPa)。
所有进入绿色通道的患者,均提前签署再通治疗和头颅CT血管造影(CT angiography, CTA)检查知情同意书。先予头颅CT检查,若CT提示既往脑梗死范围大于1/3大脑半球或脑出血,患者退出通道。否则立即在同一检查台上行头颅CTA检查,根据其不同结果,选择如下治疗方案:①同时具有介入取栓指征(大血管闭塞)和静脉溶栓指征(尚在时间窗4.5 h内),立即给予rt-PA静脉溶栓(总剂量按0.9 mg/kg体质量计算,先将10%药量静脉推注5 min,余下药物静脉维持1 h),同时进行介入术前准备, 衔接血管内取栓治疗。②静脉溶栓或介入治疗仅有一项指征,则给予相应治疗。③两者皆无,则退出绿色通道。所有完成绿色通道治疗患者,继续住院接受神经科相关治疗和后续的康复治疗。再通治疗后第1天、第3天定期复查头颅CT,症状加重则随时复查头颅CT,明确是否有症状性脑出血。定期随访30 d,给予NIHSS评分。
1.2 方法共有153例急性脑梗死患者完成绿色通道治疗,本研究入选标准为其中头颅CTA显示颈内动脉(internal carotid artery, ICA)或大脑中动脉(middle cerebral artery, MCA)梗死者。排除标准为既往存在严重的心肺不全或遗留神经功能缺失。按该标准,共有94例患者纳入研究。本研究观测终点为再通治疗后30 d,近期预后改善指符合以下全部标准:期间患者存活、未发生症状性脑出血,并且30 d NIHSS评分较治疗前提升 > 4分[9-10],否则认为近期预后不良。研究患者的相关临床因素,分析引发不良预后的危险因素。纳入的临床因素包括年龄、性别、既往史(房颤、高血压、糖尿病)、治疗时间、治疗方式、梗死部位、侧支循环状况。部分因素的定义区分如下:年龄高低以≥70岁或 < 70岁区分;治疗时间指从症状出现至首次进行溶栓或介入治疗的时间,时间早晚以 < 4 h或≥4 h区分;治疗方式分为仅溶栓、仅介入、溶栓衔接介入治疗;梗死部位指闭塞或狭窄部位发生在ICA或MCA;侧支循环状况参照软脑膜侧支评分(pial collateral score)[11]:1分-闭塞血管的远端部分有侧支循环重建;2分-侧支重建血管出现在与闭塞血管相邻的近端部分;3分-侧支重建血管出现在与闭塞血管相邻的远端部分;4分-侧支重建血管出现在闭塞血管两段远端;5分-闭塞血管支配区无或仅有较少的侧支血管重建。以1~2分为侧支循环良好,3~5分为侧支循环不良[10], 见图 1。
|
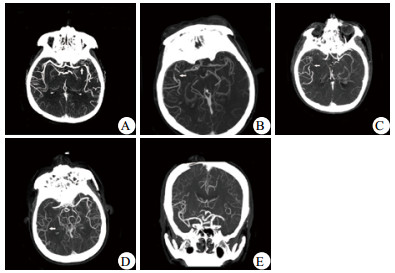
| A: 1分,左侧大脑中动脉M1闭塞,M1远端重建;B: 2分,右侧大脑中动脉M1闭塞,M2近端重建;C: 3分,右侧大脑中动脉M1闭塞,M2远端重建;D:4分,右侧大脑中动脉M1闭塞,M3分支重建;E: 5分,左侧大脑中动脉M1闭塞,其支配区仅有少量血管重建。箭头示侧支重建血管出现位置 图 1 软脑膜侧支评分 Figure 1 Pial collateral score |
|
|
按以上软脑膜侧支评分,将患者分为侧支良好组(1~2分)和侧支不良组(3~5分),分别研究各组患者预后受治疗时间的影响。按接受再通治疗时间 < 4 h或≥4 h分为早、晚两个治疗亚组,分别在不同侧支循环状况下,比较治疗早、晚两亚组的预后改善率。
1.3 统计学方法采用SPSS 19.0软件进行统计分析,计数资料两组间比较用χ2或Fisher精确概率法。采用多元Logistic回归模型分析影响患者预后的危险因素,纳入模型前各因素先行单因素分析,以P < 0.1为进入模型的标准。以P < 0.05为差异有统计学意义。
2 结果 2.1 患者预后的单因素分析和多元Logistic回归分析纳入研究的患者中预后改善36例,预后不良58例,后者包括死亡2例、症状性脑出血5例。经单因素分析(表 1),年龄、侧支循环状况、治疗时间、治疗方式符合进入后续多元回归模型的标准(P < 0.1)。将它们纳入多元Logistic回归分析(表 2),结果显示,高龄(≥70岁)及侧支循环不良为患者近期不良预后的影响因素(P < 0.05),而治疗时间、治疗方式对预后无明显影响(P > 0.05)。
| 临床因素 | 例数 | 预后不良(例, %) | χ2值 | P值 |
| 年龄 | 8.220 | 0.004 | ||
| ≥70岁 | 54 | 40 (74.1) | ||
| < 70岁 | 40 | 18 (45.0) | ||
| 性别 | 0.391 | 0.532 | ||
| 男 | 56 | 36 (64.3) | ||
| 女 | 38 | 22 (57.9) | ||
| 房颤 | 1.357 | 0.224 | ||
| 有 | 25 | 13 (52.0) | ||
| 无 | 69 | 45 (65.2) | ||
| 高血压 | 0.345 | 0.557 | ||
| 有 | 48 | 31 (64.6) | ||
| 无 | 46 | 27 (58.7) | ||
| 糖尿病 | 1.447 | 0.229 | ||
| 有 | 19 | 14 (73.7) | ||
| 无 | 75 | 44 (58.7) | ||
| 再通治疗时间 | 3.696 | 0.055 | ||
| ≥4 h | 56 | 39 (69.6) | ||
| < 4 h | 38 | 19 (50.0) | ||
| 再通治疗方式 | 7.150 | 0.028 | ||
| 仅溶栓 | 28 | 15 (53.6) | ||
| 仅介入 | 34 | 27 (79.4) | ||
| 溶栓+介入 | 32 | 16 (50.0) | ||
| 梗死部位 | 0.862 | 0.353 | ||
| MCA | 68 | 40 (58.8) | ||
| ICA | 26 | 18 (69.2) | ||
| 侧支循环 | 4.251 | 0.039 | ||
| 不良 | 33 | 25 (75.8) | ||
| 良好 | 61 | 33 (54.1) |
| 临床因素 | B值 | 标准误 | Wald | OR | 95% CI | P值 |
| 年龄≥70岁 | 0.975 | 0.491 | 3.943 | 2.651 | 1.013~6.937 | 0.047 |
| 治疗时间≥4 h | 0.579 | 0.600 | 0.931 | 1.784 | 0.550~5.782 | 0.335 |
| 侧支循环不良 | 1.151 | 0.533 | 4.667 | 3.160 | 1.113~8.977 | 0.031 |
| 再通方式a | 3.098 | 0.212 | ||||
| 1 vs.2 | -0.658 | 0.791 | 0.693 | 0.518 | 0.110~2.440 | 0.405 |
| 3 vs.2 | -1.080 | 0.624 | 3.000 | 0.339 | 0.100~1.153 | 0.083 |
| 3 vs.1 | -0.422 | 0.633 | 0.445 | 1.931 | 0.410~9.099 | 0.505 |
| 注:a再通方式三种治疗方式作为无序多分类变量,行哑变量处理;1:仅溶栓;2:仅介入;3:溶栓+介入 | ||||||
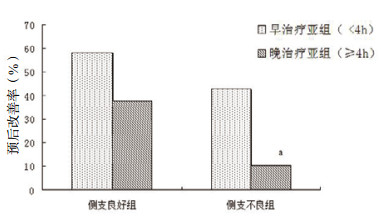
对于侧支循环良好的脑梗死患者,再通治疗延长至4 h以后仍有较好的效果,治疗时间 < 4 h和≥4 h两组患者的预后改善率差异无统计学意义(58.3% vs. 37.8%, χ2=2.463, P=0.117);而侧支循环不良患者受治疗时间影响较大,4 h以后接受再通治疗的脑梗死患者,预后改善率明显低于治疗时间 < 4 h的患者(42.9% vs. 10.5%, P=0.047),见图 2。
|
| 在相同侧支状况组内,与早治疗亚组比较,aP<0.05;侧支不良组总例数33, 其早、晚治疗亚组分别为14例、19例,两者比较采用Fisher精确概率法 图 2 不同侧支循环状况患者的预后受再通时间的影响 Figure 2 Effects of recanalization treatment time on the prognosis of patients with different collateral circulation |
|
|
年龄是影响脑梗死预后的重要因素之一,80岁以上脑梗死患者的长期预后明显差于80岁以下者[12]。一项大样本(50万例以上脑梗死患者)的队列研究显示,年龄超过90岁,则脑梗死导致的死亡风险升高2~3倍[13]。尽管高龄不是脑梗死再通治疗的禁忌证,但仍有不少rt-PA溶栓研究将80岁以上患者排除在外[14-15]。一份总结13项研究的Meta分析指出,80岁以上的脑梗死溶栓患者,获得良好预后的机会比80岁以下者低50%[7]。另有一项研究显示,年龄高于70岁是脑梗死溶栓患者发生临床严重脑出血(clinically significant intracranial hemorrhage)的独立危险因素[16]。根据2016年ASA/AHA提出的指南意见[9],虽然脑梗死溶栓时间窗已延长至4.5 h,但对于80岁以上且发病3~4.5 h的患者,rt-PA溶栓治疗获益仍缺乏足够依据支持(Ⅱb推荐,B级证据),需充分权衡利弊。本研究的观察结果与之类似,经多元回归分析发现高龄(≥70岁)是脑梗死再通治疗预后不良的独立危险因素。此外,本课题组此前曾对脑梗死溶栓患者行对照研究发现,侧支循环良好者较之不良者30 d NIHSS评分明显下降,病死率也更低[6]。本次研究在此基础上进一步发现,侧支循环不良或缺失可能是不良预后的独立危险因素。这些也与以往报道相符:具有较完整一级侧支循环,即Willis环,可作为脑梗死患者3个月神经功能改善的独立预测因素[17];软脑膜动脉作为二级侧支循环,若代偿良好,脑梗死溶栓患者将有更好预后[18];在并发症方面,侧支循环不良是血管内治疗致脑出血的危险因素[20]。
目前研究一般认为再通治疗时间与脑梗死预后密切相关,患者越早被开通堵塞血管预后越好。2004年4项国际多中心研究汇总分析显示:脑梗死患者于1.5 h、1.5~3 h、3~4.5 h接受rt-PA治疗与接受安慰剂相比,预后良好率提高但随时间延长而逐步下降,3个时间段的OR值分别为2.81(95%CI:1.75~4.50)、1.55(95%CI:1.12~2.15)、1.40(95%CI:1.05~1.85)[8]。随后的研究也得出类似结论[20-21]。不过在本研究中,多元回归分析却未显示治疗时间对预后有显著影响。为探究原因,本课题组进一步将患者依据侧支循环优劣分为两组,分别研究两组患者预后受治疗时间早晚的影响。结果发现,侧支循环良好患者即使延迟至4 h后接受治疗仍有较好预后改善率,与4 h内差异无统计学意义;对于侧支循环不良患者,4 h内治疗组预后改善率同样尚可,而4 h后则明显下降,此时尽管在时间窗内,但鲜有预后改善者。根据以上结果,可推测本研究的多因素分析与以往报道不一致的可能原因:本研究的样本量相对不足,同时其中侧支循环不良者占比可能和以往研究也有差异。
对图 2结果可做出如下思考:对于侧支循环良好的脑梗死患者, 在时间窗之后可能仍有再通治疗指征;而如果患者侧支循环不良,对再通治疗时间要求将更为急迫,若再通时间偏晚(如 > 4 h),即使在时间窗内可能仍难有神经功能改善。有研究就曾根据CTA区分脑梗死患者的侧支循环优劣,发现其中侧支良好者的介入治疗时间窗可以适当延长[22]。可能的机制为,脑梗死发生时,血液可经良好的侧支循环向缺血半暗区输入,增强其缺血耐受性,为再通治疗争取时间并使更多的神经细胞存活。在恢复期随着新生血管逐渐长入,这些细胞将代偿性地发挥更多作用[23]。仅由侧支循环的差异就可得知,脑梗死患者对缺血的耐受时间是千差万别的,目前一刀切的再通治疗时间窗(静脉溶栓4.5 h内、血管内取栓治疗6 h内)只是无奈情况下的折中选择。一个可能的发展方向是,充分评估每位脑梗死患者的缺血组织活力或缺血半暗区,给予每个人个体化的“时间窗”[24-25]。现实中的难点一方面是需要使用到磁共振灌注/扩散失配(MRI perfusion/diffusion mismatch)、CT灌注(CT perfusion)等昂贵的影像学设备,并且这些影像学评估尚未取得公认的标准;另一方面,过多的检查很可能会推延原本就非常宝贵的治疗时间[26]。本研究在开展脑梗死绿色通道上改善了流程,于患者头颅CT排除脑出血后,立即在同一检查台上行头颅CTA检查。一方面避免了二次搬运,减少因检查而延迟的治疗时间;另一方面以头颅CTA评估患者的侧支循环状况,也许是探索此类患者个体化治疗的另一条道路。
最后需要指出的是,本研究虽然分析了影响脑梗死再通治疗预后的危险因素,但若对其过分担心而使符合条件患者失去再通治疗机会,则非本意。对于自身条件(年龄、侧支循环等)良好的患者,是否可以延长再通治疗时间窗,需要今后进一步研究阐述。
| [1] | 陈寿权, 雷远丽. 常见急症抗凝溶栓治疗规范的进展[J]. 中华急诊医学杂志, 2015, 24(4): 352-355. DOI:10.3760/cma.j.issn.1671-0282.2015.04.002 |
| [2] | 重组组织型纤溶酶原激活剂治疗缺血性卒中共识专家组. 重组组织型纤溶酶原激活剂静脉溶栓治疗缺血性卒中中国专家共识(2012版)[J]. 中华内科杂志, 2012, 51(12): 1006-1100. DOI:10.3760/cma.j.issn.0578-1426.2012.12.022 |
| [3] | Liu M, Wang HR, Liu JF, et al. Therapeutic effect of recombinant tissue plasminogen activator on acute cerebral infarction at different times[J]. World J Emerg Med, 2013, 4(3): 205-209. DOI:10.5847/wjem.j.issn.1920–8642.2013.03.009 |
| [4] | Jin JF, Guo ZT, Zhang YP, et al. Prediction of motor recovery after ischemic stroke using diffusion tensor imaging: a meta-analysis[J]. World J Emerg Med, 2017, 8(2): 99-105. DOI:10.5847/wjem.j.1920-8642.2017.02.003 |
| [5] | Jauch EC, Saver JL, Adams HP, et al. Guidelines for the early management of patients with acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association[J]. Stroke, 2013, 44(3): 870-947. DOI:10.1161/STR.0b013e318284056a |
| [6] | 何斌, 邵斌霞, 张劲松, 等. 侧支循环丰富程度对大脑中动脉梗死患者溶栓预后的影响[J]. 中华急诊医学杂志, 2017, 26(8): 910-913. DOI:10.3760/cma.j.issn.1671-0282.2017.08.016 |
| [7] | Bhatnagar P, Sinha D, Parker RA, et al. Intravenous thrombolysis in acute ischaemic stroke: a systematic review and meta-analysis to aid decision making in patients over 80 years of age[J]. J Neurol Neurosurg Psychiatry, 2011, 82(7): 712-717. DOI:10.1136/jnnp.2010.223149 |
| [8] | Hacke W, Donnan G, Fieschi C, et al. Association of outcome with early stroke treatment: pooled analysis of ATLANTIS, ECASS, and NINDS rt-PA stroke trials[J]. ACC Curr J Rev, 2004, 13(5): 19. DOI:10.1016/S0140-6736(04)15692-4 |
| [9] | Chuang YM, Chan L, Lai YJ, et al. Configuration of the circle of Willis is associated with less symptomatic intracerebral hemorrhage in ischemic stroke patients treated with intravenous thrombolysis[J]. J Crit Care, 2013, 28(2): 166-172. |
| [10] | Ribo M, Flores A, Rubiera M, et al. Extending the time window for endovascular procedures according to collateral pial circulation[J]. Stroke, 2011, 42(12): 3465-3469. DOI:10.1161/STROKEAHA.111.623827 |
| [11] | Liebeskind DS. Collateral circulation[J]. Stroke, 2003, 34(9): 2279-2284. DOI:10.1161/01.STR.0000086465.41263.06 |
| [12] | Gensicke H, Seiffge DJ, Polasek AE, et al. Long-term outcome in stroke patients treated with Ⅳ thrombolysis[J]. Neurology, 2013, 80(10): 919-925. DOI:10.1212/WNL.0b013e3182840c35 |
| [13] | Fonarow GC, Reeves MJ, Zhao X, et al. Age-related differences in characteristics, performance measures, treatment trends, and outcomes in patients with ischemic stroke[J]. Circulation, 2010, 121(7): 879-891. DOI:10.1161/CIRCULATIONAHA.109.892497 |
| [14] | Albers GW, Clark WM, Madden KP, et al. ATLANTIS trial:results for patients treated within 3 hours of stroke onset: alteplase thrombolysis for acute noninterventional therapy in ischemic stroke[J]. Stroke, 2002, 33(2): 493-495. DOI:10.1161/hs0202.102599 |
| [15] | Bluhmki E, Chamorro A, Davalos A, et al. Stroke treatment with alteplase given 3.0-4.5 h after onset of acute ischaemic stroke (ECASS Ⅲ): additional outcomes and subgroup analysis of a randomised controlled trial[J]. Lancet Neurol, 2009, 8(12): 1095-1102. DOI:10.1016/S1474-4422(09)70264-9 |
| [16] | Ho BL, Chen CF, Lin RT, et al. Clinical implication of hemorrhagic transformation in ischemic stroke patients treated with recombinant tissue plasminogen activator[J]. Neurol Sci, 2016, 37(11): 1-7. DOI:10.1007/s10072-016-2667-x |
| [17] | Christoforidis GA, Mohammad Y, Kehagias D, et al. Angiographic assessment of pial collaterals as a prognostic indicator following intra-arterial thrombolysis for acute ischemic stroke[J]. AJNR Am J Neuroradiol, 2005, 26(7): 1789-1797. |
| [18] | Bang OY, Saver JL, Kim SJ, et al. Collateral flow averts hemorrhagic transformation after endovascular therapy for acute ischemic stroke[J]. Stroke, 2011, 42(8): 2235-2239. DOI:10.1161/STROKEAHA.110.604603 |
| [19] | Emberson J, Lees KR, Lyden P, et al. Effect of treatment delay, age, and stroke severity on the effects of intravenous thrombolysis with alteplase for acute ischaemic stroke:a meta-analysis of individual patient data from randomised trials[J]. Lancet, 2014, 384(9958): 1929-1935. DOI:10.1016/S0140-6736(14)60584-5 |
| [20] | Fonarow GC, Zhao X, Smith EE, et al. Door-to-needle times for tissue plasminogen activator administration and clinical outcomes in acute ischemic stroke before and after a quality improvement initiative[J]. JAMA, 2014, 311(16): 1632-1640. DOI:10.1001/jama.2014.3203 |
| [21] | Henninger N, Fisher M. Extending the time window for endovascular and pharmacological reperfusion[J]. Transl Stroke Res, 2016, 7(4): 1-10. DOI:10.1007/s12975-015-0444-4 |
| [22] | Nishijima Y, Akamatsu Y, Weinstein PR, et al. Collaterals: Implications in cerebral ischemic diseases and therapeutic interventions[J]. Brain Res, 2015, 1623: 18-29. DOI:10.1016/j.brainres.2015.03.006 |
| [23] | Hirano T. Searching for salvageable brain: the detection of ischemic penumbra using various imaging modalities[J]. J Stroke Cerebrovasc Dis, 2014, 23(5): 795-798. DOI:10.1016/j.jstrokecerebrovasdis.2013.10.003 |
| [24] | An H, Ford AL, Vo KD, et al. Imaging oxygen metabolism in acute stroke using MRI[J]. Curr Radiol Rep, 2014, 2(3): 39. DOI:10.1007/s40134-013-0039-3 |
| [25] | Kidwell CS, Jahan R, Gornbein J, et al. MR RESCUE Investigators. A trial of imaging selection and endovascular treatment for ischemic stroke[J]. N Engl J Med, 2013, 368(10): 914-923. DOI:10.1056/NEJMoa1212793 |
| [26] | Mishra NK, Albers GW, Davis SM, et al. Mismatch-based delayed thrombolysis: a meta-analysis[J]. Stroke, 2010, 41(1): e25-33. DOI:10.1161/STROKEAHA.109.566869 |
 2018, Vol. 27
2018, Vol. 27




