急性胸痛是成人急诊就诊的最常见原因之一。据统计,美国2010年有超过7百万胸痛患者至急诊科就诊,占急诊就诊总量的5.4%。我国北京地区的横断面研究显示,胸痛患者占急诊就诊患者的4.7%。急性胸痛病因构成复杂,病情千变万化,疾病谱危险程度跨度巨大,不仅包括急性冠脉综合征(acute coronary syndrome,ACS)、急性主动脉夹层(acute aortic dissection,AAD)、急性肺栓塞(pulmonary embolism,PE)及张力性气胸等致命性高危疾病,也包括胃食管反流、肋间神经痛、神经官能症等相对良性的低危疾病。临床实践中,应强调“早期诊断、危险分层、正确分流、科学救治”。
对于急性胸痛,医生往往首先想到ACS,然而事实上仅仅不足5%的胸痛患者被明确诊断为ST段抬高型心肌梗死(ST-segment elevation myocardial infarction,STEMI),近25%的患者为非ST段抬高型ACS(NSTE-ACS)。所以快速、准确地鉴别诊断心源性和非心源性胸痛是急诊处理的难点和重点。即使在欧美国家,在急性胸痛的评估和管理方面也存在高危患者救治不利、低危患者过度诊治的问题。例如,在美国约有5%的ACS患者因症状不典型从急诊直接离院,其中16%的患者因不适当离院导致错失救治时机而死亡。与此同时,因胸痛收入院的患者中,只有10%~15%被诊断为急性心肌梗死(acute myocardial infarction,AMI),约70%的患者最终除外ACS或未发现任何疾病。目前我国尚缺少大型临床注册研究来提供国内相关数据,预计情况同样不容乐观。
急性胸痛患者优化处理、危险分层是临床诊治的关键。早期、快速诊断治疗ACS、AAD、PE等致命性疾病,争取最佳抢救时机,改善患者临床预后,并尽快合理分流ACS 低危人群及其他非致命性胸痛,避免不必要的检查和治疗,是目前急诊科医师面临的巨大挑战之一。
1.2 生物标志物在急性胸痛患者评估和管理中的作用近20年来,临床医师可获得的实验室知识急剧增多,能够应用的医学检验项目大量出现,生物标志物研究及临床应用发展迅速,已成为临床上评估急性胸痛患者的重要指标。以心肌肌钙蛋白(cardiac troponin,cTn)为核心,肌酸激酶同工酶(creatine kinase-MB,CK-MB)、脑钠肽(brain natriuretic peptide,BNP)、D-二聚体、C-反应蛋白(C-reactin protein,CRP)为代表的标志物,不仅能用于疾病的快速诊断和鉴别,也能在危险分层、预后判断与治疗决策中起到关键性的作用。特别是cTn检测技术的出现促使了ACS新的分类与诊断标准的形成。另外,新的生物标志物,如心型脂肪酸结合蛋白(heart type-fatty acid binding protein,H-FABP)、缺血修饰白蛋白(ischemia modified albumin,IMA)和髓过氧化物酶(myeloperoxidase,MPO)等在一定程度上反映了心肌缺血和(或)斑块不稳定性等病理生理学过程,在ACS诊断和预后评价中可能发挥重要作用。
急性非创伤性胸痛急诊评估相关的生物标志物,如心肌损伤生物标志物、心脏功能生物标志物等,虽然均可通过中心实验室进行检测,但由于耗时较长且检测时间和地点相对固定,急诊患者多、病情重且流动性大,中心检测并不能完全满足急诊诊疗对胸痛患者快速实时诊断的强烈需求,因此,床旁检测技术越来越凸显出它的巨大价值。床旁检测技术(point of care testing,POCT)又称床旁即时检验,是指用轻便的设备、简单的操作、随意的地点,即时快速地提供准确的报告。POCT简化了检验过程,缩短了样本分析前的处理时间和分析后的报告时间,也降低了发生差错的机会,提高了急诊患者的诊治效率。
1.3 编写专家共识的意义“急性胸痛”病因构成复杂、危险分层关键,急诊医生科学、规范地应用生物标志物的能力大小不一,特别是在联合检测及动态检测方面尚有不足。因此,为了满足临床医生工作需要、规范急性胸痛特别是高危胸痛的诊治,中华医学会急诊医学分会及《中华急诊医学杂志》编辑委员会组织国内急诊领域相关专家,遵循借鉴国内外相关指南和专家共识,结合中国国情,组织编写了本共识。共识包括6个部分,即前言、心肌损伤生物标志物、心脏功能生物标志物、止凝血生物标志物、胸痛相关炎性生物标志物及标志物的联合检测的作用和意义,以期指导临床医师能早期科学合理分流及救治急诊胸痛患者。
2 心肌损伤生物标志物在急性胸痛患者中,ACS发病率高,致死致残率高,早期评估、快速诊断和及时治疗能明显降低病死率,改善预后。目前诊断缺血性胸痛常用的心肌损伤标志物包括cTn、 CK-MB和肌红蛋白(myoglobin,MYO)。超敏cTn(high-sensitivity cardiac troponin,hs-cTn)的检测比传统检测方法的敏感度和特异度更高,目前已在国内逐步使用。一些新型心肌损伤标志物的发现,包括H-FABP、IMA和MPO等,在ACS的早期诊断与评估中也发挥着重要作用。需要强调的是,cTn是目前诊断心肌坏死敏感和特异的首选心肌损伤标志物,是诊断AMI和对ACS危险分层的主要依据。
2.1心肌肌钙蛋白(cTn) 2.1.1 概述肌钙蛋白(troponin,Tn)是横纹肌收缩的一种调节蛋白,是骨骼肌和心肌的结构蛋白,由TnI、TnT和TnC 3个亚基组成的复合体,与原肌球蛋白一起和肌动蛋白结合,90%位于横纹肌肌丝上。TnC与钙离子结合,TnI将肌钙蛋白复合物固定在肌球蛋白上,TnI是抑制亚单位。TnI和TnT的心肌亚型(cTnI和cTnT)与骨骼肌中对应的蛋白来自不同的基因,具有独特的抗原表位,心肌特异度较高。当心肌缺血导致心肌损伤时,首先是胞浆中游离的少量cTnI和cTnT迅速释放进入血液循环,外周血中浓度迅速升高,在发病后4 h内即可测得。随着心肌肌丝缓慢而持续的降解,cTnI和cTnT不断释放进入血液,cTnI 升高持续时间为4~10 d,cTnT为5~14 d,有很长的诊断窗口期。
2.1.2 应用指征(1)早期诊断 cTn对心肌损伤具有很高的敏感度和特异度,已取代CK-MB成为ACS诊断的首选心肌损伤标志物。cTn测定值高于参考范围上限第99百分位值[变异系数(CV) ≤10%]时提示心肌损伤。对临床可疑的胸痛、胸闷及其他不典型症状或包括心电图在内的辅助检查异常,临床医生需除外ACS时应立即检测cTn,患者来院即刻采血测定cTn,推荐对于无法早期确诊的胸痛患者,首次cTn为阴性,可间隔3~6 h或在症状发作10~12 h后复查以排除AMI。出现症状后24 h内至少有1次cTn化验值超过正常上限第99百分位时提示AMI或心肌损伤;解读cTn结果时应综合考虑患者临床表现、胸痛发作时间以及静息12导联ECG的结果。临床实践中不能因等待患者的心肌损伤标志物结果而延误早期治疗。
对于用传统方法不能检测到而用超敏感方法检测到的低水平cTn(<10 μg/L)或把符合要求的检测变异系数≤10%的最小检测值接近第99百分位值的cTn,或把能在健康人群中检测到cTn同时第99百分位值变异系数≤10%,称为hs-cTn。hs-cTn检测范围是传统cTn范围的1/100到1/10,可以更早诊断更微小的心肌损伤,使更多的AMI患者提早明确诊断,发病后3 h以内2次检测对诊断AMI的敏感度可达100%。在临床研究证据基础上,欧洲心脏病学会(ESC)在2011年颁布的NSTE-ACS指南已将hs-cTn作为ACS诊断和危险分层的主要依据。
另外,最近多个国内外研究显示,部分患者外周血中存在cTn自身抗体,AMI患者cTn自身抗体的发生率在10%~20%,自身抗体的干扰能够导致假阴性结果或检出延迟,在临床上需要引起重视。
(2)危险分层与预后判断 高度可疑ACS患者,应根据临床症状、体征、心电图和心肌损伤标志物进行早期危险分层,其中cTn是进行危险分层的首选标志物。临床症状符合ACS的患者,无论CK-MB结果是否升高,cTn峰值超过正常上限第99百分位数,将预示其病死率和缺血事件再发率的危险增加。对于AMI患者,监测cTn动态变化可评估再梗死(由于cTn持续时间较长,在评估再梗死时不如CK-MB)及死亡风险。
2.1.3 诊断临界值目前ESC、美国心脏学会(ACC)/美国心脏协会(AHA)等相关指南均一致推荐使用第99百分位作为cTn的正常上限参考值。此参考值的应用,可以更早诊断微小心肌损伤,具有更高的阴性预测值。
2.1.4 鉴别诊断cTn 不是AMI特有的标志物,cTn 水平升高仅提示心肌细胞受损。在cTn升高但没有动态变化或缺少心肌缺血临床证据时,应考虑其他可能导致心肌坏死的病因,包括急性和慢性充血性心力衰竭、肾功能衰竭、快速性或缓慢性心律失常、心肺复苏术后、急性神经系统疾病、PE和肺动脉高压、心脏挫伤/消融/起搏/复律、浸润性心脏疾病(如淀粉样变性和硬皮病)、炎性疾病(如心肌炎)、触电、中暑、药物毒性、AAD、肥厚型心肌病、甲状腺功能减退、心尖球型综合征、横纹肌溶解伴心肌损伤、脓毒症等严重疾病。
检测方法的改进及更低参考值(第99百分位)的使用,增加了cTn的阳性检出率。结合患者基本资料及心电图,连续观察cTn的动态变化是准确区分AMI和其他病因的比较可靠的方法。
2.2 肌酸激酶同工酶(CK-MB) 2.2.1 概述CK包括同工酶BB、MB和MM。CK-BB主要存在于脑组织中,CK-MM主要存在于骨骼肌中,CK-MB主要存在于心肌细胞的外浆层。当心肌受损后,CK-MB释放入血,4~6 h开始升高,24 h达高峰,持续2~3 d。当不能测定cTn时,可选择测量CK-MB(测定CK-MB质量浓度)。CK-MB的组织特异性低于cTn,因此在大多数情况下推荐连续两次测定CK-MB浓度,以提高诊断准确性。
2.2.2 应用指征(1)早期诊断 CK-MB对判断心肌坏死也有较高的特异性。如果没有条件检测cTn,采用CK-MB作为最佳替换指标。溶栓治疗后梗死相关动脉开通时CK-MB峰值前移(14 h以内)。由于检测窗口期相对较短,CK-MB测定也适于诊断再发心肌梗死。
(2)危险分层及预后判断 如检测到CK-MB升高则预示着心肌坏死,是ACS患者评估中的重要预后指标。尤其是NSTE-ACS患者,入院后CK-MB浓度与30 d病死率呈正相关性,CK-MB浓度低于参考范围上限者30 d病死率为1.8%,浓度为参考范围上限1~2倍者为3.3%,而浓度大于参考范围上限10倍者为8.3%。
2.2.3 诊断临界值CK-MB的诊断界值定义为性别特异参考人群的第99百分位数。
2.2.4 鉴别诊断CK-MB升高还可见于皮肌炎、肌肉劳损、肾功能不全等患者。
2.3 肌红蛋白(MYO) 2.3.1 概述MYO为一种能与氧结合的小分子细胞浆血红素蛋白,广泛存在于骨骼肌、心肌和平滑肌组织,是肌肉内转运和储存氧的蛋白质,约占肌肉蛋白的2%。MYO由153个氨基酸组成,相对分子质量为16 700。主要经肾脏排泄。心肌或横纹肌损伤时,迅速从破损细胞释放到血液中,1~3 h血中浓度迅速上升,6~9 h达峰值,24~36 h恢复到正常水平。肌红蛋白在骨骼肌中的浓度较高,因此对判断心肌损伤的特异性差。但因其相对分子质量小,有早期释放及快速排泄的代谢特点,与cTn或CK-MB联合应用有助于AMI的早期排除诊断。
2.3.2 应用指征(1)早期诊断 对于症状发作6 h以内的患者,除cTn以外,还应该考虑早期心肌坏死标志物。MYO是目前研究最广泛的用于早期诊断和鉴别诊断的标志物。
(2)判断再梗死或梗死范围有否扩展 心肌损伤后血MYO水平6~9 h达高峰,如AMI发生10 h后血MYO再次升高,应考虑发生再梗死或心肌梗死范围扩大。
(3)连续检测可排除急性损伤 由于MYO特异性差,阳性不能单独用于确诊心肌损害,但阴性预测值近100%,因此胸痛发作2~12 h内,检测阴性可排除AMI。
(4)判断心脏手术患者心肌损伤程度和愈合情况 心脏手术后血MYO水平可升高,并与心肌损伤程度成正比,监测血MYO可评估心肌损伤程度。
2.3.3 诊断临界值健康人的血液中MYO很少,男性20~80 μg/L,女性10~70 μg/L。大于100 μg/L即有诊断意义。
2.3.4 鉴别诊断骨骼肌损伤(包括肌肉注射、剧烈运动/创伤、休克、直流电复律及遗传性肌肉疾病等)时也可升高。肌红蛋白与心型脂肪酸结合蛋白的比值(MYO/ H-FABP)有鉴别意义。AMI 期间MYO/ H-FABP比值为5左右,而 AMI 后电除颤可使血MYO/ H-FABP高达60。多发性肌炎、肌营养不良患者血MYO水平可升高,临床疾病研究发现,假性肥大型肌营养不良者血清MYO最高可达1 150 μg/L。严重肾脏疾病时肌红蛋白在血中清除受阻,血浓度升高,循环时间亦相应延长。严重充血性心力衰竭者MYO也可升高。
2.4 心型脂肪酸结合蛋白(H-FABP)FABP广泛存在于各种组织细胞胞质内,有9种亚型,其中H-FABP是心肌细胞中富含的一种小分子可溶性胞浆蛋白质,具有心肌组织特异性,与心肌内长链脂肪酸代谢有关。正常情况下,血浆中H-FABP含量极少(通常<5 μg/L)。当心肌细胞损伤后被迅速大量释放到血液中,AMI发作后20 min开始升高,1~3 h内可以在血中检测出,4~6 h达到峰值,20~30 h内血浆中的浓度恢复正常水平,其释放量与心肌损伤范围成正比。H-FABP主要经肾脏排泄,症状发作后1.5 h尿液浓度升高,肾衰及骨骼肌损伤时可影响H-FABP代谢。
H-FABP早期释放及快速排出的代谢动力学特点与MYO类似,但其心肌特异性明显高于MYO。H-FABP 与 cTn、CK-MB 联合检测,在时间窗上合理互补将是一种临床诊治缺血性心脏病的理想选择。H-FABP释放量与心肌损伤范围成正比,疑似ACS患者,低H-FABP浓度预示低风险,而高血H-FABP浓度预示患者未来发生心血管事件的风险明显增加。但是需要注意的是H-FABP是新型的心肌损伤标志物,与经典的cTn、CK-MB等比较,暂未进入临床指南,其大规模的临床使用还需要累积更多的临床证据。
2.5 缺血修饰白蛋白(IMA)IMA是人血清白蛋白在流经缺血组织时产生的,当缺血导致缺氧、自由基产生、酸中毒等细胞改变后,血清白蛋白N末端Asp-Ala-His-Lys片段发生改变,N乙酰化或缺失,致使白蛋白与过渡金属的结合能力下降,形成IMA,这些变化在数分钟内完成。心肌缺血5~10 min后IMA开始上升,1~2 h达高峰,3~6 h恢复正常,常用于心肌缺血的早期诊断,也可用于心肌缺血后再次发生的诊断。IMA对ACS的检出灵敏度约为cTnT的4倍,是美国食品药品管理局(FDA)认可的第一个检测心肌缺血的生物标志物,但不是心肌损伤标志物。IMA具有高敏感度、高阴性预测值的特点,但特异性较低。IMA能否用于急性胸痛患者的危险分层目前存在争议。IMA升高也见于休克、终末期肾病、肿瘤、急性感染、肝硬化、遗传缺陷所致白蛋白N端氨基酸缺失等。
3 心脏功能生物标志物利钠肽作为心脏功能生物标志物不仅在心力衰竭早期诊断、预后判断方面具有重要价值,对急性胸痛的鉴别诊断、危险分层和预后判断等方面也具有重要作用。利钠肽是一个大家族,主要成员包括心房利钠肽(atrial natriuretic peptide,ANP)、脑钠肽(BNP)、C-利钠肽(C-type natriuretic peptide,CNP),以及新近发现的N-心钠素、尿钠素、心室利钠肽等。其中,BNP和氨基末端脑钠肽前体(N-terminal pro-B-type natriuretic peptide,NT-proBNP)是目前最重要的心脏功能生物标志物。
3.1 概述BNP是一个由32个氨基酸组成的多肽,含一个17个氨基酸组成的环状结构,是由心脏分泌的短肽激素。在心肌细胞合成的134个氨基酸的Prepro-BNP,在进入血循环后降解产生含108个氨基酸的BNP前体(proBNP),proBNP在内切酶的作用下形成一个具有生物活性的BNP和一个无活性的76个氨基酸片段NT-proBNP。刺激BNP释放的主要因素是心肌张力的增加。BNP的合成、分泌释放调节主要在基因表达水平。BNP在外周血中的生物半衰期短于NT-proBNP,在外周血中的浓度也比NT-proBNP低。
刺激BNP和ANP释放的主要因素是心肌张力的增加,但神经体液因素如血管紧张素Ⅱ、内皮素等可能也起一定作用。利钠肽的主要生理作用包括:增加尿钠排出量和尿量,扩张血管,抗细胞增殖,对抗内皮素和肾素-血管紧张素-醛固酮系统等。
3.2 应用指征 3.2.1 临床诊断BNP诊断心力衰竭敏感且特异,如果BNP <100 pg/mL,心衰的可能性极小,其阴性预测值为90%;如果BNP>500 pg/mL,心衰的可能性极大,其阳性预测值为90%。
基础和临床研究均证实急性心肌缺血、缺氧可以导致利钠肽的释放。有研究显示,BNP≥100 pg/mL诊断AMI的特异性为68.9%,敏感性为70.8%,阳性预测值为22.7%,阴性预测值为94.8%。BNP或NT-proBNP敏感性和特异性不足以诊断心肌缺血,无症状的左心功能不全、PE等也可导致其升高。
3.2.2 危险分层和预后判断BNP和(或)NT-proBNP可预测心衰患者长期死亡风险,对心衰诊断具有高特异性和敏感性,与心衰严重程度呈正相关。NT-proBNP >5 000 pg/mL提示心衰患者短期死亡风险较高;>1 000 pg/mL提示长期死亡风险较高。动态监测BNP或NT-proBNP可作为心衰疗效评估的辅助手段,BNP和(或)NT-proBNP水平降幅≥30%可作为治疗有效的标准。心衰患者住院期间BNP和(或)NT-proBNP水平显著升高或居高不降,或降幅<30%,均预示再住院和死亡风险增加。
2014年AHA/ACC NSTE-ACS指南中指出,BNP或NT-proBNP可用于可疑ACS患者的危险分层。研究发现,在ACS患者中BNP浓度与短期和长期病死率明显相关,BNP浓度低于四分位数的患者病死率为1%,而高于四分位数的患者病死率为15%。BNP或NT-proBNP是心力衰竭发展或存在左室收缩功能受损的强有力的预测因素。BNP也可以协助判断胸痛患者的预后,BNP或NT-proBNP升高与PE患者严重不良事件和死亡相关,在检测右室功能方面BNP比NT-proBNP敏感性和特异性更高。
3.2.3 临床决策对于存在呼吸困难的胸痛患者,BNP或NT-proBNP的检查有助于临床决策的制定。有研究显示,对ACS患者,BNP或NT-proBNP升高者早期介入治疗受益非常明显,进行强化他汀类药物治疗有助于降低病死率和心功能不全的发生。利钠肽随时间推移明显降低者预后良好。
3.3 诊断临界值BNP<100 pg/mL,NT-proBNP<300 pg/mL为排除急性心衰的临界值;诊断急性心衰时NT-proBNP水平应根据年龄和肾功能不全进行分层:50岁以下的成人血浆NT-proBNP浓度>450 pg/mL,50岁以上血浆浓度>900 pg/mL,75岁以上应大于1 800 pg/mL,肾功能不全(肾小球滤过率<60 mL/min)时应>1 200 pg/mL。见表 1。
| 指标 | 年龄 | 排除心衰 | 可能存在心衰(需考虑其他因素影响) | 存在心衰 |
| BNP | 全部 | <100 | 100~500 | >500 |
| NT-proBNP | <50岁 | <300 | 300~450 | >450 |
| 50~75岁 | <300 | 450~900 | >900 | |
| >75岁 | <300 | 900~1800 | >1800 |
BNP和NT-proBNP在不同的测定时间,就诊即刻、症状发作24 h内或2~5 d后测定均有预测价值,其浓度随着时间而改变,其评估及预测价值与采血测定时间有关,连续监测能提供更多信息。
3.4 鉴别诊断BNP和NT-proBNP升高见于多种心血管疾病,包括:①心肌病变(心肌肥厚,心肌纤维化,心肌浸润性病变等);②心脏瓣膜病变;③缺血性心脏病;④心律失常(心房纤颤或房扑);⑤心包疾病(心包积液或填塞,缩窄性心包炎);⑥先心病。BNP和NT-proBNP升高也见于一些非心血管疾病,如急性呼吸窘迫综合征、睡眠呼吸暂停综合征、贫血、败血症、烧伤、卒中、肾功能异常和休克等。需结合临床评估,根据患者病情作出综合性评价。
4 止凝血生物标志物 4.1 D-二聚体 4.1.1 概述D-二聚体是纤维蛋白单体经活化因子Ⅷ交联后,再经纤溶酶水解所产生的一种特异性降解产物,包含γ链相连2个D片段的终末产物之一。D-二聚体是最简单的纤维蛋白降解产物,在体内起着调节纤溶-凝血间平衡的重要作用,因此D-二聚体的生成和其水平增高反映了血浆中凝血系统和纤溶系统的激活,临床上视D-二聚体为体内高凝状态和纤溶亢进的分子标志物。
4.1.2 应用指征(1)排除PE与深静脉血栓(deep venous thrombosis,DVT)
肺血管造影是PE诊断的金标准,但该法为侵入性操作,增加患者痛苦和风险,且价格较高。D-二聚体检测诊断PE的阴性预测值及敏感性极高,可作为PE诊断的首选过筛试验。D-二聚体<5 00 μg/mL的可疑病例,如无法进行影像学检查,应予以动态检测D-二聚体水平。Yamakit等报道将D-二聚体600 μg/mL作为排除DVT的临界值。多项临床研究证实,依据年龄调整D-二聚体临界值的方法能可靠地排除PE以及深静脉血栓的患者。依据年龄调整D-二聚体的临界值方法分为两种方式,第一种方式是年龄大于50岁时,D-二聚体临界值为年龄乘以10;第二种方式是年龄大于60岁时,D-二聚体临界值固定为750 μg/mL。
(2)排除AAD
AAD是急诊高危胸痛和猝死的常见原因,早期诊断和治疗能够降低患者的病死率,减少医疗风险,高敏感度的D-二聚体检测可用于AAD的筛查和排除,研究发现D-二聚体质量浓度<500 μg/mL作为临界值,其检测敏感度97%,阴性预测值96%,特异性56%,阳性预测值60%,D-二聚体检测用于排除AAD的临床价值与静脉血栓栓塞症的价值基本一致。
(3)ACS的病情评估
有研究发现,冠状动脉病变程度及类型不同,其血浆D-二聚体水平不同,复杂病变组高于简单病变组。D-二聚体水平在不同冠心病类型中的改变可能为该病的早期诊断提供依据。
4.1.3 鉴别诊断研究表明在严重感染后出现休克、DIC之前,血液即存在高凝状态及微血管内凝血。高敏感性的D-二聚体检测有助于脓毒症的诊断、严重程度分级和预后评估。
D-二聚体在临床上被广泛应用,除以上提到的疾病外,在糖尿病、急性重症胰腺炎、系统性红斑狼疮、类风湿关节炎、创伤等疾病中也可见D-二聚体升高,且含量一般随病情严重程度及治疗情况发生相应变化。因此,动态监测D-二聚体在诊治急危重症和对病情转归评估中具有较高的临床价值。
5 胸痛相关炎性生物标志物 5.1 C-反应蛋白(CRP)CRP是应用最广泛的炎症标志物。在炎症因子的刺激下,由肝细胞合成。在感染或创伤发生4~6 h内就可升高,且时间较长。CRP本身也是一种促炎因子,它可促进粘附分子的表达以及诱导炎症细胞的合成。在胸痛患者中,对比非冠脉病变所导致的胸痛,CRP的升高可在很大程度上预测急性冠脉事件的发生,且与CK-MB的增高平行。在AMI的患者中,CRP高峰可持续48 h,且高峰值与心梗面积有关。同时CRP>7.9 mg/L时还预示着AMI后心脏收缩及舒张功能障碍,左室充盈压力的升高,远期心衰发生率及病死率的增高。研究还发现CRP在不稳定心绞痛患者中也可明显升高,它可预测心血管相关事件的不良结局,如死亡、心衰、再发缺血等,但其敏感性和特异性不高。
5.2 超敏C反应蛋白(hypersensitive C-reactive protein,hs-CRP)应用新技术提高CRP分析的灵敏度,检测出低水平(0.1~10 mg/L)的CRP,称为hs-CRP。2003年AHA以及疾病控制和预防中心已经将hs-CRP作为ACS风险评估的重要手段。一项纳入117例胸痛患者的临床研究发现,当hs-TnT>0.7 ng/L同时hs-CRP>2 mg/L时,影像学发现超过92%的患者存在相应的心脏血管及功能障碍,故同时测量两种标志物可识别冠脉疾病以及心功能不全。当ACS发生后,hs-CRP明显升高,其可与cTn及CK-MB一起作为早期AMI或不稳定型心绞痛患者的诊断标准。在稳定型心绞痛中,hs-CRP也可以作为不良冠脉事件的预测因子。然而hs-CRP同CRP一样缺乏特异性,不能以单一指标来诊断ACS。
5.3 髓过氧化物酶(MPO)MPO在急性炎症期由巨噬细胞及中性粒细胞释放,不仅仅是稳定型缺血性心脏病的生物标志物,还是急性心肌坏死的标志物,MPO升高提示冠状动脉易损斑块炎症反应。研究发现,MPO>20.34 ng/mL预测冠心病患者2年内心梗的发生率明显升高;在AMI患者中发现,MPO的增加(MPO>55 ng/mL)预示左室收缩功能下降,与NT-proBNP升高相一致。在一项纳入604例因胸痛而就诊的急诊患者研究中发现,由于MPO在心肌坏死2 h内就可以升高,因而对于cTnI<0.1 ng/mL的患者,也可以作为AMI的预测因子;同时,研究还发现MPO可以独立预测30 d及6 个月的不良冠脉事件的发生,因而MPO的检测可以识别可能的高危心肌缺血性胸痛患者。
5.4 降钙素原(procalcitonin,PCT)PCT是降钙素的前体,是由116个氨基酸组成的多肽。正常情况下由甲状腺滤泡旁细胞产生,在健康人血中浓度极低,常<0.1 ng/mL。微生物感染时则主要由甲状腺外的组织,如肝、肾、胰腺、脂肪细胞等产生。2条途径可导致PCT升高,一是微生物毒素(尤其革兰阴性杆菌的内毒素)直接刺激产生,二是由微生物激发的炎症因子(如IL-1,IL-6、 TNF-α等)间接刺激产生。就急性胸痛患者早期的诊断与鉴别诊断而言,PCT的作用不大,不应作为ACS、PE、AAD等高危胸痛早期常规检测的标志物。研究表明,PCT在ACS中均无明显升高,只有在并发心源性休克的STEMI才会有轻度升高。但PCT有助于早期检出急性胸痛的感染并发症,对于各种可能在后期并发感染的胸痛,建议动态监测PCT,以便及时发现感染和指导抗菌素治疗。
5.5 磷脂酶A2(phospholipaseA2,PLA2)PLA2是一种能催化磷脂甘油分子上二位酰基的水解酶,所产生的脂质介质在炎症和组织损伤过程中发挥重要作用。人类几乎所有的细胞均含PLA2,哺乳类细胞外PLA2为正常生理分泌物。在病理状态下,激活的单核细胞、巨噬细胞及中性粒细胞分泌释放大量PLA2,是重要的炎症反应和组织损伤标志物之一。其中,脂蛋白相关性PLA2(Lp-PLA2)与冠心病关系密切。Lp-PLA2由血管内膜巨噬细胞及泡沫细胞产生,绝大多数的Lp-PLA2与低密度脂蛋白结合,能水解其上的氧化卵磷脂,使之生成溶血卵磷脂和氧化型游离脂肪酸,后两者是促炎介质,损伤血管内皮、引起单核细胞浸润、泡沫细胞沉积,促进粥样斑块形成和发展,导致斑块易损,甚至破裂。Lp-PLA2主要用于冠心病的危险分层,其可作为评估动脉粥样硬化进程中炎症反应的标志物,尤其可作为血管特异性炎症的危险因子。动脉粥样硬化血栓形成事件复发的高危患者中,有条件可进行Lp-PLA2检查,以预测冠脉事件发生的风险。
5.6 大内皮素-1 (big-endothelin-1,Big ET-1)内皮素-1(endothelin-1,ET-1)是一种由21个氨基酸组成的具有强大缩血管活性的多肽,其家族内还有ET-2和ET-3两种异构体,以ET-1为主要,广泛分布于组织和细胞,是一种自分泌和旁分泌激素。ET-1由其前体Big ET-1在内皮素转化酶(endothelin-converting enzyme,ECE)作用下产生,由于ET-1循环浓度低,在血浆中的半衰期短(大约1.5 min),且稳定性差,所以难以保证测量的准确度。而Big ET-1在血浆中的半衰期是30 min,同时又是稳定肽,作为一种循环标志物具有更高的敏感度。多项研究业已证实肺动脉高压患者血浆中Big ET-1水平显著升高。Big ET-1是参与ACS发生、发展的重要递质,其水平的升高促发动脉粥样硬化的进程。Big ET-1可对心功能不全患者进行心脏不良事件再发生的危险分层和预后评估。有研究提示Big ET-1的含量>4.16 pmol/L的心功能不全患者,应作为心衰后心血管不良事件再发生的高危人群,并给予重点随访和治疗。
6 急性胸痛生物标志物联合检测在指导急诊胸痛临床决策中的作用及意义急性非创伤性胸痛病因繁多、病程复杂多样,但根据疾病特点、危险程度及救治需求,可将其归纳为三大类:①ACS;②致命性非心肌缺血性胸痛(PE、AAD、急性张力性气胸等);③非致命性非心肌缺血性胸痛(胃食管反流、肋软骨炎、带状疱疹等)。急诊医师面对胸痛患者时,应强调“急诊思维”而不是“心血管思维”,即在全面考虑胸痛可能病因的基础上,结合病史、临床表现、ECG及生物标志物检测,有针对性地对患者进行早期诊断、鉴别诊断和危险分层,快速地将急性胸痛患者有序分拣入上述三类疾病中,实现高危患者早期救治和低危患者合理分流。
所有急诊接诊的急性非创伤胸痛患者,均应进行病史采集(简短、有针对性)、体格检查及静息12导联ECG。如果患者存在ACS、PE及AAD等高危胸痛的危险因素及发病特征,且出现以下三种情况中的至少一种时,即血流动力学不稳定、心电活动不稳定或提示心力衰竭,应及时对症处理且尽早联合检测心肌损伤标志物(主要为cTn)、BNP/NT-proBNP及D-二聚体;如果没有上述三种情况,可根据具体病因考虑,有针对性的检测一类或两类指标完成疾病的诊断或排除诊断,确诊后再联合检测其他指标实现危险分层和预后判断。见图 1。
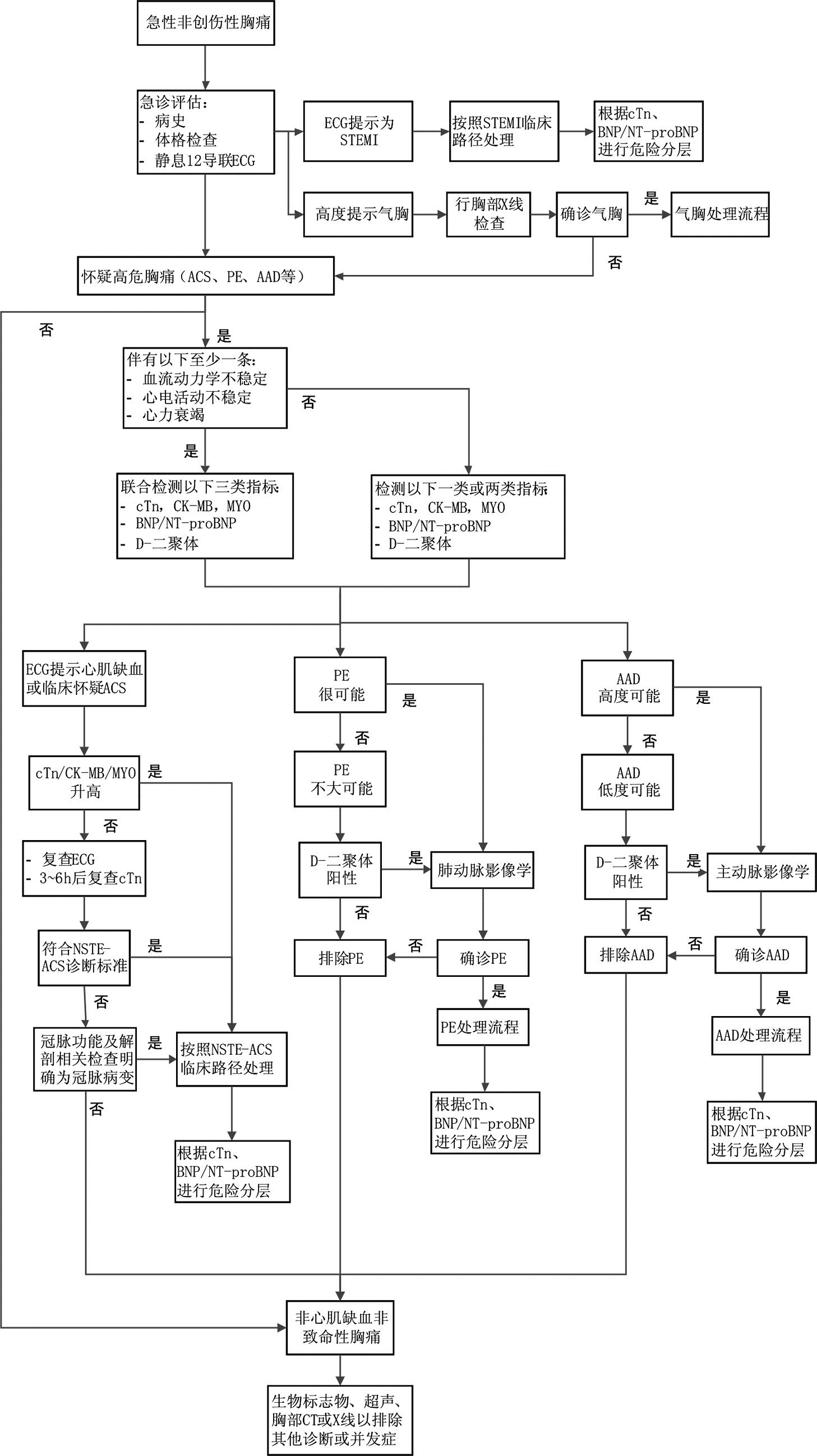 |
| 图 1 急性胸痛生物标志物联合检测流程图 |
缺血性心脏病(主要是ACS)是导致急性致命性胸痛的主要原因,且诊断方法简单明确,应避免漏诊、尽早诊治。其中入院静息12导联ECG如提示为STEMI,则按照STEMI临床路径处理,无需等待心肌损伤标志物的结果。由于代谢动力学及检测方法的限制,cTn的敏感性依赖于心肌缺血的持续时间以及从发病到检测的时间,因此,在发病6 h以内的胸痛患者,联合检测CK-MB及MYO具有更高的敏感性和阴性预测值,可以有效地提高AMI的检出和排除率。且由于cTn在血中持续时间较长,难以鉴别近期内再梗死,建议联合检测CK-MB或MYO提高再梗死的检出率。
另外,标志物的动态检测在提高AMI检出和排除诊断方面具有重要意义。2012年心肌梗死全球统一定义中明确指出,心梗诊断的必要条件是:
动态检测心脏生物标志物(主要为cTn)水平升高和(或)下降,至少有一个检测值超过参考值上限(URL)第99 百分位。且2014年AHA / ACC NSTE-ACS管理指南中推荐,初次ECG无心肌缺血诊断价值且cTn阴性时,应注意复查ECG,且3~6 h后动态检测cTn,如符合NSTE-ACS诊断标准按照NSTE-ACS临床路径处理。如多次ECG及cTn均为阴性,可考虑行冠脉功能及解剖相关检查最终排除ACS。
心脏生物标志物不仅用来明确AMI的诊断,也成为评估再发临床事件风险和评价干预治疗效果的便捷的非侵入性手段。随着对ACS发病机制的深入了解和治疗方法的不断改进,多种标志物联合检测能够依据不同的病理生理机制,反映心肌坏死、心脏功能、出凝血危险和炎症等各种过程,增强现有工具对临床决策和风险分层的能力。如对ACS患者联合检测BNP/NT-proBNP,有助于明确其是否并发心力衰竭,以及心衰的严重程度及预后;对于怀疑出血风险增加的患者,联合凝血功能及血栓弹力图检测可明确患者的出凝血状态及血小板功能,指导抗栓药物方案的选择;如患者出现发热,可加查PCT、CRP等指标协助诊断是否存在感染。有研究表明,cTnT、NT-proBNP和CRP三者联合策略较单一标志物检测能更好地进行危险分层,其中两项或三项指标同时升高则预示NSTE-ACS患者的6个月不良事件风险增加。
6.2 致命性非心肌缺血性胸痛急诊常见的致命性胸痛除ACS外,还有PE、AAD及急性张力性气胸等。除依靠详细的病史、症状、体征及ECG外,确诊一般依靠CTA、胸部X线或/和超声等影像学检查,而生物标志物联合检测则是鉴别诊断、危险分层与预后评估的重要工具。
急诊医师在面对这类急性胸痛患者时,应首先考虑各种高危病因的可能性,区分出高度可疑和中低度可疑的患者,有针对性的对高度可疑患者进行确诊性影像学检查,争取治疗的黄金时间;将中低度可疑患者合理分流入“非致命性非心肌缺血性胸痛”,节约医疗资源。2014 年ESC 急性PE诊治指南推荐,应用Wells评分对不伴有休克或低血压的疑似PE患者进行可能性评估(见表 2),Wells评分≤4的“不大可能”患者,如果D-二聚体为阴性,可无需进行影像学检查,直接排除PE;Wells评分>4的“很可能”患者,无需关注D-二聚体结果,直接进行螺旋CT或血管造影检查来明确诊断。2014年ESC主动脉疾病诊断和治疗指南推荐,根据评分工具识别急性胸痛患者AAD的高度及低度可能性(见表 3),在临床低度可能的患者,D-二聚体阴性可以认为排除夹层;高度可能的患者,D-二聚体检查无额外意义,不建议常规检查。
| 项目 | 分值 |
| 深静脉血栓的临床症状和体征(下肢肿胀和深静脉触痛) | 3分 |
| PE的可能性大于其他疾病 | 3分 |
| 心率大于100次/min | 1.5分 |
| 最近4周内有手术史或制动史 | 1.5分 |
| 既往有深静脉血栓史或PE史 | 1.5分 |
| 咯血 | 1分 |
| 恶性肿瘤史(正在治疗或近6个月内治疗过或姑息治疗) | 1分 |
| PE Wells评分法 | 总分 |
| 低度临床可能 | <2分 |
| 中度临床可能 | 2~6分 |
| 高度临床可能 | >6分 |
| PE两分类Wells评分法 | 总分 |
| 不大可能 | ≤4分 |
| 很可能 | >4分 |
| 项目 |
| 注:具备某高危特征类别中的任意一条,即为满足该特征类别,满足一个特征类别即记1分,最高为具备三个高危特征类别每类别中的任意一条以上,则满足3个类别,记3分。0~1分为低度可能,2~3分为高度可能 |
| 高度风险基础疾病或情况 |
| 马凡综合征(或其他结缔组织病) |
| 主动脉疾病家族史 |
| 已知主动脉瓣疾病 |
| 已知胸主动脉瘤 |
| 曾行主动脉操作(包括外科手术) |
| 高度风险疼痛性质 |
| 胸背或腹部疼痛具有以下特点 |
| 突发疼痛 |
| 疼痛剧烈 |
| 疼痛呈撕裂样、尖锐性疼痛 |
| 高度风险体格检查 |
| 有灌注缺损的证据 |
| 脉搏短绌 |
| 四肢收缩压差 |
| 局灶神经病变体征(伴疼痛) |
| 主动脉反流性杂音(新发或伴疼痛) |
| 低血压或休克 |
在PE患者预后判断方面,D-二聚体升高与患者短期病死率增加有关;低水平BNP和NT-proBNP可预测患者短期转归良好,阴性预测值较高;血浆cTn升高提示PE预后不良。作为心肌损伤的早期标志物,H-FABP也发现对PE的预后有预测价值。
因高危胸痛中张力性气胸的诊断简单明了,一般无需标志物检测,病史和查体即具有很强的提示意义,如患者为男性青壮年瘦高体型或患有慢支、肺气肿、肺结核者,突发一侧胸痛伴憋喘,一侧呼吸音明显降低甚至消失可高度怀疑气胸的可能,应尽快行胸部X线片检查明确诊断。
6.3 非致命性非心肌缺血性胸痛非致命性非心肌缺血性胸痛,如胸膜炎、胃食管反流、肋软骨炎、带状疱疹等,多依靠典型的临床表现以及排除其他致命性疾病后得以诊断。可根据具体的临床实际情况选择需要检测的生物标志物。
综上所述,生物标志物合理的联合检测,可以为急性胸痛患者的诊疗工作提供更好的客观依据,有利于提高疾病诊断的敏感性和特异性,提高危险分层及预后判断的能力,避免漏诊和误诊,同时减少不必要的昂贵检查,缩短留观时间,减少医疗资源的浪费。当然,由于急诊工作的特殊性和急迫性,并不是每一位患者都需要同时测定上述多种生物标志物,急诊医师应根据患者的临床表现和疾病的发展阶段,结合每种标志物的代谢动力学特点及临床意义,有针对性的进行标志物联合应用,并酌情进行相应的影像学或其他进一步检查。
专家组成员(按姓名汉语拼音排序) :陈锋、陈凤英、蔡卫东、陈晓辉、曹钰、柴艳芬、陈玉国、楚英杰、方邦江、封启明、干建新、郭树彬、何新华、黄亮、李春盛、李莉、廖晓星、林兆奋、刘励军、刘晓亮、刘志、卢中秋、吕传柱、马青变、马岳峰、潘曙明、裴红红、乔佑杰、商德亚、孙树印、童朝阳、王秀杰、谢苗荣、徐杰、杨光田、杨亚非、于学忠、曾红、曾红科、詹红、张长乐、张国强、张劲松、赵敏、郑亚安、周长勇、周亚雄、朱继红
| [1] | National Hospital Ambulatory Medical Care Survey:2010 Emergency Department Summary Tables. http://www.cdc.gov/nchs/data/ahcd/nhamcs_emergency/2010_ed_web_tables.pdf . Accessed April 5, 2015. |
| [2] | 薛军,韩占红,王明晓,等. 北京市急诊胸痛的病因学调查分析[J]. 中国综合临床, 2012,28(10):1042-1046. |
| [3] | Amsterdam EA, Kirk JD, Bluemke DA, et al. Testing of low-risk patients presenting to the emergency department with chest pain:ascientific statement from the American Heart Association[J]. Circulation, 2010,122(17):1756-1776. |
| [4] | “胸痛中心”建设中国专家共识组. “胸痛中心”建设中国专家共识[J]. 中国心血管病研究, 2011,9(5):325-334. |
| [5] | Farah CS, Reinach FC. The troponin complex and regulation of muscle contraction[J]. FASEB J, 1995,9(9):755-767. |
| [6] | Morrow DA, Cannon CP, Jesse RL, et al. National Academy of Clinical Biochemistry Laboratory Medicine Practice Guidelines: Clinical characteristics and utilization of biochemical markers in acute coronary syndromes[J]. Circulation, 2007,115(13):e356-375. |
| [7] | O’ Gara PT, Kushner FG, Ascheim DD, et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction:areport of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines[J]. Circulation, 2013,127(4):e362-425. |
| [8] | 中华医学会心血管病学分会,中华心血管病杂志编辑委员会. 急性ST段抬高型心肌梗死诊断和治疗指南[J]. 中华心血管病杂志, 2015,43(5):380-393. |
| [9] | Eriksson S, Hellman J, Pettersson K. Autoantibodies against cardiac troponins[J].NEnglJMed, 2005,352(1):98-100. |
| [10] | Panteghini M, Pagani F, Yeo KT, et al. Evaluation of imprecision for cardiac troponin assays at low-range concentrations[J]. Clin Chem, 2004,50(2):327-332. |
| [11] | Vasile VC, Saenger AK, Kroning JM, et al. Biological and analytical variability ofanovel high-sensitivity cardiac troponinTassay[J]. Clin Chem, 2010,56(7):1086-1090. |
| [12] | Weber M, Bazzino O, Navarro EJL, et al. Improved diagnostic and prognostic performance ofanew high-sensitive troponinTassay in patients with acute coronary syndrome[J]. Am Heart J, 2011,162(1):81-88. |
| [13] | Hamm CW, Bassand JP, Agewall S, et al. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: The Task Force for the management of acute coronary syndromes (ACS) in patients presenting without persistent ST-segment elevation of the European Society of Cardiology (ESC)[J]. Eur Heart J, 2011,32(23):2999-3054. |
| [14] | Than M, Cullen L, Aldous S, et al. 2-Hour accelerated diagnostic protocol to assess patients with chest pain symptoms using contemporary troponins as the only biomarker: the ADAPT trial[J].JAm Coll Cardiol, 2012,59(23):2091-2098. |
| [15] | Reichlin T, Hochholzer W, Bassetti S, et al. Early diagnosis of myocardial infarction with sensitive cardiac troponin assays[J].NEnglJMed, 2009,361(9):858-867. |
| [16] | Keller T, Zeller T, Peetz D, et al. Sensitive troponinIassay in early diagnosis of acute myocardial infarction[J].NEnglJMed, 2009,361(9):868-877. |
| [17] | Mills NL, Lee KK, McAllister DA, et al. Implications of lowering threshold of plasma troponin concentration in diagnosis of myocardial infarction: cohort study[J]. BMJ, 2012,344:e1533. |
| [18] | Bonaca M, Scirica B, Sabatine M, et al. Prospective evaluation of the prognostic implications of improved assay performance withasensitive assay for cardiac troponin I[J].JAm Coll Cardiol, 2010,55(19):2118-2124. |
| [19] | Celik S, Giannitsis E, Wollert KC, et al. Cardiac troponinTconcentrations above the 99th percentile value as measured byanew high-sensitivity assay predict long-term prognosis in patients with acute coronary syndromes undergoing routine early invasive strategy[J]. Clin Res Cardiol, 2011,100(12):1077-1085. |
| [20] | Alexander JH, Sparapani RA, Mahaffey KW, et al. Association between minor elevations of creatine kinase-MB level and mortality in patients with acute coronary syndromes without ST-segment elevation. PURSUIT Steering Committee. Platelet Glycoprotein IIb/IIIa in Unstable Angina: Receptor Suppression Using Integrilin Therapy[J]. JAMA, 2000,283(3):347-353. |
| [21] | Tanaka T, Hirota Y, Sohmiya K, et al. Serum and urinary human heart fatty acid-binding protein in acute myocardial infarction[J]. Clin Biochem, 1991,24(2):195-201. |
| [22] | Chan CP, Sanderson JE, Glatz JF, et al.Asuperior early myocardial infarction marker. Human heart-type fatty acid-binding protein[J].ZKardiol, 2004,93(5):388-397. |
| [23] | Seino Y, Tomita Y, Takano T, et al. Office cardiologists cooperative study on whole blood rapid panel tests in patients with suspicious acute myocardial infarction: comparison between heart-type fatty acid-binding protein and troponinTtests[J]. Circ J, 2004,68(2):144-148. |
| [24] | Orak M, Ustundag M, Guloglu C, et al. The role of the heart-type fatty acid binding protein in the early diagnosis of acute coronary syndrome and its comparison with troponinIand creatine kinase-MB isoform[J]. AmJEmerg Med, 2010,28(8):891-896. |
| [25] | Kim KS, Lee HJ, Kim K, et al. Heart-type fatty acid binding protein as an adjunct to cardiac troponin-I for the diagnosis of myocardial infarction[J].JKorean Med Sci, 2011,26(1):47-52. |
| [26] | Kilcullen N, Viswanathan K, Das R, et al. Heart-type fatty acid-binding protein predicts long-term mortality after acute coronary syndrome and identifies high-risk patients across the range of troponin values[J].JAm Coll Cardiol, 2007,50(21):2061-2067. |
| [27] | Viswanathan K, Kilcullen N, Morrell C, et al. Heart-type fatty acid-binding protein predicts long-term mortality and re-infarction in consecutive patients with suspected acute coronary syndrome who are troponin-negative[J].JAm Coll Cardiol, 2010,55(23):2590-2598. |
| [28] | Collinson PO, Gaze DC, Bainbridge K, et al. Utility of admission cardiac troponin and “Ischemia Modified Albumin” measurements for rapid evaluation and rule out of suspected acute myocardial infarction in the emergency department[J]. Emerg Med J, 2006,23(4):256-261. |
| [29] | Peacock F, Morris DL, Anwaruddin S, et al. Meta-analysis of ischemia-modified albumin to rule out acute coronary syndromes in the emergency department[J]. Am Heart J, 2006,152(2):253-262. |
| [30] | Keating L, Benger JR, Beetham R, et al. The PRIMA study: presentation ischaemia-modified albumin in the emergency department[J]. Emerg Med J, 2006,23(10):764-768. |
| [31] | Yiadom MY. Acute coronary syndrome clinical presentations and diagnostic approaches in the emergency department[J]. Emerg Med Clin North Am, 2011,29(4):689-697, v. |
| [32] | Lindsell CJ, Anantharaman V, Diercks D, et al. The Internet Tracking Registry of Acute Coronary Syndromes (i*trACS):amulticenter registry of patients with suspicion of acute coronary syndromes reported using the standardized reporting guidelines for emergency department chest pain studies[J]. Ann Emerg Med, 2006,48(6):666-677. |
| [33] | Yandle TG. Biochemistry of natriuretic peptides[J].JIntern Med, 1994,235(6):561-576. |
| [34] | Boomsma F, van den Meiracker AH. Plasma A- and B-type natriuretic peptides: physiology, methodology and clinical use[J]. Cardiovasc Res, 2001,51(3):442-449. |
| [35] | Sabatine MS, Morrow DA, de Lemos JA, et al. Acute changes in circulating natriuretic peptide levels in relation to myocardial ischemia[J].JAm Coll Cardiol, 2004,44(10):1988-1995. |
| [36] | Staub D, Nusbaumer C, Zellweger MJ, et al. Use of B-type natriuretic peptide in the detection of myocardial ischemia[J]. Am Heart J, 2006,151(6):1223-1230. |
| [37] | Bassan R, Potsch A, Maisel A, et al. B-type natriuretic peptide:anovel early blood marker of acute myocardial infarction in patients with chest pain and no ST-segment elevation[J]. Eur Heart J, 2005,26(3):234-240. |
| [38] | Amsterdam EA, Wenger NK, Brindis RG, et al. 2014 AHA/ACC Guideline for the Management of Patients with Non-ST-Elevation Acute Coronary Syndromes:areport of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines[J].JAm Coll Cardiol, 2014,64(24):e139-228. |
| [39] | de Lemos JA, Morrow DA, Bentley JH, et al. The prognostic value of B-type natriuretic peptide in patients with acute coronary syndromes[J].NEnglJMed, 2001,345(14):1014-1021. |
| [40] | Heeschen C, Hamm CW, Mitrovic V, et al. N-terminal pro-B-type natriuretic peptide levels for dynamic risk stratification of patients with acute coronary syndromes[J]. Circulation, 2004,110(20):3206-3212. |
| [41] | Haaf P, Reichlin T, Corson N, et al. B-type natriuretic peptide in the early diagnosis and risk stratification of acute chest pain[J]. AmJMed, 2011,124(5):444-452. |
| [42] | ICSI. Diagnosis and Treatment of Chest Pain and Acute Coronary Syndrome (ACS)https://www.icsi.org/_asset/ydv4b3/ACS-Interactive1112b.pdf,2012. |
| [43] | Lega JC, Lacasse Y, Lakhal L, et al. Natriuretic peptides and troponins in pulmonary embolism:ameta-analysis[J]. Thorax, 2009,64(10):869-875. |
| [44] | James SK, Lindback J, Tilly J, et al. Troponin-T and N-terminal pro-B-type natriuretic peptide predict mortality benefit from coronary revascularization in acute coronary syndromes:aGUSTO-IV substudy[J].JAm Coll Cardiol, 2006,48(6):1146-1154. |
| [45] | “D-二聚体检测”急诊临床应用专家共识[J]. 中华急诊医学杂志, 2013,22(8):827-836. |
| [46] | Goldhaber SZ, Bounameaux H. Pulmonary embolism and deep vein thrombosis[J]. Lancet, 2012,379(9828):1835-1846. |
| [47] | Ng AC, Chung T, Yong AS, et al. Long-term cardiovascular and noncardiovascular mortality of 1023 patients with confirmed acute pulmonary embolism[J]. Circ Cardiovasc Qual Outcomes, 2011,4(1):122-128. |
| [48] | Yang Y, Liang L, Zhai Z, et al. Pulmonary embolism incidence and fatality trends in chinese hospitals from 1997 to 2008:amulticenter registration study[J]. PLoS One, 2011,6(11):e26861. |
| [49] | 钟海英,周贞学. 检测血浆D-二聚体、FDP、TNT对心肌梗死病人的临床意义[J]. 中国实验诊断学, 2010,14(4):577-579. |
| [50] | De Servi S, Mariani M, Mariani G, et al. C-reactive protein increase in unstable coronary disease cause or effect?[J].JAm Coll Cardiol, 2005,46(8):1496-1502. |
| [51] | Frangogiannis NG, Smith CW, Entman ML. The inflammatory response in myocardial infarction[J]. Cardiovasc Res, 2002,53(1):31-47. |
| [52] | Sharma S, Ghalaut VS, Dixit R, et al. Microalbuminuria and C-reactive protein asapredictor of coronary artery disease in patients of acute chest pain[J].JCardiovasc Dis Res, 2013,4(1):37-39. |
| [53] | James SK, Oldgren J, Lindback J, et al. An acute inflammatory reaction induced by myocardial damage is superimposed onachronic inflammation in unstable coronary artery disease[J]. Am Heart J, 2005,149(4):619-626. |
| [54] | Suleiman M, Khatib R, Agmon Y, et al. Early inflammation and risk of long-term development of heart failure and mortality in survivors of acute myocardial infarction predictive role of C-reactive protein[J].JAm Coll Cardiol, 2006,47(5):962-968. |
| [55] | Shacham Y, Topilsky Y, Leshem-Rubinow E, et al. Association between C-reactive protein level and echocardiography assessed left ventricular function in first ST-segment elevation myocardial infarction patients who underwent primary coronary intervention[J].JCardiol, 2014,63(6):402-408. |
| [56] | Aldous SJ. Cardiac biomarkers in acute myocardial infarction[J]. IntJCardiol, 2013,164(3):282-294. |
| [57] | Schlett CL, Truong QA, Ahmed W, et al. High-sensitivity troponinTand C-reactive protein to identify patients without cardiac structural and functional abnormalities as assessed by cardiac CT and SPECT imaging: can biomarkers predict cardiac health?[J]. IntJCardiovasc Imaging, 2013,29(4):865-873. |
| [58] | Amanvermez R, Acar E, Gunay M, et al. Hsp 70, hsCRP and oxidative stress in patients with acute coronary syndromes[J]. BosnJBasic Med Sci, 2012,12(2):102-107. |
| [59] | Sawicki M, Sypniewska G, Kozinski M, et al. Diagnostic efficacy of myeloperoxidase for the detection of acute coronary syndromes[J]. EurJClin Invest, 2011,41(6):667-671. |
| [60] | Peacock WF, Nagurney J, Birkhahn R, et al. Myeloperoxidase in the diagnosis of acute coronary syndromes: the importance of spectrum[J]. Am Heart J, 2011,162(5):893-899. |
| [61] | Chen Y, Zhang F, Dong L, et al. Long-term prognostic value of myeloperoxidase on acute coronary syndrome:ameta-analysis[J]. Arch Med Res, 2011,42(5):368-374. |
| [62] | Searle J, Shih J, Muller R, et al. The role of myeloperoxidase (MPO) for prognostic evaluation in sensitive cardiac troponinInegative chest pain patients in the emergency department[J]. Eur HeartJAcute Cardiovasc Care, 2013,2(3):203-210. |
| [63] | Roman RM, Camargo PV, Borges FK, et al. Prognostic value of myeloperoxidase in coronary artery disease: comparison of unstable and stable angina patients[J]. Coron Artery Dis, 2010,21(3):129-136. |
| [64] | Mocatta TJ, Pilbrow AP, Cameron VA, et al. Plasma concentrations of myeloperoxidase predict mortality after myocardial infarction[J].JAm Coll Cardiol, 2007,49(20):1993-2000. |
| [65] | Di SR, Di BV, Barsotti MC, et al. Inflammatory markers and cardiac function in acute coronary syndrome: difference in ST-segment elevation myocardial infarction (STEMI) and in non-STEMI models[J]. Biomed Pharmacother, 2009,63(10):773-780. |
| [66] | Falcao GP, Menezes FL, Duque PI. Procalcitonin as biomarker of infection: implications for evaluation and treatment[J]. AmJTher. 2015 Mar 23. [Epub ahead of print] |
| [67] | Picariello C, Lazzeri C, Valente S, et al. Procalcitonin in acute cardiac patients[J]. Intern Emerg Med, 2011,6(3):245-252. |
| [68] | Hausfater P. Biomarkers and infection in the emergency unit[J]. Med Mal Infect, 2014,44(4):139-145. |
| [69] | Picariello C, Lazzeri C, Attana P, et al. The impact of admission procalcitonin on prognosis in acute coronary syndromes:apilot study[J]. Biomarkers, 2012,17(1):56-61. |
| [70] | Bektas F, Soyuncu S, Gunduz I, et al. The value of procalcitonin,anovel inflammatory marker, in the diagnosis of myocardial infarction and evaluation of acute coronary syndrome patients[J].JEmerg Med, 2011,41(5):524-530. |
| [71] | Holst-Albrechtsen S, Kjaergaard M, Huynh AN, et al. Can lipoprotein-associated phospholipase A2 be used asapredictor of long-term outcome in patients with acute coronary syndrome?[J]. Curr Cardiol Rev, 2013,9(4):310-315. |
| [72] | Krintus M, Kozinski M, Kubica J, et al. Critical appraisal of inflammatory markers in cardiovascular risk stratification[J]. Crit Rev Clin Lab Sci, 2014,51(5):263-279. |
| [73] | Rubens C, Ewert R, Halank M, et al. Big endothelin-1 and endothelin-1 plasma levels are correlated with the severity of primary pulmonary hypertension[J]. Chest, 2001,120(5):1562-1569. |
| [74] | 汪隆海, 陈启松, 夏芳, 等. 定量检测大内皮素-1对心血管疾病的诊断价值[J]. 国际检验医学杂志, 2011,32(6):646-647. |
| [75] | Thygesen K, Alpert JS, Jaffe AS, et al. Third universal definition of myocardial infarction[J]. Eur Heart J, 2012,33(20):2551-2567. |
| [76] | Tello-Montoliu A, Marin F, Roldan V, et al.Amultimarker risk stratification approach to non-ST elevation acute coronary syndrome: implications of troponin T, CRP, NT pro-BNP and fibrin D-dimer levels[J].JIntern Med, 2007,262(6):651-658. |
| [77] | Geersing GJ, Erkens PM, Lucassen WA, et al. Safe exclusion of pulmonary embolism using the Wells rule and qualitative D-dimer testing in primary care: prospective cohort study[J]. BMJ, 2012,345:e6564. |
| [78] | Erbel R, Aboyans V, Boileau C, et al. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases: Document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC)[J]. Eur Heart J, 2014,35(41):2873-2926. |
| [79] | Konstantinides SV. 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism[J]. Eur Heart J, 2014,35(45):3145-3146. |
| [80] | Becattini C, Lignani A, Masotti L, et al. D-dimer for risk stratification in patients with acute pulmonary embolism[J].JThromb Thrombolysis, 2012,33(1):48-57. |
| [81] | Klok FA, Mos IC, Huisman MV. Brain-type natriuretic peptide levels in the prediction of adverse outcome in patients with pulmonary embolism:asystematic review and meta-analysis[J]. AmJRespir Crit Care Med, 2008,178(4):425-430. |
| [82] | Lankeit M, Friesen D, Aschoff J, et al. Highly sensitive troponinTassay in normotensive patients with acute pulmonary embolism[J]. Eur Heart J, 2010,31(15):1836-1844. |
| [83] | Boscheri A, Wunderlich C, Langer M, et al. Correlation of heart-type fatty acid-binding protein with mortality and echocardiographic data in patients with pulmonary embolism at intermediate risk[J]. Am Heart J, 2010,160(2):294-300. |
 2015, Vol. 24
2015, Vol. 24


