2. 上海健康医学院附属嘉定区中心医院心内科,上海 201800
免疫检查点抑制剂(Immune Checkpoint Inhibitors, ICIs)伊匹木单抗和纳武利尤单抗分别是针对细胞毒性T淋巴细胞相关抗原4(cytotoxic T lymphocyte associated antigen-4, CTLA-4)和靶向程序性死亡受体-1(programmed cell death protein-1, PD-1)的单克隆抗体,可解除T细胞免疫抑制,增强抗肿瘤效应,在多种晚期恶性肿瘤的治疗中示出良好的治疗前景,部分患者可获得长期缓解[1],但也带来了免疫相关毒性反应(immune-related adverse events, irAEs)的风险[2]。T细胞介导的自身免疫反应可能导致免疫系统攻击正常组织,诱发多系统损害[3]。
在各类irAEs中,心脏毒性发生率不高,但致死风险突出。其中ICIs相关心肌炎的发病率报道不一,约为0.27%~1.14%[4-6]。该病起病隐匿、进展迅猛,病死率高,早期识别与及时干预是改善预后的关键[7-8]。目前临床中尚未常规将心电图与心肌损伤标志物作为ICIs治疗的必查监测项目,亚临床心肌炎易被忽视,部分患者可快速进展为暴发性心肌炎、电风暴乃至心源性猝死。已有研究证实,ICIs相关重症心肌炎可合并房室传导阻滞、QT间期延长、心力衰竭甚至猝死[4]。由于发病机制尚未完全阐明,诊疗仍缺乏统一规范,尤其合并电风暴时救治难度大、病死率高,亟需院前、院内及多学科团队协同管理。
本文报道1例老年男性结肠癌患者,接受伊匹木单抗单药治疗后,突发恶性心律失常,确诊为ICIs相关重症心肌炎合并电风暴,24 h内共发生7次需电复律的恶性室性心律失常,经积极救治后好转。结合临床资料并复习相关文献,旨在提高临床对这一少见高危并发症的认知,为早期诊断与个体化救治提供依据。本研究经过上海市嘉定区中心医院医学研究伦理委员会(伦理审批号:20250222)审批,符合伦理相关的法律法规要求。
1 资料与方法患者男,69岁,无高血压、糖尿病、高脂血症等心血管危险因素。2月前确诊结肠癌(cTx Nx M1b,ⅣB期)伴双肺、肝脏及髋关节转移,予奥沙利铂联合卡培他滨化疗联合伊匹木单抗(50 mg,每6周1次)单药免疫治疗。
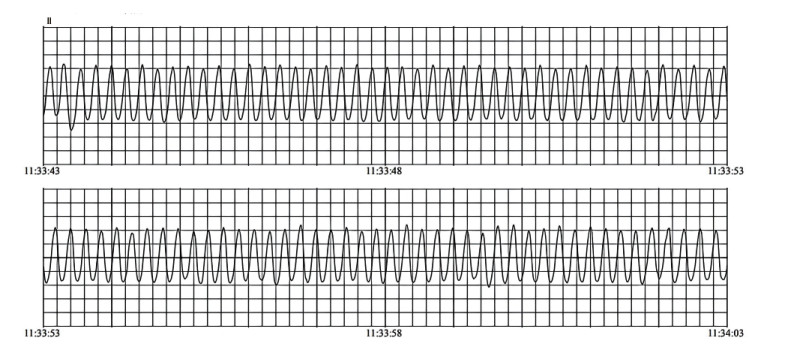
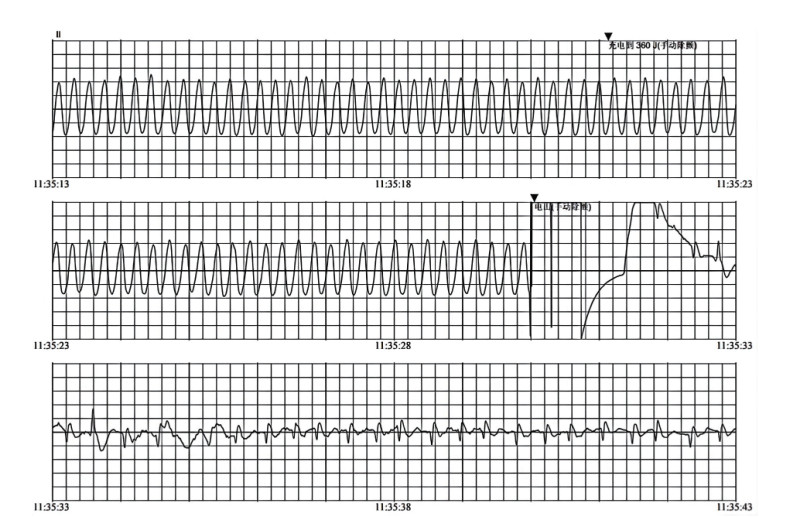
免疫治疗第60天,11:16患者因突发“心脏不适40 min ”拨打急救电话求助。救护车于11:20到达现场,经采集病史和初步评估后立即予以吸氧、建立静脉通道、第一时间全程心电监护,并启程转运。11:33途中患者突发意识丧失,颈动脉搏动消失,心电图示宽QRS心律(图 1),判定为无脉性室速(pulseless ventricular tachycardia, pVT)。急救医生立即给予360 J非同步电除颤一次,成功转复为窦性心动过速,心率150次/min(图 2),患者意识恢复,血压145/103 mmHg,11:38收入急诊抢救室。
|
| 图 1 首次监测显示室性心动过速,规则的R-R间期、快速的心室率伴有不可分辨的心房率(P波缺失)、房室分离和宽QRS波群(大于0.12 s) |
|
|
|
| 图 2 首次电复律成功心电图 |
|
|
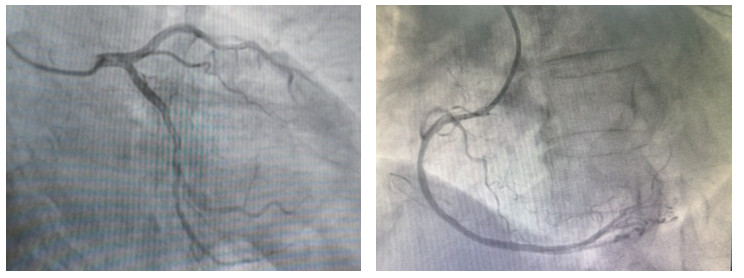
入院后按照急性冠脉综合征的流程诊疗,12:20紧急行冠状动脉造影,结果显示(图 3)左主干、前降支、回旋支及右冠状动脉血管通畅,TIMI 3级血流,未见明确狭窄或血栓形成,未行介入治疗。术中患者再次发生pVT,予以电除颤3次,并静脉注射胺碘酮(150 mg,15 min内静推)与艾司洛尔(10 mg,缓慢静推)控制心律。患者入住病房后仍反复出现恶性心律失常:13:10、13:15先后发生pVT,各予200J同步电复律;13:21出现心室颤动(ventricular fibrillation, VF),电除颤5次,并予利多卡因100 mg静推。后续予艾司洛尔、胺碘酮、利多卡因持续静脉维持,甲泼尼龙500 mg/d冲击,奥美拉唑抑酸,辅酶Q10及极化液等支持治疗。
|
| 图 3 冠脉造影结果显示左主干、前降支、回旋支及右冠状动脉血管通畅,未见明显狭窄或血栓形成 |
|
|
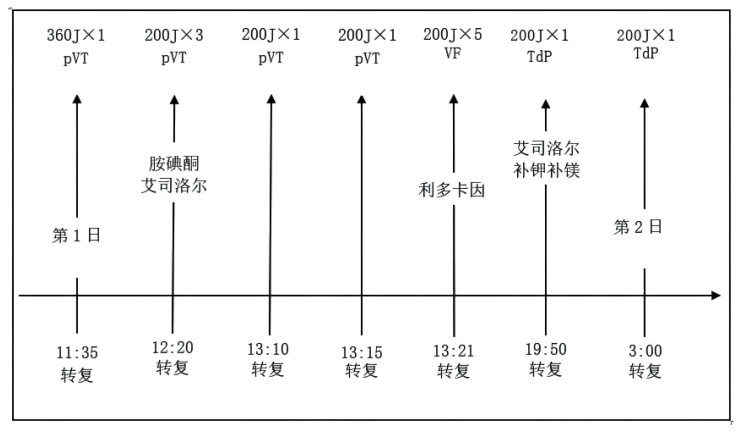
24 h内累计发生7次需电复律的恶性室性心律失常事件(图 4),当日19:50及次日03:00心电监护发现患者尖端发生扭转型室速(torsades de pointes, TdP),均行1次电除颤成功转复,QTc间期延长(>480 ms),提示交感神经风暴,遂停用胺碘酮,继续泵注艾司洛尔,并加强补钾补镁治疗(目标血钾维持在4.0~4.5mmol/L,血镁>1.0mmol/L),心律逐渐趋于稳定。
|
| 注:共记录7次需电复律的恶性室性心律失常事件,包括4次pVT、1次VF和2次TdP,所有事件均复律成功,期间抗心律失常药物方案随事件演进多次调整 图 4 患者24 h内电风暴事件的时间轴 |
|
|
实验室检查提示急性心肌损伤:超敏肌钙蛋白Ⅰ 0.94 ng/mL,CKMB 30.76 ng/mL,NTproBNP 136.67 pg/mL,肌红蛋白71.11 ng/mL,均明显升高,血气提示代谢性酸中毒。见表 1。心电图示窦性心律、完全性右束支传导阻滞,Ⅱ、aVF、V4导联ST段压低,aVR导联轻度抬高。结合近期免疫治疗史、无其他诱因、反复室性心律失常、左室射血分数(left ventricular ejection fraction, LVEF)降至29%,临床高度怀疑ICIs相关心肌炎。经多学科会诊后,予大剂量甲泼尼龙500 mg/d冲击3 d后逐步减量,联合心肌保护、维持内环境稳定等治疗。患者近期无感染、电解质紊乱、药物误用史,既往无心肌炎病史。综合近期使用伊匹木单抗、反复室性心律失常、心功能急剧下降(EF降至29%)等表现,临床高度怀疑免疫相关性心肌炎。次日多学科(普外科、风湿免疫科、肿瘤科、消化内科及药剂科)会诊后,统一意见启动大剂量糖皮质激素冲击治疗(甲泼尼龙500 mg/d×3 d,后减量),辅以维生素C、护肝药、改善心肌代谢、持续使用极化液及电解质调整。
| 入院首次检测指标 | 检测值 | 参考值 |
| 超敏肌钙蛋白Ⅰ | 0.94 HH | ≤ 0.1 ng/mL |
| 肌酸激酶同工酶 | 30.76 HH | ≤ 5 ng/mL |
| N末端-B型钠尿肽前体 | 136.67 H | ≤ 110 pg/mL |
| 降钙素原 | 0.31 HH | < 0.05 ng/mL |
| D-二聚体 | 17.66 HH | 0~0.55 mg/L |
| 酸碱度 | 7.42 | 7.35~7.45 |
| 二氧化碳分压 | 16 LL | 35-45 mmHg |
| 实际碳酸氢根 | 10.4 LL | 22~27 mmol/L |
| 标准碳酸氢根 | 16.3 LL | 22~31 mmol/L |
| 剩余碱 | -14.1 LL | -3-+3 mmol/L |
| 注:参考值标准取自于医院设定的参考范围为准;H/L表示检测值高于或低于参考范围;HH/LL表示达到危急值的标准 | ||
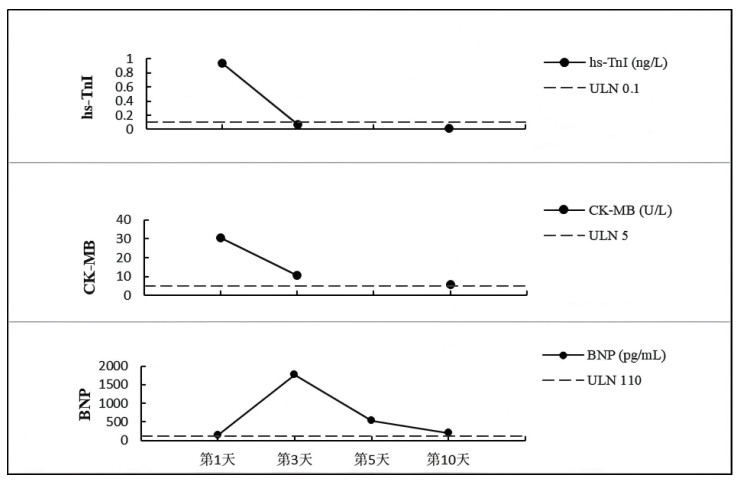
治疗第5日超声心动图提示LVEF回升至54%,第10日复查肌钙蛋白I降至0.02 ng/mL,NT-proBNP下降至199.84 pg/mL(图 5)。患者康复出院,神经功能分类(Cerebral Performance Category, CPC)为1级,心律稳定,免疫指标改善。为预防再次发生恶性心律失常,遂转至上级医院行ICD植入术,进行二级预防性治疗。
|
| 注:超敏肌钙蛋白Ⅰ与肌酸激酶同工酶于当日(电风暴发作日)显著升高后迅速回落,符合急性心肌损伤的典型演变过程。N末端B型利钠肽原在第3天出现峰值后持续下降,提示心肌损伤后伴随一过性的心功能不全或容量负荷加重,随后功能逐渐恢复。至第10日,三项指标均接近或降至正常参考上限附近,表明心肌损伤与心功能压力得到有效控制 图 5 关键心脏标志物的时序变化趋势 |
|
|
ICIs相关心肌炎是严重且致命的irAEs,一项荟萃分析显示,在ICI相关致死性不良反应中,心肌炎致死率高达39.69%,显著高于其他器官毒性,且在CTLA4抑制剂联合PD1/PDL1抑制剂时风险更高[9]。本例患者在伊匹木单抗治疗第60天发病,略晚于文献报道的中位发病时间约34 d[10],提示可能由亚临床心肌炎缓慢进展为暴发性发作。
2.1 临床表现的复杂性与非特异性ICIs相关心肌炎临床表现多样,可表现为心悸、胸痛、心力衰竭等,也可起病隐匿,仅轻微症状或无症状,易被基础肿瘤病情掩盖[11]。本例患者突发心脏骤停前仅主诉心脏不适,无典型心肌炎症状,提示对接受ICIs治疗、出现非特异性心脏不适的患者,均应高度警惕亚临床心肌炎可能,尽早开展评估。
2.2 心电图与肌钙蛋白监测的重要性本例以电风暴为首发表现,多次出现pVT、TdP、VF,心肌损伤标志物显著升高,支持急性重症心肌炎。越来越多证据支持将心电图与肌钙蛋白作为ICIs治疗期间的常规监测项目,尤其在治疗前2个月内密切监测,有助于早期识别[12]。院前急救阶段应将胸部不适按高危胸痛处置,尽早完成心电图、持续监护并启动远程指导,为后续抢救争取时间[13, 22]。部分患者心电图、心脏MRI可无典型异常,但心肌活检可见炎症浸润[14],对高度可疑病例,在生命体征稳定前提下可考虑心肌活检确诊;但对危重患者,不应因等待检查而延误激素等关键救治。
2.3 电风暴提示严重电生理重构本例突出特点为电风暴,24 h内7次恶性室性心律失常需电复律,提示广泛心肌炎症浸润、离子通道紊乱及交感电风暴。TdP发作伴QTc显著延长,与炎症、电解质紊乱及抗心律失常药物影响有关。此类表现需与急性冠脉综合征、原发性室性心律失常、药物致心律失常等快速鉴别。
2.4 治疗策略与反应本例在多学科协作下,予大剂量甲泼尼龙冲击治疗,联合抗心律失常、纠正电解质、心肌保护等综合措施,心律失常得到控制,心功能快速恢复。目前指南推荐,糖皮质激素为ICIs相关重症心肌炎首选一线治疗,可快速抑制T细胞活化、减轻心肌免疫损伤[16, 17],对激素反应不佳的难治性病例,可考虑阿巴西普、英夫利昔单抗等二线免疫调节治疗[16, 24-25]。
2.5 发病机制的免疫基础与前沿研究基础研究显示,PD1与CTLA4在维持心肌免疫耐受中具有重要作用。PD1敲除小鼠可出现自发性心肌炎,CTLA4敲除小鼠可发生致死性心肌炎[18-19]。ICIs阻断上述通路后,可打破心肌免疫耐受,激活T细胞与体液免疫,导致心肌炎性损伤。炎症状态下心肌细胞PDL1表达上调,发挥“免疫刹车”作用,ICIs治疗后该保护作用消失,进一步加重免疫攻击[4, 20]。
2.6 启示与建议本例提示,ICIs相关心肌炎可隐匿起病,首发即表现为电风暴,猝死风险极高。对接受ICIs治疗的患者,建议在治疗前、中早期(尤其是前2个月)定期监测心电图和cTnI。对不明原因心律失常、心肌酶升高或QTc延长者提高警惕;及时行影像学、必要时心肌活检协助诊断。一旦确诊应立即停药并启动免疫抑制治疗。本病例结合既往文献经验,支持在ICIs治疗人群中建立心脏安全性监测策略,尤其应在高危患者中加强预警机制,以期减少ICIs相关心肌炎的致残与致死结局[16, 21]。
利益冲突 所有作者声明无利益冲突
作者贡献声明 王庆峰:酝酿和研究设计、数据收集、论文起草;林全洪:酝酿和研究设计、论文指导、论文修改;陆瑜:数据收集及整理;许向东:数据收集、解释数据、论文修改与指导
| [1] | Long GV, Nair N, Marbach D, et al. Neoadjuvant PD-1 and LAG-3-targeting bispecific antibody and other immune checkpoint inhibitor combinations in resectable melanoma: the randomized phase 1b/2 Morpheus-Melanoma trial[J]. Nat Med, 2025, 31(11): 3700-3712. DOI:10.1038/s41591-025-03967-2 |
| [2] | Hao CY, Tian JH, Liu HL, et al. Efficacy and safety of anti-PD-1 and anti-PD-1 combined with anti-CTLA-4 immunotherapy to advanced melanoma: a systematic review and meta-analysis of randomized controlled trials[J]. Medicine(Baltimore), 2017, 96(26): e7325. DOI:10.1097/md.0000000000007325 |
| [3] | Robert L, Tsoi J, Wang XY, et al. CTLA4 blockade broadens the peripheral T-cell receptor repertoire[J]. Clin Cancer Res, 2014, 20(9): 2424-2432. DOI:10.1158/1078-0432.ccr-13-2648 |
| [4] | Johnson DB, Balko JM, Compton ML, et al. Fulminant myocarditis with combination immune checkpoint blockade[J]. N Engl J Med, 2016, 375(18): 1749-1755. DOI:10.1056/nejmoa1609214 |
| [5] | Wang F, Sun XC, Qin SK, et al. A retrospective study of immune checkpoint inhibitor-associated myocarditis in a single center in China[J]. Chin Clin Oncol, 2020, 9(2): 16. DOI:10.21037/cco.2020.03.08 |
| [6] | Mahmood S, Fradley MG, Cohen JV, et al. Myocarditis in patients treated with immune checkpoint inhibitors[J]. J Am Coll Cardiol, 2018, 71(11): A699. DOI:10.1016/s0735-1097(18)31240-3 |
| [7] | Salem JE, Manouchehri A, Moey M, et al. Cardiovascular toxicities associated with immune checkpoint inhibitors: an observational, retrospective, pharmacovigilance study[J]. Lancet Oncol, 2018, 19(12): 1579-1589. DOI:10.1016/s1470-2045(18)30608-9 |
| [8] | Hu JR, Florido R, Lipson EJ, et al. Cardiovascular toxicities associated with immune checkpoint inhibitors[J]. Cardiovasc Res, 2019, 115(5): 854-868. DOI:10.1093/cvr/cvz026 |
| [9] | Wang DY, Salem JE, Cohen JV, et al. Fatal toxic effects associated with immune checkpoint inhibitors: a systematic review and meta-analysis[J]. JAMA Oncol, 2018, 4(12): 1721. DOI:10.1001/jamaoncol.2018.3923 |
| [10] | Mahmood S, Fradley MG, Cohen JV, et al. Myocarditis in patients treated with immune checkpoint inhibitors[J]. J Am Coll Cardiol, 2018, 71(11): A699. DOI:10.1016/s0735-1097(18)31240-3 |
| [11] | Heinzerling L, Ott PA, Hodi FS, et al. Cardiotoxicity associated with CTLA4 and PD1 blocking immunotherapy[J]. J Immunother Cancer, 2016, 4(1): 50. DOI:10.1186/s40425-016-0152-y |
| [12] | Brahmer JR, Lacchetti C, Schneider BJ, et al. Management of immune-related adverse events in patients treated with immune checkpoint inhibitor therapy: American society of clinical oncology clinical practice guideline[J]. J Clin Oncol, 2018, 36(17): 1714-1768. DOI:10.1200/jco.2017.77.6385 |
| [13] | 林全洪, 许向东, 张云柯, 等. 不同来院方式急性ST段抬高心肌梗死患者再灌注时间与预后影响因素分析[J]. 中华急诊医学杂志, 2020, 29(7): 921-928. DOI:10.3760/cma.j.issn.1671-0282.2020.07.006 |
| [14] | Zhang LL, Jones-O'Connor M, Awadalla M, et al. Cardiotoxicity of immune checkpoint inhibitors[J]. Curr Treat Options Cardiovasc Med, 2019, 21(7): 32. DOI:10.1007/s11936-019-0731-6 |
| [15] | Weinmann SC, Pisetsky DS. Mechanisms of immune-related adverse events during the treatment of cancer with immune checkpoint inhibitors[J]. Rheumatology (Oxford), 2019, 58(Suppl 7): vii59-vii67. DOI:10.1093/rheumatology/kez308 |
| [16] | Brahmer JR, Lacchetti C, Schneider BJ, et al. Management of immune-related adverse events in patients treated with immune checkpoint inhibitor therapy: American Society of Clinical Oncology Clinical Practice Guideline[J]. J Clin Oncol, 2018, 36(17): 1714-1768. DOI:10.1200/jco.2017.77.6385 |
| [17] | Salem JE, Allenbach Y, Vozy A, et al. Abatacept for severe immune checkpoint inhibitor-associated myocarditis[J]. N Engl J Med, 2019, 380(24): 2377-2379. DOI:10.1056/nejmc1901677 |
| [18] | Okazaki T, Honjo T. PD-1 and PD-1 ligands: from discovery to clinical application[J]. Int Immunol, 2007, 19(7): 813-824. DOI:10.1093/intimm/dxm057 |
| [19] | Wei SC, Duffy CR, Allison JP. Fundamental mechanisms of immune checkpoint blockade therapy[J]. Cancer Discov, 2018, 8(9): 1069-1086. DOI:10.1158/2159-8290.cd-18-0367 |
| [20] | Palaskas N, Lopez-Mattei J, Durand JB, et al. Immune checkpoint inhibitor myocarditis: pathophysiological characteristics, diagnosis, and treatment[J]. J Am Heart Assoc, 2020, 9(2): e013757. DOI:10.1161/jaha.119.013757 |
| [21] | Moslehi JJ, Salem JE, Sosman JA, et al. Increased reporting of fatal immune checkpoint inhibitor-associated myocarditis[J]. Lancet, 2018, 391(10124): 933. DOI:10.1016/s0140-6736(18)30533-6 |
| [22] | 张茂, 徐善祥. 中国急诊医学临床研究现状与展望[J]. 中华急诊医学杂志, 2024, 33(1): 1-6. DOI:10.3760/cma.j.issn.1671-0282.2024.01.001 |
| [23] | Li T, Zhang L, Chen Y, et al. Clinical characteristics and early warning indicators of immune checkpoint inhibitor-related myocarditis[J]. World J Emerg Med, 2024, 15(2): 112-118. DOI:10.5847/wjem.j.1920-8642.2024.039 |
| [24] | Wang H, Li Y, Liu Y, et al. Multidisciplinary team collaboration in the management of severe immune checkpoint inhibitor myocarditis[J]. World J Emerg Med, 2023, 14(6): 411-417. DOI:10.5847/wjem.j.1920-8642.2023.226 |
| [25] | 周荣斌, 董磊. 免疫检查点抑制剂相关心血管不良反应的急诊识别与处置[J]. 中华急诊医学杂志, 2024, 33(6): 827-832. DOI:10.3760/cma.j.issn.1671-0282.2024.06.017 |
 2026, Vol. 35
2026, Vol. 35