肝硬化作为一种重大的健康问题,是多种慢性肝病发展的共同终末阶段。据统计,2019年我国肝硬化发患者数较1999年增加了32.08%[1]。全球疾病负担研究显示,以肝硬化及其并发症为主要死因的肝病在全球死因中位列第11位,每年导致约200万人死亡,占总死亡人数的4%[2]。肝硬化进入失代偿期后,急性上消化道出血是其最常见且凶险的并发症,病死率高且明确高于非肝硬化患者[3]。尽管医疗技术不断进步,其6周内病死率仍达11%,临床预后极差[4]。内镜检查虽然是诊断和治疗AUGIB的“金标准”[5],但属侵入性操作,存在一定风险且患者耐受性差。肝静脉压力梯度(hepatic venous pressure gradient, HVPG)检测和瞬时弹性成像等技术被指南推荐用于门脉高压和静脉曲张的评估,但因操作有创或因成本与技术门槛,均未能在临床广泛推广[6-7]。近年来,多种无创模型被探索用于预测肝硬化患者出血风险[8-11]。然而,关于这些指标的预测效能在不同研究中结论不一,尚存争议[12]。因此,为建立一种更高效、实用的无创出血风险预测工具,本研究整合临床及影像学资料,拟开发与验证一个可视化列线图模型,以辅助临床早期识别高危患者,并为制定个体化干预策略提供参考。
1 资料与方法 1.1 研究对象本研究采用回顾性分析方法,选取2022年6月至2025年6月于辽宁省健康产业集团抚矿总医院的肝硬化住院患者。纳入标准:①符合2019年中华医学会肝病学分会《肝硬化诊治指南》[15]中的诊断标准;②临床资料完整可靠;③上消化道出血:存在呕血、黑便等和(或)失血性周围循环衰竭的临床表现,呕吐物或粪便隐血试验阳性,血红蛋白下降。排除标准:①合并肾衰竭、恶性肿瘤、血液系统疾病等;②严重心肺功能不全;③肝、脾切除术后;④肝移植术后。所有检测均得到患者和(或)家属的知情同意,且经伦理委员会同意批准(伦理审批号:20251210)。
1.2 研究方法收集(1)一般资料:性别、年龄、肝硬化病因、合并症(高血压、糖尿病、冠心病)、有无肝性脑病(hepatic encephalopathy,HE)、个人史(吸烟、饮酒史)、入院时收缩压(systolic blood pressure,SBP)、临床表现(黑便、便血、呕血、腹痛、腹胀、乏力、头晕)、住院天数;(2)实验室资料:白细胞(white blood cell, WBC)、中性粒细胞百分比(neutrophil percentage, NEUT%)、中性粒细胞计数(neutrophil count, NEUT)、淋巴细胞计数(lymphocyte count, LYM)、血红蛋白(hemoglobin, HB)、红细胞分布宽度-变异系数(red blood cell distribution width-coefficient of variation, RDW-CV)、红细胞分布宽度-标准差(red blood cell distribution width-standard deviation, RDW-SD)、血小板(platelet, PLT)、凝血酶原活动度(prothrombin activity, PTA)、国际标准化比值(international normalized ratio, INR)、活化部分凝血活酶时间(activated partial thromboplastin time, APTT)、凝血酶原时间(prothrombin time, PT)、凝血酶时间(thrombin time, TT)、纤维蛋白原(fibrinogen, FIB)、D-二聚体(D-dimer, D-D)、丙氨酸氨基转移酶(alanine aminotransferase, ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase, AST)、总蛋白(total protein, TP)、白蛋白(albumin, ALB)、球蛋白(globulin, GLB)、白球比(albumin-to-globulin ratio, A/G)、总胆红素(total bilirubin, TBil)、直接胆红素(direct bilirubin, DBil)、间接胆红素(indirect bilirubin, IBil)、γ-谷氨酰转肽酶(gamma-glutamyl transpeptidase, GGT)、碱性磷酸酶(alkaline phosphatase, ALP)、尿素氮(blood urea nitrogen, BUN)、肌酐(creatinine, Cr)、尿酸(uric acid, UA)、血清钠离子水平(serum sodium, Na+);(3)影像学资料:有无腹水、有无脾大、脾长径(spleen diameter, SD)、门静脉最大直径(portal vein diameter, PVD)、脾静脉最大直径(splenic vein diameter, SVD)。测量方法:于CT轴位图像测量:脾长径取脾脏最大长轴层面的最大连线距离;门静脉最大直径于肝门部门静脉主干最宽处测量内径;脾静脉最大直径于脾门附近或脾静脉主干最宽处测量内径。并计算ALBI、APRI、AAR、GPR、PSR、NLR、PLR、RPR、RLR、FIB-4、King's评分及PALBI共12种评分或比值。
1.3 统计学方法本研究的统计分析均使用R语言(版本4.5.1)完成。计量资料经正态性检验后,符合正态分布者以均数±标准差(x±s)表示,组间比较采用两独立样本t检验;不符合者以中位数(四分位数间距)[M(Q1,Q3)]表示,组间比较采用Mann-Whitney U检验。计数资料以例数(百分比)[n(%)]表示,组间比较根据理论频数选择χ2检验或Fisher确切概率法。将数据按照7:3比例随机分为训练集325例和验证集139例。在训练集中,先采用LASSO回归分析筛选变量,依据λ.min与λ.1se准则分别保留变量。将筛选出的变量进一步纳入多因素Logistic回归,以确定独立预测因素,据此构建并绘制列线图预测模型。模型性能通过AUC评估区分度,校准度采用Hosmer-Lemeshow检验及校准曲线评估,并通过决策曲线分析评估临床实用性。此外,对12种传统评分进行单因素Logistic回归分析,筛选出有预测意义的评分,并与新建模型在区分度、校准度及临床实用性方面进行综合对比。以P < 0.05为差异有统计学意义。
评分
公式
注:upper limit of normal for AST: 女35(U/L),男40(U/L);upper limit of normal for GGT:女45(U/L),男60(U/L)
ALBI[14]
(log10TBil(μmol/L) × 0.66) + (ALB(g/L) × -0.085)
PALBI[15]
[2.02×log10TBil(μmol/L)] + [-0.37×(log10TBil(μmol/L))2] + [-0.04×ALB(g/L)]+[-3.48×log10PLT(109/L)] + [1.01×(log10PLT(109/L))2]
APRI[16]
[(AST(U/L)/ upper limit of normal for AST(ULN)) / PLT (109 /L)] × 100
AAR[17]
AST(U/L) / ALT(U/L)
GPR[18]
(GGT(U/L)/ upper limit of normal for GGT(ULN)) / PLT (109/L) × 100
PSR[19]
PLT (109/L)/SD(mm)
NLR[20]
NEUT(109/L)/LYM(109/L)
PLR[21]
PLT (109/L) / LYM(109/L)
RPR[22]
RDW(%)/PLT(109/L)
RLR[23]
RDW(%)/LYM(109/L)
FIB-4[24]
[Age (year) × AST(U/L)) / (PLT (109/L) × ALT(U/L)1/2]
King's Score[25]
(Age (years) × AST(U/L) × INR) / PLT (109/L)
本研究共纳入464例肝硬化患者。以是否发生急性上消化道出血进行分层,按7:3比例将总体随机分配至训练集(325例)与验证集(139例)。对两组基线资料进行系统性比较,仅AST一项组间差异有统计学意义(P < 0.05),其余变量均无统计学意义,提示数据集划分具有良好的可比性,见表 1。
| 特征 | 训练集(n =325) | 验证集(n = 139) | Z/χ2值 | P值 |
| 性别a | 0.22 | 0.641 | ||
| 男 | 220 (67.69) | 91 (65.47) | ||
| 女 | 105 (32.31) | 48 (34.53) | ||
| 年龄(岁)b | 63.00 (57.00, 71.00) | 63.00 (57.00, 70.00) | -0.18 | 0.855 |
| 住院天数(d)b | 5.00 (3.00, 8.00) | 6.00 (4.00, 8.00) | -1.08 | 0.279 |
| 肝硬化病因a | 0.07 | 0.965 | ||
| 病毒性 | 107 (32.92) | 44 (31.65) | ||
| 酒精性 | 124 (38.15) | 54 (38.85) | ||
| 其他 | 94 (28.92) | 41 (29.50) | ||
| 高血压a | 1.02 | 0.312 | ||
| 否 | 253 (77.85) | 114 (82.01) | ||
| 是 | 72 (22.15) | 25 (17.99) | ||
| 糖尿病a | 0.87 | 0.350 | ||
| 否 | 256 (78.77) | 104 (74.82) | ||
| 是 | 69 (21.23) | 35 (25.18) | ||
| 冠心病a | 1.08 | 0.298 | ||
| 否 | 281 (86.46) | 115 (82.73) | ||
| 是 | 44 (13.54) | 24 (17.27) | ||
| 肝性脑病a | 0.01 | 0.991 | ||
| 否 | 248 (76.31) | 106 (76.26) | ||
| 是 | 77 (23.69) | 33 (23.74) | ||
| 吸烟史a | 2.07 | 0.150 | ||
| 否 | 147 (45.23) | 73 (52.52) | ||
| 是 | 178 (54.77) | 66 (47.48) | ||
| 饮酒史a | 1.16 | 0.282 | ||
| 否 | 160 (49.23) | 76 (54.68) | ||
| 是 | 165 (50.77) | 63 (45.32) | ||
| 腹水a | 0.02 | 0.900 | ||
| 否 | 86 (26.46) | 36 (25.90) | ||
| 是 | 239 (73.54) | 103 (74.10) | ||
| 脾肿大a | 0.03 | 0.857 | ||
| 否 | 47 (14.46) | 21 (15.11) | ||
| 是 | 278 (85.54) | 118 (84.89) | ||
| 收缩压(mmHg)b | 120.00 (110.00, 132.00) | 123.00 (109.00, 135.50) | -0.51 | 0.613 |
| WBC(×109/L)b | 5.50 (3.89, 8.13) | 5.59 (3.54, 8.31) | -0.18 | 0.861 |
| NEUT%b | 72.20 (62.10, 80.20) | 72.20 (63.70, 81.65) | -0.46 | 0.644 |
| NEUT(×109/L)b | 3.92 (2.30, 5.95) | 3.60 (2.16, 6.55) | -0.32 | 0.753 |
| LYM(×109/L)b | 0.90 (0.60, 1.41) | 0.86 (0.60, 1.35) | -0.07 | 0.943 |
| HB(g/L)b | 88.00 (68.00, 113.00) | 82.00 (63.50, 113.00) | -0.99 | 0.324 |
| RDW-CV(%)b | 16.10 (14.20, 18.90) | 16.60 (14.30, 18.95) | -0.73 | 0.464 |
| RDW-SD(fL)b | 52.60 (48.60, 57.70) | 53.00 (47.65, 58.60) | -0.07 | 0.941 |
| PLT(×109/L)b | 101.00 (70.00, 141.00) | 98.00 (70.00, 155.50) | -0.01 | 0.989 |
| PT(s)b | 16.02 (14.42, 17.70) | 16.20 (14.57, 17.87) | -0.51 | 0.611 |
| INRb | 1.31 (1.13, 1.45) | 1.31 (1.15, 1.46) | -0.54 | 0.588 |
| PTA(%)b | 64.00 (54.00, 80.44) | 63.00 (54.00, 77.00) | -0.5 | 0.619 |
| APTT(s)b | 37.50 (33.90, 41.80) | 37.30 (33.35, 41.55) | -0.18 | 0.859 |
| FIB(g/L)b | 2.04 (1.51, 2.57) | 1.94 (1.57, 2.46) | -0.01 | 0.993 |
| TT(s)b | 19.90 (17.90, 22.00) | 19.50 (18.00, 21.65) | -1.02 | 0.308 |
| D-D(μg/mL)b | 1.64 (0.71, 2.88) | 2.06 (0.88, 3.30) | -1.45 | 0.147 |
| ALT(U/L)b | 27.00 (18.00, 42.00) | 23.00 (17.00, 38.50) | -1.36 | 0.175 |
| AST(U/L)b | 42.00 (29.00, 70.00) | 35.00 (25.50, 58.00) | -2.13 | 0.033 |
| TP(g/L)b | 65.80 (59.20, 71.80) | 66.40 (60.15, 72.45) | -0.53 | 0.594 |
| ALB(g/L)b | 32.00 (27.30, 36.20) | 31.50 (27.80, 35.60) | -0.31 | 0.760 |
| GLB(g/L)b | 32.60 (28.10, 38.10) | 33.60 (28.40, 38.45) | -0.97 | 0.332 |
| A/Gb | 0.99 (0.77, 1.21) | 0.98 (0.78, 1.17) | -0.34 | 0.735 |
| TBil(μmol/L)b | 25.00 (17.00, 38.90) | 22.90 (16.60, 36.15) | -0.83 | 0.409 |
| DBil(μmol/L)b | 8.70 (5.60, 17.10) | 8.80 (5.50, 17.70) | -0.35 | 0.724 |
| IBil(μmol/L)b | 14.90 (9.30, 23.40) | 13.10 (9.25, 19.40) | -1.53 | 0.126 |
| GGT(U/L)b | 59.00 (31.00, 151.00) | 50.00 (27.00, 129.50) | -1.22 | 0.223 |
| ALP(U/L)b | 101.00 (70.00, 143.00) | 94.00 (68.50, 130.00) | -0.95 | 0.341 |
| BUN(mmol/L)b | 7.90 (5.60, 12.40) | 7.90 (5.35, 11.45) | -0.68 | 0.498 |
| Cr(μmol/L)b | 64.50 (50.40, 82.20) | 69.30 (53.30, 86.35) | -1.11 | 0.266 |
| UA(μmol/L)b | 324.00 (244.00, 429.90) | 329.00 (265.65, 432.15) | -1.17 | 0.240 |
| NA+(mmol/L)b | 139.00 (136.50, 141.00) | 138.90 (135.45, 141.00) | -1.01 | 0.315 |
| SD(mm)b | 128.93 (111.69, 153.87) | 131.03 (109.08, 151.49) | -0.03 | 0.976 |
| PVD(mm)b | 14.14 (12.35, 16.46) | 14.60 (12.54, 16.46) | -0.41 | 0.680 |
| SVD(mm)b | 9.86 (8.14, 11.86) | 10.16 (8.03, 12.80) | -1.18 | 0.236 |
| 注:a为例(%),b为M(Q1,Q3) | ||||
对训练集325例肝硬化患者的基线资料分析显示,出血组共191例,未出血组共134例。二者相比,出血组患者年龄更低[(62±11)岁vs.(66±11)岁],肝性脑病发生率更高(32% vs. 12%),且入院收缩压、HB、PLT、ALB、PTA及FIB等指标显著降低(均P < 0.05),而NEUT%、PT、INR、PVD及SVD等指标显著升高(均P < 0.05)。两组在性别、肝硬化病因、合并症(高血压、糖尿病、冠心病)以及ALT、AST、TBIL等指标上差异无统计学意义。见表 2。
| 变量 | 研究样本(n=325) | 未出血(n=134) | 出血(n=191) | t/Z/χ2值 | P值 |
| 性别a | 0.085 | 0.771 | |||
| 男 | 220 (68) | 89 (66) | 131 (69) | ||
| 女 | 105 (32) | 45 (34) | 60 (31) | ||
| 年龄(岁)b | 63 ± 11 | 66 ± 11 | 62 ± 11 | 3.682 | < 0.001 |
| 住院天数(d)c | 5 (3, 8) | 5 (3, 8) | 5 (3, 8) | -0.876 | 0.382 |
| 肝硬化病因a | 5.886 | 0.053 | |||
| 病毒性 | 107 (33) | 34 (25) | 73 (38) | ||
| 酒精性 | 124 (38) | 57 (43) | 67 (35) | ||
| 其他 | 94 (29) | 43 (32) | 51 (27) | ||
| 高血压a | 3.419 | 0.064 | |||
| 否 | 253 (78) | 97 (72) | 156 (82) | ||
| 是 | 72 (22) | 37 (28) | 35 (18) | ||
| 糖尿病a | 0.000 | 0.989 | |||
| 否 | 256 (79) | 105 (78) | 151 (79) | ||
| 是 | 69 (21) | 29 (22) | 40 (21) | ||
| 冠心病a | 2.061 | 0.151 | |||
| 否 | 281 (86) | 111 (83) | 170 (89) | ||
| 是 | 44 (14) | 23 (17) | 21 (11) | ||
| 肝性脑病a | 16.330 | < 0.001 | |||
| 否 | 248 (76) | 118 (88) | 130 (68) | ||
| 是 | 77 (24) | 16 (12) | 61 (32) | ||
| 吸烟史a | 0.000 | 1 | |||
| 否 | 147 (45) | 61 (46) | 86 (45) | ||
| 是 | 178 (55) | 73 (54) | 105 (55) | ||
| 饮酒史a | 0.110 | 0.741 | |||
| 否 | 160 (49) | 64 (48) | 96 (50) | ||
| 是 | 165 (51) | 70 (52) | 95 (50) | ||
| 腹水a | 0.272 | 0.602 | |||
| 否 | 86 (26) | 38 (28) | 48 (25) | ||
| 是 | 239 (74) | 96 (72) | 143 (75) | ||
| 脾肿大a | 12.697 | < 0.001 | |||
| 否 | 47 (14) | 31 (23) | 16 (8.4) | ||
| 是 | 278 (86) | 103 (77) | 175 (92) | ||
| 收缩压(mmHg)c | 120 (110, 132) | 130 (120, 138) | 118 (105, 130) | 6.391 | < 0.001 |
| WBC(×109/L)c | 5.5 (3.9, 8.1) | 4.7 (3.2, 7.0) | 6.2 (4.5, 8.8) | -3.300 | 0.001 |
| NEUT%c | 72 (62, 80) | 67 (59, 76) | 75 (66, 82) | -4.079 | < 0.001 |
| NEUT(×109/L)c | 3.9 (2.3, 6.0) | 2.9 (1.9, 4.6) | 4.6 (2.9, 6.8) | -3.771 | < 0.001 |
| LYM(×109/L)c | 0.90 (0.60, 1.41) | 0.80 (0.55, 1.40) | 0.90 (0.60, 1.42) | -0.424 | 0.672 |
| HB(g/L)c | 88 (68, 113) | 101 (78, 126) | 78 (61, 105) | 6.584 | < 0.001 |
| RDW-CV(%)c | 16.10 (14.20, 18.90) | 15.55 (13.90, 18.60) | 16.50 (14.60, 19.20) | -2.232 | 0.026 |
| RDW-SD(fL)c | 53 (49, 58) | 52 (47, 58) | 53 (49, 58) | -0.614 | 0.540 |
| PLT(×109/L)c | 101 (70, 141) | 111 (76, 173) | 98 (63, 129) | 3.148 | 0.002 |
| PT(s)c | 16.02 (14.42, 17.70) | 14.95 (13.80, 16.60) | 16.62 (15.20, 18.62) | -6.943 | < 0.001 |
| INRc | 1.31 (1.13, 1.45) | 1.19 (1.06, 1.34) | 1.36 (1.22, 1.57) | -7.330 | < 0.001 |
| PTA(%)c | 64 (54, 80) | 76 (61, 90) | 59 (48, 71) | 7.467 | < 0.001 |
| APTT(s)c | 38 (34, 42) | 39 (36, 43) | 37 (33, 41) | 2.854 | 0.005 |
| FIB(g/L)c | 2.04 (1.51, 2.57) | 2.42 (2.05, 2.95) | 1.68 (1.35, 2.16) | 8.273 | < 0.001 |
| TT(s)c | 19.90 (17.90, 22.00) | 18.75 (17.60, 20.50) | 20.90 (18.40, 23.20) | -5.827 | < 0.001 |
| D-D(μg/mL)c | 1.64 (0.71, 2.88) | 1.97 (0.72, 3.78) | 1.36 (0.70, 2.69) | 0.225 | 0.822 |
| ALT(U/L)c | 27 (18, 42) | 23 (14, 38) | 29 (21, 45) | -0.446 | 0.656 |
| AST(U/L)c | 42 (29, 70) | 42 (27, 70) | 43 (30, 74) | -0.290 | 0.772 |
| TP(g/L)b | 65 ± 10 | 70 ± 10 | 63 ± 10 | 6.332 | < 0.001 |
| ALB(g/L)b | 32 ± 7 | 33 ± 7 | 31 ± 6 | 3.327 | 0.001 |
| GLB(g/L)c | 33 (28, 38) | 35 (29, 42) | 31 (27, 35) | 4.708 | < 0.001 |
| A/Gc | 0.99 (0.77, 1.21) | 0.95 (0.73, 1.27) | 1.00 (0.82, 1.18) | -0.065 | 0.948 |
| TBIL(μmol/L)c | 25 (17, 39) | 24 (16, 40) | 25 (18, 39) | -0.908 | 0.364 |
| DBIL(μmol/L)c | 9 (6, 17) | 10 (6, 21) | 8 (5, 15) | 0.177 | 0.860 |
| IBIL(μmol/L)c | 15 (9, 23) | 12 (9, 21) | 17 (10, 27) | -3.189 | 0.002 |
| GGT(U/L)c | 59 (31, 151) | 64 (30, 182) | 58 (32, 127) | 0.355 | 0.723 |
| ALP(U/L)c | 101 (70, 143) | 113 (78, 156) | 93 (68, 136) | 2.626 | 0.009 |
| BUN(mmol/L)c | 7.9 (5.6, 12.4) | 6.0 (4.5, 8.1) | 9.6 (6.8, 13.7) | -6.338 | < 0.001 |
| Cr(μmol/L)c | 65 (50, 82) | 65 (51, 86) | 64 (49, 80) | -0.244 | 0.808 |
| UA(μmol/L)c | 324 (244, 430) | 362 (277, 466) | 292 (221, 409) | 3.715 | < 0.001 |
| Na(mmol/L)c | 139.0 (136.5, 141.0) | 139.0 (136.9, 141.3) | 139.0 (136.1, 141.0) | 0.391 | 0.696 |
| SD(mm)c | 129 (112, 154) | 122 (100, 145) | 135 (116, 158) | -3.936 | < 0.001 |
| PVD(mm)c | 14.1 (12.4, 16.5) | 13.0 (10.9, 14.4) | 15.5 (13.6, 17.8) | -9.216 | < 0.001 |
| SVD(mm)c | 9.9 (8.1, 11.9) | 8.9 (7.2, 10.6) | 10.4 (8.9, 12.6) | -5.728 | < 0.001 |
| 注:a为n(%),b为 x±s,c为M(Q1,Q3) | |||||
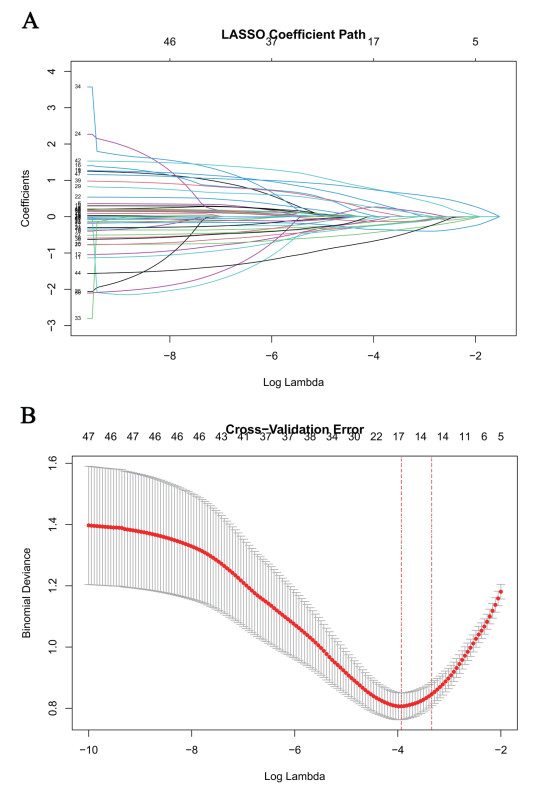
为解决数据中多重共线性与过拟合问题,本研究采用LASSO回归对预测变量进行初步筛选。以急性上消化道出血是否发生作为因变量,共纳入46个自变量,通过十倍交叉验证确定最优惩罚系数λ。变量系数路径图(图 1A)显示,随着惩罚系数λ增大(沿横坐标log(λ)向右),自变量的标准化回归系数逐渐被压缩,部分系数被缩减至零并从模型中剔除。十倍交叉验证误差曲线(图 1B)表明,在λ.min =0.0176时模型预测误差最小(左侧红色虚线),共保留17个变量(Age、肝性脑病、吸烟史、饮酒史、收缩压、WBC、NEUT、HB、PTA、APTT、FIB、TT、GLB、IBIL、BUN、UA、PVD);在λ.1se=0.0335时(右侧红色虚线),其预测误差在最小误差一个标准误范围内,共保留14个变量(年龄、肝性脑病、收缩压、NEUT%、NEUT、HB、PTA、APTT、FIB、TT、GLB、BUN、UA、PVD)。
|
| 注:A:自变量系数与lambda(λ)对数值之间的变化轨迹; B:各lambda下的置信区间。左侧虚线对应于最小λ值,右侧虚线对应于最小λ+1标准误差 图 1 LASSO回归分析筛选危险因素 Fig 1 Screening of risk factors using LASSO regression analysis |
|
|
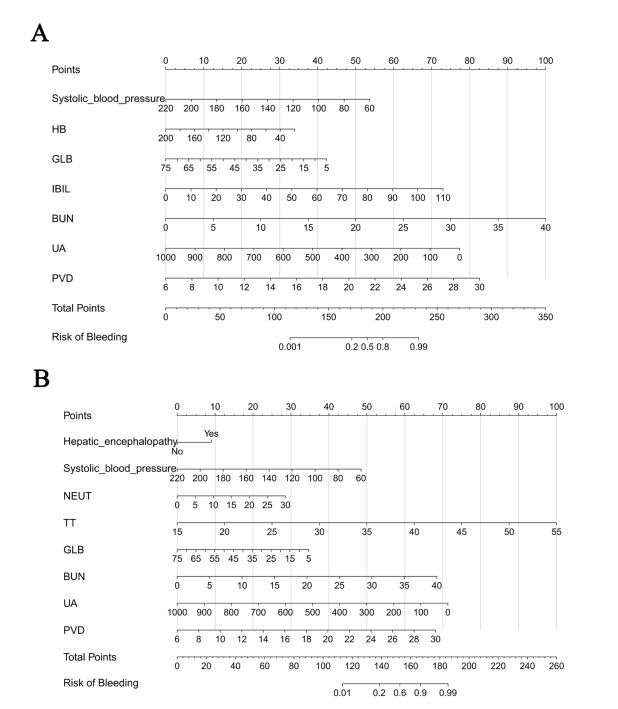
将LASSO回归筛选出的λ.min与λ.1se变量集分别纳入多因素Logistic回归。基于λ.min变量集构建的模型最终保留7项独立预测因子(均P < 0.05),其中收缩压、HB、GLB及UA为保护因素,IBIL、BUN和PVD为危险因素(表 3)。基于λ.1se变量集的模型则筛选出8项独立预测因子(均P < 0.05),危险因素包括肝性脑病、NEUT、TT、BUN和PVD,保护因素包括收缩压、GLB、UA(表 4)。最后,分别对两组预测模型(min与1se模型)进行可视化绘制列线图,见图 2。
| 预测变量 | 回归系数 | OR值 | 95%CI | P值 | |
| 下限 | 上限 | ||||
| 收缩压 | -0.033 | 0.968 | 0.949 | 0.985 | 0.001 |
| HB(g/L) | -0.016 | 0.984 | 0.969 | 0.998 | 0.025 |
| GLB(g/L) | -0.054 | 0.947 | 0.899 | 0.995 | 0.036 |
| IBIL(μmol/L) | 0.044 | 1.044 | 1.003 | 1.092 | 0.043 |
| BUN(mmol/L) | 0.211 | 1.234 | 1.129 | 1.363 | < 0.001 |
| UA(μmol/L) | -0.008 | 0.992 | 0.989 | 0.995 | < 0.001 |
| PVD(mm) | 0.333 | 1.396 | 1.212 | 1.628 | < 0.001 |
| 预测变量 | 回归系数 | OR值 | 95%CI | P值 | |
| 下限 | 上限 | ||||
| 肝性脑病 | 0.994 | 2.703 | 1.038 | 7.355 | 0.045 |
| 收缩压(mmHg) | -0.032 | 0.969 | 0.950 | 0.986 | 0.001 |
| NEUT(×109/L) | 0.144 | 1.155 | 1.014 | 1.334 | 0.038 |
| TT(s) | 0.189 | 1.208 | 1.027 | 1.438 | 0.027 |
| GLB(g/L) | -0.053 | 0.948 | 0.902 | 0.995 | 0.034 |
| BUN(mmol/L) | 0.205 | 1.227 | 1.124 | 1.354 | < 0.001 |
| UA(μmol/L) | -0.008 | 0.992 | 0.988 | 0.995 | < 0.001 |
| PVD(mm) | 0.293 | 1.340 | 1.171 | 1.553 | < 0.001 |
|
| 注:A为基于λ.min筛选变量的模型;B为基于λ.1se筛选变量的模型 图 2 肝硬化患者并发急性上消化道出血的列线图预测模型 Fig 2 Nomogram prediction model for acute upper gastrointestinal bleeding in patients with cirrhosis |
|
|
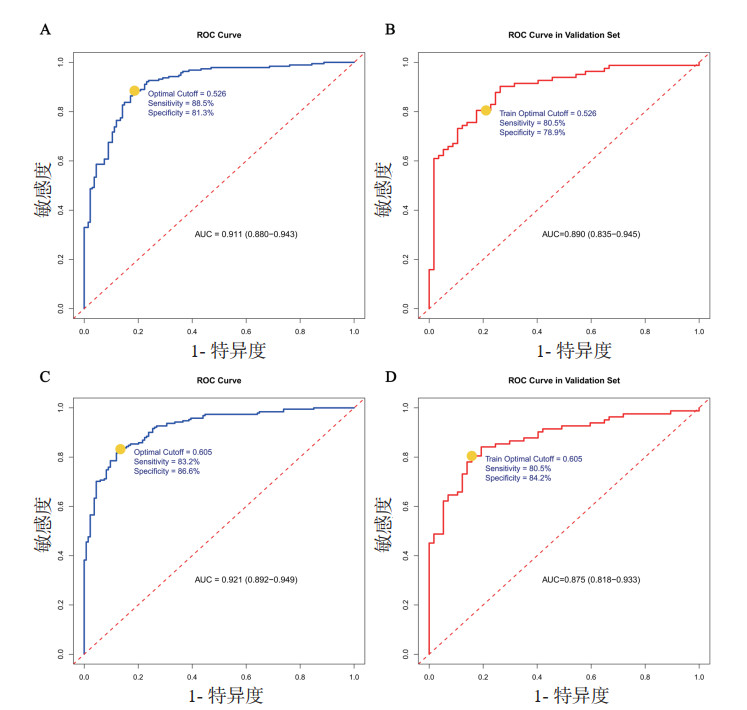
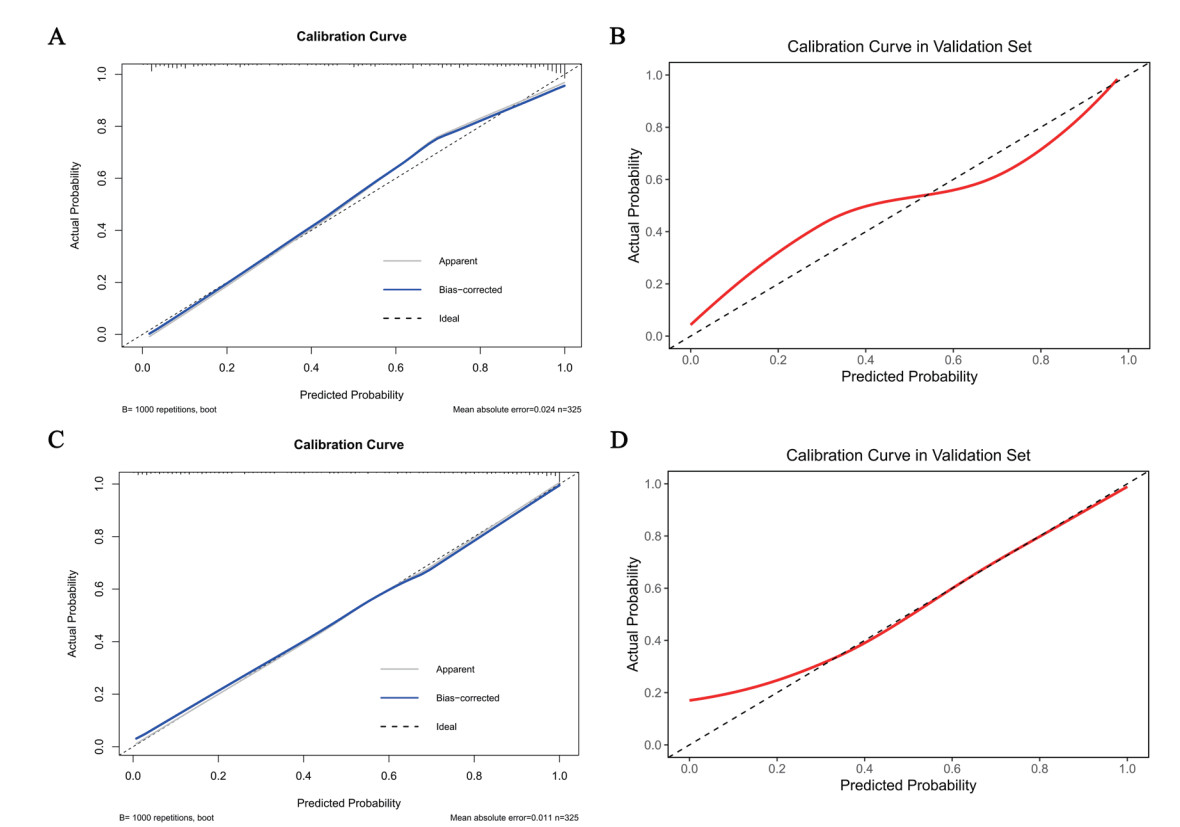
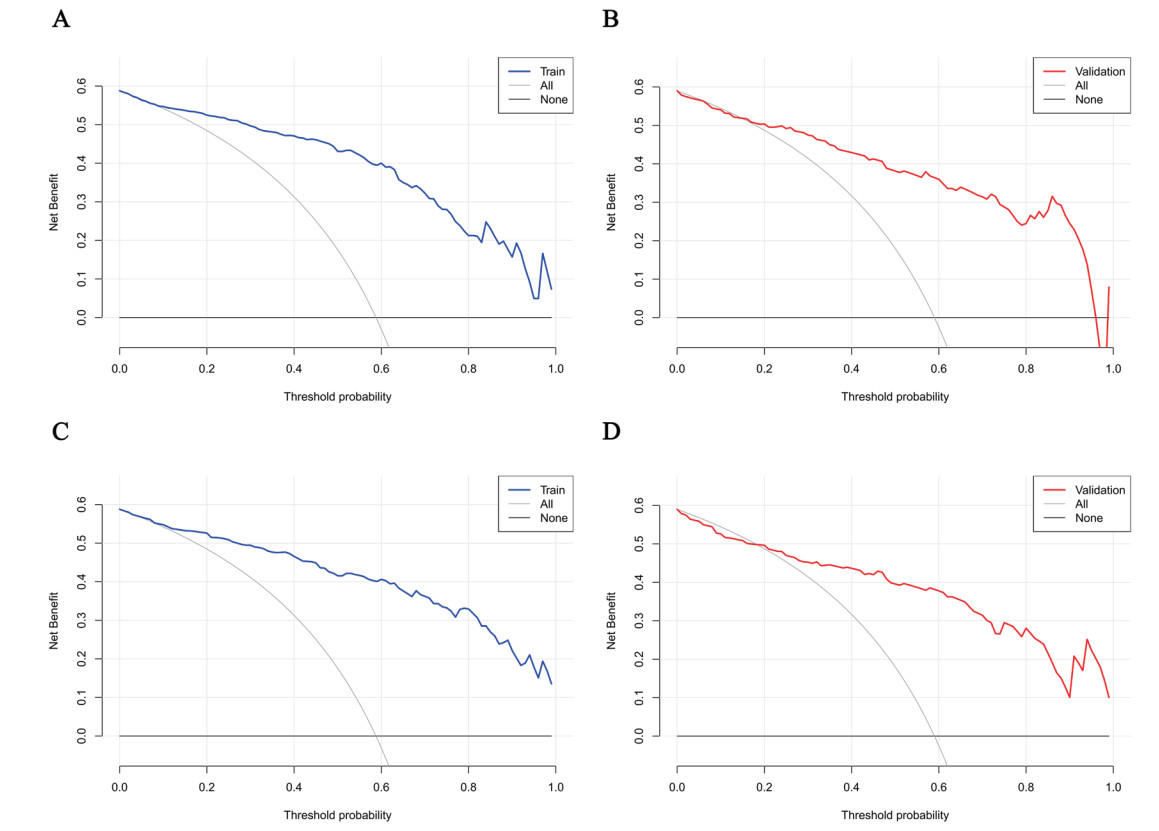
ROC结果显示,min模型与1se模型均表现出良好的判别能力。其AUC在训练集分别为0.911(0.880~0.943)和0.921(0.892~0.949),在验证集中分别为0.890(0.835~0.945)和0.875(0.818~0.933)。在敏感度相近水平下,1se模型在训练集与验证集中均表现出更高的特异度,见图 3。校准度方面,1se模型在训练集(H-L检验P=0.934)与验证集(P=0.068)中均未出现显著偏差,校准曲线贴近理想线,整体优于min模型(验证集P=0.016),见图 4。DCA曲线进一步显示1se模型在更宽的阈值概率范围内具有更高且更稳定的临床净获益,见图 5。所以,1se模型在判别、校准与临床实用性方面均表现更优,具有良好的推广价值。
|
| 注:A:min模型训练集;B:min模型验证集;C:1se模型训练集;D:1se模型验证集;Optimal Cutoff为最佳截断值,Sensitivity为敏感度, Specificity为特异度 图 3 预测模型的ROC曲线 Fig 3 ROC curves of the prediction model |
|
|
|
| 注:A为min模型训练集;B为min模型验证集;C为1se模型训练集;D为1se模型验证集;纵轴表示实际概率,横轴表示预测概率 图 4 预测模型的校准曲线 Fig 4 Calibration curves of the prediction model |
|
|
|
| 注:A为min模型训练集;B为min模型验证集;C为1se模型训练集;D为1se模型验证集;横坐标为阈值概率,纵坐标为净获益 图 5 预测模型的临床决策曲线 Fig 5 DCA of the prediction model |
|
|
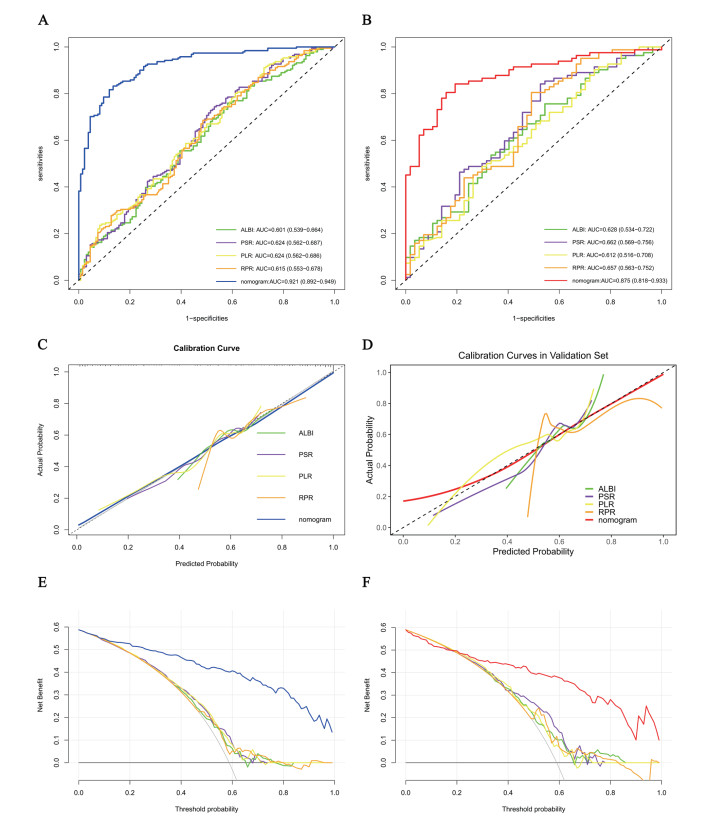
对12种无创评分进行单因素Logistic回归分析,仅ALBI、PSR、PLR和RPR这4种评分与出血风险显著相关(均P < 0.05),其余8种评分无预测价值,见表 5。ROC曲线分析表明,新建1se模型显著优于所有传统无创评分(Delong检验P < 0.001),见表 6。校准曲线显示,传统评分较理想曲线均出现明显偏离。DCA进一步证实,传统评分的临床实用性相对有限。见图 6。
| 变量 | OR值 | 95%CI下限 | 95%CI上限 | P值 |
| ALBI | 1.814 | 1.262 | 2.606 | 0.001 |
| APRI | 1.081 | 0.971 | 1.203 | 0.154 |
| AAR | 0.886 | 0.752 | 1.044 | 0.148 |
| GPR | 1.001 | 0.970 | 1.033 | 0.938 |
| PSR | 0.522 | 0.379 | 0.720 | < 0.001 |
| NLR | 1.010 | 0.971 | 1.052 | 0.613 |
| PLR | 0.995 | 0.993 | 0.998 | < 0.001 |
| RPR | 18.783 | 2.941 | 119.948 | 0.002 |
| RLR | 0.994 | 0.984 | 1.004 | 0.232 |
| FIB-4 | 1.017 | 0.987 | 1.047 | 0.276 |
| King's Score | 1.004 | 1.000 | 1.007 | 0.052 |
| PALBI | 1.434 | 0.841 | 2.446 | 0.186 |
| 项目 | 训练集 | 验证集 | |||||||
| AUC | 95%CI下限 | 95%CI上限 | P值 | AUC | 95%CI下限 | 95%CI上限 | P值 | ||
| ALBI | 0.601 | 0.539 | 0.664 | < 0.001 | 0.628 | 0.534 | 0.722 | < 0.001 | |
| PSR | 0.624 | 0.562 | 0.687 | < 0.001 | 0.662 | 0.569 | 0.756 | < 0.001 | |
| PLR | 0.624 | 0.562 | 0.686 | < 0.001 | 0.612 | 0.516 | 0.708 | < 0.001 | |
| RPR | 0.615 | 0.533 | 0.678 | < 0.001 | 0.657 | 0.563 | 0.752 | < 0.001 | |
| 1se | 0.921 | 0.892 | 0.949 | - | 0.875 | 0.818 | 0.933 | — | |
| 注:表中P值为预测模型与四个无创评分的比较 | |||||||||
|
| 注:A、C、E为训练集,B、D、F为验证集 图 6 ALBI、PSR、PLR、RPR及列线图的ROC曲线、校准曲线、DCA曲线 Fig 6 ROC, Calibration, and DCA Curves of the ALBI, PSR, PLR, RPR and the Nomogram |
|
|
本研究基于常规临床及影像学指标成功构建了一个用于预测肝硬化患者急性上消化道出血风险的列线图模型。分别采用了LASSO回归中λ.min与λ.1se两种准则进行变量初筛,并进一步通过多因素Logistic回归建立了两个预测模型,发现1se模型在统计严谨性与临床实用性间取得了更佳平衡。性能评估显示,1se模型在训练集和验证集中均表现出卓越的判别能力,且其最佳截断值(0.605)在保证敏感度(80.5%)的同时,提供了更高的特异性(84.2%)。校准曲线与决策曲线分析进一步证实该模型具有稳定的预测准确度和广泛的临床净获益。为全面评估新模型价值,本研究将其与12种传统无创评分进行了系统比较。通过筛选,最终纳入分析的相关评分为ALBI、PSR、PLR、RPR。结果显示,新建模型在关键性能指标上全面优于传统无创评分。
肝硬化时,肝内血管结构重塑导致阻力增加,引发门静脉血流动力学改变,使门静脉直径成为评估门脉高压的关键影像学标志。研究普遍证实PVD与肝静脉压力梯度呈正相关。Haag等[26]及Wang等[27]的研究均支持这一观点,后者更明确指出PVD增宽是HVPG升高的独立危险因素。鉴于HVPG > 12 mmHg是静脉曲张出血的明确风险标志[28],PVD与此关联性为其用于出血风险评估提供了理论依据。此外,PVD扩张不仅与食管胃底静脉曲张破裂风险相关,也加重门脉高压性胃病,从而提升非静脉曲张性出血的风险[29]。本研究数据表明,PVD每增加1 mm,出血风险即升高34.0%(OR=1.340),这与既往前瞻性队列研究的结论相吻合[30]。因此,在临床实践中,对肝硬化患者行腹部超声或CT检查时,应常规测量并关注PVD值。其数值的微小增加可能预示着显著升高的出血风险,这为识别高危患者提供了一个易于获取、可量化的影像学预警信号。
肝性脑病与急性上消化道出血同为肝硬化失代偿表现,HE的存在提示门体分流严重和肝功能储备衰竭[7]。门体分流不仅促使肠源性毒素入血诱发HE,亦显著增加食管胃静脉曲张破裂风险[31-32]。值得注意的是,AUGIB后肠道积血会加重血氨负荷,出血所致低血容量休克进一步损害肝肾功能、削弱氨代谢能力,同时出血后感染风险上升,炎症因子与血氨协同加重脑水肿,形成“出血-HE恶化”的恶性循环[33]。多项研究支持HE与出血风险的关联[34-35]。对于因肝性脑病入院的肝硬化患者,即使暂无出血症状,也应被视为出血的极高危人群,需要考虑更积极的预防策略。
尿素氮升高与尿酸降低在本研究中共同揭示了肝硬化出血患者的两种关键病理状态。BUN作为蛋白质代谢终产物,上消化道出血后其升高主要源于肠道对积血中蛋白质分解产物的吸收及继发的肾前性氮质血症[36],使其成为评估出血严重程度及预后的重要生物标志物[37-38]。与之相反,UA作为血浆中重要的抗氧化剂,具备清除多种活性氧及自由基的强大能力[39-40]。据此推测,在肝硬化伴随的氧化应激与内毒素血症状态下,UA可能通过减轻氧化损伤而在维持血管内皮稳态中发挥防御作用。然而,在肝功能严重受损及营养不良状态下,UA合成不足致使其水平下降,抗氧化防御系统衰竭,从而显著增加血管破裂及黏膜糜烂风险。BUN与UA分别从毒性物质蓄积和内源性保护耗竭两个方面,共同构成了评估出血风险的互补生物学指标。
中性粒细胞计数升高被认为与失代偿期的全身性炎症状态密不可分[41]。在肠道菌群移位及肝细胞损伤的触发下,中性粒细胞作为一线免疫细胞被大量活化。活化的中性粒细胞通过释放炎症因子、活性氧及蛋白酶类物质,直接损伤血管内皮,破坏微循环稳态。即便在疾病后期出现功能失调,表现为“免疫麻痹”,其早期活化所触发的炎症级联反应及微循环损伤仍可能持续影响血管稳态。所以,中性粒细胞计数的升高实质上反映了机体高炎症负荷与免疫调节紊乱的病理状态,共同构成了血管稳定性下降和出血风险增加的生物学基础。
球蛋白水平下降可能反映了肝硬化患者病情的严重失代偿与免疫功能受损。此类免疫防线损伤(如黏膜IgA减少)会削弱肠道屏障,促使菌群易位,加剧全身炎症与血管内皮损伤[42]。此外,免疫功能受损增加了感染风险,而感染导致内源性肝素样物质的产生,正是诱发失代偿期患者出血倾向的潜在途径[42-43]。
凝血酶时间延长是评估肝硬化凝血功能障碍的重要指标,直接反映纤维蛋白原向纤维蛋白转化的终末环节效率[44]。肝硬化时肝脏合成功能衰竭,一方面导致纤维蛋白原数量减少[45],另一方面引起纤维蛋白原分子结构异常,即异常纤维蛋白原血症[46]。TT检测对纤维蛋白原的“量不足”与“质缺陷”均高度敏感。此外,肝硬化常见的高纤溶状态可通过抑制纤维蛋白单体聚合,进一步阻碍稳固凝块形成[47]。因此,TT延长同时捕捉了纤维蛋白原质/量缺陷和高纤溶状态对凝血最终步骤的抑制。这使得TT不仅能评估出血风险,还可能为是否需要联合抗纤溶治疗提供线索。
通过监测对比患者的入院收缩压证明了其对急性上消化道出血的保护作用。这一发现凸显了维持全身血流动力学稳定对代偿门脉系统的重要意义。适当的收缩压水平有助于保障内脏器官的有效灌注,缓解门脉高压所致的肠道黏膜缺血与屏障功能损伤[42, 48],最终降低消化道出血的发生风险。
本研究构建的列线图模型,其核心临床价值在于将多维度的指标整合为一个量化、可视化的综合风险评分。为临床实践提供了以下意义:首先,在急诊或门诊时,医生可依据常规检查及影像数据,通过模型快速计算患者的个体化出血风险,从而优先安排高危患者接受紧急内镜干预。其次,可用于住院患者的动态病情评估。此外,模型所选指标均为临床常规检查项目,各级医院均可推广。
然而,本研究为回顾性、单中心,且样本量有限,可能影响模型的普适性,未来需要通过大样本、多中心的前瞻性研究进行外部验证。其次,本研究未针对出血的具体病因进行分层分析,可能会限制模型在不同亚组患者中的精准性,后续研究可在此方面加以深化。综上所述,本研究整合临床及影像学指标通过LASSO回归及多因素Logistic回归,成功构建了一个具有良好的区分度、校准度、临床实用性的列线图预测模型,为肝硬化并发急性上消化道出血的风险预测提供了性能优异的新型工具。
利益冲突 所有作者声明无利益冲突
作者贡献声明 李泽曦:研究设计、数据收集与分析、图表绘制、论文撰写;李静:研究指导、论文审阅与修改
| [1] | 郑文敏, 田元元. 1990-2019年中国肝硬化发病和死亡年龄-时期-队列分析及预测[J]. 疾病监测, 2024, 39(11): 1489-1494. DOI:10.3784/jbjc.202401290061 |
| [2] | Devarbhavi H, Asrani SK, Arab JP, et al. Global burden of liver disease: 2023 update[J]. J Hepatol, 2023, 79(2): 516-537. DOI:10.1016/j.jhep.2023.03.017 |
| [3] | Lecleire S, Di Fiore F, Merle V, et al. Acute upper gastrointestinal bleeding in patients with liver cirrhosis and in noncirrhotic patients: epidemiology and predictive factors of mortality in a prospective multicenter population-based study[J]. J Clin Gastroenterol, 2005, 39(4): 321-327. DOI:10.1097/01.mcg.0000155133.50562.c9 |
| [4] | Zullo A, Soncini M, Bucci C, et al. Clinical outcomes in cirrhotics with variceal or nonvariceal gastrointestinal bleeding: a prospective, multicenter cohort study[J]. J Gastro And Hepatol, 2021, 36(11): 3219-3223. DOI:10.1111/jgh.15601 |
| [5] | Long B, Gottlieb M. Emergency medicine updates: Upper gastrointestinal bleeding[J]. Am J Emerg Med, 2024, 81: 116-123. DOI:10.1016/j.ajem.2024.04.052 |
| [6] | de Franchis R, Bosch J, Garcia-Tsao G, et al. Baveno Ⅶ-Renewing consensus in portal hypertension[J]. J Hepatol, 2022, 76(4): 959-974. DOI:10.1016/j.jhep.2021.12.022 |
| [7] | de Franchis R, Baveno Ⅵ Faculty. Expanding consensus in portal hypertension: Report of the Baveno Ⅵ Consensus Workshop: Stratifying risk and individualizing care for portal hypertension[J]. J Hepatol, 2015, 63(3): 743-752. DOI:10.1016/j.jhep.2015.05.022 |
| [8] | Glisic T, Stojkovic Lalosevic M, Milovanovic T, et al. Diagnostic value of non-invasive scoring systems in the prediction of esophageal varices in patients with liver cirrhosis: single center experience[J]. Medicine, 2022, 58(2): 158. DOI:10.3390/medicina58020158 |
| [9] | Cifci S, Ekmen N. Evaluation of non-invasive fibrosis markers in predicting esophageal variceal bleeding[J]. Clin Endosc, 2021, 54(6): 857-863. DOI:10.5946/ce.2021.028 |
| [10] | 房延儒, 王聪, 虎骁龙, 等. 肝硬化静脉曲张患者上消化道大出血风险的预测模型研究[J]. 中华急诊医学杂志, 2024, 33(5): 671-676. DOI:10.3760/cma.j.issn.1671-0282.2024.05.013 |
| [11] | Wang W, Ju HL, Zhang W, et al. Relationship between platelet-to-lymphocyte ratio and early rebleeding after endoscopic variceal ligation: a bicenter retrospective study[J]. Ann Med, 2024, 56(1): 1-10. DOI:10.1080/07853890.2024.2400315 |
| [12] | Kraja B, Mone I, Akshija I, et al. Predictors of esophageal varices and first variceal bleeding in liver cirrhosis patients[J]. World J Gastroenterol, 2017, 23(26): 4806. DOI:10.3748/wjg.v23.i26.4806 |
| [13] | 中华医学会肝病学分会. 肝硬化诊治指南[J]. 中华肝脏病杂志, 2019, 27(11): 846-865. DOI:10.3760/cma.j.issn.1007-3418.2019.11.008 |
| [14] | Johnson PJ, Berhane S, Kagebayashi C, et al. Assessment of liver function in patients with hepatocellular carcinoma: a new evidence-based approach: the ALBI grade[J]. J Clin Oncol, 2015, 33(6): 550-558. DOI:10.1200/jco.2014.57.9151 |
| [15] | Elshaarawy O, Allam N, Abdelsameea E, et al. Platelet-albumin-bilirubin score-a predictor of outcome of acute variceal bleeding in patients with cirrhosis[J]. World J Hepatol, 2020, 12(3): 99-107. DOI:10.4254/wjh.v12.i3.99 |
| [16] | Wai CT, Greenson JK, Fontana RJ, et al. A simple noninvasive index can predict both significant fibrosis and cirrhosis in patients with chronic hepatitis C[J]. Hepatology, 2003, 38(2): 518-526. DOI:10.1053/jhep.2003.50346 |
| [17] | Cohen JA, Kaplan MM. The SGOT/SGPT ratio: an indicator of alcoholic liver disease[J]. Dig Dis Sci, 1979, 24(11): 835-838. DOI:10.1007/BF01324898 |
| [18] | Lemoine M, Shimakawa Y, Nayagam S, et al. The gamma-glutamyl transpeptidase to platelet ratio (GPR) predicts significant liver fibrosis and cirrhosis in patients with chronic HBV infection in West Africa[J]. Gut, 2016, 65(8): 1369-1376. DOI:10.1136/gutjnl-2015-309260 |
| [19] | Giannini E, Botta F, Borro P, et al. Platelet count/spleen diameter ratio: proposal and validation of a non-invasive parameter to predict the presence of oesophageal varices in patients with liver cirrhosis[J]. Gut, 2003, 52(8): 1200-1205. DOI:10.1136/gut.52.8.1200 |
| [20] | Zhang HG, Sun QQ, Mao WL, et al. Neutrophil-to-lymphocyte ratio predicts early mortality in patients with HBV-related decompensated cirrhosis[J]. Gastroenterol Res Pract, 2016, 2016: 4394650. DOI:10.1155/2016/4394650 |
| [21] | Zhao ZD, Liu JH, Wang JX, et al. Platelet-to-lymphocyte ratio (PLR) and neutrophil-to-lymphocyte ratio (NLR) are associated with chronic hepatitis B virus (HBV) infection[J]. Int Immunopharmacol, 2017, 51: 1-8. DOI:10.1016/j.intimp.2017.07.007 |
| [22] | Chen BD, Ye B, Zhang J, et al. RDW to platelet ratio: a novel noninvasive index for predicting hepatic fibrosis and cirrhosis in chronic hepatitis B[J]. PLoS One, 2013, 8(7): e68780. DOI:10.1371/journal.pone.0068780 |
| [23] | Zhang XY, Wang DW, Chen ZM, et al. Red cell distribution width-to-lymphocyte ratio: a novel predictor for HBV-related liver cirrhosis[J]. Medicine, 2020, 99(23): e20638. DOI:10.1097/md.0000000000020600 |
| [24] | Sterling RK, Lissen E, Clumeck N, et al. Development of a simple noninvasive index to predict significant fibrosis in patients with HIV/HCV coinfection‡[J]. Hepatology, 2006, 43(6): 1317-1325. DOI:10.1002/hep.21178 |
| [25] | Cross TJS, Rizzi P, Berry PA, et al. Kingʼs Score: an accurate marker of cirrhosis in chronic hepatitis C[J]. Eur J Gastroenterol Hepatol, 2009, 21(7): 730-738. DOI:10.1097/meg.0b013e32830dfcb3 |
| [26] | Haag K, Rössle M, Ochs A, et al. Correlation of duplex sonography findings and portal pressure in 375 patients with portal hypertension[J]. Am J Roentgenol, 1999, 172(3): 631-635. DOI:10.2214/ajr.172.3.10063849 |
| [27] | Wang P, Hu XH, Xie F. Predictive value of liver and spleen stiffness measurement based on two-dimensional shear wave elastography for the portal vein pressure in patients with compensatory viral cirrhosis[J]. Peer J, 2023, 11: e15956. DOI:10.7717/peerj.15956 |
| [28] | Garcia-Tsao G, Groszmann RJ, Fisher RL, et al. Portal pressure, presence of gastroesophageal varices and variceal bleeding[J]. Hepatology, 1985, 5(3): 419-424. DOI:10.1002/hep.1840050313 |
| [29] | Zardi EM, Ghittoni G, Margiotta D, et al. Portal hypertensive gastropathy in cirrhotics without varices: a case-control study[J]. Eur J Gastroenterol Hepatol, 2015, 27(1): 91-96. DOI:10.1097/meg.0000000000000234 |
| [30] | Tan BG, Tang Z, Ou J, et al. A novel model based on liver/spleen volumes and portal vein diameter on MRI to predict variceal bleeding in HBV cirrhosis[J]. Eur Radiol, 2023, 33(2): 1378-1387. DOI:10.1007/s00330-022-09107-5 |
| [31] | He XL, Hu MY, Xu Y, et al. The gut-brain axis underlying hepatic encephalopathy in liver cirrhosis[J]. Nat Med, 2025, 31(2): 627-638. DOI:10.1038/s41591-024-03405-9 |
| [32] | Juncu S, Minea H, Girleanu I, et al. Clinical implications and management of spontaneous portosystemic shunts in liver cirrhosis[J]. Diagnostics (Basel), 2024, 14(13): 1372-1385. DOI:10.3390/diagnostics14131372 |
| [33] | Sanyal AJ, Bosch J, Blei A, et al. Portal hypertension and its complications[J]. Gastroenterology, 2008, 134(6): 1715-1728. DOI:10.1053/j.gastro.2008.03.007 |
| [34] | 刘佳, 谷建俐. 回顾性分析肝硬化并上消化道出血的临床特征及预后危险因素[J]. 现代消化及介入诊疗, 2018, 23(1): 52-54. DOI:10.3969/j.issn.1672-2159.2018.01.016 |
| [35] | 朱思奇, 赵祥安, 王甦. 肝硬化伴食管胃底静脉曲张出血的影响因素及3种模型对再出血的预测价值[J]. 实用临床医药杂志, 2021, 25(16): 49-53. DOI:10.7619/jcmp.20211353 |
| [36] | Cohn TD, Lane M, Zuckerman S, et al. Induced azotemia in humans following massive protein and blood ingestion and the mechanism of azotemia in gastrointestinal hemorrhage[J]. Am J Med Sci, 1956, 231(4): 394-401. DOI:10.1097/00000441-195604000-00004 |
| [37] | 李珍艳, 杨小莉, 李罗红, 等. GPDA、BUN及Cr在消化道出血患者中的水平及意义[J]. 四川医学, 2020, 41(6): 593-596. DOI:10.16252/j.cnki.issn1004-0501-2020.06.008 |
| [38] | Kumar NL, Claggett BL, Cohen AJ, et al. Association between an increase in blood urea nitrogen at 24 hours and worse outcomes in acute nonvariceal upper GI bleeding[J]. Gastrointest Endosc, 2017, 86(6): 1022-1027.e1. DOI:10.1016/j.gie.2017.03.1533 |
| [39] | Ames BN, Cathcart R, Schwiers E, et al. Uric acid provides an antioxidant defense in humans against oxidant- and radical-caused aging and cancer: a hypothesis[J]. Proc Natl Acad Sci U S A, 1981, 78(11): 6858-6862. DOI:10.1073/pnas.78.11.6858 |
| [40] | Cutler RG. Urate and ascorbate: their possible roles as antioxidants in determining longevity of mammalian species[J]. Arch Gerontol Geriatr, 1984, 3(4): 321-348. DOI:10.1016/0167-4943(84)90033-5 |
| [41] | Engelmann C, Clària J, Szabo G, et al. Pathophysiology of decompensated cirrhosis: Portal hypertension, circulatory dysfunction, inflammation, metabolism and mitochondrial dysfunction[J]. J Hepatol, 2021, 75: S49-S66. DOI:10.1016/j.jhep.2021.01.002 |
| [42] | Albillos A, de Gottardi A, Rescigno M. The gut-liver axis in liver disease: Pathophysiological basis for therapy[J]. J Hepatol, 2020, 72(3): 558-577. DOI:10.1016/j.jhep.2019.10.003 |
| [43] | Tripodi A, Mannucci PM. The coagulopathy of chronic liver disease[J]. N Engl J Med, 2011, 365(2): 147-156. DOI:10.1056/nejmra1011170 |
| [44] | Undas A. Determination of fibrinogen and thrombin time (TT)[M]//Hemostasis and Thrombosis. New York, NY: Springer New York, 2017: 105-110. DOI: 10.1007/978-1-4939-7196-1_8. |
| [45] | Usmani A, Laknezhad S, De Simone N, et al. Observed incidence of hypofibrinogenemia in cirrhotic patients[J]. Liver Int, 2021, 41(10): 2523-2524. DOI:10.1111/liv.15035 |
| [46] | Cunningham MT, Brandt JT, Laposata M, et al. Laboratory diagnosis of dysfibrinogenemia[J]. Arch Pathol Lab Med, 2002, 126(4): 499-505. DOI:10.5858/2002-126-0499-ldod |
| [47] | Ferro D, Celestini A, Violi F. Hyperfibrinolysis in liver disease[J]. Clin Liver Dis, 2009, 13(1): 21-31. DOI:10.1016/j.cld.2008.09.008 |
| [48] | Iwakiri Y, Groszmann RJ. The hyperdynamic circulation of chronic liver diseases: from the patient to the molecule[J]. Hepatology, 2006, 43(Supplement 1): S121-S131. DOI:10.1002/hep.20993 |
 2026, Vol. 35
2026, Vol. 35