2. 南昌大学江西医学院第一附属医院重症医学科, 南昌 330006;
3. 温州医科大学附属苍南医院肿瘤内科, 温州 325800;
4. 南昌大学江西医学院第一附属医院心脏大血管外科ICU, 南昌 330006
2. Department of Critical Care Medicine, the First Affiliated Hospital, Jiangxi Medical College, Nanchang University, Nanchang 330006, China;
3. Department of Oncology, The People's Hospital of Cangnan Zhejiang, Wenzhou Medical University, Wenzhou 325800, China;
4. Department of Cardiovascular Surgery ICU, The First Affiliated Hospital, Jiangxi Medical College, Nanchang University, Nanchang 330006, China
脓毒症是一种由感染引发的危及生命的临床综合征[1],其全球发病率与病死率仍居高不下。据统计,全球每年约有1.66亿脓毒症病例,其中2 140万例患者死于脓毒症[2]。尽管早期救治水平不断提高,脓毒症幸存者仍面临严重的远期并发症,以进行性肌肉萎缩与功能障碍最为显著[3-4]。其病理过程不仅涉及急性期的高分解代谢与炎症风暴,更与慢性的持续性炎症、免疫抑制及蛋白质代谢紊乱密切相关[5-7]。为系统描述这一临床表型,Gentile等[8]提出了“持续性炎症-免疫抑制-分解代谢综合征”(persistent inflammation, immunosuppression, and catabolism syndrome,PICS)的概念,旨在阐明脓毒症后慢性阶段中炎症、免疫与分解代谢三者间的复杂相互作用机制。
骨骼肌是机体最主要的蛋白质储备库,在脓毒症期间成为蛋白质分解代谢的关键靶点[9]。肌肉萎缩不仅直接导致躯体功能下降,还与胰岛素抵抗、感染风险增加及不良预后密切相关。值得注意的是,肌肉萎缩并非脓毒症的孤立局部表现,而是与全身性炎症反应紧密关联,这进一步凸显了深入研究脓毒症后肌肉萎缩的重要性。因此,建立能准确模拟临床脓毒症不同阶段肌肉萎缩特征的动物模型,对于深入揭示其发病机制、探索有效干预策略至关重要。经典的盲肠结扎穿刺(cecal ligation and puncture, CLP)模型被广泛用于模拟脓毒症急性期,但其在复现慢性肌肉消耗过程方面存在局限[10]。
为此,近年来基于PICS的脓毒症晚期观察模型,以及PICS联合脂多糖(lipopolysaccharide, LPS)二次打击(PIICS)等模型逐渐受到关注[11-12]。然而,既往研究多侧重于单一时间点或急性期的病理改变,对不同模型在模拟脓毒症肌肉萎缩病理进程方面缺乏系统性比较。本研究旨在系统比较CLP、PICS及PIICS三种方法在构建小鼠脓毒症肌肉萎缩模型中的效果,以期为相关机制研究筛选出更贴近临床的理想动物模型。
1 材料与方法 1.1 实验动物本研究选用C57BL/6J小鼠,6周龄,雄性,体重20~22 g,购于杰禾开(南昌)生物科技有限责任公司。所有小鼠都饲养在特定的无病原体设施中,并保持定期的12 h明暗循环,饲养温度维持在22~27 ℃,湿度控制在45%~55 %之间。所有动物均可自由获取标准饲料和饮水。本研究中所有涉及动物的实验程序均已通过南昌大学第一附属医院实验动物福利伦理审查委员会的批准,批准号为:CDYFY-IACUC-202512GR040。所有操作均符合实验动物福利伦理的规定。
1.2 主要仪器和试剂本实验主要试剂及使用仪器如下:苏木精-伊红(H & E)染液购自武汉金开瑞生物工程有限公司。TransZol Up总RNA提取试剂盒及PerfectStart® Green qPCR SuperMix购自北京全式金生物技术股份有限公司(TransGen Biotech)。Hifair® Ⅲ 1st Strand cDNA Synthesis SuperMix for qPCR(gDNA digester plus)购自上海翌圣生物科技股份有限公司(Yeasen)。主要仪器:CO2培养箱(赛默飞世尔科技公司),离心机(Esco),NanoDrop One分光光度计(赛默飞世尔科技公司),LightCycler 96 Instrument实时荧光定量PCR仪(上海罗氏制药有限公司)。Kondziela倒置金属网格(上海欣软信息科技有限公司),跑步机(上海欣软信息科技有限公司)。
1.3 实验分组及处理按随机数字表法将小鼠分为4组:假手术组(Sham)、CLP组、PICS组、PICS联合LPS二次打击组(PIICS),每组10只。CLP组是通过盲肠结扎穿孔的外科手术诱发,先对小鼠进行异氟烷吸入麻醉(诱导3%,维持1.5%~2%),并做一个小的中线腹部切口。然后将盲肠外化,盲肠远端的33%用5-0丝结扎,用21 G针头刺穿结扎的盲肠一次,从穿孔轻轻挤出少量粪便,确保穿刺通畅。然后将盲肠重新纳入腹腔,并闭合切口。在Sham组中,开腹后仅游离盲肠,不进行结扎与穿孔,其余步骤与CLP组相同。所有小鼠在CLP术后接受1 mL无菌PBS进行液体复苏。在PICS组中,在CLP术后,不予以任何干预,持续观察至第8天,处死小鼠,用于模拟PICS状态。在PIICS组中,在CLP术后第11天,对存活小鼠腹腔注射1 mg/kg LPS[12],以模拟二次打击,并持续观察至第14天,处死小鼠。实验终点时,先采用异氟烷深度麻醉小鼠至无知觉状态,确认麻醉深度后实施颈椎脱臼法处死。
1.4 检测指标及方法 1.4.1 生存率、体重及饮食变化监测于CLP术前及术后每日定时采用电子天平称量并记录各组小鼠的体重。连续观察14 d,记录各组小鼠的死亡情况。绘制体重变化曲线和生存曲线,并计算最终生存率。每日称量小鼠饲料重量,绘制摄食量变化曲线。
1.4.2 功能学评估在实验终点,采用Kondziela倒置筛检测试评估各组小鼠的肌力、递增重量测试测定前肢握力及跑步机训练用来测试耐力。Kondziela倒置筛检:测试时,将小鼠置于金属网格中心,2 s内将其旋转至头朝下倒置状态,并记录小鼠在网格上悬挂的持续时间。重量测试:测试装置包含7个重量砝码(20、33、46、59、72、85和98 g)。测试时,实验者握住小鼠尾部中段,使其前爪抓握置于实验台上的金属丝。待小鼠前爪握紧后,缓慢向上提起,直至小鼠完全离开台面。若小鼠能保持抓握3 s,则换用下一个较重砝码;若在3 s内掉落,则记录当前砝码重量。最终总分的计算方法为最重链中保持完整3 s的链接数量乘以保持时间(s)。跑步机训练:使用电动速度可控的跑步机系统对小鼠进行运动能力测试。正式测试前,小鼠先进行适应性训练:以0 m/min的初始速度适应5 min,随后以6 m/min的低速再适应5 min。正式测试时,起始速度设定为6 m/min,每2 min增加3 m/min,直至小鼠力竭。疲劳判定标准为小鼠后肢在电击栅格上停留超过10 s。
1.4.3 后肢骨骼肌质量评估在实验终点处死小鼠后,迅速剥离并称量双侧后肢的胫骨前肌和腓肠肌的湿重。通过计算肌肉质量与体重的百分比(肌肉质量/体重×100%),以评估各组小鼠的肌肉萎缩程度。
1.4.4 实时荧光定量PCR(RT-qPCR)检测基因表达取小鼠胫骨前肌组织,使用TransZol Up试剂盒提取总RNA。简要步骤如下:将组织置于含钢珠的研磨管中,加入1 mL TRIzol进行匀浆。随后依照试剂盒说明书进行RNA提取。使用DEPC处理水溶解RNA沉淀。利用NanoDrop One分光光度计测定RNA的浓度和纯度。取1 μg总RNA,使用Hifair® Ⅲ 1st Strand cDNA Synthesis SuperMix for qPCR(gDNA digester plus)试剂盒将其逆转录为cDNA。引物设计基于GenBank基因序列,利用NCBI Primer-BLAST在线工具设计。所有引物均经过熔解曲线分析和标准曲线验证,扩增效率在90%以上。以合成的cDNA为模板,使用PerfectStart® Green qPCR SuperMix在LightCycler® 96系统上进行反应,扩增循环数为45。检测肌肉萎缩相关基因(Atrogin-1, Murf-1)及炎症因子(IL-4, IL-6, IL-10, TNF-α)的mRNA相对表达水平。以Actin为内参基因,采用2-ΔΔCt法进行数据分析。引物序列见表 1。
| 基因 | 引物序列 |
| Atrogin-1 | F:CTTCTCGACTGCCATCCTGGAT |
| R:TCTTTTGGGCGATGCCACTCAG | |
| Murf1 | F:TACCAAGCCTGTGGTCATCCTG |
| R:ACGGAAACGACCTCCAGACATG | |
| IL-4 | F:GGTCTCAACCCCCAGCTAGT |
| R:GCCGATGATCTCTCTCAAGTGAT | |
| IL-6 | F:TAGTCCTTCCTACCCCAATTTCC |
| R:TTGGTCCTTAGCCACTCCTTC | |
| IL-10 | F:GCTCTTACTGACTGGCATGAG |
| R:CGCAGCTCTAGGAGCATGTG | |
| TNF-α | F:CCCTCACACTCAGATCATCTTCT |
| R:GCTACGACGTGGGCTACAG | |
| Actin | F:GGCTGTATTCCCCTCCATCG |
| R:CCAGTTGGTAACAATGCCATGT |
取新鲜胫骨前肌组织,置于4 %多聚甲醛溶液中固定48 h。固定后的组织经梯度乙醇脱水、二甲苯透明、石蜡浸润和包埋后,制备成3~5 μm厚的石蜡切片。将切片进行HE染色。在光学显微镜下观察肌肉组织的病理学形态改变,并采集图像。使用Image J软件测量肌纤维的横截面积(Cross-sectional area,CSA)并进行量化分析。
1.5 统计学方法所有数据采用SPSS 29.0和GraphPad Prism 10.1.2软件进行统计分析。所有计量资料均进行Shapiro-Wilk正态性检验和Levene方差齐性检验。符合正态分布且方差齐的计量资料以均数±标准差(x±s)表示,组间的均数比较采用单因素方差分析(One-way ANOVA),事后两两比较采用Tukey's test;不符合正态分布的资料以中位数(四分位数间距)表示,多组间比较采用Kruskal-Wallis H检验,事后两两比较采用Dunn's test。采用Kaplan-Meier法绘制生存曲线,并使用Log-rank检验进行组间生存率比较。所有检验均为双侧检验,以P < 0.05为差异有统计学意义。
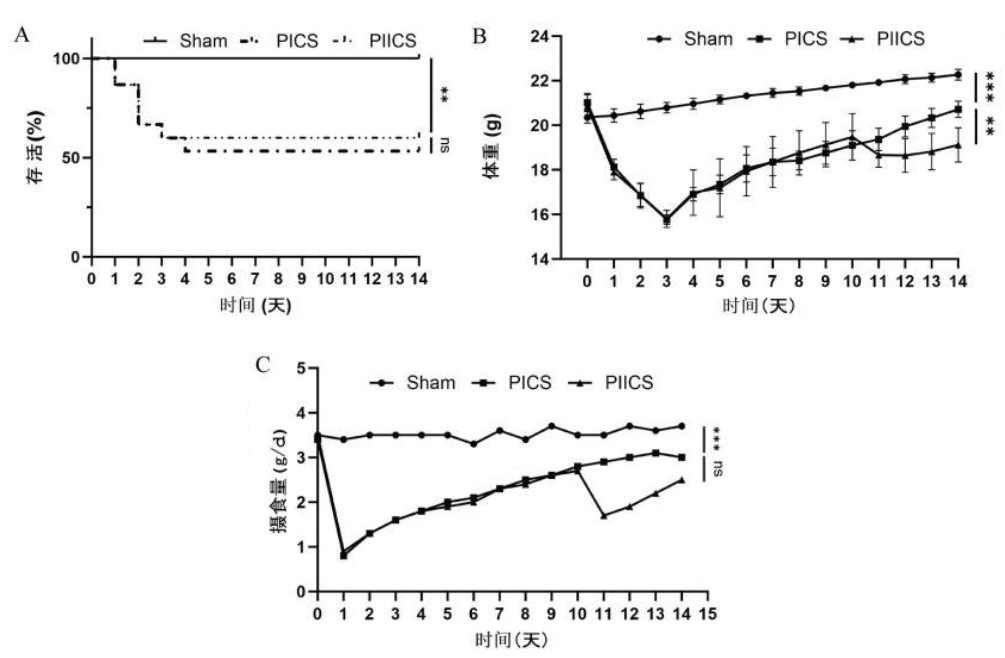
2 结果 2.1 小鼠生存率、体重及摄食量变化连续14 d监测了各组小鼠的生存率和体重变化。如图 1A所示,与Sham组相比,PICS组与PIICS组小鼠的14 d累积生存率显著降低(P < 0.05)。体重变化趋势如图 1B所示。Sham组小鼠体重在观察期内呈现稳步增长。相反,PICS组和PIICS组小鼠体重在术后3 d内急剧下降。从第4天起,PICS组小鼠体重停止下降并开始缓慢恢复。PIICS组小鼠体重同样在第4天后开始回升,但在第11天经LPS二次打击后,其体重增加趋势显著减慢(P < 0.05)。摄食量如图 1C所示。与Sham组相比,PICS组和PIICS组小鼠术后摄食量均显著降低(P < 0.05)。Sham组小鼠摄食量在14 d观察期内维持稳定水平。PICS组小鼠摄食量在术后第1天急剧下降,随后逐步恢复。PIICS组小鼠摄食量变化趋势与PICS组相似,第11天经LPS二次打击后,PIICS组小鼠摄食量出现一过性下降,但与PICS组相比差异无统计学意义(P > 0.05)。见图 1。
|
| 注:A为不同建模方法小鼠的14d存活率;B为不同建模方法小鼠的握力测试;C为不同建模方法小鼠摄食量的变化 图 1 不同建模方法对脓毒症小鼠生存曲线、体重及摄食量变化的影响(n=15) Fig 1 Effects of different sepsis models on survival rate, body weight and food intake changes in mice(n=15) |
|
|
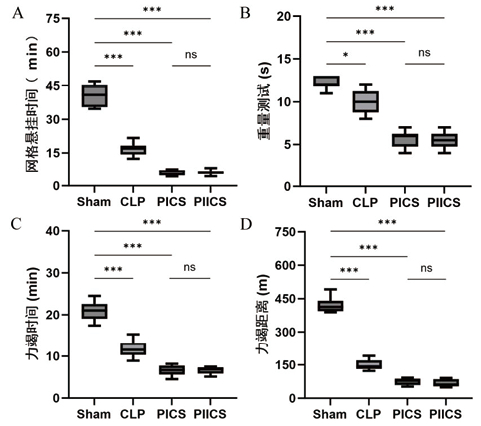
与Sham组相比,CLP组小鼠悬挂时间(图 2A)、前肢抓力(图 2B)、运动力竭时间(图 2C)及力竭距离(图 2D)均显著降低(P < 0.05),提示脓毒症急性期即出现全身性肌肉功能障碍。进一步比较发现,PICS组与PIICS组上述指标较CLP组进一步下降,表明脓毒症后遗症期肌肉功能损害持续进展。值得注意的是,PICS组与PIICS组间各指标差异均无统计学意义(P > 0.05)。见图 2。
|
| 注:A为不同建模方法小鼠网格悬挂的时间;B为不同建模方法小鼠重量的测试,每组;C为不同建模方法小鼠力竭的时间;D为不同建模方法小鼠力竭的距离 图 2 不同建模方法对脓毒症小鼠肌肉力量的影响(n=6) Fig 2 Effects of different sepsis models on muscle strength in mice(n=6) |
|
|
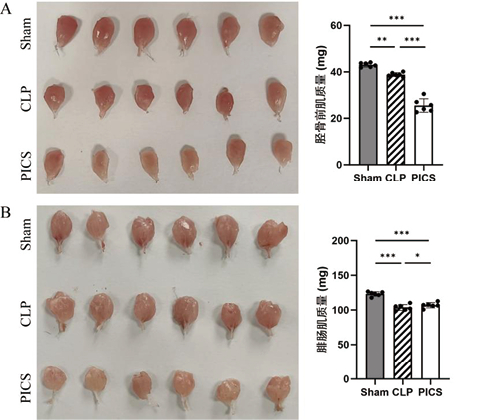
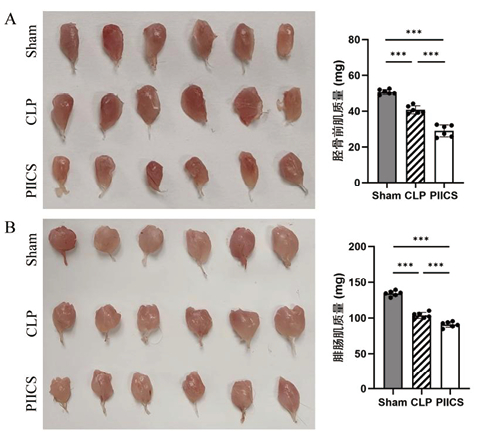
为评估肌肉质量的变化,在实验终点测量了小鼠后肢胫骨前肌和腓肠肌的湿重。结果显示,与Sham组相比,CLP组的胫骨前肌和腓肠肌湿重降低差异有统计学意义(P < 0.05),表明脓毒症成功诱导了肌肉萎缩。进一步比较发现,与CLP组相比,PICS组和PIICS组的胫骨前肌和腓肠肌湿重均进一步显著下降(P < 0.05),提示脓毒症晚期会加剧肌肉的消耗。见图 3及图 4。
|
| 注:A为Sham组、CLP组、PICS组小鼠胫骨前肌的大体照片和湿重;B为Sham组、CLP组、PIICS组小鼠腓肠肌的大体照片和湿重 图 3 Sham、CLP、PICS组小鼠后肢骨骼肌质量的比较(代表性图片,n=6) Fig 3 Comparison of hindlimb skeletal muscle mass among Sham, CLP, and PICS groups(Representative image, n=6) |
|
|
|
| 注:A为Sham组、CLP组、PIICS组小鼠胫骨前肌的大体照片和湿重;B为Sham组、CLP组、PIICS组小鼠腓肠肌的大体照片和湿重 图 4 Sham、CLP、PⅡCS组小鼠后肢骨骼肌质量的比较(代表性图片,n=6) Fig 4 Comparison of hindlimb skeletal muscle mass among Sham, CLP, and PIICS groups(Representative image, n=6) |
|
|
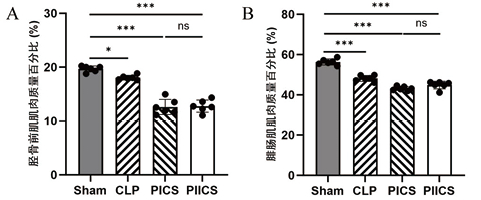
为了校正体重变化对肌肉质量的影响,计算了肌肉湿重与体重的百分比。与Sham组相比,CLP组、PICS组和PIICS组小鼠的胫骨前肌与腓肠肌质量占体重百分比均显著下降(P < 0.05)。相似地,与CLP组相比,PICS组和PIICS组出现了更为严重的肌肉丢失(P < 0.05),而PICS组与PIICS组之间差异无统计学意义(P > 0.05)。见图 5。
|
| 注:A为各组小鼠胫骨前肌的质量百分比;B为各组小鼠腓肠肌的质量百分比 图 5 Sham、CLP、PICS、PIICS组小鼠后肢骨骼肌质量减少程度的比较(n=6) Fig 5 Comparison of hindlimb skeletal muscle atrophy among the Sham, CLP, PICS, and PIICS groups(n=6) |
|
|
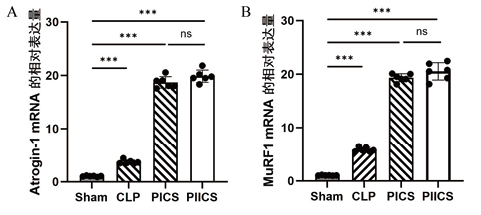
与Sham组相比,CLP组、PICS组和PIICS组小鼠胫骨前肌中促肌肉蛋白降解基因Atrogin-1与Murf1的表达均上调(P < 0.05),且PICS组与PIICS组显著高于CLP组(P < 0.05)。见图 6。
|
| 注:A为各组小鼠胫骨前肌Atrogin-1的相对表达水平(n=6);B为各组小鼠胫骨前肌Murf1的相对表达水平 图 6 Sham、CLP、PICS、PIICS组小鼠促肌肉分解蛋白基因表达水平的比较(n=6) Fig 6 Comparison of muscle atrophy-related gene expression among the Sham, CLP, PICS, and PIICS groups(n=6) |
|
|
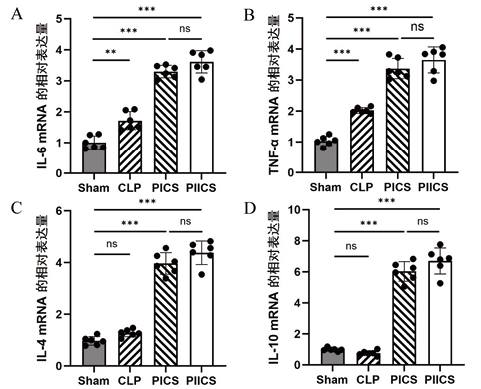
为评估肌肉组织的局部炎症状态,检测了促炎及抗炎细胞因子的表达水平。与Sham组相比,CLP组、PICS组及PIICS组小鼠胫骨前肌中促炎因子IL-6与Tnf-α表达水平均显著升高(P < 0.05)。同时抗炎因子IL-4与IL-10表达在PICS组及PIICS组中也呈现出升高趋势(P < 0.05)。见图 7。
|
| 注:A为各组小鼠胫骨前肌IL-6 mRNA的相对表达水平;B为各组小鼠胫骨前肌TNF-α mRNA的相对表达水平;C为各组小鼠胫骨前肌IL-4 mRNA的相对表达水平;D为各组小鼠胫骨前肌IL-10 mRNA的相对表达水平 图 7 Sham、CLP、PICS、PIICS肌肉组织炎症细胞因子表达水平的比较(n=6) Fig 7 Comparison of inflammatory cytokine expression in skeletal muscle among the Sham, CLP, PICS, and PIICS groups(n=6) |
|
|
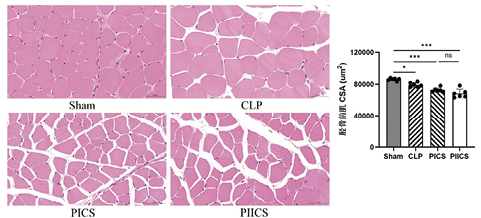
通过HE染色,观察了各组小鼠胫骨前肌的组织形态学变化。Sham组小鼠胫骨前肌肌纤维排列整齐、形态规则,CLP组、PICS组及PIICS组则可见肌纤维横截面积减小、间隙增宽,伴炎性细胞浸润,提示肌肉组织发生明显萎缩与炎症改变。
为了量化肌肉萎缩程度,测量了肌纤维的横截面积,与Sham组相比,CLP组、PICS组及PIICS组肌纤维横截面积均减小(P < 0.05)。值得注意的是,与CLP组相比,PICS组及PIICS组肌纤维横截面积进一步减小(P < 0.05),这与肌肉湿重的测量结果一致。见图 8。
|
| 图 8 Sham、CLP、PICS、PⅡCS胫骨前肌的HE染色和肌纤维横截面积的比较(n = 6) Fig 8 H & E staining and analysis of myofiber cross-sectional area in the tibialis anterior muscle from the Sham, CLP, PIICS, and PIICS groups(n = 6) |
|
|
本研究通过构建并对比经典的CLP急性脓毒症模型、模拟慢性危重症的PICS模型,以及模拟二次打击的PIICS模型,系统评估了它们在诱导小鼠骨骼肌萎缩方面的共性与差异。研究结果表明,这三种模型均能成功诱导脓毒症相关的肌肉萎缩,但其病理生理过程的动态演变和临床模拟的侧重点各有不同。从表型上看,单纯CLP模型引发了急性的体重下降和肌肉萎缩,而PICS与PIICS模型展现了更为持久和复杂的体重及肌力变化和肌肉组织病理改变。尤其是在PIICS模型中,LPS的二次打击显著阻碍了摄食量及体重的恢复趋势。PICS与PIICS模型的肌肉萎缩程度都显著高于CLP模型,这一现象有力地证明,脓毒症肌肉萎缩不仅仅出现在急性代谢紊乱阶段,脓毒症晚期慢性消耗状态,或继发感染导致的肌肉萎缩更为严重。
本研究的核心发现证实,3种模型均能从多个维度诱导显著的骨骼肌萎缩。无论是肌肉的绝对质量还是校正体重后的相对质量,模型组均显著低于假手术组。组织病理学检查直观地展示了肌纤维横截面积的缩小和组织结构的紊乱,这是肌肉萎缩的关键证据。在分子机制层面,笔者发现肌肉萎缩的关键分子标志物,E3泛素连接酶Atrogin-1与MuRF1的mRNA表达在所有模型组中均显著上调[13-14]。这表明,无论是在急性还是慢性阶段,泛素-蛋白酶体系统的过度激活都是驱动脓毒症肌肉蛋白降解的核心通路。
研究发现脓毒症可诱导肌肉中中性粒细胞浸润,进而导致肌肉萎缩和肌力下降,这与本研究中各模型组均出现肌纤维横截面积减小、排列紊乱等典型萎缩改变相呼应,进一步证实了脓毒症诱导肌肉萎缩的炎症机制[15]。此外,TNF-α、IL-6会增加血管通透性,诱发局部组织水肿,减慢毛细血管的流动,减少肌肉的营养供应,并导致肌肉萎缩[16]。本研究结果显示,促炎因子IL-6、TNF-α的表达在各模型组中均上升,抗炎因子IL-4、IL-10也呈现相应改变,提示模型成功诱发了局部与全身炎症与抗炎反应,与临床脓毒症免疫紊乱特征相符[17]。PICS模型中,抗炎因子的升高反映了CLP术后持续8 d的慢性免疫抑制状态,属于代偿性抗炎反应综合征的渐进性发展[8];而PIICS模型中,尽管第14天检测时IL-4、IL-10表达水平与PICS组相近,但其经历了CLP术后11 d的慢性期基础叠加LPS二次打击的急性应激反应,抗炎因子的升高可能呈现“基线水平持续+二次打击后持续升高”的特征[12]。这一推测与Gentile等提出的PICS概念及Chen等构建的PIICS模型原理相符——PIICS通过模拟临床脓毒症恢复期患者继发感染的病理过程,更能反映免疫抑制状态下机体应对新挑战的反应性缺陷[8, 18]。从肌肉萎缩角度看,两种模型中IL-4、IL-10的持续高表达均与Atrogin-1、MuRF1的上调及肌纤维横截面积减小密切相关,提示无论抗炎反应是渐进性还是波动型,其最终都通过激活泛素-蛋白酶体系统促进肌肉蛋白降解。未来研究若能补充LPS二次打击后不同时间点的动态检测,有望揭示PIICS模型中抗炎因子表达的“双峰”特征,从而更精准地模拟临床脓毒症晚期免疫抑制的时相性变化。
不同类型的脓毒症动物模型适用于回答不同的科学问题。经典的CLP模型因其高重复性和对急性期病理生理的高度模拟,是研究急性脓毒症及其早期并发症的理想工具[19-20]。然而,临床上许多脓毒症患者的肌肉萎缩问题主要出现在存活后的慢性恢复期。本研究中的PICS模型,通过延长观察周期,展现了持续的体重减轻、肌肉消耗和免疫紊乱,这与先前研究构建的慢性危重症模型表型高度一致,证明其是模拟脓毒症后慢性消耗与代谢异常的可靠模型[21]。而PIICS模型则精准地模拟了临床上脓毒症恢复期患者因二次感染而导致病情反复和功能恶化的情景,具有独特的临床转化价值[18]。
本研究存在一定的局限性:机制层面,未检测自噬-溶酶体通路(LC3、P62等)及泛素-蛋白酶体系统标志物,也未评估神经肌肉接头结构与功能,对肌萎缩的分子机制认识不够深入;模型层面,未叠加机械通气、长期制动等ICU常见因素,与真实临床场景存在一定差距;观察层面,本研究虽已监测摄食量和体重变化,但未对小鼠的自发活动进行量化评估,因此无法完全排除组间活动度差异对肌肉质量的潜在混杂影响。后续研究可补充自噬流检测和神经肌肉接头电生理记录,并增加行为学测试以评估肢体活动功能;尝试构建复合因素模型。
综上所述,CLP、PICS与PIICS三种建模方法均能有效诱导小鼠产生脓毒症相关肌肉萎缩,其特征涵盖了宏观肌肉质量下降、组织病理学改变、关键分解代谢通路激活以及复杂的局部炎症反应。然而,鉴于临床上脓毒症导致的严重肌肉萎缩和功能障碍更多是其迁延不愈的晚期并发症,传统的CLP模型在模拟这一长期病程方面存在局限。因此,能够更好模拟持续性炎症、免疫抑制和分解代谢综合征的PICS模型,以及模拟二次打击的PIICS模型,是研究脓毒症晚期肌肉萎缩潜在机制及评估长期干预策略的更优选择,为未来的转化研究提供了更为精准的动物模型。
利益冲突 所有作者声明无利益冲突
作者贡献声明 李洋、黄美玲:研究设计、实验操作、论文撰写;陈辉、杨馨怡、温学欢:数据整理、统计分析;刘芬、白松杰:监督指导、论文审阅与修订
| [1] | Dellinger RP, Rhodes A, Evans L, et al. Surviving sepsis campaign[J]. Crit Care Med, 2023, 51(4): 431-444. DOI:10.1097/ccm.0000000000005804 |
| [2] | GBD 2021 Global Sepsis Collaborators. Global, regional, and national sepsis incidence and mortality, 1990-2021: a systematic analysis[J]. Lancet Glob Health, 2025, 13(12): e2013-e2026. |
| [3] | Meyer NJ, Prescott HC. Sepsis and septic shock[J]. N Engl J Med, 2024, 391(22): 2133-2146. DOI:10.1056/nejmra2403213 |
| [4] | Wu ZS, Chen FH, Xiao C, et al. Long-term cardiovascular outcomes and risk factors in adult sepsis survivors: a systematic review and meta-analysis[J]. World J Emerg Med, 2025, 16(5): 423. DOI:10.5847/wjem.j.1920-8642.2025.098 |
| [5] | Deinhardt-Emmer S, Chousterman BG, Schefold JC, et al. Sepsis in patients who are immunocompromised: diagnostic challenges and future therapies[J]. Lancet Respir Med, 2025, 13(7): 623-637. DOI:10.1016/s2213-2600(25)00124-9 |
| [6] | 王亚南, 王梦晴, 任云飞, 等. 脓毒症免疫抑制细胞的变化及其与预后关系的研究进展[J]. 中华急诊医学杂志, 2025, 34(2): 264-271. DOI:10.3760/cma.j.issn.1671-0282.2025.02.021 |
| [7] | Chadda KR, Puthucheary Z. Persistent inflammation, immunosuppression, and catabolism syndrome (PICS): a review of definitions, potential therapies, and research priorities[J]. Br J Anaesth, 2024, 132(3): 507-518. DOI:10.1016/j.bja.2023.11.052 |
| [8] | Gentile LF, Cuenca AG, Efron PA, et al. Persistent inflammation and immunosuppression: a common syndrome and new horizon for surgical intensive care[J]. J Trauma Acute Care Surg, 2012, 72(6): 1491-1501. DOI:10.1097/ta.0b013e318256e000 |
| [9] | Pang XS, Zhang P, Chen XP, et al. Ubiquitin-proteasome pathway in skeletal muscle atrophy[J]. Front Physiol, 2023, 14: 1289537. DOI:10.3389/fphys.2023.1289537 |
| [10] | Owen AM, Patel SP, Smith JD, et al. Chronic muscle weakness and mitochondrial dysfunction in the absence of sustained atrophy in a preclinical sepsis model[J]. eLife, 2019, 8: e49920. DOI:10.7554/elife.49920 |
| [11] | Pugh AM, Auteri NJ, Goetzman HS, et al. A murine model of persistent inflammation, immune suppression, and catabolism syndrome[J]. Int J Mol Sci, 2017, 18(8): 1741. DOI:10.3390/ijms18081741 |
| [12] | Chen XC, Li XJ, Lu HM, et al. Mouse model of critical persistent inflammation, immunosuppression, and catabolism syndrome[J]. Shock, 2022, 57(2): 238-245. DOI:10.1097/shk.0000000000001878 |
| [13] | Cong HL, Sun LQ, Liu CM, et al. Inhibition of atrogin-1/MAFbx expression by adenovirus-delivered small hairpin RNAs attenuates muscle atrophy in fasting mice[J]. Hum Gene Ther, 2011, 22(3): 313-324. DOI:10.1089/hum.2010.057 |
| [14] | Adams V, Schauer A, Augstein A, et al. Targeting MuRF1 by small molecules in a HFpEF rat model improves myocardial diastolic function and skeletal muscle contractility[J]. J Cachexia Sarcopenia Muscle, 2022, 13(3): 1565-1581. DOI:10.1002/jcsm.12968 |
| [15] | Nakanishi N, Ono Y, Miyazaki Y, et al. Sepsis causes neutrophil infiltration in muscle leading to muscle atrophy and weakness in mice[J]. Front Immunol, 2022, 13: 950646. DOI:10.3389/fimmu.2022.950646 |
| [16] | Bolton CF. Neuromuscular manifestations of critical illness[J]. Muscle And Nerve, 2005, 32(2): 140-163. DOI:10.1002/mus.20304 |
| [17] | Kim MJ, Choi EJ, Choi EJ. Evolving paradigms in sepsis management: a narrative review[J]. Cells, 2024, 13(14): 1172. DOI:10.3390/cells13141172 |
| [18] | Wang N, Lu YL, Zheng J, et al. Of mice and men: Laboratory murine models for recapitulating the immunosuppression of human sepsis[J]. Front Immunol, 2022, 13: 956448. DOI:10.3389/fimmu.2022.956448 |
| [19] | Dejager L, Pinheiro I, Dejonckheere E, et al. Cecal ligation and puncture: the gold standard model for polymicrobial sepsis?[J]. Trends Microbiol, 2011, 19(4): 198-208. DOI:10.1016/j.tim.2011.01.001 |
| [20] | Hartwig C, Drechsler S, Vainshtein Y, et al. From gut to blood: spatial and temporal pathobiome dynamics during acute abdominal murine sepsis[J]. Microorganisms, 2023, 11(3): 627. DOI:10.3390/microorganisms11030627 |
| [21] | Lei MX, Feng TJ, Zhang MM, et al. Chronic critical illness-induced muscle atrophy: insights from a trauma mouse model and potential mechanism mediated via serum amyloid a[J]. Shock, 2024, 61(3): 465-476. DOI:10.1097/shk.0000000000002322 |
 2026, Vol. 35
2026, Vol. 35