2. 湖南省人民医院(湖南师范大学附属第一医院)急诊医学科 湖南省急危重症临床研究中心, 长沙 410005
2. Department of Emergency Medicine, Hunan Provincial People's Hospital(The First Affiliated Hospital of Hunan Normal University), Hunan Provincial Critical Care Clinical Research Center, Changsha, 410005 China
脓毒症是由宿主对感染反应失调引发的危及生命的器官功能障碍综合征[1],其病死率高达30%[2]。目前认为,免疫功能障碍导致的全身性炎症失控和多器官衰竭是造成脓毒症高病死率的关键因素[3]。当病原体入侵时,其携带的病原体相关分子模式(PAMPs)或宿主损伤细胞释放的损伤相关分子模式(DAMPs)可通过模式识别受体(PRRs)激活天然免疫系统,触发以细胞因子风暴和趋化因子级联释放为特征的过度炎症反应[4]。随后,机体代偿性抗炎反应综合征(CARS)的激活会导致免疫稳态失衡,最终发展为多器官功能障碍综合征(MODS)[5]。由此可见,免疫紊乱在脓毒症的病理进程中具有决定性作用。研究发现,脓毒症后期的持续性免疫抑制是导致脓毒症患者死亡的重要诱因[6],其不但增加继发感染风险,还降低免疫调节治疗与抗菌药物疗效。临床证据显示,脓毒症患者的外周血淋巴细胞持续减少与28 d病死率、住院时长及继发感染率呈显著正相关。值得注意的是,肺部作为脓毒症最易受累的靶器官之一,其发生免疫抑制会显著削弱病原体清除能力,进而加剧疾病进展和死亡风险[7]。然而,目前关于脓毒症进程中过度炎症反应向免疫抑制转变的关键时间节点尚未明确。
单细胞测序技术已成为生物医学研究的重要手段之一[8]。该技术以其高通量、高灵敏度、高准确性、高分辨率等特点,被广泛应用于细胞分化、基因表达、突变检测、蛋白质相互作用等方面的研究[9]。本研究将采用单细胞测序技术分析脓毒症小鼠肺组织免疫微环境动态变化,以期为脓毒症的临床治疗提供参考。
1 材料与方法 1.1 盲肠结扎穿孔制备脓毒症模型6~8周龄雄性C57BL/6小鼠异氟烷吸入麻醉,沿腹部正中线作长约1~2 cm切口,游离肠系膜和盲肠,4-0号丝线在盲肠盲端1 cm处结扎,21 G针头于盲肠末端对合穿孔,挤出少许肠内容物,将盲肠放回腹腔内,逐层关腹。术后皮下注射1mL生理盐水补充体液,CLP手术后第1、3、7、14天收集小鼠肺组织。
1.2 scRNA-seq文库构建新鲜肺组织样品采集后30 min内,使用SCelLive®组织保存液(Singleron公司)冰上保存。组织经Hanks平衡盐溶液(HBSS)洗涤3次后切成小块,加入3 mL SCelLive®组织解离液,通过Singleron PythoT®组织解离系统于37℃消化15min。所得细胞悬浮液经40 µm滤膜过滤,加入GEXSCOPE®红细胞裂解缓冲液(RCLB)室温孵育5 min去除红细胞,随后4℃、300×g离心5 min,弃上清液后用PBS轻柔重悬。将单细胞悬液(2×105 cells/mL)加载至Singleron Matrix®单细胞处理系统的微孔芯片,收集结合mRNA的条形码磁珠进行逆转录获得cDNA,经PCR扩增后片段化并连接测序适配器。使用GEXSCOPE®单细胞RNA文库试剂盒构建scRNA-seq文库,单个文库稀释至4 nmol/L合并后,在Illumina NovaSeq 6000平台进行双端150 bp测序。用Cell Ranger软件(v7.0.0,10x Genomics,Pleasanton,CA 94588 USA)分析测序数据,并获得每个细胞的基因表达信息,以及将Cell Ranger输出加载到Seurat(v4.1.1)软件上,用于scRNA-seq数据的降维、聚类和分析。
1.3 scRNA-seq数据分析 1.3.1 定量分析使用R v4.1.2对原始基因表达矩阵进行预处理分析。首先整合不同时间点的单细胞数据(Seurat v4.3),基于唯一分子标识符(UMI) > 1 000,检测基因数 > 500,log10 > 0.8,线粒体基因占比 < 20%筛选细胞。合格细胞经SCTransform函数归一化后,通过典型相关分析(CCA)与相互最近邻算法(MNN)校正批次效应,构建标准化表达矩阵,并使用前10个PC进行聚类和t分布随机邻居嵌入(tSNE)分析。
1.3.2 聚类及可视化通过Seurat中的“Find All Markers”功能对细胞亚群差异表达基因(differential expression genes, DEG)进行鉴定,并采用CD4、CD8,Ly6G、CD19、CD20等经典分子注释各细胞亚群(排除表达两种以上分子的细胞),并对主要细胞类型进行聚类分析,进一步检测每种细胞亚群的异质性。
1.5 功能富集分析采用“clusterProfiler”包中的“compareCluster”功能对细胞亚群差异基因(differential expression gene)进行GO富集分析。
1.6 聚类与可视化分析通过Seurat中的“Find All Markers”功能对细胞亚群差异表达基因(differential expression genes, DEG)进行鉴定,并采用CD4、CD8,Ly6G、CD19、CD20等经典分子注释各细胞亚群(排除表达两种以上分子的细胞),并对主要细胞类型进行聚类分析,进一步检测每种细胞亚群的异质性。
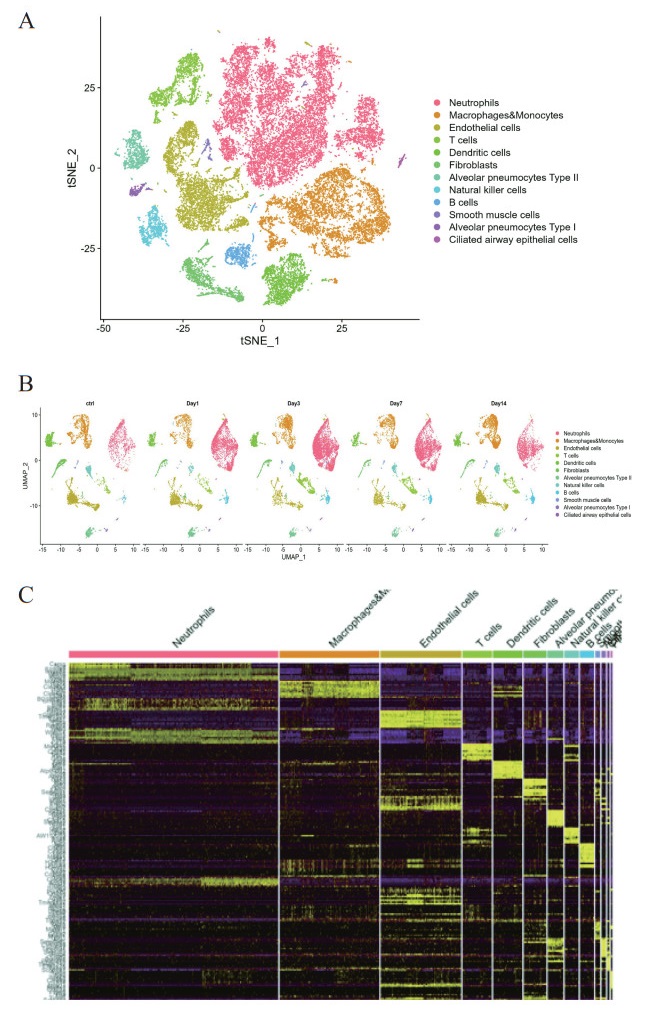
2 结果 2.1 CLP后小鼠肺组织细胞组成分析为了探讨脓毒症病理进程中免疫细胞的多样性及其动态变化,采用CLP构建脓毒症小鼠模型,收集分别代表早期、进展期、晚期脓毒症小鼠的肺组织(day 0、day 1、day 3、day 7、day 14), 采用10X基因组学进行单细胞测序分析。经过质控后(UMI > 1000, gene > 500,基因比率lg10 > 0.8,线粒体基因百分比 < 20%),共收集到2×105个细胞,并鉴定出中性粒细胞、单核-巨噬细胞、内皮细胞、T细胞、树突状细胞等12群细胞(图 1A),中性粒细胞为主要免疫细胞,CLP 1d后,中性粒细胞急剧扩增,14 d逐渐下降(图 1B)。
|
| 注:A为小鼠肺组织细胞组成;B为CLP后不同时间小鼠细胞组成动态变化;C为单细胞测序鉴定出的12个细胞簇的基因表达谱 图 1 脓毒症小鼠肺组织细胞组成分析与动态变化(n=3) Fig 1 Analysis of Cellular Composition and Dynamic Changes in Lung Tissues of Septic Mice(n=3) |
|
|
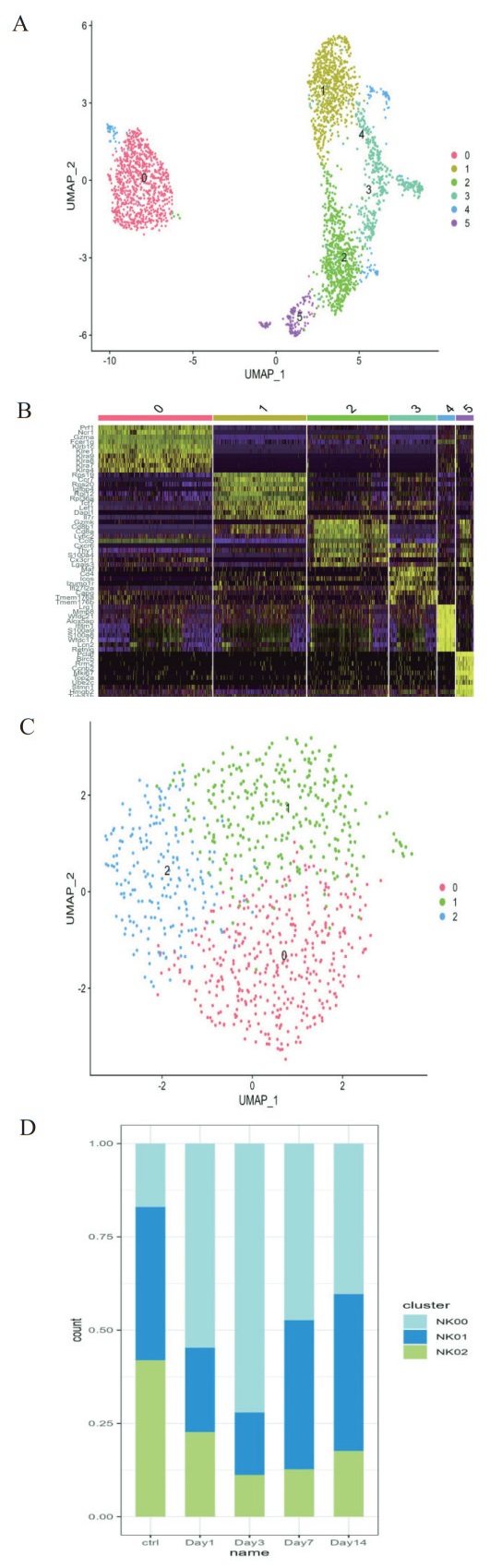
T细胞与NK细胞为机体重要免疫细胞,在清除病原菌、炎症因子释放等方面发挥关键作用。根据聚类分析,可将T细胞与NK细胞分为N0、N1、N2、N2、N3、N4、N5等细胞亚群(图 2A)。N0细胞高表达Gzmb、Gzma、Nkg7、Klrb1c等NK细胞相关分子,表明该群细胞可能为NK细胞(图 2B)。N1细胞高表达CCR7,提示其可能为初始T淋巴细胞,N2高表达CD8a分子,N3高表达CD4分子,可能分别是CD8+、CD4+T淋巴细胞,N4高表达S100A8,S100A9,MMP8等炎症介质,提示其可能为辅助T淋巴细胞(图 2B)。进一步将NK细胞进行聚类分析,共获得NK0、NK1、NK2三大细胞亚群(图 2C)。CLP后NK0细胞百分比逐渐增加,第3天达到高峰;NK1与NK2细胞则逐渐减少,第3天开始逐渐增加(图 2D)。
|
| 注:A为T细胞与NK细胞UMAP图;B为不同亚群T细胞与NK细胞高表达分子;C为NK细胞UMAP图;D为不同亚群NK细胞百分比 图 2 脓毒症不同阶段小鼠肺组织T细胞与NK细胞动态变化(n=3) Fig 2 Dynamic Changes of T Cells and NK Cells in Lung Tissues of Septic Mice Across Disease Stages(n=3) |
|
|
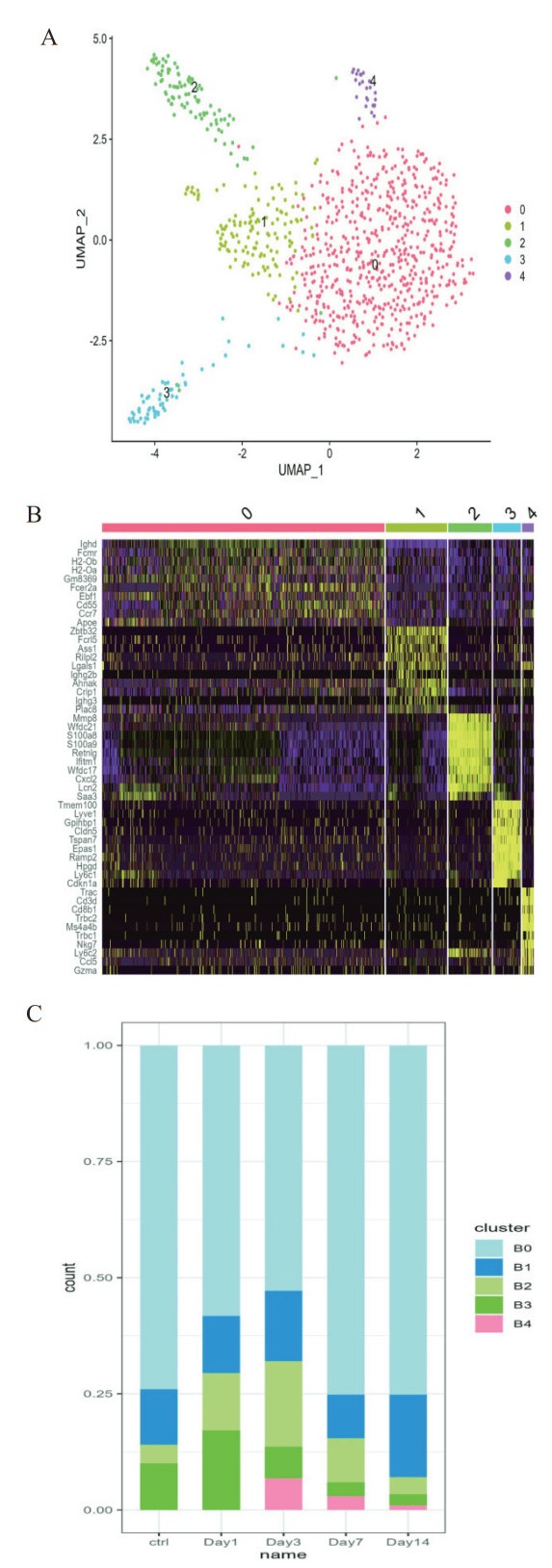
B细胞在获得性免疫中发挥重要作用。抗原刺激时,B细胞分化成浆细胞并分泌抗体,执行机体的体液免疫。单细胞测序聚类分析将B细胞分成B0、B1、B2、B3、B4等细胞亚群(图 3A)。B0高表达Ighd,B1高表达Zbtb32,B2高表达Cxcl2,B3高表达Slco2a1,B4高表达Lck等(图 3B)。进一步分析发现CLP 3 d时B4细胞显著增加,第7天时逐渐减少(图 3C)。B0与B3细胞手术后逐渐减少,第7天时逐渐增加(图 3C)。
|
| A为B细胞UMAP图;B为不同亚群B细胞高表达分子;C为不同亚群B细胞百分比。 图 3 脓毒症不同阶段小鼠肺组织B细胞亚群动态变化(n=3) Fig 3 Dynamic Changes of B Cell Subsets in Lung Tissues of Septic Mice Across Disease Stages(n=3) |
|
|
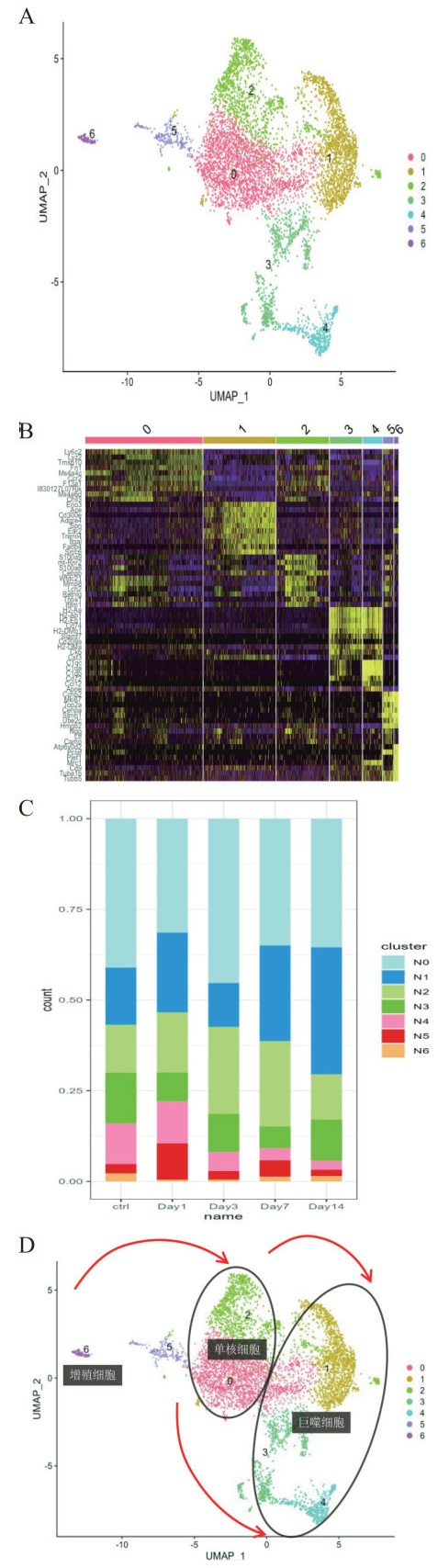
巨噬细胞是机体重要的固有免疫细胞,发挥清除病原微生物与受损组织的功能。根据不同亚群表达谱不同,将巨噬细胞分为M0、M1、M2、M3、M4、M5、M6等细胞亚群。M0、M2高表达、Ly6c2、CCR2,提示该群细胞为单核细胞(图 4A);M1、M3、M4高表达补体、Adgre1,S100A8、SAA3等(图 4A),提示上述细胞亚群为活化巨噬细胞,M5、M6高表达Ki67(图 4B),表明其可能为祖细胞。进一步分析结果显示M5、M6 CLP 1 d达高峰(图 4C),第3天开始逐渐减少,M0、M2第1天开始逐渐增加,第3天达到高峰(图 4C),M1、M3、M4 CLP 1d开始增加,第7天达到高峰(图 4C)。拟时序分析结果显示脓毒症小鼠肺组织巨噬细胞由M5、M6先向M0、M2分化后向M1、M3、M4分化(图 4D)。
|
| 注:A为巨噬细胞UMAP图;B为不同亚群巨噬细胞高表达分子;C为不同亚群巨噬细胞百分比;D为不同亚群巨噬细胞分化图 图 4 脓毒症不同阶段小鼠肺组织巨噬细胞亚群动态变化(n=3) Fig 4 Dynamic Changes of Macrophage Subsets in Lung Tissues of Septic Mice Across Disease Stages(n=3) |
|
|
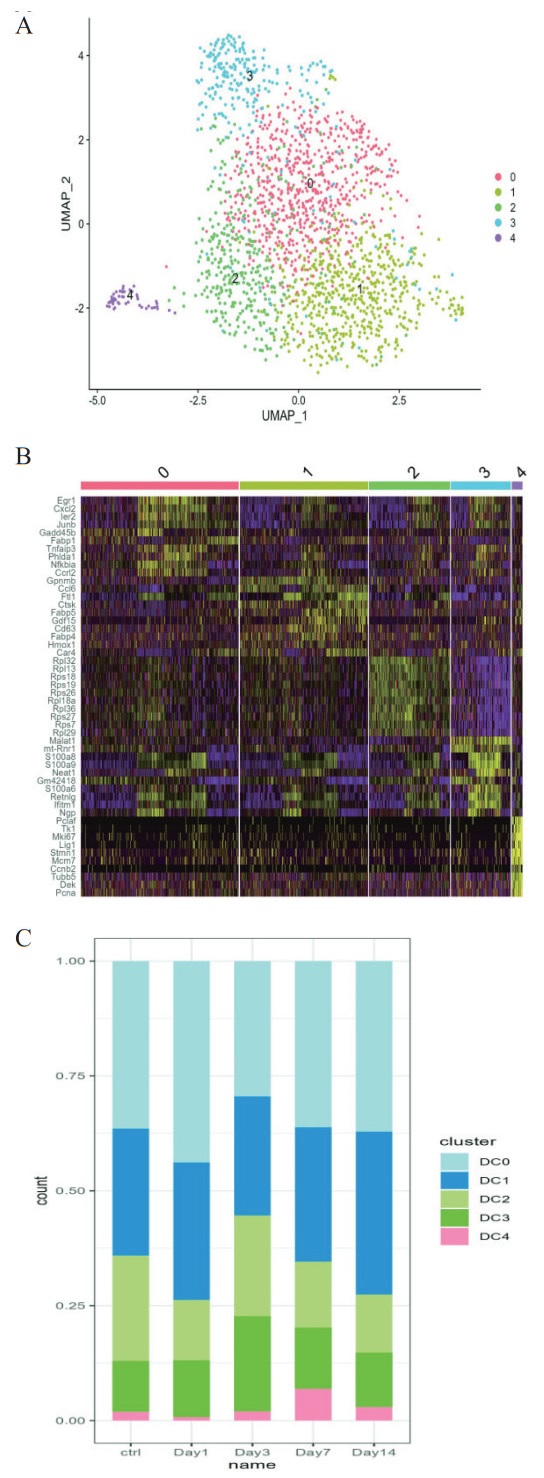
树突状细胞(dendritic cell,DC)是固有免疫与获得性免疫的桥梁细胞。根据不同亚群表达谱不同,将树突状细胞分为DC0、DC1、DC2、DC3、DC4等5群细胞(图 5A)。DC0高表达Cxcl12、Fabp1等,DC1高表达CC了6、CD63等,DC2高表达Rpl13、Rps26等,DC3高表达S100A8、S100A9等,DC4高表达Mki67等,表明DC4可能为祖细胞(图 5B)。进一步分析结果显示DC0细胞在脓毒症后第1天增加,第3天后恢复正常(图 5C),DC3在第3天逐渐增加,第7天逐渐恢复正常(图 5C)。
|
| 注:A为树突状细胞UMAP图;B为不同亚群树突状细胞高表达分子;C为不同亚群树突状细胞百分比 图 5 脓毒症不同阶段小鼠肺组织树突状细胞亚群动态变化(n=3) Fig 5 Dynamic Changes of Dendritic Cell Subsets in Lung Tissues of Septic Mice Across Disease Stages(n=3) |
|
|
脓毒症病理生理机制复杂,过度炎症和免疫抑制交织存在[10-11]。急性肺损伤是脓毒症常见并发症,脓毒症肺损伤时免疫细胞呈高度异质性[12]。Van der Poll等在《Immunity》上发表的综述详细论述了脓毒症的免疫学研究进展[13];Rubio团队则围绕脓毒症中关键免疫细胞的作用、淋巴细胞减少的原因、器官特异性免疫学、相关免疫改变的动力学、微生物组的作用以及免疫测试的标准化等方面进行了全面的分析与讨论[14];此外,《Nature Immunology》上发表的一篇基于组学技术和系统医学的精准疗法文章,也对脓毒症免疫变化与治疗的相关知识进行了全面回顾[15]。然而,上述研究并未阐明脓毒症发病后时序性免疫细胞亚群演化规律。本研究发现,CLP 1 d时中性粒细胞急剧扩增(后逐渐衰减),提示其为早期细胞因子风暴的关键效应细胞;CLP 3 d后T/B淋巴细胞比例持续升高,标志获得性免疫应答激活;至CLP 14 d则出现T细胞急剧耗竭,揭示晚期免疫抑制状态的形成机制。
本研究采用单细胞测序探讨脓毒症不同阶段肺组织中免疫微环境动态变化,共鉴定出中性粒细胞、巨噬细胞、T细胞、B细胞、NK细胞、DC细胞等6类免疫细胞,其中中性粒细胞在CLP 1d后急剧扩增,后逐渐下降,提示中性粒细胞可能是脓毒症感染早期触发细胞因子风暴的主要细胞。CLP 3 d后,T、B淋巴细胞百分比逐渐增加,提示获得性免疫反应被激活。脓毒症进展到晚期时,免疫系统被抑制,此时免疫细胞呈耗竭状态,表现为数量减少或功能耗竭。本研究发现,CLP 14 d后T细胞急剧减少,提示脓毒症晚期T细胞耗竭。
固有免疫应答是人体抵抗病原体的重要防线。其中,中性粒细胞、巨噬细胞是固有免疫系统的重要组成部分,其数量或功能变化与固有免疫反应密切相关。研究显示,不同疾病巨噬细胞呈高度异质性。在脑胶质瘤组织中,共鉴定出8群功能各异的巨噬细胞[16]。在牙周炎患者牙周组织中,共鉴定出5群巨噬细胞(C1: MHCIIhighCD44+; C2: MHCIIlowCXCL8+; C3: MHCIIlowCD44+; C4: MHCIIlowCD44-; C5: MHCIIhighCD44-)[17]。本研究采用单细胞测序揭示了早、中、晚期脓毒症小鼠肺组织巨噬细胞动态变化,共鉴定出M0、M1、M2、M3、M4、M5、M6等7个细胞亚群,且高表达Ki67的M5、M6细胞在CLP后第1天达高峰,表明其在脓毒症早期急剧扩增。接着,高表达炎症分子的M1、M3、M4占主导,表明该类细胞为脓毒症早期肺组织的主要炎症细胞。
淋巴细胞属于白细胞的一种,由淋巴器官产生,是机体免疫应答功能的重要细胞成分。按其发生迁移、表面分子和功能的不同,可分为T细胞、B细胞和自然杀伤(NK)细胞。外周淋巴器官的T细胞与抗原接触后,在不同细胞因子的作用下分化成具有不同效应功能的T细胞亚群。按T细胞所处的活化阶段,将T细胞分为初始T细胞、效应T细胞和记忆T细胞等。按CD4、CD8的分子表型,将T细胞分为辅助T细胞(CD4+T细胞)、杀伤T细胞(CD8+T细胞)等。CD4+T细胞具有辅助其他免疫细胞分化和调节(促进或抑制)免疫应答的作用[12]。CD8+T细胞则能释放穿孔素、颗粒酶特异性直接杀伤靶细胞。NK细胞也称为自然杀伤细胞,为具有直接杀伤靶细胞效应的特殊淋巴细胞系,具有抗肿瘤、抗感染、免疫调节的功能,且表现为速发效应,被称作是人体抵抗癌细胞和病毒感染细胞的第一道防线。根据NK细胞释放细胞因子不同,将NK细胞分为NK1、NK2与NK322。本研究共鉴定出初始T细胞、CD8+、CD4+T淋巴细胞、辅助T细胞等细胞亚群。其中CD8+T细胞、CD4+T细胞CLP 1d后逐渐增加,提示获得性免疫系统逐渐激活,且CLP 3 d后炎症反应达高峰。B淋巴细胞产生抗体,其与抗原结合形成抗原抗体复合物,继而被吞噬细胞清除。外周淋巴器官中B细胞具有异质性,可依据CD5是否表达分为B1和B2两亚群。本研究聚类分析将B细胞分成B0、B1、B2、B3、B4等细胞亚群。B0高表达Ighd,B1高表达Zbtb[32],B2高表达Cxcl2,B3高表达Slco2a1,B4高表达Lck等。进一步分析发现CLP 3 d时B4细胞显著增加,第7天时逐渐减少。B0与B3细胞CLP后逐渐减少,第7天时逐渐增加。
总之,本研究揭示了脓毒症肺组织免疫微环境的动态变化,明确了不同阶段关键免疫细胞亚群的演化规律,深化了对脓毒症免疫机制的理解,为脓毒症的精准免疫治疗提供了新的理论依据,为改善临床预后提供了潜在的新方向。
利益冲突 所有作者声明无利益冲突
作者贡献声明 顾潇宵、刘艳娟:实验操作、论文撰写;谢远嘱:数据收集及整理、统计学分析;陈芳、蒋宇:研究设计、论文修改
| [1] | Gong C, Xu SY, Pan YL, et al. Effects of probiotic treatment on the prognosis of patients with sepsis: a systematic review[J]. World J Emerg Med, 2025, 16(1): 18. DOI:10.5847/wjem.j.1920-8642.2025.018 |
| [2] | Costa RT, Nassar AP Jr, Caruso P. The comparisons and limitations of sepsis 2.0 and sepsis 3.0[J]. J Crit Care, 2018, 47: 351. DOI:10.1016/j.jcrc.2018.07.016 |
| [3] | Yao RQ, Ren C, Zheng LY, et al. Advances in immune monitoring approaches for sepsis-induced immunosuppression[J]. Front Immunol, 2022, 13: 891024. DOI:10.3389/fimmu.2022.891024 |
| [4] | Yan JH, Zhang JW, Wang YN, et al. Rapidly inhibiting the inflammatory cytokine storms and restoring cellular homeostasis to alleviate sepsis by blocking pyroptosis and mitochondrial apoptosis pathways[J]. Adv Sci, 2023, 10(14): 2207448. DOI:10.1002/advs.202207448 |
| [5] | Chen ZY, Zhang J, Gao SJ, et al. Suppression of Skp2 contributes to sepsis-induced acute lung injury by enhancing ferroptosis through the ubiquitination of SLC3A2[J]. Cell Mol Life Sci, 2024, 81(1): 325. DOI:10.1007/s00018-024-05348-3 |
| [6] | Nedeva C, Menassa J, Duan MB, et al. TREML4 receptor regulates inflammation and innate immune cell death during polymicrobial sepsis[J]. Nat Immunol, 2020, 21(12): 1585-1596. DOI:10.1038/s41590-020-0789-z |
| [7] | Zhao Q, Ma JF, Xiao JG, et al. Data driven analysis reveals prognostic genes and immunological targets in human sepsis-associated acute kidney injury[J]. World J Emerg Med, 2024, 15(2): 91. DOI:10.5847/wjem.j.1920-8642.2024.026 |
| [8] | Xu G, Liu Y, Li HJ, et al. Dissecting the human immune system with single cell RNA sequencing technology[J]. J Leukoc Biol, 2020, 107(4): 613-623. DOI:10.1002/jlb.5mr1019-179r |
| [9] | Saviano A, Henderson NC, Baumert TF. Single-cell genomics and spatial transcriptomics: Discovery of novel cell states and cellular interactions in liver physiology and disease biology[J]. J Hepatol, 2020, 73(5): 1219-1230. DOI:10.1016/j.jhep.2020.06.004 |
| [10] | Nascimento DC, Viacava PR, Ferreira RG, et al. Sepsis expands a CD39+ plasmablast population that promotes immunosuppression via adenosine-mediated inhibition of macrophage antimicrobial activity[J]. Immunity, 2021, 54(9): 2024-2041. e8. DOI:10.1016/j.immuni.2021.08.005 |
| [11] | Karki R, Sharma BR, Tuladhar S, et al. Synergism of TNF-α and IFN-γ triggers inflammatory cell death, tissue damage, and mortality in SARS-CoV-2 infection and cytokine shock syndromes[J]. Cell, 2021, 184(1): 149-168. e17. DOI:10.1016/j.cell.2020.11.025 |
| [12] | Zhang SW, Zhang N, Han J, et al. Dynamic immune status analysis of peripheral blood mononuclear cells in patients with Klebsiella pneumoniae bloodstream infection sepsis using single-cell RNA sequencing[J]. Front Immunol, 2024, 15: 1380211. DOI:10.3389/fimmu.2024.1380211 |
| [13] | van der Poll T, Shankar-Hari M, Wiersinga WJ. The immunology of sepsis[J]. Immunity, 2021, 54(11): 2450-2464. DOI:10.1016/j.immuni.2021.10.012 |
| [14] | Rubio I, Osuchowski MF, Shankar-Hari M, et al. Current gaps in sepsis immunology: new opportunities for translational research. Lancet Infect Dis 2019 doi: 10.1016/s1473-3099(19)30567-5 [published Online First: 2019/10/22] |
| [15] | Giamarellos-Bourboulis EJ, Aschenbrenner AC, Bauer M, et al. The pathophysiology of sepsis and precision-medicine-based immunotherapy[J]. Nat Immunol, 2024, 25(1): 19-28. DOI:10.1038/s41590-023-01660-5 |
| [16] | Ochocka N, Segit P, Walentynowicz KA, et al. Single-cell RNA sequencing reveals functional heterogeneity of glioma-associated brain macrophages[J]. Nat Commun, 2021, 12: 1151. DOI:10.1038/s41467-021-21407-w |
| [17] | Agrafioti P, Morin-Baxter J, Tanagala KKK, et al. Decoding the role of macrophages in periodontitis and type 2 diabetes using single-cell RNA-sequencing[J]. FASEB J, 2022, 36(2): e22136. DOI:10.1096/fj.202101198r |
 2026, Vol. 35
2026, Vol. 35