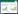急诊科是急危重症救治的前沿阵地,面对患者数量庞大、病种复杂、病情瞬息万变的严峻挑战,诊疗决策的迅速与精准至关重要。许多危急重症的救治高度依赖“黄金时间窗”[1],而急诊医生的专业背景与经验各异,在快速准确选择检验项时常常面临困难。因此,快速、精准且可靠的实验室检测已成为急诊诊疗决策不可或缺的支撑,其结果直接影响患者分诊、病因判断、危险分层、治疗方案选择及预后评估。为满足急诊对检验速度与质量的双重要求,亟需构建以临床需求为导向的急诊检验策略体系。本共识旨在保障医生在关键抢救时间窗内获取精准可靠的检验结果,为常见急诊场景的临床决策提供支持。实验室通过提升检测能力,包括引入高敏肌钙蛋白(high-sensitivity cardiac troponin, hs-cTn)、开展血气与凝血分析、优化微生物培养与分子检测流程等,为急性胸痛、感染性疾病及复杂病情的评估提供核心支持。同时,通过设立急诊专属检测单元、优化样本传输与处理流程等举措,显著缩短危急重症的标本周转时间(turnaround time, TAT),确保在关键窗口期迅速提供可靠结果。信息系统对检验数据的实时整合,进一步强化了“快速初筛、精准确认”的闭环管理能力。
综上,本共识(指南共识注册编号:PREPARE-2025CN1447)致力于为急诊医生提供基于循证医学的检验策略指导,覆盖核心急症场景与关键技术环节,推动检验与临床高效协同,最终实现优化急诊流程、提升救治效率与改善患者预后的目标。
本共识的制定步骤及方法如下:(1)成立共识筹备组;(2)通过检索PubMed、中国知网、万方、中国生物医学文献数据库等数据库进行文献筛选,检索时间为各数据库建立至2025年6月26日;(3)应用分级系统确定推荐级别,根据对共识推荐意见的证据级别、获益、风险、保险负担和费用的综合判断,分为强推荐,有条件推荐与弱推荐;(4)经急诊科,检验科,护理学等专家讨论并使用GRADE方法形成明确的证据分级,最终确定推荐意见。见表 1。
| 证据等级 | 定义 | 典型研究类型 |
| 证据水平等级 | ||
| 高 | 未来研究几乎不可能改变现有结论的可信度 | 设计良好的RCT、Meta分析 |
| 中 | 未来研究可能对现有结论产生重要影响,但当前证据仍具较高可信度 | 存在偏倚的RCT、大样本队列研究 |
| 低 | 未来研究极可能改变现有结论,当前证据可信度有限 | 小样本观察性研究、病例对照研究 |
| 极低 | 现有证据非常不确定,结论多为推测性 | 个案报告、专家观点 |
| 推荐强度分级 | ||
| 强推荐 | 该方案大多数患者、医生和政策制定者都会采纳 | |
| 有条件推荐 | 该方案多数人会采纳,但仍有部分人不采纳,要结合患者具体情况做出体现其价值观和意愿的决定 | |
| 弱推荐 | 证据不足,需要患者、医生和政策制定者共同讨论决定 |
氧合状态与组织灌注是评估危重患者生命支持需求的核心指标。在急诊环境中,低氧血症(SpO2 < 90%或PaO2 < 60 mmHg,1 mmHg=0.133 kPa)是呼吸衰竭、休克、多器官功能障碍的早期预警信号,未及时纠正者24 h内病死率可达30%[2]。氧合不足不仅影响脑、心脏等关键器官功能,还会加重代谢性酸中毒,形成恶性循环。急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)患者若未在1 h内改善氧合,住院病死率将上升至50%。值得注意的是,心脏骤停患者中63%存在严重代谢性酸中毒(pH < 7.2且碱剩余 < -5 mmol/L),此类患者接受床旁血气分析指导的针对性治疗(如碳酸氢钠)后存活出院率显著提升[3]。乳酸作为无氧代谢的终产物,是反映组织缺氧和灌注不足的敏感标志物。正常动脉血乳酸水平为0.5~1.5 mmol/L,≥4 mmol/L提示严重组织缺氧(如脓毒性休克、失血性休克),此类患者28 d病死率高达40%[4]。在心脏骤停患者中,92%存在高乳酸血症(> 2.5 mmol/L),且乳酸水平与存活率显著负相关[3, 5]。因此,氧合与乳酸监测是急诊危重患者识别、分层管理与预后评估的基石。
动脉血气分析是评估氧合(PaO2)、通气(PaCO2)及酸碱平衡的金标准。动脉血乳酸直接反映全身组织灌注状态,准确性高于静脉血。研究显示,动脉乳酸水平与静脉血存差异有统计学意义(平均高0.8 mmol/L),尤其在低灌注状态下静脉血可能低估病情[5]。无法获取动脉血时,可采集中心静脉血替代,但其结果需校正:中心静脉乳酸检测值需增加0.5~1.0/mmol/L,以匹配动脉血乳酸水平。外周静脉血因受局部代谢影响误差更大,仅适用于初筛[3, 5]。在心脏骤停等极端场景中,可识别17%的致命性电解质紊乱(血钾 < 2.5 mmol/L或 > 6.0 mmol/L)并指导针对性治疗,可能改善神经功能预后[3]。
对昏迷患者进行神经功能预后评估是临床决策(尤其关于是否继续维持生命支持治疗)的关键。多模态方法(包括临床检查、电生理、影像学和生物标志物)在自主循环恢复(return of spontaneous circulation, ROSC)至少72 h进行。传统的血清生物标志物,如神经元特异性烯醇化酶(neuron-specific enolase, NSE),已被推荐用于评估神经损伤和不良预后,但其对于预后精准的判断阈值仍无法确定,S-100β水平增高推荐可用于判断不良预后,也可以用于心脏骤停后神经功能的评估[6]。其他标志物如神经丝轻链(neurofilament light chain, Nf-L)、胶质纤维酸性蛋白(glial fibrillary acidic protein, GFAP)、泛素羧基末端水解酶L1和血清Tau蛋白也显示出潜力,但尚未被常规推荐用于神经预测[7]。
鉴于现有标志物存在预测准确性不高、敏感度和特异度欠佳以及潜在误分类风险等问题,凸显了对新型、互补性生物标志物的迫切需求。高通量组学技术的发展(基因组学、转录组学、蛋白质组学、代谢组学等)为发现更精准的预后标志物提供了新的契机。
推荐意见1:所有急诊患者宜在首次医疗接触5 min内完成生命体征评估(心率、血压、呼吸频率、体温、SPO2),指测SPO2<90%需立即行血气分析。(推荐级别:强推荐,证据等级:高)
推荐意见2:对生命体征不稳定或疑似组织灌注不足(如意识改变、皮肤湿冷)的患者,宜在30 min内完成动脉血气分析(含乳酸、电解质检测),静脉血仅用于无法获取动脉血时(乳酸值需结合临床校正)。(推荐级别:强推荐,证据等级:高)
推荐意见3:对于心脏呼吸骤停患者,在积极进行心肺复苏及病因排查的同时,进行神经损伤相关生物标志物如NSE、S-100β检测,为后续神经功能预后评估提供早期参考信息。需注意,其解读需结合临床、电生理及影像学等多模态评估,且不作为终止复苏的独立依据。(推荐级别:有条件推荐,证据等级:低)
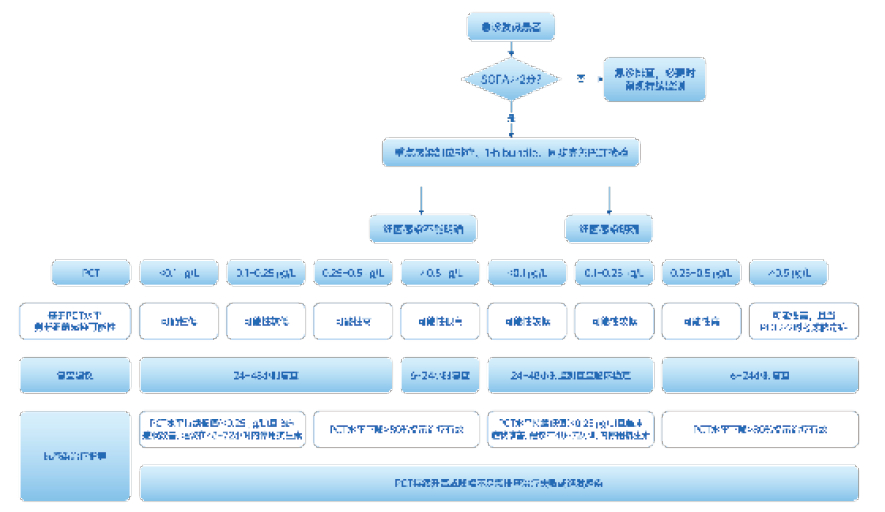
1.2 感染相关标志物动态监测策略感染相关生物标志物与分子检测技术的进步显著提升了急诊感染性疾病的诊疗效率。考虑到急诊患者的紧迫性和初步诊断需求,建议将涂片(革兰氏染色)作为常规快速初筛工具:该检查可在20 min内提供关键形态学线索(如区分革兰阳性/阴性菌、真菌形态),为初步判断病原体类型和优化初始抗感染策略(如经验性抗菌药物选择)提供即时依据[8-9]。在急诊感染性疾病诊疗体系中,降钙素原(procalcitonin, PCT)凭借其独特的动态变化规律:感染后2~4 h快速升高,12~24 h达峰,感染控制后迅速下降,成为临床快速决策的关键时间窗工具[10-12]。作为细菌感染的特异性指标(其病原学鉴别价值优于C反应蛋白(C-reactive protein, CRP)[13],PCT的定量水平可实现多重临床目标:在早期诊断与分层方面,血清PCT > 0.5 ng/mL高度提示细菌感染,> 2 ng/mL预示高风险的严重脓毒症或感染性休克,> 10 ng/mL高度提示严重细菌性脓毒症或脓毒症休克[12, 14-16];除细菌感染的诊断分层外,PCT也可用来指导抗生素的使用,基于PCT的降阶梯策略(如PCT < 0.25 ng/mL或较峰值下降≥80%时停用抗生素),可显著缩短抗菌药物使用时长约2.4 d且不增加病死率[17];在预后评估中,治疗72 h后PCT未下降≥80%的患者28 d死亡风险增加近2倍,是独立于临床评分的预警信号。需强调动态监测必要性,单次检测易受术后创伤等非感染因素干扰,而24~48 h系列监测可捕捉趋势[18-19]。PCT应定位为急诊感染诊疗链的核心检测指标[20-21]:在涂片初筛提供病原形态线索后,PCT可快速锁定细菌感染、排除病毒/非感染性炎症,并驱动抗菌药物精准管理(起始、调整及停用)(具体急诊流程见图 1)。PCT常用检测方法包括化学发光法和酶联免疫荧光法,二者检测特异度敏感度都较高,目前专家共识或指南所推荐的截断值都是基于溯源到BRAHMS的平台,故非溯源到BRAHMS平台的检测方法可能存在临床截断值差异[22]。PCT低浓度的截断值对抗生素停药指导更具临床意义,POCT与溯源性PCT在低浓度值的检测差异更大,因此要求POCT类产品直接使用临床已有截断值或参考区间时,需加强质量管理,避免带来不良的临床后果。
|
| 图 1 急诊重症感染患者PCT指导流程 |
|
|
CRP虽敏感度高但特异度较低,联合PCT可提高细菌感染鉴别准确性[23]。白介素(interleukin, IL)-6作为固有免疫应答的早期关键细胞因子,其升高早于CRP和PCT且持续时间长,可辅助急性感染的早期预警(细菌感染后2 h可达高峰)[24],虽然其鉴别感染与非感染(如手术、创伤、无菌性胰腺炎、自身免疫病)的特异度不如PCT和CRP[25],但IL-6水平(如 > 1 000 pg/L)仍可用于评价感染严重程度及提示预后不良[26]。乳酸水平 > 2 mmol/L提示组织低灌注,是脓毒症休克早期预警的核心指标[27],而血气分析(含乳酸、电解质)可同步评估酸碱失衡与氧合状态,指导液体复苏与呼吸支持。
感染性疾病的急诊处理需严格遵循“早定位、早靶向”原则:对于存在体腔积液(如胸腔积液、腹腔积液、关节腔积液)或局部脓肿的患者,急诊超声引导下的穿刺引流不仅能缓解症状,还可通过积液常规(细胞计数、蛋白)、生化(葡萄糖、乳酸脱氢酶)及革兰染色快速区分感染性与非感染性病因,并直接为涂片和后续检测提供样本。对于呼吸道及其他体液感染,在涂片初筛的基础上,多重病原体核酸检测可在1~2 h内实现病原体精准识别,显著缩短靶向抗感染治疗时间并减少抗生素滥用[28-30];微生物培养仍是病原学诊断的“金标准”,但其阳性率受限于采样时机等因素,宏基因组测序(mNGS)技术通过无偏倚检测样本中全部微生物核酸,将病原体总体检出敏感度提升至78.05%(较传统培养提高53.66%),在免疫抑制患者中敏感度达93.75%,并能精准识别罕见病原体(如水霉、马尔尼菲篮状菌等)[31]。此外,感染定位需结合影像学(如胸部CT排查肺炎、超声心动图筛查感染性心内膜炎)与实验室数据(如血培养、血清G试验/GM试验鉴别真菌感染),形成多维度证据链。这种以涂片快速初筛为基础、结合精准生物标志物检测、分子诊断及靶向感染灶定位(穿刺引流/影像学)的分层递进策略,既避免了盲目广谱抗菌治疗带来的耐药风险,又为危重患者争取了针对性治疗的黄金时间窗,最终实现“降阶梯”治疗与个体化管理的平衡。
推荐意见4:对考虑脓毒症患者,及时完成血培养的同时,宜同步进行WBC+PCT+IL-6+CRP检测,用于临床鉴别诊断、监测疗效和评估预后。生命体征异常(呼吸 > 22次/min、心率 > 120次/min、收缩压 < 100 mmHg)者,立即检测血气分析(含乳酸、电解质)。(推荐级别:强推荐,证据等级:高)
推荐意见5:疑似呼吸道感染患者,加测呼吸道病原体核酸。(推荐级别:强推荐,证据等级:中)
推荐意见6:对考虑感染患者,须在急诊着重感染定位的排查,所有呼吸道感染患者,疑似感染性体腔积液(如胸腔积液、腹腔积液、关节腔积液)及脓肿患者,在引流后,必须立即对痰液或积液染色涂片,行形态学检查,以快速区分感染性病因(如细菌、真菌)并指导初始抗菌治疗。(推荐级别:强推荐,证据等级:中)
推荐意见7:脓毒症/脓毒性休克患者的乳酸监测必须严格遵循"1小时集束化治疗(1-hour bundle)"时效框架:(1)基线乳酸需在识别后立即检测;(2)初始乳酸 > 2 mmol/L者,须在复苏后2~4 h(优先2 h)复测评估清除率;(3)延误检测或未按时复测将导致复苏不足,增加病死率。(推荐级别:强推荐,证据等级:高)
推荐意见8:感染性疾病患者疗效监测应避免冗余炎症指标检测。对诊断明确、治疗有效且病情稳定的患者,推荐仅动态监测PCT;其他炎症指标仅在病情加重、疗效不佳或存在复杂因素(如免疫抑制)时选择性使用。(推荐级别:强推荐,证据等级:中)
推荐意见9:对初始诊断为脓毒症且感染源已得到充分控制的成人患者,建议使用PCT联合临床评估决定何时停用抗生素。(推荐级别:强推荐,证据等级:中)
1.3 心血管病相关生物标志物检测与鉴别诊断策略急性胸痛是急诊科最常见的就诊症状之一,其病因复杂且病情进展迅速,涵盖急性冠脉综合征(acute coronary syndrome, ACS)、肺栓塞(pulmonary embolism, PE)、主动脉夹层(aortic dissection, AD)、心包填塞、张力性气胸等高危疾病。这些疾病的早期识别与鉴别直接关系到患者预后,但因其临床表现重叠性强、部分患者症状不典型,仅依赖病史采集、体格检查和常规心电图(electrocardiogram, ECG)往往难以快速明确诊断。据研究统计,全球每年约10%~15%的急诊胸痛患者最终被诊断为ACS[32],约30%的疑似ACS患者被明确诊断为非心脏性疾病,且其30 d内主要不良事件风险显著降低,但即使在这类患者中,30 d不良事件发生率仍达4%[33]。同样具有致命性的非心源性胸痛如PE和AD,其早期漏诊率可达20%以上[34]。因此,如何在有限时间内通过精准的检验策略完成危险分层、缩小鉴别范围并指导治疗决策,成为急诊胸痛管理的核心挑战。心血管生物标志物的检测技术发展为急诊胸痛精准管理提供了关键工具,能够为心肌损伤、心力衰竭和血栓形成等多种病例状态提供及时、可靠的检测结果。
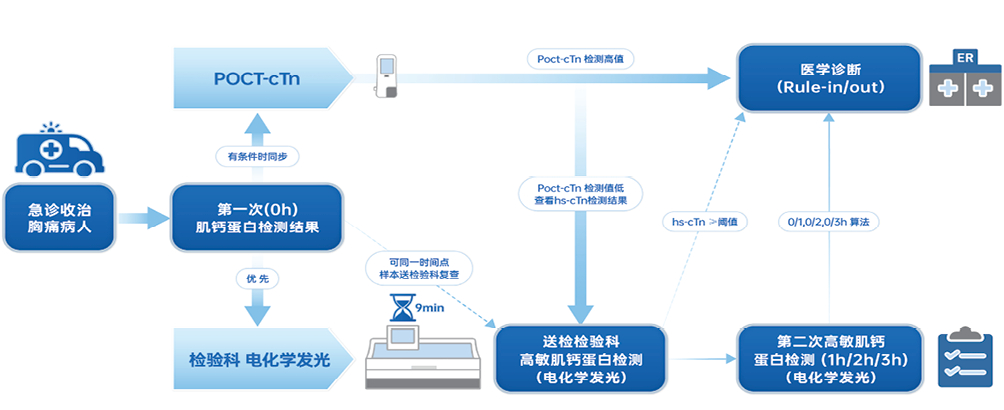
肌钙蛋白是由TnI、TnT和TnC三个亚基组成的异三聚体复合物,而cTnT和cTnI具有高度心肌特异性,当心肌损伤或坏死时释放到外周血,是心肌损伤特异性的标志物。特别是hs-cTn,因其高度的敏感度和特异度,已成为心肌损伤评估的首选标志物,特别是对非ST段抬高型ACS(Non-ST-Segment elevation acute coronary syndrome,NSTE-ACS)的早期诊断尤为重要[35]。hs-cTn可在心肌缺血后1~3 h内达到可检测阈值,结合0 h /1 h或0 h /2 h快速算法(依赖极低浓度阈值及Δ值变化≥20%)能显著缩短NSTE-ACS的诊断时间窗[36](具体流程见图 2)。《非ST段抬高型急性冠脉综合征诊断和治疗指南(2024)》推荐hs-cTnT的0 h/1 h方案用于排除或诊断非ST段抬高型心肌梗死(non-ST-elevation myocardial infarction, NSTEMI)[37]。初始cTn水平升高与ACS患者短期和长期死亡风险有关,hs-cTnT和hs-cTnI对急性心肌梗死诊断准确性相当,而hs-cTnT在全因死亡的预后评估中有更高的准确性[38]。cTn的免疫检测会受到嗜异性抗体、自身抗体和巨肌钙蛋白的影响,由于抗体结合特异性,cTnI更容易受巨肌钙蛋白复合物的影响,出现假阳性[39]。在一项免疫检查点抑制剂相关心肌炎患者进行的研究中发现,cTnT诊断敏感度显著优于cTnI[40],应根据临床情况和患者特征合理选择适当的检测方法。需要强调的是,hs-cTn特指满足严格性能标准的检测方法[41],且快速算法的界值需与检测系统严格匹配,POCT设备检测的传统肌钙蛋白与中心实验室hs-cTn存在显著性能差异:POCT传统肌钙蛋白虽具快速便捷优势(TAT < 20 min),但其分析敏感度(检出限通常 > 10 ng/L)和精密度(CV常 > 10%)无法满足hs-cTn标准,导致其难以支持依赖低浓度微小变化的快速算法,阴性结果不能可靠排除早期NSTEMI(尤其症状发作 < 3 h者)[42-43]。研究显示,POCT检测cTnI与电化学发光法检测hs-cTnT的一致性仅中等水平,尤其在低值样本中存在漏诊风险[43]。因此,中心实验室hs-cTn是实现快速算法和精准分层的金标准,POCT传统肌钙蛋白仅推荐用于资源有限场景的初筛或STEMI的辅助支持,若结果可疑需通过中心实验室确认[44-45]。hs-cTn检测常使用电化学发光法和间接化学发光法,电化学发光法具备反应体系可控、检测快速、高精密度、高敏感度及宽广检测范围等显著优势,而间接化学发光法其酶标记物对环境和存储条件要求苛刻,导致试剂稳定性差,会影响检测结果的重复性和稳定性。相比之下,肌酸激酶同工酶因心肌特异性不足,已退居为cTn不可及时检测时的辅助工具[46]。
|
| 图 2 急诊胸痛患者肌钙蛋白使用及0 h/1 h,0 h/2 h,0 h/3 h算法执行流程 |
|
|
心肌损伤标志物领域,心肌肌球蛋白结合蛋白C是心肌特异性的结构和调控蛋白,通过调节肌球蛋白头部与肌丝作用,影响肌肉收缩,在心肌缺血发生30 min可快速释放入血,早于肌钙蛋白的升高(峰值6~8 h),该检测可用于辅助排除疑似急性冠状动脉综合征患者的心肌梗死,并且辅助识别30 d内重大心血管不良事件风险较低的患者,在胸痛早期的诊断效能优于hs-cTn(尤其胸痛发作 < 3 h), 在AMI分诊效能也优于hs-cTn[47]。心型脂肪酸结合蛋白(heart-type fatty acid-binding protein,H-FABP)因其低相对分子质量(15 000)及心肌富集特性,在心肌缺血后1 h内即可释放,早于肌钙蛋白(峰值6~8 h)[48]。其早期诊断ACS的敏感度显著优于cTn,然而其心肌特异度有限(骨骼肌亦有表达),需联合cTn提升诊断精度[49]。
氧化应激与炎症标志物为胸痛病理机制提供新视角。生长分化因子-15(growth differentiation factor 15, GDF-15)是转化生长因子超家族成员,能反映心血管功能和疾病的独立炎症生化标志物,发生心肌梗死后90 min可达峰值,发病后持续高浓度达52 h, 可作为ACS早期诊断的检测指标[50],GDF-15 > 1 800 ng/L与冠心病患者长期主要心血管不良事件及全因死亡率的发生显著相关,为ACS全球注册研究(Global Registry of Acute Coronary Events, GRACE)危险评分增加预测信息[51-52]。GDF-15水平也是慢性心衰患者全因死亡及心衰再入院的独立预测因子[53]。髓过氧化物酶通过氧化低密度脂蛋白胆固醇(low-density lipoprotein cholesterol, LDL)、削弱一氧化氮生物利用度及促进斑块不稳定,直接参与冠状动脉事件链[54]。其在心血管风险评估中的预测价值已得到多项研究证实[55-57]。
利钠肽包括B型利钠肽(B-type natriuretic peptide, BNP)和N末端脑钠肽前体(N-terminal pro-brain natriuretic peptide, NT-proBNP)作为心脏功能的标志物,在心力衰竭预测、诊断/排除诊断、危险分层、治疗决策及预后评估有重要价值,国内外指南均推荐用于所有疑似心衰患者的诊断:其低截断值(BNP < 100 ng/L或NT-proBNP < 300 ng/L)可有效排除急性心衰[35]。在诊断急性心衰时,NT-proBNP诊断界值需按年龄和肾功能分层:50岁以下患者NT-proBNP > 450 ng/L,50~75岁 > 900 ng/L,75岁以上 > 1 800 ng/L,肾功能不全(肾小球滤过率 < 60 mL/min)时 > 1 200 ng/L[35]。NT-proBNP因半衰期更长、体外稳定性更佳且不受血管紧张素受体-脑啡肽酶抑制剂(angiotensin receptor-neprilysin inhibitor, ARNI)类药物干扰,在特定用药患者中推荐优先使用[58]。此外,可溶性致瘤抑制因子2(soluble suppression of tumorigenicity 2, sST2)通过竞争性抑制IL-33/ST2L心肌保护通路,直接参与心肌纤维化与心室重构进程[59],且临界值> 35 ng/mL可独立预测心血管死亡与心力衰竭再住院风险,其预测能力受年龄及肾功能影响较小。将sST2与NT-proBNP联合使用,可进一步提高对急性冠脉综合征患者住院期间心力衰竭及心律失常事件的预测效能[60]。
D-二聚体作为纤维蛋白降解产物,在排除静脉血栓栓塞和主动脉综合征(如夹层)中扮演核心角色,由于D-二聚体检测结果差别攸关严重临床结局事件,各品牌试剂制造商应依据《中华人民共和国医药行业标准》建立相应静脉血栓形成排除诊断截断值[61],临床医生必须结合验前概率及对应D-二聚体试剂的截断值进行静脉血栓形成阴性排除临床应用[62]。对于低至中危PE患者,阴性结果(使用年龄校正或肾功能校正的阈值)可安全排除PE,避免不必要的CTPA检查[63-65]。然而,D-二聚体禁用于高危患者(需直接影像学检查),且其升高非特异(常见于感染、肿瘤、创伤等),假阳性率高;超高水平(> 5 000 ng/mL)更常提示严重潜在疾病(如恶性肿瘤、脓毒症)而非PE,且与极高病死率相关[66-67]。D-二聚体可与其他指标联用(如肌钙蛋白比值排除NSTEMI,或结合ADD-RS评分排除AD)提高效率。D-二聚体不具备国际标准品,临床应用需要注意不同品牌、不同检测方法(ELISA、免疫比浊法等)及不同报告单位的检测结果不具可比性。
这些新型标志物通过多通路互补,构建了从心肌损伤、心衰代偿到全身性炎症反应的立体评估网络。但临床转化仍需解决三大挑战:检测标准化、动态阈值优化、以及成本效益平衡。未来研究应聚焦新型标志物与人工智能辅助的实时风险预警模型开发及应用。
推荐意见10:针对表现为急性胸闷、胸痛或呼吸困难的急诊首诊患者,除常规ECG外,宜进行hs-cTn、D-二聚体、NT-proBNP/BNP等检测,以便对患者进行鉴别与诊断、危险分层、预后评估和治疗决策。(推荐级别:强推荐,证据等级:高)
推荐意见11:对于经急诊心电图明确诊断为STEMI的患者,应立即启动再灌注治疗流程(溶栓或直接PCI),无需等待肌钙蛋白检测结果;肌钙蛋白检测仅用于基线记录及后续损伤评估,不得延误关键治疗时机。(推荐级别:强推荐,证据等级:高)
推荐意见12:对于所有疑似ACS,首次心电图无ST段抬高的胸痛患者,优先选择基于中心实验室的hs-cTn检测,对于初次检验无法确诊的患者,建议行快速诊断算法(如0 h/1 h、0 h/2 h算法)。POCT(con-cTn)仅适用于资源受限环境(如救护车转运、基层医院急诊)下的快速初筛或对已明确STEMI患者的辅助支持。(推荐级别:强推荐,证据等级:高)
推荐意见13:对于疑似ACS患者,若初始hs-cTn处于诊断灰区、症状不典型、高风险(如HEART/TIMI/GRACE评分高)、症状持续时间短(< 3 h)或合并肾功能不全等干扰因素,宜采用基于中心实验室的hs-cTn动态监测(0 h/1 h或0 h/2 h算法),结合Δ值≥20%及临床/心电图演变指导诊疗。(推荐级别:强推荐,证据等级:高)
推荐意见14:对于急性胸痛或伴呼吸困难患者,宜检测NT-proBNP/BNP以排除急性心衰,其中NT-proBNP的诊断临界值需根据年龄及肾功能分层调整,且对使用ARNI或重组人BNP类药物的患者宜优先选择NT-proBNP。(推荐级别:有条件推荐,证据等级:高)
推荐意见15:D-二聚体联合临床概率评分(Wells/Geneva)应用于排除低危PE,避免过度CTA;其中D-二聚体应具备用于排除静脉血栓栓塞的截断值,若D-二聚体显著升高(如 > 5.0 μg/mL FEU)需警惕AD可能,但阴性结果不能完全排除AD,需结合症状及影像学(如CTA、经食道心脏超声)综合评估。(推荐级别:强推荐,证据等级:中)
1.4 脑血管病与意识障碍快速鉴别诊断与动态监测检验策略急性脑血管疾病(acute cerebrovascular disease, ACVD)是全球范围内致残与致死的首要病因之一[68],我国现有卒中患者超过1 700万例,高居全球首位[69],具有起病急骤、病情进展迅速的特点。欧洲44个国家的研究显示,尽管急性缺血性卒中患者及时接受静脉溶栓治疗能显著改善预后,其整体实施率仅约7.3%,远低于理想水平[70]。此外,意识障碍作为ACVD的常见伴随症状,其病因复杂多样,既可能是脑血管事件本身(如大面积梗死或脑出血)的直接表现,也可能是中毒、代谢紊乱(如低血糖、肝性脑病)或感染等继发因素所致。这种临床异质性要求急诊医生在有限时间内快速完成病因鉴别,既要避免因误诊导致治疗延误,又要防止过度干预带来的并发症风险。在此背景下,检验医学通过提供快速、精准的实验室数据,成为急诊决策的核心支撑—从凝血功能评估到毒物筛查,从生物标志物动态监测到代谢指标分析,检验技术的革新正重塑急诊脑血管病及意识障碍的诊疗路径。急诊脑血管病及意识障碍的救治需遵循“时间窗导向”与“病因导向”的双重原则。对于疑似ACVD患者,首要任务是快速完成神经功能评估(如美国国立卫生研究院卒中量表评分)及影像学检查(如CT/MRI),以明确卒中类型及溶栓/取栓适应证。然而,单纯依赖影像学可能遗漏非结构性病因(如中毒或代谢性脑病),因此需结合实验室检测构建多维证据链。例如,凝血功能检测[国际标准化比值(international normalized ratio, INR)、活化部分凝血活酶时间(activated partial thromboplastin time, APTT)]可在3 min内排除抗凝治疗禁忌,显著缩短溶栓决策时间[71];而D-二聚体联合临床评分(Wells/Geneva)可高效排除低危肺栓塞,避免不必要的CTA检查[41]。对于意识障碍患者,需同步启动代谢与中毒筛查:动脉血气分析可迅速识别酸中毒(pH < 7.3)与低氧血症;血氨、乳酸及血糖检测有助于鉴别肝性脑病、休克、低血糖及糖尿病高渗等;毒物快速筛查(如免疫层析法)则能在15 min内锁定有机磷、镇静剂等常见毒物,为解毒治疗提供依据。这种分层递进的策略不仅优化了医疗资源分配,更通过“排除-锁定-干预”的逻辑链条,显著提升了救治效率。
在急诊脑血管病及意识障碍的诊治中,检验技术贯穿始终,其价值体现在三个层面:一是快速鉴别诊断。例如,BNP/NT-proBNP是鉴别房颤相关心源性卒中的重要血清标志物,其鉴别效能可达85%。当检测数值显著增高时,应优先考虑心源性栓塞机制[72];NSE动态监测(如发病6 h > 18.6 μg/L)可早期预测神经功能缺损风险,为预后评估提供客观依据[7-3]。二是指导个体化治疗。通过凝血功能检测(如INR > 1.7),有助于评估并降低溶栓治疗后的出血风险[71];毒物浓度定量(如百草枯代谢标志物)是血液净化治疗启动的关键指标;而乳酸水平每2 h的动态监测(阈值≥4 mmol/L)则为休克复苏提供实时反馈[63]。三是优化资源利用。POCT与传统实验室的协同模式(如30 min内完成血型鉴定与交叉配血)大幅缩短术前准备时间;血栓弹力图(thromboelastography, TEG)指导下的精准输血策略使凝血因子替代治疗效率提升40%[74]。
推荐意见16:所有疑似ACVD患者应在到院15 min内完成凝血功能、血小板计数、肾功能、电解质等检测,拟行静脉溶栓者需在30 min内获取基线纤维蛋白原(fibrinogen, FIB)和凝血酶时间;若患者合并意识障碍或疑似中毒性卒中,需同步加测血氨、乳酸、血糖及毒物筛查(如尿液/血液免疫层析法),以鉴别代谢性脑病或中毒病因,并根据毒物浓度检测结果(如百草枯代谢标志物)指导血液净化治疗。(推荐级别:有条件推荐,证据等级:中)
推荐意见17:对疑似ACVD患者,若存在胸痛/背痛/呼吸困难或ECG异常,应同步检测hs-cTn和D-二聚体,高度怀疑合并缺血性心肌病或急性AD时,立即进行影像学(如CTA)排查;对生命体征不稳定或器官明显受损者(如呼吸异常、代谢性酸中毒),进行凝血功能、血气分析及脏器功能评估,并动态监测乳酸水平(每2 h)以指导复苏。(推荐级别:有条件推荐,证据等级:中)
1.5 创伤相关快速评估与凝血功能监测检验策略创伤是全球范围内致残致死的主要原因,严重创伤患者常因失血性休克和创伤性凝血病(trauma-induced coagulopathy, TIC)面临极高死亡风险。休克与组织灌注的评估需依赖动脉血气分析同步获取pH、PaCO2、电解质、碱剩余等参数,并结合血气乳酸动态监测(初始乳酸 > 4 mmol/L提示严重组织缺氧)实现休克分型与复苏效果评价。英国NICE创伤指南强调[75]:乳酸值需动态追踪变化趋势以指导复苏终点判断;血红蛋白(haemoglobin, Hb)与血细胞比容(hematocrit, Hct)应根据出血情况频繁监测,其核心目标是识别活动性出血并指导限制性输血策略—维持Hb在70~90 g/L可降低输血相关心脏并发症(如心衰、心肌梗死),且通过增加心输出量与氧摄取率代偿,不增加器官缺血风险,该阈值得到TRICC与FOCUS试验的循证支持[76-77]。
TIC的精准管理是降低死亡率的核心环节。TEG/血栓弹力凝血测定法(rotational thromboelastometry, ROTEM)技术通过三大核心优势革新传统凝血监测模式[78]:其一,在时效性上较常规凝血检测(PT/APTT)提前15 min预测大输血需求与TIC,美国东部创伤外科协会指南强调TEG/ ROTEM通过实时、全面监测凝血-纤溶动态过程,精准指导血液制品输注,减少创伤患者不必要的输血并降低死亡率[79]。其二,具备全流程评估能力,可同步分析凝血因子(R时间延长 > 8 min提示凝血因子缺乏,需输注新鲜冰冻血浆)、FIB功能(α角 < 60°或K值> 3 min提示FIB不足,需补充冷沉淀或FIB浓缩物)、血小板活性(最大振幅(maximum amplitude, MA) < 50 mm提示功能低下,需输注血小板)及纤溶状态(LY30 > 3%提示纤溶亢进,需静注氨甲环酸),其中纤溶亢进的识别能力为传统检测所缺失[78, 80-82]。其三,具有显著资源优化价值,TEG指导的成分输血策略使血制品用量降低30%~40%,同时降低病死率[83]。需注意其局限性:对新型抗凝剂(如利伐沙班/阿哌沙班)敏感度有限(仅12.5%异常)[84],且不同设备参数不可直接互换(如TEG-MA较VCM-MCF高29.5 mm)[85]。在严重创伤患者,尤其是存在活动性出血或休克的高危TIC患者的管理中,TEG/ROTEM技术凭借其快速、全面、功能导向的凝血监测能力,显著优于传统凝血检测[80, 83]。本专家共识基于现有最佳证据,强烈推荐有条件单位将TEG/ROTEM作为TIC管理及指导成分输血的首选监测工具。其应用能实现更早期的干预、更精准的输血治疗,最终达到降低病死率、减少输血相关并发症、优化血液资源利用的核心目标。医疗机构应着力提升TEG/ROTEM的可及性和规范应用能力,同时充分认识其局限性,确保其在创伤救治中发挥最大效益。
创伤性颅脑损伤的检验辅助评估在影像资源受限时尤为重要。GFAP在伤后3 h检测的阳性预测值达94%,其动态变化与CT显示的脑实质损伤体积呈正相关;对于格拉斯哥昏迷评分13~15分的轻型创伤性颅脑损伤患者,GFAP联合S-100β检测可将不必要的头部CT检查率降低35%[86-87]。
推荐意见18:所有严重创伤患者到院10 min内完成动脉血气(含乳酸与电解质)检测,30 min内完成TEG/ROTEM凝血功能动态监测(替代传统PT/APTT),并依据TEG/ROTEM结果以指导成分输血。(推荐级别:强推荐,证据等级:高)
推荐意见19:TEG/ROTEM参数异常时启动目标导向输血:R时间 > 8 min需输注新鲜冰冻血浆(fresh frozen plasma, FFP);α角 < 60°或K > 3 min需补充FIB制剂/冷沉淀;MA < 50 mm需输注血小板;LY30 > 3%需静注氨甲环酸1 g。(推荐级别:强推荐,证据等级:高)
推荐意见20:所有严重创伤患者应动态监测Hb和Hct,同时持续动态监测TEG/ROTEM(每30~60 min)直至凝血参数稳定;若MA持续降低伴D-二聚体升高,需排查迟发性凝血病并评估抗凝指征。(推荐级别:强推荐,证据等级:中)
1.6 消化道出血风险评估与凝血功能检测策略急性消化道出血是急诊科常见的致命性急症,年发病率约(50~150)/10万人,病死率高达10%~14%,未及时干预的休克患者病死率可骤增至40%以上[88]。其病因可分为上消化道(如静脉曲张破裂、消化性溃疡)与下消化道(如憩室、肿瘤)出血,其中肝硬化门脉高压所致的食管胃底静脉曲张破裂最为凶险[89]。患者早期可表现为呕血、黑便或血便,但部分隐匿性出血仅以血流动力学不稳定(收缩压 < 90 mmHg、心率 > 100次/min)为首发表现,迅速进展至失血性休克及多器官衰竭风险极高,因此推荐对所有疑似患者立即监测生命体征并启动休克流程(包括快速循环支持如液体复苏、输血),以稳定病情并为后续诊治争取时间窗[90]。
急诊检验的核心作用需聚焦快速评估与个体化凝血管理:基础评估要求在到院30 min内完成血常规(Hb < 70 g/L提示重度出血,需警惕急性期血液浓缩致假性正常)、凝血功能(INR > 1.5提示肝硬化/抗凝药物/弥散性血管内凝血相关凝血障碍)、肝功能(ALT、AST、白蛋白)及血小板计数(< 50×109/L增加再出血风险),同时同步检测动脉血气(乳酸 > 4 mmol/L提示组织缺氧)及尿素氮/肌酐比值(> 30∶1支持上消化道出血)。对于肝硬化患者,传统凝血指标(如INR)常高估出血风险(因抗凝因子同步缺乏),此时TEG/ROTEM可提供更真实的凝血状态评估—研究证实其参数中R时间延长与PT呈正相关,MA降低与血小板计数相关,基于此指导的成分输血策略使FFP用量减少25%、血小板输注量减少20.8%,尤其在内镜或手术前可避免无谓输血[91-94];需注意设备间存在差异,相同肝硬化患者中ROTEM指导组较TEG组FFP用量减少30%[93]。在急性消化道出血,尤其是合并肝硬化的高危患者管理中,无谓输血(特别是FFP)带来的风险不容忽视。主要风险包括:输血相关循环超负荷、输血相关急性肺损伤、加重门脉压力与再出血风险、延误确定性治疗(如内镜/手术)、宝贵的血液资源浪费、免疫抑制与感染风险增加等。依赖传统INR等指标易导致过度治疗。TEG/ROTEM技术通过提供更真实、全面的功能性凝血评估,成为实现精准输血管理、规避无谓输血风险的核心工具。本专家共识基于循证证据,强烈推荐有条件单位对符合指征的消化道出血患者,特别是肝硬化患者,采用TEG/ROTEM指导血液制品输注决策。这不仅优化了患者预后(减少输血并发症),也极大提高了宝贵血液资源的利用效率,是急诊精准医学实践的重要体现。
分层干预策略遵循"稳定-评估-靶向"原则:初始阶段通过休克流程稳定生命体征,实施限制性液体复苏(目标收缩压90~100 mmHg);继而依据Blatchford≥6进行危险分层,高危者优先12~24 h内行内镜干预;肝硬化患者需专属管理,包括联合抗生素预防与血管活性药物(如特利加压素),并依据TEG/ROTEM参数指导成分输血(R时间 > 8 min输注FFP,MA < 50 mm输注血小板)[92];最终通过增强CT或内镜技术精准定位出血点,实施止血。
推荐意见21:到院30 min内完成血常规(Hb、Hct)、凝血功能(PT/APTT/INR)及血型检测,疑似肝硬化门脉高压出血者,加测肝功能(ALT、AST、白蛋白)及血小板计数。对血流动力学不稳定者,同步检测动脉血气(含乳酸、电解质)及尿素氮/肌酐比值。(推荐级别:强推荐,证据等级:高)
推荐意见22:肝硬化门脉高压所致消化道出血患者,凝血管理应优先采用TEG或ROTEM检测(替代传统INR/血小板计数),依据参数异常指导成分输血:R时间 > 8 min输注FFP,MA < 50 mm输注血小板。(推荐级别:强推荐,证据等级:高)
推荐意见23:所有行紧急内镜或手术的肝硬化患者,术前需完成TEG/ROTEM检测以避免过度输血(如INR升高但TEG正常者无需输注FFP)。(推荐级别:强推荐,证据等级:高)
1.7 内分泌及代谢急症检测策略内分泌及代谢急症症状非特异、进展迅猛,常使临床决策陷入困境,其本质是激素、代谢或反馈调节失控导致机体稳态濒临崩溃的复杂网络(从低血糖昏迷到肾代谢异常),早期识别预警征象并解析病理驱动因素是抢救生命和预防多器官功能障碍的核心。尽管诊疗技术进步提升了救治成功率,但面对高龄化社会的共病挑战,构建个体化精准应急管理体系仍具挑战。在这一背景下,检验技术在急诊中的应用尤为关键,可实现快速评估与精准干预的高效结合。以肾脏急症为例,如急性肾损伤(acute kidney injury, AKI)或慢性肾病急性加重,推荐的核心实验室检测包括血肌酐、尿素氮、胱抑素C及血气分析(涵盖pH、电解质及乳酸),并需重点监测血钾水平以防范高钾血症风险[95]。尿液学检查如尿沉渣、尿白蛋白/肌酐比值和尿电解质,有助于鉴别AKI的分型。若怀疑免疫或血管炎相关急进展性肾炎,应尽早进行自身抗体及补体检测,以明确病因并指导治疗。在糖尿病急症方面,以糖尿病酮症酸中毒为例,所有疑似患者到院后应优先完成血气分析、血糖及β-羟丁酸定量检测,以实现快速识别与初步处理。同时,传统实验室需同步开展糖化血红蛋白、C肽及胰岛素水平测定,这不仅有助于明确糖尿病分型,还可评估胰岛β细胞功能,为制定个体化控糖方案提供依据[96]。检验指标在急诊中的合理应用,贯穿从快速初筛到精准分型、从急性期干预到长期管理的全过程,显著提升了对复杂内分泌与代谢急症的诊治效率与安全性。
推荐意见24:在肾脏急症的诊疗中,推荐的核心实验室检测包括血肌酐、尿素氮、胱抑素C及血气分析(pH、电解质及乳酸),并重点监测电解质尤其是血钾水平。尿液学检查如尿沉渣、尿白蛋白/肌酐比值和尿电解质可帮助鉴别AKI的分型。对于疑似免疫性或血管炎相关的急进展性肾炎,应尽早行自身抗体及补体检测。(推荐级别:强推荐,证据等级:中)
推荐意见25:所有疑似糖尿病酮症酸中毒的患者,到院优先进行血气、血糖监测及β-羟丁酸定量,快速识别糖尿病酮症酸中毒;传统实验室检测需同步完成糖化血红蛋白、C肽及胰岛素水平测定,以明确糖尿病分型并评估胰岛β细胞功能,从而制定个体化控糖方案。(推荐级别:强推荐,证据等级:中)
1.8 急诊术前传染病筛查联合检测策略急诊患者如重大创伤常需紧急手术、输血或侵入性操作,术前传染病筛查是保障医疗安全、防止医源性感染的关键环节。依据《临床输血技术规范》《医疗机构临床用血管理办法》及《医院感染管理办法》要求,所有拟行手术、输血或侵入性操作的患者,应在术前完成传染病四项联合检测(HBsAg、抗-HCV、HIV-Ag/Ab、抗-TP),并将其纳入医院感染防控体系[97-99]。在此基础上,结合急诊患者病情紧急、周转快的特点,建议扩展至“传染病八项”筛查(含HBsAg、HBsAb、HBeAg、HBeAb、HBcAb、抗-HCV、HIV-Ag/Ab、抗-TP),以更全面评估感染风险、优化围术期管理及职业暴露防护[100-102]。
在HBV感染的诊断与分期中,除常规血清学标志物外,HBV核心抗体IgM(抗-HBc IgM)是鉴别急性感染或慢性感染急性发作的关键指标。抗-HBc IgM在急性HBV感染后早期出现(症状出现后1~2周),可持续3~12个月,其水平显著升高提示现症感染或病毒复制活跃[103]。对于HBsAg阳性但临床未能明确感染状态的患者,检测抗-HBc IgM有助于区分急性感染与慢性携带状态,指导抗病毒治疗时机及感染控制策略。HCV感染具有高隐匿性,传统抗-HCV检测虽可识别既往或现症感染,但在窗口期(约40~70 d)存在漏检风险。HCV核心抗原是病毒复制的直接标志物,感染后1~2周即可检出,较抗体出现提前数周。因此,HCV抗原抗体联合检测显著缩短窗口期,提高急性HCV感染的早期诊断率,尤其适用于急诊疑似暴露或高危人群(如静脉药瘾者、不明原因肝功异常者)。研究显示,HCV抗原抗体联合检测的敏感度达99%,特异度达99.9%,可有效避免窗口期漏诊,为急诊术前筛查提供更可靠的病原学依据[104-105]。
推荐意见26:所有拟行急诊手术、输血或侵入性操作的患者,术前应在完成血常规、出凝血功能等常规检测的基础上,采用中心实验室检测平台同步完成传染病八项筛查(HBsAg、HBsAb、HBeAg、HBeAb、HBcAb、抗-HCV、HIV-Ag/Ab、抗-TP)。此项筛查应纳入医院感染控制与用血管理核心流程,确保检测结果实时嵌入电子病历系统并触发闭环管理。(推荐级别:强推荐,证据等级:高)
推荐意见27:医疗机构应建立急诊术前传染病快速筛查绿色通道,通过流程优化确保中心实验室检测时效,满足急诊急救需求,同时建立完善的阳性结果追溯与多部门协同处置机制。(推荐级别:强推荐,证据等级:高)
推荐意见28:对HBsAg阳性或HBV感染状态不明的急诊术前患者,推荐采用中心实验室平台检测采取HBV DNA检测,若HBV DNA检测不可及,HBV核心抗体IgM(抗-HBc IgM),以鉴别急性感染、慢性感染急性发作或既往感染,为指导临床干预、抗病毒治疗与感染控制提供依据。(推荐级别:强推荐,证据等级:高)
推荐意见29:推荐采用HCV抗原抗体联合检测作为急诊术前HCV筛查策略,以缩短窗口期、提高检测灵敏度,尤其适用于高危人群或疑似急性暴露者。筛查阳性结果需采用核酸检测(HCV RNA)进行确认。(推荐级别:强推荐,证据等级:中)
推荐意见30:推荐将HIV抗原抗体联合检测作为急诊科HIV筛查的首选方案。三级医院应常规开展;二级医院可根据本地区HIV流行情况及高危人群暴露风险选择开展;所有筛查有反应性结果需进一步进行补充试验确认。(推荐级别:强推荐,证据等级:高)
根据上述急诊常见场景的检验策略分析,构建分层检验推荐体系(表 2),旨在实现精准、快速的临床决策。内容强调以循证为依据,针对不同急诊场景推荐最具诊断效能的关键生物标志物。同时,重视关键指标的动态监测与临床流程整合,从而全面提升急诊救治效率与安全性。
| 病种/场景 | 核心检验项目(强推荐,诊断/排除必备) | 补充检验项目(有条件推荐,用于分层/鉴别/预后) | 可选/新兴检验项目(探索性,需结合其他评估) |
| 氧合与组织灌注评估 | 动脉血气分析(pH、PaO2、PaCO2、乳酸,电解质) | 中心静脉血乳酸(无法获取动脉血时,需校正) | 外周静脉血乳酸(仅限初筛,准确性有限) |
| 胸痛 | 高敏肌钙蛋白(hs-cTn) | POCT(con-cTn) BNP/NT-proBNP肌酸激酶同工酶(CK-MB) D-二聚体肌红蛋白(Myo) |
心肌肌球蛋白结合蛋白C(cMyBP-C) 心型脂肪酸结合蛋白(H-FABP) sST2、GDF-15、MPO(炎症与预后评估) |
| 脓毒症 | 降钙素原(PCT) 血常规(WBC) 涂片革兰染色培养血气分析(含乳酸) |
超敏C反应蛋白(CRP) 白细胞介素-6(IL-6) 病原体核酸检测(如呼吸道多重PCR) 微生物培养 |
宏基因组测序(mNGS)(疑难、危重、免疫抑制患者) G试验/GM试验(真菌感染鉴别) |
| 脑血管病与意识障碍 | 凝血功能(INR、APTT、PLT) 血糖血小板电解质 |
血氨(鉴别肝性脑病) 血气分析D-二聚体(排除栓塞事件) 毒物筛查(疑似中毒时) BNP/NT-proBNP(鉴别心源性卒中) |
神经元特异性烯醇化酶(NSE) S-100β 胶质纤维酸性蛋白(GFAP) 神经丝轻链(Nf-L)(神经功能预后评估) |
| 严重创伤 | 血栓弹力图(TEG/ROTEM) 动脉血气(含乳酸) 血红蛋白(Hb)/血细胞比容(Hct) |
传统凝血四项(PT、APTT、TT、FIB)(若TEG不可及) | 胶质纤维酸性蛋白(GFAP)S-100β(轻型颅脑损伤,用于减少不必要的CT检查) |
| 消化道出血 | 血栓弹力图(TEG/ROTEM)(尤其肝硬化患者) 血常规(Hb、Hct、PLT) 血型 |
肝功能(ALT、AST、Alb) 尿素氮/肌酐比值(BUN/Cr) 凝血功能(PT、APTT、INR) 动脉血气(含乳酸)(血流动力学不稳定者) |
— |
| 内分泌与代谢急症 | 血糖血气分析电解质(尤其血钾) β-羟丁酸(疑似DKA时) |
糖化血红蛋白(HbA1c) C肽胰岛素肾功能(Cr、BUN、Cys-C) 尿常规(酮体、糖、沉渣) |
自身抗体及补体(疑似免疫性肾病) |
| 急诊术前筛查 | 传染病四项(HBsAg、抗-HCV、HIV-Ag/Ab、抗-TP) | 扩展至八项(HBsAg、HBsAb、HBeAg、HBeAb、HBcAb、抗-HCV、抗-HIV、抗-TP) HBV核心抗体IgM(抗-HBc IgM)(鉴别急性感染) |
HCV抗原抗体联合检测(缩短窗口期) HCV RNA(确认现症感染) |
急诊检验项目涵盖检验医学中各专业方向,科室应该根据急诊检验的工作内容,配备数量充足、具备相应资质的检验人员,经过系统培训、考核合格后授权上岗承担急诊检验工作。科室定期对急诊检验人员提供培训,培训内容应涵盖质量管理体系、岗位职责与技术能力、实验室生物安全、伦理及患者信息保护等方面。对于POCT,检测人员多为护理人员或临床医生,可能存在培训不足及质控意识薄弱的问题。建议由检验科POCT主要负责人(应具备医学检验专业主管检验师及以上资质)负责以下工作:仪器与试剂的质量评估、制定POCT标准操作流程、室内质控的监督、室间质量评价的实施、失控原因的分析并制定相关管理制度[106]。检验科应制定系统的培训计划和严格的考核制度,定期指派专人赴各临床学科操作人员进行培训和考核授权。各临床科室专职人员在POCT设备使用过程中遇到问题,应及时向检验科或设备科联系反馈,确保POCT工作规范、有序开展。
2.2 急诊检验仪器配置及流程优化临床实验室仪器使用和管理的核心目标是确保仪器性能符合规定标准,并满足检验项目的相关要求。《医疗机构临床实验室管理办法》和《医学实验室质量和能力认可准则》都对此提出明确要求,以保障检验结果的准确可靠[107-108]。急诊检验仪器须满足急诊医疗需求,保证结果及时、准确,为疾病诊治争取时间。快速准确的分析系统、低频的维修保养、适宜的通量和检测能力、稳定可靠的售后服务是急诊检验仪器需要符合的几大特征。检验科应全面评估并选用符合急诊需求、契合临床实际的检验设备,同时综合考虑实验室空间与环境条件。自动化流水线可节省人力、缩短标本周转时间(TAT)、降低生物安全风险并减少人为操作失误,而生化免疫一体机能够有效整合资源、提高检测速度。因此急诊检验实验室在评估时可根据自身情况,优先考虑自动化流水线和生化免疫一体机。急诊实验室选用的检验仪器应具备实时通信功能,能够将检测结果实时传输到实验室信息系统;应具备高效的样品条码识别能力,可自动识别主流的标准条形码;应具备双工通讯功能[109]。此外,急诊检验仪器应设优先通道,支持紧急样本加急检测,以满足危重症患者优先处理需求,确保检测快速完成并回报。设备故障时须启动应急预案,如启用备用机或临时调用非急诊设备。同时,检验仪器厂家应提供应提供7×24 h服务,并在接到售后服务电话30 min内响应;若电话无法解决,同城应在4 h内、异地24 h内、偏远地区48 h内到达现场(法定节假日除外)。
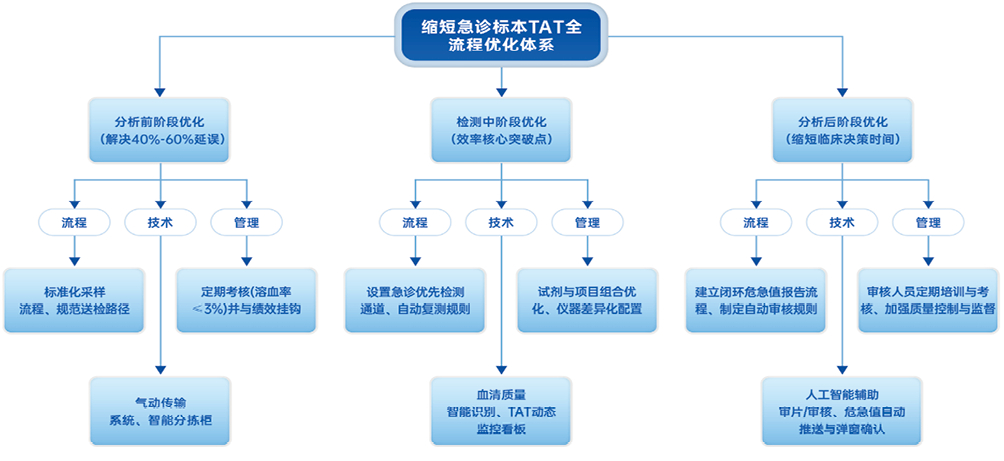
急诊检验室应在保障质量与控制成本的基础上快速、准确地提供检验报告,实验室内TAT至少应满足血、尿、便常规项目 < 30 min出报告,生化、免疫项目 < 2 h出报告,有条件的医院应满足生化项目 < 1 h出报告。在急诊检验管理中融入精益化管理理念,从环境、设备、人力、信息等多维度进行持续改进,利用科学的管理方法结合信息化、自动化、智能化改善检验科内、外的工作流程,缩短TAT并保证其稳定性。需针对分析前、中、后阶段实施精准干预。分析前环节(占TAT延误40%~60%)需严控标本质量:通过定期考核护理人员溶血率(目标≤3%)减少复采;采用气动传输系统与智能分拣柜确保急诊标本优先流转;利用信息系统和智慧屏对急诊检验标本全流程追踪和提示,动态监控TAT达标率及试剂余量或标本检测量[110]。分析中阶段为效率突破核心:仪器增设急诊专用检测模块,集成血清质量智能识别与异常结果自动复测功能;结合微流控芯片等新技术开发快速试剂[111]。分析后环节聚焦临床决策加速:应用人工智能辅助阅片和自动审核结果,缩短报告时间30%;建立闭环危急值警报系统,即时推送并强制弹窗确认。见图 3。
|
| 图 3 急诊检验标本全流程优化体系 |
|
|
项目检测必须使用仪器、试剂、校准品、操作程序和人员组成的检测分析系统, 若检测分析系统缺乏完整性和有效性,则无法保证检验结果质量。目前,我国实验室检测分析系统存在配套和非配套系统。配套系统可确保每项检测结果溯源清晰,便于监管与质控,保障检测过程准确性。同时,标准化的操作流程也利于提高工作效率,缩短检测TAT,实现资源的合理分配和高效利用。非配套系统(例如试剂与仪器不匹配)会破坏系统完整性,引入更多不确定因素,可能导致流程复杂化、TAT延长及结果准确性下降。
开展检验项目结果的可比性验证,有利于确保同一检测项目在不同环境、仪器、试剂或操作人员间的结果一致,为临床诊疗与质控提供可靠数据支持。可比性验证的实施还能促进实验室间交流合作,提升整体检测水平。
急诊检验实验室应建立完善的质量控制体系,定期进行设备校准和性能验证,确保在高强度工作环境下检验结果的准确可靠。需关注常见干扰因素(如溶血、脂血、黄疸、单克隆免疫球蛋白及某些还原性物质等)及环境干扰(如温度、湿度、噪音、水质、电流稳定性、电磁干扰等),制定目干扰因素的识别和处理程序, 并优先选择抗干扰能力强的检测方法。在比较分析方法间抗干扰能力时, 实验室可根据临床需求、厂家声明和样品特点(实际可能存在的干扰物质及达到的浓度)选择需要验证的干扰物种类及浓度。
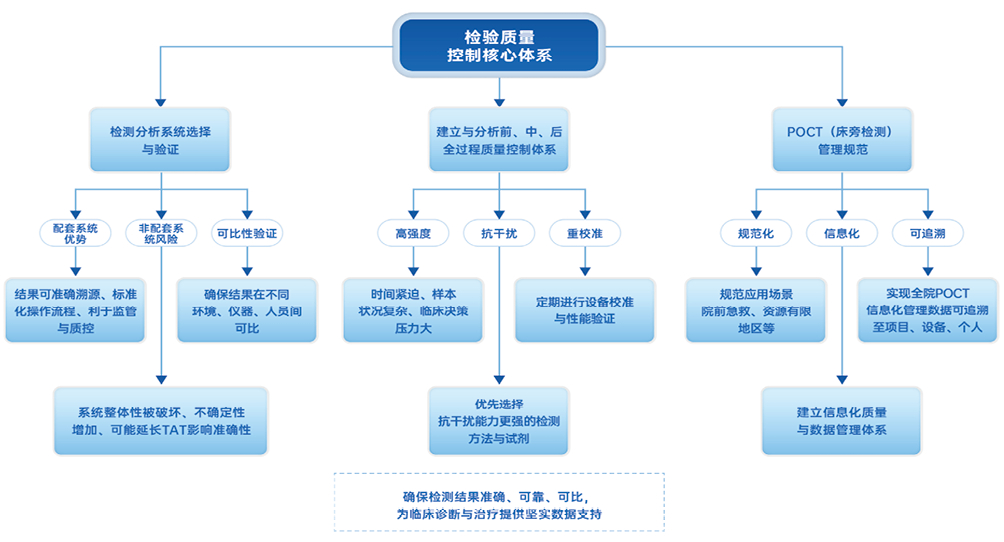
POCT的应用应聚焦于心搏骤停、严重创伤、急性心脑血管事件等需快速决策的场景,在院前急救及资源有限地区可突破电力与冷链限制[112-113]。POCT须具备规范的数据管理和质控体系,借助医疗信息系统对数据进行信息化处理;检验结果应该包含完整的报告单内容,操作人员资质和设备信息应该实时更新并同步至系统;院前急救(如“120”救护车)的POCT应该通过网络与院内系统连接,实现远程实时患者信息管理。POCT数据包含检验、人员、设备、质量四大模块,数据中心可实时统计并记录院内检验量、检验项目失控情况、人员资质培训情况、设备运行状态、耗材使用情况等全院POCT实况。数据应支持逐层钻取,可具体查看某一检验项目、设备或医护人员的检测详情、质控记录、设备生命周期及培训情况等,实现全院POCT信息化管理。院前急救POCT可通过5G网络与院内系统互联,在救护车上完成远程患者信息管理。见图 4。
|
| 图 4 急诊检验质量控制核心体系 |
|
|
前沿技术正深刻改变急诊检验模式:微流控芯片整合样本处理与检测全流程,实现感染病原体快速鉴定[114];纳米孔测序技术6 h内完成脓毒症全血病原体检测,诊断率提升35%;可穿戴生物传感器动态监测组织灌注与血糖水平,减少急症采血频次。未来需构建“技术-流程-政策”三位一体体系:技术上持续推进检测方法的创新与优化,拓展精准、快速的检测技术在慢性病管理等更广泛临床场景中的应用[115];流程上完善分级诊疗衔接与危急值响应机制,确保急诊检验与临床诊疗的高效协同;政策层面力推动建立统一的质量控制标准框架,并通过医保政策覆盖与信息系统无缝对接,促进先进检测技术的普惠性应用。
推荐意见31:明确POCT与中心实验室的临床应用边界与分工。POCT应聚焦于需即时治疗决策的关键场景(如院前急救、生命体征不稳定患者的初步评估),如快速的POCT血气分析检测,有助于关键场景下疾病严重评估及治疗监测;中心实验室则承担确诊性检验、复杂项目检测及POCT结果的复核。二者应通过信息化系统实现数据实时整合、质控联动与闭环管理。(推荐级别:强推荐,证据等级:高)
推荐意见32:所有POCT设备需100%接入医院实验室信息系统(LIS)和医院信息系统(HIS),自动传输原始检测数据(含质控记录与操作者信息)。系统应预设智能规则,在POCT结果符合以下条件时,自动向中心实验室发送复核指令并延迟结果临床发布:(1)与患者历史检测结果相比,偏差超出该项目的常规生物学变异或公认的临床允许误差范围;(2)本次检测伴随质量控制数据异常。中心实验室需建立复核绿色通道,确保此类样本得到优先检测,实现检测证据链的闭环管理,最大限度保障患者安全。(推荐级别:强推荐,证据等级:中)
推荐意见33:医疗机构应建立资源动态调配策略,为POCT与中心实验室的协同提供支撑。中心实验室须规划并预留专门的应急检测能力,用于快速响应并完成POCT异常结果的复核与确认。急诊科与检验科需紧密协同,通过流程再造与技术升级(如采用全自动流水线、气动传输系统及智能分拣技术),持续优化急诊检验流程,致力于达成并维持国际共识所倡导的急诊关键检测项目TAT目标。(推荐级别:强推荐,证据等级:中)
3 总结与展望本共识系统构建了以临床需求为导向的急诊检验分层优化策略体系,旨在通过检验技术的精准应用与流程优化,全面提升急危重症救治效率与患者预后。共识强调了中心实验室在确诊性检验中的核心地位(如hs-cTn用于ACS精准诊断、NT-proBNP优选于心衰评估、TEG/ROTEM提升创伤凝血病输血效率达40%),同时讨论了POCT在危重患者初步评估中的作用(如血气、乳酸、电解质等检测可缩短脓毒症、ACS等疾病的救治时间窗)。通过规范中心实验室与POCT的协同机制(初筛占比≤40%,复核时间≤30 min),实现了“快速初筛—精准确认”的闭环管理,有效支撑了急诊临床决策。
展望未来,急诊检验仍面临诸多挑战与发展机遇。技术层面,需进一步突破高敏标志物的普及与应用瓶颈,开发内置智能质控模块的新型设备(如解决血气检测中约9%的溶血率问题),推动微流控、纳米孔测序、可穿戴传感等前沿技术在急诊场景的落地。流程层面,应深化人工智能与多学科协作机制,构建覆盖“院前-急诊-ICU”的全流程数据整合与危急值响应体系,实现检验与临床的无缝衔接。政策与体系建设层面,需推动全球统一的质控标准与医保支付政策支持,促进高价值检验技术的普惠应用,最终实现“黄金时间窗”内的个体化精准救治。通过“技术—流程—政策”三位一体的系统推进,急诊检验必将在未来急危重症救治体系中发挥更加核心的支撑作用。
执笔人:陈棚棚李喜红龚凌寒黄佳捷(浙江大学医学院附属邵逸夫医院)
专家组成员(以姓名汉语拼音为序):
蔡文伟(浙江省人民医院)柴艳芬(天津医科大学总医院)陈安保(昆明医科大学第二附属医院)陈鸣(陆军军医大学西南医院)杜工亮(陕西省人民医院)杜俊凯(西安交通大学第一附属医院)高艳霞(郑州大学第一附属医院郑东院区)何谦(西安交通大学第二附属医院)何小军(《中华急诊医学杂志》)洪广亮(温州医科大学附属第一医院)洪玉才(浙江大学医学院附属邵逸夫医院)胡北(广东省人民医院)蒋浩琴(复旦大学附属华山医院)李传保(山东大学齐鲁医院)李俊杰(空军军医大学西京医院)李铁刚(中国医科大学附属盛京医院)李卫东(川北医学院附属医院)李文放[海军军医大学第二附属医院(上海长征医院)] 罗益锋(中山大学附属第一医院)吕立文(广西壮族自治区人民医院)马岳峰(浙江大学医学院附属第二医院)牛凯(山西省人民医院和平院区)孙武平(南方医科大学第五附属医院)邰文琳(昆明医科大学第二附属医院)陶志华(浙江大学医学院附属第二医院)唐朝贵(淮安市第一人民医院)田兆兴(首都医科大学附属北京积水潭医院)王军(南京鼓楼医院)王海滨(解放军总医院第四医学中心)夏剑(武汉大学中南医院)徐建(江苏省人民医院)燕宪亮(徐州医科大学附属医院)杨正飞(中山大学孙逸仙纪念医院)袁育林(广西壮族自治区人民医院)曾洁(国家卫生健康委临床检验中心)曾涛(广东医科大学附属医院)张东山(中南大学湘雅二医院)张国强(中日友好医院)张娟(四川省人民医院)张钧(浙江大学医学院附属邵逸夫医院)郑俊全(内蒙古医科大学附属医院)郑磊(南方医科大学附属南方医院)郑阳(辽宁省肿瘤医院)仲华(河南医药大学第一附属医院)周丽萍(浙江大学医学院附属邵逸夫医院)周平(四川省人民医院)祝成亮(武汉大学人民医院)庄一渝(浙江大学医学院附属邵逸夫医院)
利益冲突 所有作者声明无利益冲突
| [1] | De Luca G, Suryapranata H, Ottervanger JP, et al. Time delay to treatment and mortality in primary angioplasty for acute myocardial infarction: every minute of delay counts[J]. Circulation, 2004, 109(10): 1223-1225. DOI:10.1161/01.CIR.0000121424.76486.20 |
| [2] | Lee S, Song J, Lee S, et al. Impact of point-of-care lactate testing for sepsis on bundle adherence and clinical outcomes in the emergency department: a pre-post observational study[J]. J Clin Med, 2024, 13(18): 5389. DOI:10.3390/jcm13185389 |
| [3] | Gruebl T, Ploeger B, Wranze-Bielefeld E, et al. Point-of-care testing in out-of-hospital cardiac arrest: a retrospective analysis of relevance and consequences[J]. Scand J Trauma Resusc Emerg Med, 2021, 29(1): 128. DOI:10.1186/s13049-021-00943-w |
| [4] | Villar J, Short JH, Lighthall G. Lactate predicts both short- and long-term mortality in patients with and without sepsis[J]. Infect Dis, 2019, 12: 1178633719862776. DOI:10.1177/1178633719862776 |
| [5] | Rampersaud VM Jr, Barberis T, Thode HC Jr, et al. The role of point-of-care testing in cardiac arrest patients[J]. Am J Emerg Med, 2023, 74: 32-35. DOI:10.1016/j.ajem.2023.09.006 |
| [6] | 心肺复苏后昏迷患者早期神经功能预后评估专家共识组. 心肺复苏后昏迷患者早期神经功能预后评估专家共识[J]. 中华急诊医学杂志, 2019, 28(2): 156-162. DOI:10.3760/cma.j.issn.1671-0282.2019.02.006 |
| [7] | Bharosay A, Bharosay VV, Saxena K, et al. Role of brain biomarker in predicting clinical outcome in hypertensive cerebrovascular ischemic stroke[J]. Indian J Clin Biochem, 2018, 33(2): 178-183. DOI:10.1007/s12291-017-0664-3 |
| [8] | Ogawa H, Kitsios GD, Iwata M, et al. Sputum Gram stain for diagnosing causative bacterial pathogens and guiding antimicrobial therapies in community-acquired pneumonia: a systematic review and meta-analysis protocol[J]. Fujita Med J, 2019, 5(3): 79-84. DOI:10.20407/fmj.2018-019 |
| [9] | Noyon B, Loghin AD, Grandjean-Blanchet C, et al. Association between time to gram stain positivity and true bacteremia in pediatric emergency department patients[J]. Am J Emerg Med, 2025, 95: 72-76. DOI:10.1016/j.ajem.2025.05.019 |
| [10] | Ogbonna G, Atienza JR, Singleton DW, et al. Clinical and analytical performance evaluation of an automated procalcitonin assay[J]. J Appl Lab Med, 2025, 10(2): 359-369. DOI:10.1093/jalm/jfae114 |
| [11] | Saura O, Luyt CE. Procalcitonin as a biomarker to guide treatments for patients with lower respiratory tract infections[J]. Expert Rev Respir Med, 2023, 17(8): 651-661. DOI:10.1080/17476348.2023.2251394 |
| [12] | Foulon N, Haeger SM, Okamura K, et al. Procalcitonin levels in septic and nonseptic subjects with AKI and ESKD prior to and during continuous kidney replacement therapy (CKRT)[J]. Crit Care, 2025, 29(1): 171. DOI:10.1186/s13054-025-05414-7 |
| [13] | Juneja D, Jain N, Singh O, et al. Comparison between presepsin, procalcitonin, and CRP as biomarkers to diagnose sepsis in critically ill patients[J]. J Anaesthesiol Clin Pharmacol, 2023, 39(3): 458-462. DOI:10.4103/joacp.joacp_560_21 |
| [14] | 中国医药教育协会感染疾病专业委员会. 降钙素原指导抗菌药物临床合理应用专家共识[J]. 中华医学杂志, 2020, 100(36): 2813-2821. DOI:10.3760/cma.j.cn112137-20200714-02112 |
| [15] | Gupta S, Klompas M, Rhee C. Reassessing procalcitonin-guided antibiotic therapy in critically ill patients with sepsis: lessons from the ADAPT-sepsis trial[J]. Clin Infect Dis, 2025: ciaf336. DOI:10.1093/cid/ciaf336 |
| [16] | Evans L, Rhodes A, Alhazzani W, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021[J]. Intensive Care Med, 2021, 47(11): 1181-1247. DOI:10.1007/s00134-021-06506-y |
| [17] | Kiya GT, Asefa ET, Abebe G, et al. Procalcitonin guided antibiotic stewardship[J]. Biomark Insights, 2024, 19: 11772719241298197. DOI:10.1177/11772719241298197 |
| [18] | Zhang Y, La M, Sun JH, et al. Diagnostic value and prognostic significance of procalcitonin combined with C-reactive protein in patients with bacterial bloodstream infection[J]. Comput Math Methods Med, 2022, 2022: 6989229. DOI:10.1155/2022/6989229 |
| [19] | Chew CR, Patel D, Rynarzewska AI, et al. Procalcitonin use for predicting mortality and morbidity of patients diagnosed with sepsis within the intensive care unit[J]. Cureus, 2023, 15(10): e48080. DOI:10.7759/cureus.48080 |
| [20] | Yurttutan Uyar N, Sayar AK, Kocagöz AS, et al. Sepsis biomarkers for early diagnosis of bacteremia in emergency department[J]. J Infect Dev Ctries, 2023, 17(6): 832-839. DOI:10.3855/jidc.17221 |
| [21] | Lawandi A, Oshiro M, Warner S, et al. Reliability of admission procalcitonin testing for capturing bacteremia across the sepsis spectrum: real-world utilization and performance characteristics, 65 U.S. hospitals, 2008-2017[J]. Crit Care Med, 2023, 51(11): 1527-1537. DOI:10.1097/CCM.0000000000005968 |
| [22] | Erdem Kinas B, Etem Akagac A, Erek Toprak A, et al. Comparison of enzyme-linked fluorescent assay and electrochemiluminescence immune assay in procalcitonin measurement[J]. Turk J Biochem, 2022, 47(1): 19-22. DOI:10.1515/tjb-2020-0474 |
| [23] | Fan LP, Ding XG. Procalcitonin and C-reactive protein/procalcitonin ratio for distinguishing between infectious and neoplastic fever in cancer patients[J]. Altern Ther Health Med, 2023, 29(7): 365-369. |
| [24] | Yang J, Yang L, Wang YJ, et al. Interleukin-6 related signaling pathways as the intersection between chronic diseases and sepsis[J]. Mol Med, 2025, 31(1): 34. DOI:10.1186/s10020-025-01089-6 |
| [25] | Gan K, Chen Y, Tao LT, et al. Diagnostic value of circulating IL-6 in adult sepsis: a meta-analysis[J]. Minerva Anestesiol, 2024, 90(11): 1041-1050. DOI:10.23736/S0375-9393.24.18100-X |
| [26] | Varga NI, Bagiu IC, Vulcanescu DD, et al. IL-6 baseline values and dynamic changes in predicting sepsis mortality: a systematic review and meta-analysis[J]. Biomolecules, 2025, 15(3): 407. DOI:10.3390/biom15030407 |
| [27] | Puskarich MA, Trzeciak S, Shapiro NI, et al. Whole blood lactate kinetics in patients undergoing quantitative resuscitation for severe sepsis and septic shock[J]. Chest, 2013, 143(6): 1548-1553. DOI:10.1378/chest.12-0878 |
| [28] | Lau T, Nurek M, Singhal A, et al. Point-of-care tests, diagnostic uncertainty and antimicrobial stewardship in the ICU: procalcitonin or PCR to aid antibiotic-stop decisions - an observational cohort study[J]. BMJ Open, 2024, 14(12): e084872. DOI:10.1136/bmjopen-2024-084872 |
| [29] | Zhang PP, Li BS, Wang Y, et al. Development and multi-center clinical trials of an up-converting phosphor technology-based point-of-care (UPT-POCT) assay for rapid COVID-19 diagnosis and prediction of protective effects[J]. BMC Microbiol, 2022, 22(1): 42. DOI:10.1186/s12866-022-02450-z |
| [30] | Teoh TK, Powell J, Kelly J, et al. Outcomes of point-of-care testing for influenza in the emergency department of a tertiary referral hospital in Ireland[J]. J Hosp Infect, 2021, 110: 45-51. DOI:10.1016/j.jhin.2021.01.004 |
| [31] | Zhang HY, Zhou FL, Liu XY, et al. Clinical application of metagenomic next-generation sequencing in patients with different organ system infection: a retrospective observational study[J]. Medicine, 2024, 103(4): e36745. DOI:10.1097/MD.0000000000036745 |
| [32] | Reichlin T, Twerenbold R, Wildi K, et al. Prospective validation of a 1-hour algorithm to rule-out and rule-in acute myocardial infarction using a high-sensitivity cardiac troponin T assay[J]. CMAJ, 2015, 187(8): E243-E252. DOI:10.1503/cmaj.141349 |
| [33] | Hollander JE, Robey JL, Chase MR, et al. Relationship between a clear-cut alternative noncardiac diagnosis and 30-day outcome in emergency department patients with chest pain[J]. Acad Emerg Med, 2007, 14(3): 210-215. DOI:10.1197/j.aem.2006.09.053 |
| [34] | Kwok CS, Wong CW, Lovatt S, et al. Misdiagnosis of pulmonary embolism and missed pulmonary embolism: a systematic review of the literature[J]. Health Sci Rev, 2022, 3: 100022. DOI:10.1016/j.hsr.2022.100022 |
| [35] | Zwart B, Claessen BEPM, Damman P, et al. 2023 European Society of Cardiology guidelines for the management of acute coronary syndromes[J]. Neth Heart J, 2024, 32(10): 338-345. DOI:10.1007/s12471-024-01896-2 |
| [36] | Mueller C, Giannitsis E, Christ M, et al. Multicenter evaluation of a 0-hour/1-hour algorithm in the diagnosis of myocardial infarction with high-sensitivity cardiac troponin T[J]. Ann Emerg Med, 2016, 68(1): 76-87. e4. DOI:10.1016/j.annemergmed.2015.11.013 |
| [37] | 中华医学会心血管病学分会, 中华心血管病杂志编辑委员会. 非ST段抬高型急性冠脉综合征诊断和治疗指南(2024)[J]. 中华心血管病杂志, 2024, 52(6): 615-646. DOI:10.3760/cma.j.cn112148-20240107-00014 |
| [38] | Rubini Gimenez M, Twerenbold R, Reichlin T, et al. Direct comparison of high-sensitivity-cardiac troponin Ⅰ vs. T for the early diagnosis of acute myocardial infarction[J]. Eur Heart J, 2014, 35(34): 2303-2311. DOI:10.1093/eurheartj/ehu188 |
| [39] | Laguë M, Turgeon PY, Thériault S, et al. A false-positive troponin assay leading to the misdiagnosis of myopericarditis[J]. CMAJ, 2022, 194(12): E456-E459. DOI:10.1503/cmaj.211842 |
| [40] | Lehmann LH, Heckmann MB, Bailly G, et al. Cardiomuscular biomarkers in the diagnosis and prognostication of immune checkpoint inhibitor myocarditis[J]. Circulation, 2023, 148(6): 473-486. DOI:10.1161/CIRCULATIONAHA.123.062405 |
| [41] | Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR guideline for the evaluation and diagnosis of chest pain: a report of the American College of Cardiology/American Heart Association Joint Committee on clinical practice guidelines[J]. Circulation, 2021, 144(22): e368-e454. DOI:10.1161/CIR.0000000000001029 |
| [42] | Cullen L, Collinson PO, Giannitsis E. Point-of-care testing with high-sensitivity cardiac troponin assays: the challenges and opportunities[J]. Emerg Med J, 2022, 39(11): 861-866. DOI:10.1136/emermed-2021-211907 |
| [43] | Ter Avest E, Visser A, Reitsma B, et al. Point-of-care troponin T is inferior to high-sensitivity troponin T for ruling out acute myocardial infarction in the emergency department[J]. Eur J Emerg Med, 2016, 23(2): 95-101. DOI:10.1097/MEJ.0000000000000225 |
| [44] | Clerico A, Zaninotto M, Plebani M. Rapid rule-in and rule-out protocols of acute myocardial infarction using hs-cTnI and hs-cTnT methods[J]. Clin Chem Lab Med, 2023, 62(2): 213-217. DOI:10.1515/cclm-2023-1010 |
| [45] | Mohammadzadeh S, Matani N, Soleimani N, et al. Comparison of point-of-care and highly sensitive laboratory troponin testing in patients suspicious of acute myocardial infarction and its efficacy in clinical outcome[J]. Cardiol Res Pract, 2022, 2022: 6914979. DOI:10.1155/2022/6914979 |
| [46] | Beamish D, Maniuk T, Mukarram M, et al. Role of creatine kinase in the troponin era: a systematic review[J]. West J Emerg Med, 2021, 22(6): 1291-1294. DOI:10.5811/westjem.2020.11.47709 |
| [47] | Kaier TE, Alaour B, Marber M. Cardiac myosin-binding protein C-from bench to improved diagnosis of acute myocardial infarction[J]. Cardiovasc Drugs Ther, 2019, 33(2): 221-230. DOI:10.1007/s10557-018-6845-3 |
| [48] | Goel H, Melot J, Krinock MD, et al. Heart-type fatty acid-binding protein: an overlooked cardiac biomarker[J]. Ann Med, 2020, 52(8): 444-461. DOI:10.1080/07853890.2020.1800075 |
| [49] | Bruins Slot MHE, Reitsma JB, Rutten FH, et al. Heart-type fatty acid-binding protein in the early diagnosis of acute myocardial infarction: a systematic review and meta-analysis[J]. Heart, 2010, 96(24): 1957-1963. DOI:10.1136/hrt.2010.208272 |
| [50] | Stiermaier T, Adams V, Just M, et al. Growth differentiation factor-15 in Takotsubo cardiomyopathy: diagnostic and prognostic value[J]. Int J Cardiol, 2014, 173(3): 424-429. DOI:10.1016/j.ijcard.2014.03.014 |
| [51] | Li M, Duan L, Cai YL, et al. Growth differentiation factor-15 is associated with cardiovascular outcomes in patients with coronary artery disease[J]. Cardiovasc Diabetol, 2020, 19(1): 120. DOI:10.1186/s12933-020-01092-7 |
| [52] | Wang YB, Zhen C, Wang R, et al. Growth-differentiation factor-15 predicts adverse cardiac events in patients with acute coronary syndrome: a meta-analysis[J]. Am J Emerg Med, 2019, 37(7): 1346-1352. DOI:10.1016/j.ajem.2019.04.035 |
| [53] | Javaheri A, Ozcan M, Moubarak L, et al. Association between growth differentiation factor-15 and adverse outcomes among patients with heart failure: a systematic literature review[J]. Heliyon, 2024, 10(16): e35916. DOI:10.1016/j.heliyon.2024.e35916 |
| [54] | Frangie C, Daher J. Role of myeloperoxidase in inflammation and atherosclerosis (Review)[J]. Biomed Rep, 2022, 16(6): 53. DOI:10.3892/br.2022.1536 |
| [55] | Nicholls SJ, Wilson Tang WH, Brennan D, et al. Risk prediction with serial myeloperoxidase monitoring in patients with acute chest pain[J]. Clin Chem, 2011, 57(12): 1762-1770. DOI:10.1373/clinchem.2011.166827 |
| [56] | Kolodziej AR, Abo-Aly M, Elsawalhy E, et al. Prognostic role of elevated myeloperoxidase in patients with acute coronary syndrome: a systemic review and meta-analysis[J]. Mediators Inflamm, 2019, 2019: 2872607. DOI:10.1155/2019/2872607 |
| [57] | Zhang N, Wang JX, Wu XY, et al. Correlation analysis of plasma myeloperoxidase level with global registry of acute coronary events score and prognosis in patients with acute non-ST-segment elevation myocardial infarction[J]. Front Med, 2022, 9: 828174. DOI:10.3389/fmed.2022.828174 |
| [58] | 中华医学会心血管病学分会, 中国医师协会心血管内科医师分会, 中国医师协会心力衰竭专业委员会, 等. 中国心力衰竭诊断和治疗指南2024[J]. 中华心血管病杂志, 2024, 52(3): 235-275. DOI:10.3760/cma.j.cn112148-20231101-00405 |
| [59] | Kim H, Lee TH, Hur M, et al. Performance evaluation of AFIAS ST2 and ichroma ST2 assays in comparison with presage ST2 assay[J]. Rev Cardiovasc Med, 2023, 24(4): 100. DOI:10.31083/j.rcm2404100 |
| [60] | Huang AN, Qi X, Hou WG, et al. Prognostic value of sST2 and NT-proBNP at admission in heart failure with preserved, mid-ranged and reduced ejection fraction[J]. Acta Cardiol, 2018, 73(1): 41-48. DOI:10.1080/00015385.2017.1325617 |
| [61] | 国家食品药品监督管理局. YY/T 1579-2018/ISO 23640: 2011体外诊断医疗器械体外诊断试剂稳定性评价[S]. 北京: 中国标准出版社, 2018. |
| [62] | Kristoffersen AH, Ajzner E, Bauça JM, et al. Pre- and post-test probabilities of venous thromboembolism and diagnostic accuracy of D-dimer, estimated by European clinicians working in emergency departments[J]. Thromb Res, 2017, 159: 19-23. DOI:10.1016/j.thromres.2017.09.012 |
| [63] | Akhter M. D-dimer in high-risk pulmonary embolism workup[J]. Acad Emerg Med, 2025, 32(2): 186. DOI:10.1111/acem.15079 |
| [64] | Kruger RA, du Plessis J, Muller H. Pulmonary embolism diagnosis with D-dimer levels and computed tomography[J]. SA Gesondheid, 2024, 29: 2620. DOI:10.4102/hsag.v29i0.2620 |
| [65] | Price CP, Fay M, Hopstaken RM. Point-of-care testing for D-dimer in the diagnosis of venous thromboembolism in primary care: a narrative review[J]. Cardiol Ther, 2021, 10(1): 27-40. DOI:10.1007/s40119-020-00206-2 |
| [66] | Innocenti F, Lazzari C, Ricci F, et al. D-dimer tests in the emergency department: current insights[J]. Open Access Emerg Med, 2021, 13: 465-479. DOI:10.2147/OAEM.S238696 |
| [67] | Schafer K, Goldschmidt E, Oostra D, et al. The clinical significance of ultra-high D-dimer levels[J]. J Vasc Surg Venous Lymphat Disord, 2022, 10(1): 8-13. DOI:10.1016/j.jvsv.2021.06.011 |
| [68] | Berge E, Whiteley W, Audebert H, et al. European Stroke Organisation (ESO) guidelines on intravenous thrombolysis for acute ischaemic stroke[J]. Eur Stroke J, 2021, 6(1): I-LXII. DOI:10.1177/2396987321989865 |
| [69] | 中华医学会神经病学分会, 中华医学会神经病学分会脑血管病学组. 中国重症卒中管理指南2024[J]. 中华神经科杂志, 2024, 57(7): 698-714. DOI:10.3760/cma.j.cn113694-20231024-00261 |
| [70] | Aguiar de Sousa D, von Martial R, Abilleira S, et al. Access to and delivery of acute ischaemic stroke treatments: a survey of national scientific societies and stroke experts in 44 European countries[J]. Eur Stroke J, 2019, 4(1): 13-28. DOI:10.1177/2396987318786023 |
| [71] | Dolscheid-Pommerich RC, Dolscheid S, Eichhorn L, et al. Thrombolysis in stroke patients: Comparability of point-of-care versus central laboratory international normalized ratio[J]. PLoS One, 2018, 13(1): e0190867. DOI:10.1371/journal.pone.0190867 |
| [72] | Wu ZX, Yang LH, Huang W, et al. The value of the use of plasma B-type natriuretic peptide among acute ischemic stroke patients in a Chinese emergency department[J]. Clin Neurol Neurosurg, 2013, 115(9): 1671-1676. DOI:10.1016/j.clineuro.2013.02.021 |
| [73] | Singh HV, Pandey A, Shrivastava AK, et al. Prognostic value of neuron specific enolase and IL-10 in ischemic stroke and its correlation with degree of neurological deficit[J]. Clin Chim Acta, 2013, 419: 136-138. DOI:10.1016/j.cca.2013.02.014 |
| [74] | Pîrlog BO, Grotta JC. The applicability of thromboelastography in acute ischemic stroke: a literature review[J]. Semin Thromb Hemost, 2022, 48(7): 842-849. DOI:10.1055/s-0042-1753529 |
| [75] | National Institute for Health and Care Excellence (NICE). Major trauma: assessment and initial management [EB/OL]. London: NICE; 2016: 1-25. [2026-02-09]. https://www.nice.org.uk/guidance/ng39. |
| [76] | Carson JL, Terrin ML, Noveck H, et al. Liberal or restrictive transfusion in high-risk patients after hip surgery[J]. N Engl J Med, 2011, 365(26): 2453-2462. DOI:10.1056/NEJMoa1012452 |
| [77] | Hébert PC, Wells G, Blajchman MA, et al. A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care[J]. N Engl J Med, 1999, 340(6): 409-417. DOI:10.1056/nejm199902113400601 |
| [78] | Carll T. Viscoelastic testing methods[M/OL]//Advances in Clinical Chemistry. Elsevier, 2023, 17: 1-52. https://doi.org/10.1016/bs.acc.2023.09.001. |
| [79] | Bugaev N, Como JJ, Golani G, et al. Thromboelastography and rotational thromboelastometry in bleeding patients with coagulopathy: Practice management guideline from the Eastern Association for the Surgery of Trauma[J]. J Trauma Acute Care Surg, 2020, 89(6): 999-1017. DOI:10.1097/TA.0000000000002944 |
| [80] | Kvint S, Gutierrez A, Venezia A, et al. Application of a TEG-platelet mapping algorithm to guide reversal of antiplatelet agents in adults with mild-to-moderate traumatic brain injury: an observational pilot study[J]. Neurocrit Care, 2022, 37(3): 638-648. DOI:10.1007/s12028-022-01535-x |
| [81] | Selby R. "TEG talk": expanding clinical roles for thromboelastography and rotational thromboelastometry[J]. Hematology Am Soc Hematol Educ Program, 2020, 2020(1): 67-75. DOI:10.1182/hematology.2020000090 |
| [82] | Gilbert BW, Bissell BD, Santiago RD, et al. Tracing the lines: a review of viscoelastography for emergency medicine clinicians[J]. J Emerg Med, 2020, 59(2): 201-215. DOI:10.1016/j.jemermed.2020.04.009 |
| [83] | Brill JB, Brenner M, Duchesne J, et al. The role of TEG and ROTEM in damage control resuscitation[J]. Shock, 2021, 56(1S): 52-61. DOI:10.1097/SHK.0000000000001686 |
| [84] | Jenrette J, Schwarz K, Trujillo T, et al. Evaluation of direct oral anticoagulant use on thromboelastography in an emergency department population[J]. Am J Emerg Med, 2022, 52: 191-195. DOI:10.1016/j.ajem.2021.12.011 |
| [85] | Panigada M, Meli A, Forastieri Molinari A, et al. Agreement between viscoelastic coagulation monitor (VCM), TEG 5000, and coagulation tests in critically ill patients: a multicenter study[J]. ASAIO J, 2023, 69(6): e230-e239. DOI:10.1097/MAT.0000000000001932 |
| [86] | Dong N, Diao Y, Ding MH, et al. The effects of 7-nitroindazole on serum neuron-specific enolase and astroglia-derived protein (S100β) levels after traumatic brain injury[J]. Exp Ther Med, 2017, 13(6): 3183-3188. DOI:10.3892/etm.2017.4411 |
| [87] | Mrozek S, Delamarre L, Capilla F, et al. Cerebral expression of glial fibrillary acidic protein, ubiquitin carboxy-terminal hydrolase-L1, and matrix metalloproteinase 9 after traumatic brain injury and secondary brain insults in rats[J]. Biomark Insights, 2019, 14: 1177271919851515. DOI:10.1177/1177271919851515 |
| [88] | Oakland K. Changing epidemiology and etiology of upper and lower gastrointestinal bleeding[J]. Best Pract Res Clin Gastroenterol, 2019, 42/43: 101610. DOI:10.1016/j.bpg.2019.04.003 |
| [89] | Edelson J, Basso JE, Rockey DC. Updated strategies in the management of acute variceal haemorrhage[J]. Curr Opin Gastroenterol, 2021, 37(3): 167-172. DOI:10.1097/MOG.0000000000000723 |
| [90] | Barkun AN, Bardou M, Kuipers EJ, et al. International consensus recommendations on the management of patients with nonvariceal upper gastrointestinal bleeding[J]. Ann Intern Med, 2010, 152(2): 101-113. DOI:10.7326/0003-4819-152-2-201001190-00009 |
| [91] | Nepal C, Kc O, Koirala M, et al. A retrospective study comparing the effect of conventional coagulation parameters vs. thromboelastography-guided blood product utilization in patients with major gastrointestinal bleeding[J]. J Clin Med Res, 2023, 15(10/11): 431-437. DOI:10.14740/jocmr5022 |
| [92] | Abdulelah M, Asghar A, Sansait M, et al. Blood product utilization in thromboelastography-aided transfusion in gastrointestinal bleeding: a single-center experience[J]. Gastroenterology Res, 2025, 18(2): 49-55. DOI:10.14740/gr2025 |
| [93] | Gopal N, Panwar S, Saluja V, et al. Impact of coagulopathy assessment with thromboelastography and thromboelastometry on transfusion requirements in critically ill cirrhosis with nonvariceal bleeding: a prospective observational study[J]. Int J Crit Illn Inj Sci, 2024, 14(2): 67-73. DOI:10.4103/ijciis.ijciis_65_23 |
| [94] | Rizvi G, Marcinkowski B, Srinivasa N, et al. Impact on blood product utilization with thromboelastography guided resuscitation for gastrointestinal hemorrhage[J]. J Intensive Care Med, 2023, 38(4): 368-374. DOI:10.1177/08850666221126661 |
| [95] | El-Khoury JM, Hoenig MP, Jones GRD, et al. AACC guidance document on laboratory investigation of acute kidney injury[J]. J Appl Lab Med, 2021, 6(5): 1316-1337. DOI:10.1093/jalm/jfab020 |
| [96] | Sacks DB, Arnold M, Bakris GL, et al. Guidelines and recommendations for laboratory analysis in the diagnosis and management of diabetes mellitus[J]. Diabetes Care, 2023, 46(10): e151-e199. DOI:10.2337/dci23-0036 |
| [97] | 国家卫生健康委. 临床用血技术规范(2025年版)[EB/OL]. (2025-11-28). https://www.nhc.gov.cn/ylyjs/zcwj/202512/1f0e99982b49476b9b076ee10ef9ca75.shtml. |
| [98] | 国家卫生健康委员会. 医疗机构临床用血管理办法[EB/OL]. (2022-01-11). https://www.nhc.gov.cn/wjw/c100221/202201/7b7da6f69f0746e1acba7a4562232511.shtml. |
| [99] | 中华人民共和国卫生部. 医院感染管理办法[EB/OL]. (2006-07-06). https://www.nhc.gov.cn/fzs/c100048/200607/27f0469cc0d64011b5f5f5dca279733e.shtml. |
| [100] | 中华医学会检验医学分会. 急诊检验实验室能力建设与规范专家共识(2025版)[J]. 中华检验医学杂志, 2025, 48(9): 1134-1148. DOI:10.3760/cma.j.cn114452-20250509-00285 |
| [101] | Liu X, Wu CY, Yuan YL, et al. Clinical performance evaluation of an HIV Duo assay: From HIV screening to acute and non-acute HIV infection detection[J]. Clin Chim Acta, 2025, 565: 119949. DOI:10.1016/j.cca.2024.119949 |
| [102] | 中国医疗保健国际交流促进会基层检验技术标准化分会. 人类免疫缺陷病毒感染检测与诊断管理的专家共识[J]. 中华预防医学杂志, 2025, 59(2): 127-137. DOI:10.3760/cma.j.cn112150-20241014-00813 |
| [103] | 中华医学会肝病学分会基础医学与实验诊断协作组. 乙型肝炎病毒标志物临床应用专家共识[J]. 中华肝脏病杂志, 2023, 31(4): 389-400. DOI:10.3760/cma.j.cn501113-20230314-00113 |
| [104] | Majchrzak M, Bronner K, Laperche S, et al. Multicenter performance evaluation of the Elecsys HCV Duo immunoassay[J]. J Clin Virol, 2022, 156: 105293. DOI:10.1016/j.jcv.2022.105293 |
| [105] | Bui TI, Brown AP, Brown M, et al. Comparison of a dual antibody and antigen HCV immunoassay to standard of care algorithmic testing[J]. J Clin Microbiol, 2024, 62(10): e00832-e00824. DOI:10.1128/jcm.00832-24 |
| [106] | 武汉医学会急诊医学分会. 即时检验在急重症的应用管理专家共识(2024)[J]. 中华危重病急救医学, 2024, 36(9): 897-909. DOI:10.3760/cma.j.cn121430-20240612-00507 |
| [107] | 中华人民共和国卫生部. 医疗机构临床实验室管理办法[EB/OL]. (2006-02-27). https://www.nhc.gov.cn/wjw/c100175/200603/9f0d0fc9690349a1a73020434d81dc3d.shtml. |
| [108] | 中国合格评定国家认可委员会. CNAS-CL02: 医学实验室质量和能力认可准则[S/OL]. (2023-06-01). http://www.cnas.org.cn/rkgf/sysrk/jbrkzz/art/2024/art_64e91231bd794eff9b9f37b7f3ac5cc2.html. |
| [109] | 中国医学装备协会检验医学分会, 中国医学装备协会应用评价分会. 急诊检验分析系统应用评价专家共识(2025版)[J]. 中华检验医学杂志, 2025, 48(7): 834-841. DOI:10.3760/cma.j.cn114452-20250212-00077 |
| [110] | White BA, Baron JM, Dighe AS, et al. Applying Lean methodologies reduces ED laboratory turnaround times[J]. Am J Emerg Med, 2015, 33(11): 1572-1576. DOI:10.1016/j.ajem.2015.06.013 |
| [111] | Zhang L, Liu ZH, Lv YJ, et al. Comprehensive improvements in the emergency laboratory test process based on information technology[J]. BMC Med Inform Decis Mak, 2023, 23(1): 292. DOI:10.1186/s12911-023-02387-x |
| [112] | Kankaanpää M, Raitakari M, Muukkonen L, et al. Use of point-of-care testing and early assessment model reduces length of stay for ambulatory patients in an emergency department[J]. Scand J Trauma Resusc Emerg Med, 2016, 24(1): 125. DOI:10.1186/s13049-016-0319-z |
| [113] | Park HD. Current status of clinical application of point-of-care testing[J]. Arch Pathol Lab Med, 2021, 145(2): 168-175. DOI:10.5858/arpa.2020-0112-RA |
| [114] | Wang YR, Chen JW, Yang ZJ, et al. Advances in nucleic acid assays for infectious disease: the role of microfluidic technology[J]. Molecules, 2024, 29(11): 2417. DOI:10.3390/molecules29112417 |
| [115] | Yang SM, Lv SS, Zhang WJ, et al. Microfluidic point-of-care (POC) devices in early diagnosis: a review of opportunities and challenges[J]. Sensors, 2022, 22(4): 1620. DOI:10.3390/s22041620 |
 2026, Vol. 35
2026, Vol. 35