心源性休克(cardiogenic shock,CS)是心脏功能衰竭导致心输出量显著下降,进而引起组织器官灌注不足的临床综合征,其短期病死率可高达50%[1-2]。静脉-动脉体外膜氧合(venous-arterial extracorporeal membrane oxygenation, VA-ECMO)作为功能最强大的机械循环支持手段,在难治性CS及心脏骤停(cardiac arrest, CA)患者中的应用日益广泛,但其实际临床获益与成本效益仍存在争议[3-4]。研究报道,VA-ECMO的撤机失败率为25%~70%[5-7],而即便成功撤机,患者院内病死率仍可达36.6%[7]。因此,高撤机失败率和短期病死率仍是当前VA-ECMO治疗中面临的核心难题。
血乳酸主要由无氧糖酵解产生,是反映危重患者组织氧输送与灌注异常的敏感指标。研究发现,血乳酸水平可作为重症患者生存结局的早期预后指标[8-9]。然而,单次乳酸检测可能难以反映患者病情变化和治疗反应。因此,乳酸清除率(lactate clearance rate, LCR),即特定时间内乳酸水平下降率,通过反映乳酸动态变化而被日益关注。然而,LCR在CS患者中应用的研究仍较有限,证据尚不充分,且多聚焦于死亡结局[10-12]。有研究显示,24 h乳酸清除与CS患者撤机成功相关[7],但对于更早期、更具临床干预价值的12 h LCR与VA-ECMO撤机结局的关系,目前尚缺乏针对性探讨。据此,本研究旨在深入探讨12 h LCR与CS患者VA-ECMO撤机结局之间的关系,以期为早期风险分层与治疗策略调整提供参考依据。
1 资料与方法 1.1 研究对象本研究为单中心回顾性研究,收集2020年1月至2025年8月于宁波大学附属第一医院重症监护室住院,并接受VA-ECMO治疗的心源性休克患者的临床资料。纳入标准为:①年龄≥18周岁;②符合心源性休克诊断标准;③因心源性休克接受VA-ECMO,其上机指征包括(1)经充分液体复苏后,大剂量血管活性药物[0.5 μg/(kg·min)去甲肾上腺素等效剂量]和(或)IABP难以纠正的难治性休克;或(2)心源性CA经复苏后仍处于难治性休克状态。排除标准为:①妊娠或哺乳期患者;②临床资料缺失;③VA-ECMO支持时间 < 12 h;④肝硬化、恶性肿瘤活动期、药物中毒、重度颅脑损伤;⑤因家属因素(临终状态除外)放弃积极治疗。心源性休克诊断标准(同时满足以下3条):①持续性低血压:收缩压 < 90 mmHg(1 mmHg=0.133 kPa)持续30 min以上或平均动脉压低于基线水平≥30 mmHg或需要血管活性药物维持血压;②组织器官低灌注表现(至少1项):神志状态改变,皮肤湿冷,尿量 < 0.5 mL/(kg·h),血乳酸水平 > 2 mmol/L等;③心超提示心脏收缩和(或)舒张功能障碍[13-14]。本研究符合医学伦理学标准,并通过医院医学伦理委员会审批(伦审2025研第RS182号)。
本研究ECMO采用静脉-动脉(veno-arterial,VA)模式,行股动脉、股静脉经皮穿刺或切开置管。ECMO管理和撤机过程参照2018《成人体外膜肺氧合循环辅助专家共识》[15]、《成人体外膜肺氧合技术操作规范(2024年版)》[16]。
本研究血乳酸浓度均通过动脉血气分析仪(酶电极法)测定。血标本均采自患者自体上肢桡动脉或肱动脉。初始乳酸值定义为ECMO上机时刻±2 h内,最接近上机时刻的乳酸值。12 h乳酸值:ECMO上机后(12±2)h内,最接近上机12 h时间点的乳酸值。12 h乳酸清除率(12 h LCR)定义为(乳酸初始值-12 h乳酸值)/乳酸初始值×100%。
1.2 数据收集(1) 人口学信息:年龄、性别、身体质量指数(body mass index, BMI);(2)基础状态:ECMO上机病因、上机前是否CA;(3)合并症:高血压、糖尿病;(4)疾病严重程度:ECMO上机当天急性生理和慢性健康状况评分(acute physiology and chronic health evaluation Ⅱ,APACHE Ⅱ);(5)ECMO相关参数:上机初始泵速、流量;(6)上机后12 h接受治疗:液体平衡量、连续性肾脏替代治疗(continuous renal replacement therapy, CRRT)、主动脉内球囊反搏(intra-aortic balloon pump, IABP);(7)上机后首次实验室监测指标:白细胞计数、血小板计数、总胆红素、血肌酐、C反应蛋白、肌钙蛋白Ⅰ。主要结局指标为VA-ECMO撤机结局。ECMO撤机失败定义为ECMO支持期间或撤机后48 h内死亡[7],次要结局为28 d生存状况。
1.3 统计学方法采用R 4.4.0软件进行统计分析。计量资料经Shapiro-Wilk正态性检验,符合正态分布者用均数±标准差(x±s)表示,偏态分布者用中位数(四分位数)M[(Q1, Q3)]表示。分类资料用例数(率)表示。计量资料多组间比较采用方差分析或Kruskal-Wallis H检验,分类资料采用卡方检验。目前12 h LCR尚无公认的临床分层界值,鉴于其呈偏态分布,本研究依据其三分位数进行分组,将患者分为低(LCR < 20.00%)、中(20.00%≤LCR < 56.65%)、高(LCR≥56.65%)LCR 3组。采用单因素和多因素Logistic回归分析12 h LCR与VA-ECMO撤机失败的关系,协变量基于单因素回归结果及临床意义进行筛选,并进一步行趋势性分析。针对CS病因进行敏感性分析。采用限制性立方样条拟合12 h LCR与VA-ECMO撤机失败的关系曲线并进行非线性检验,节点数依据贝叶斯信息准则最小值确定。亚组分析探讨亚组因素与12 h LCR是否存在交互作用。绘制受试者工作曲线(receiver operator characteristic curve, ROC)评估12 h LCR对VA-ECMO撤机结局的预测价值,根据最大约登指数确定最佳截止值。以P < 0.05为差异有统计学意义。
2 结果 2.1 基线情况本研究共纳入91例因CS接受VA-ECMO治疗患者,其中男性55例,女性36例,平均年龄54.81岁,撤机失败率39.56%(36/91),28 d全因死亡率48.35%(44/91)。根据12 h LCR三分位数将患者分为低(LCR < 20.00%)、中(20.00%≤LCR < 56.65%)、高(LCR≥56.65%)LCR 3组。三组间病因构成存在差异(χ2=6.94, P=0.031)。而年龄、性别、BMI、APACHE Ⅱ评分、合并症(高血压、糖尿病)、CA发生率、ECMO泵速、流量、初始乳酸值、液体平衡量、IABP、CRRT接受率及其他实验室指标差异无统计学意义(均P > 0.05)。三组间撤机失败率(χ2=14.71,P < 0.001)、28 d全因死亡率(χ2=8.85, P=0.012)显著不同,随LCR升高呈下降趋势。见表 1。
| 变量 | 总数(n=91) | 低乳酸清除(n=30) | 中乳酸清除(n=31) | 高乳酸清除(n=30) | 统计值 | P值 |
| 年龄(岁)a | 54.81±14.62 | 56.83±14.39 | 53.55±13.65 | 54.10±16.04 | F=0.43 | 0.650 |
| 性别b | χ2=0.40 | 0.820 | ||||
| 男 | 55(60.44) | 18(60.00) | 20(64.52) | 17(56.67) | ||
| 女 | 36(39.56) | 12(40.00) | 11(35.48) | 13(43.33) | ||
| BMI(kg/m2)a | 23.46±3.18 | 23.31±3.02 | 23.19±3.27 | 23.88±3.29 | F=0.40 | 0.671 |
| APACHE Ⅱ(分)a | 27.86±7.52 | 27.83±7.71 | 27.90±7.08 | 27.83±8.01 | F=0.00 | 0.999 |
| ECMO泵速(r/min)c | 3 435.00(3 010.00, 3 882.50) | 3 300.00(2 941.00, 3588.00) | 3 377.50(2 988.75, 4 875.00) | 3 530.00(3 161.50, 3 927.50) | H=3.27 | 0.195 |
| ECMO流量(L/min)a | 2.80±0.52 | 2.68±0.62 | 2.72±0.54 | 2.95±0.40 | F=2.04 | 0.137 |
| 液体平衡量(ml/kg)c | 16.18(4.28, 32.49) | 21.29(12.04, 34.68) | 15.82(4.36, 31.40) | 9.88(0.54, 27.33) | H=4.76 | 0.092 |
| IABPb | 23 (25.27) | 6 (20.00) | 9 (29.03) | 8 (26.67) | χ2=0.70 | 0.703 |
| CRRTb | 22 (24.18) | 8 (26.67) | 8 (25.81) | 6 (20.00) | χ2=0.43 | 0.806 |
| CAb | 34 (37.36) | 9 (30.00) | 10 (32.26) | 15 (50.00) | χ2=3.09 | 0.214 |
| 病因b | χ2=6.94 | 0.031 | ||||
| 心肌梗死相关 | 37 (40.66) | 7 (23.33) | 13 (41.94) | 17 (56.67) | ||
| 非心肌梗死相关 | 54 (59.34) | 23 (76.67) | 18 (58.06) | 13 (43.33) | ||
| 高血压b | 36 (39.56) | 9 (30.00) | 15 (48.39) | 12 (40.00) | χ2=2.16 | 0.340 |
| 糖尿病b | 34 (37.36) | 8 (26.67) | 14 (45.16) | 12 (40.00) | χ2=2.36 | 0.307 |
| 初始乳酸值(mmol/L)c | 7.50 (4.15, 12.95) | 7.45 (2.60, 11.00) | 6.30 (3.25, 12.75) | 10.75 (6.20, 13.78) | H=5.95 | 0.051 |
| 白细胞(×109/L)c | 12.90 (9.15, 18.95) | 12.07 (7.90, 15.93) | 12.40 (9.06, 21.98) | 16.25 (10.87, 19.84) | H=2.74 | 0.254 |
| 血小板(×109/L)c | 150.00 (96.50, 214.50) | 130.00 (63.75, 188.50) | 156.00 (116.50, 217.50) | 158.50 (112.25, 214.75) | H=3.21 | 0.201 |
| 白蛋白(g/L) a | 30.48 ± 5.31 | 30.00 ± 5.88 | 30.48 ± 5.08 | 30.96 ± 5.08 | F=0.24 | 0.786 |
| 总胆红素(μmol/L)c | 17.20 (9.91, 26.38) | 17.56 (9.88, 26.45) | 17.20 (9.45, 22.23) | 17.35 (11.35, 31.01) | H=1.03 | 0.598 |
| 肌酐(μmol/L)c | 142.00 (101.50, 203.50) | 179.50 (109.50, 235.75) | 142.00 (105.00, 166.50) | 121.50 (90.25, 183.75) | H=3.87 | 0.144 |
| C反应蛋白(mg/L)c | 30.92 (10.19, 89.50) | 34.99 (15.54, 137.84) | 32.99 (20.12, 89.50) | 27.88 (6.57, 48.52) | H=4.29 | 0.117 |
| 肌钙蛋白(μg/L)c | 19.77 (2.75, 72.66) | 16.22 (1.15, 68.37) | 19.77 (2.75, 56.80) | 30.58 (5.82, 94.22) | H=1.08 | 0.582 |
| 撤机失败b | 36 (39.56) | 20 (66.67) | 10 (32.26) | 6 (20.00) | χ2=14.71 | < 0.001 |
| 28 d全因死亡b | 44 (48.35) | 21 (70.00) | 13 (41.94) | 10 (30.33) | χ2=8.85 | 0.012 |
| 注:a为x±s,b为(例, %),c为M(Q1, Q3);BMI为身体质量指数,ECMO为体外膜氧合,APACHE Ⅱ为急性生理和慢性健康状况评分,IABP为主动脉内球囊反搏,CRRT为连续性肾脏替代治疗,CA为心脏骤停 | ||||||
单因素Logistic回归分析显示,APACHE Ⅱ评分(P=0.001)、IABP使用(P=0.018)、液体平衡量(P=0.019)、肌钙蛋白Ⅰ(P=0.039)及肌酐水平(P=0.010)与撤机失败显著相关。在未校正的模型1中,12 h LCR每增加10%,撤机失败OR降低至0.86(P=0.006)。与低LCR组相比,中LCR组和高LCR组撤机失败风险分别降低76%(OR=0.24,P=0.009)和87%(OR=0.13,P < 0.001)。在模型2(校正年龄、初始乳酸值、肌钙蛋白Ⅰ)、模型3(校正APACHE Ⅱ、IABP、液体平衡量)与模型4(校正肌酐、CRRT、总胆红素)中,该结果依然稳健(所有P < 0.05)。见表 2。
| 变量 | 模型1 | 模型2 | 模型3 | 模型4 | |||||||
| OR (95%CI) | P值 | OR (95%CI) | P值 | OR (95%CI) | P值 | OR (95%CI) | P值 | ||||
| 12 h LCR(每10%) | 0.86(0.77~0.96) | 0.006 | 0.82(0.72~0.93) | 0.002 | 0.83(0.73~0.94) | 0.005 | 0.86(0.77~0.97) | 0.010 | |||
| 低LCR组 | 1.00 (参考) | 1.00 (参考) | 1.00 (参考) | 1.00(参考) | |||||||
| 中LCR组 | 0.24 (0.08~0.69) | 0.009 | 0.21(0.07~0.68) | 0.009 | 0.13(0.03~0.51) | 0.003 | 0.27(0.09~0.82) | 0.021 | |||
| 高LCR组 | 0.13 (0.04~0.40) | < 0.001 | 0.04(0.01~0.21) | < 0.001 | 0.06(0.01~0.28) | < 0.001 | 0.13(0.04~0.45) | 0.001 | |||
| P趋势 | < 0.001 | < 0.001 | < 0.001 | < 0.001 | |||||||
| 注:OR为比值比;CI为置信区间;LCR为乳酸清除率;模型1: 未校正;模型2: 校正: 年龄、初始乳酸值、肌钙蛋白Ⅰ;模型3: 校正: APACHE Ⅱ评分、IABP、液体平衡量;模型4:校正:肌酐、CRRT、总胆红素 | |||||||||||
针对CS病因(是否为心梗相关)的敏感性分析显示,在校正病因后,12 h LCR每增加10%,撤机失败OR降低至0.83 (95%CI: 0.74~0.94, P= 0.004);与低LCR组相比,中、高LCR组撤机失败风险分别降低82%(OR=0.18,95%CI: 0.06~0.58,P=0.004)和92%(OR=0.08,95%CI: 0.02~0.30,P < 0.001),结果稳健。
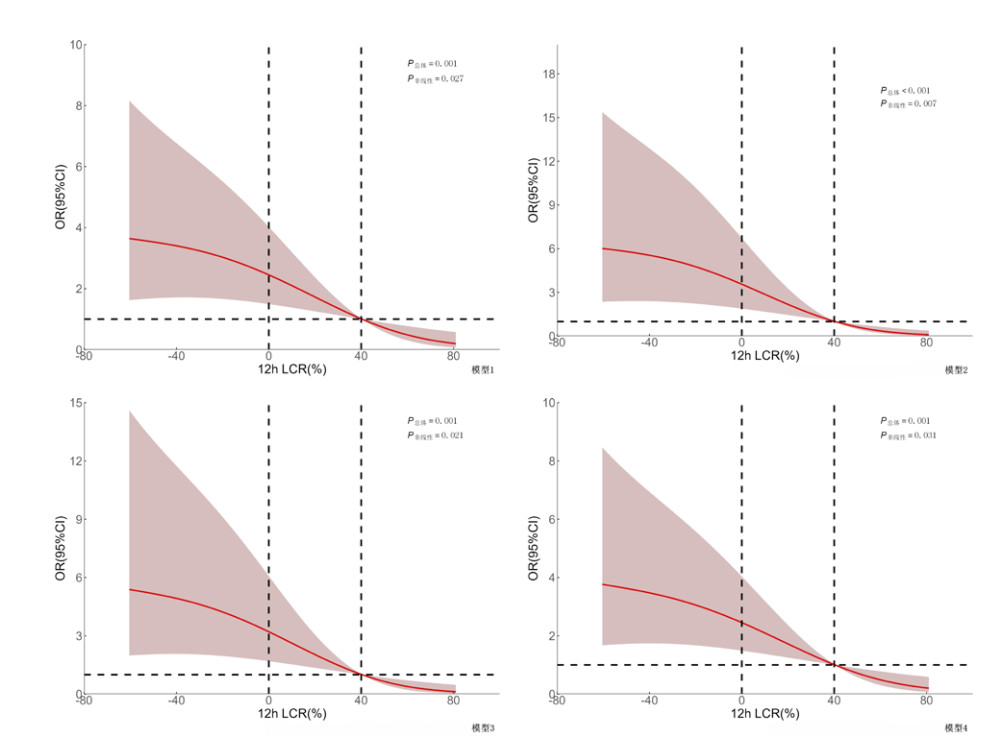
2.2.3 趋势性与非线性关联检验趋势性分析显示,在各模型中,撤机失败风险随LCR分级的升高均呈显著下降趋势(P趋势 < 0.001)(见表 2)。RCS分析显示,在各模型中,12 h LCR与VA-ECMO撤机失败风险均呈显著非线性负相关(P非线性均 < 0.05),随LCR增加,撤机失败风险呈先慢、后快、再趋缓的下降趋势。当LCR < 0%时,风险下降缓慢,当LCR处于0%~40%区间时,风险快速下降,当LCR > 40%时,风险下降再次趋缓。见图 1。
|
| 注:OR为比值比,CI为置信区间,LCR为乳酸清除率;垂直虚线对应12 h LCR分别为0%和40%,参考值选择依据曲线形态与临床意义;模型1: 未校正;模型2: 校正: 年龄、初始乳酸值、肌钙蛋白Ⅰ;模型3: 校正: APACHE Ⅱ评分、IABP、液体平衡量;模型4:校正:肌酐、CRRT、总胆红素 图 1 12 h LCR与CS患者VA-ECMO撤机失败风险的RCS曲线 Fig 1 RCS for 12-h LCR and VA-ECMO weaning failure risk in CS patients |
|
|
亚组分析显示,VA-ECMO上机病因(是否心梗相关)与12 h LCR对撤机失败不存在显著交互作用。然而,初始乳酸值(以4 mmol/L为界)、上机前是否发生CA与12 h LCR存在显著交互作用(P交互均 < 0.05)。见表 3。
| 变量 | 例数(%) | OR (95%CI) | P值 | P交互 |
| 总体(每10%) | 91 (100.00) | 0.86 (0.77~0.96) | 0.006 | |
| 上机病因 | 0.194 | |||
| 心肌梗死相关 | 37 (40.66) | 0.71 (0.52~0.96) | 0.029 | |
| 非心肌梗死相关 | 54 (59.34) | 0.87 (0.77~0.99) | 0.034 | |
| CA | < 0.001 | |||
| 否 | 57 (62.64) | 0.94 (0.85~1.02) | 0.145 | |
| 是 | 34 (37.36) | 0.35 (0.16~0.75) | 0.007 | |
| 初始乳酸值 | 0.028 | |||
| <4 mmol/L | 22 (24.18) | 0.93 (0.81~1.07) | 0.328 | |
| ≥4 mmol/L | 69 (75.82) | 0.73 (0.61~0.87) | < 0.001 | |
| 注:OR为比值比,CI为置信区间,CA为心脏骤停 | ||||
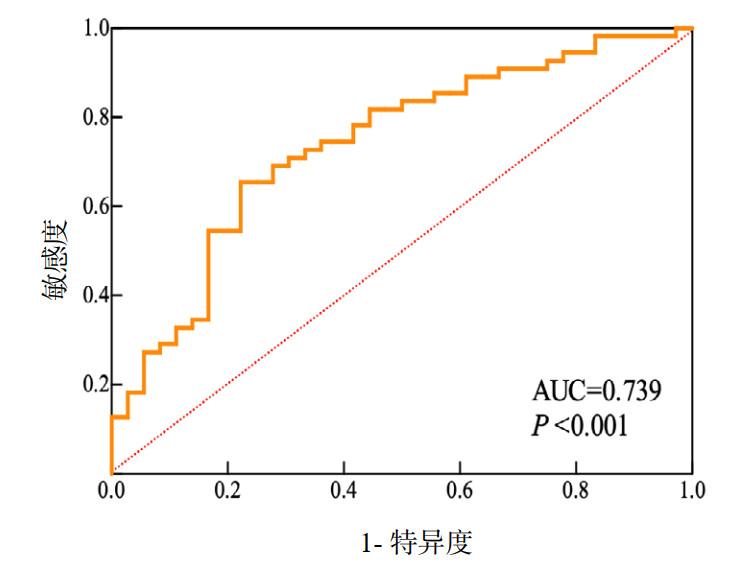
ROC曲线显示12 hLCR预测VA-ECMO撤机成功的曲线下面积(area under the curve,AUC)为0.739,截断值为42.71%,此时预测撤机成功的敏感度为65.5%,特异度为77.8%,阳性预测值为81.8%,阴性预测值为59.6%。见图 2。
|
| 注:AUC为曲线下面积 图 2 12 h LCR预测CS患者VA-ECMO撤机成功的ROC曲线 Fig 2 ROC curve for 12 h LCR in predicting VA-ECMO weaning success in CS patients |
|
|
尽管治疗手段不断进步,CS仍是具有高死亡率的临床难题。VA-ECMO作为救治重症CS患者的终极手段,其高昂的医疗成本与较高的撤机失败率构成了当前临床实践中的主要挑战。LCR已广泛应用于脓毒症和脓毒性休克的预后评估和治疗指导[17],但其与CS患者VA-ECMO撤机结局的关联尚不明确。本研究旨在深入探讨12 h LCR与CS患者VA-ECMO撤机结局的关系,以期为风险分层和临床干预提供依据。
本研究观察到CS患者VA-ECMO撤机失败率为39.56%,28 d全因死亡率为48.35%,与既往大样本研究结果相近[1, 7]。血乳酸被认为是评估危重症患者病情和预后的良好指标[18],并被最新指南纳入作为CS患者启动机械循环支持的决策参考之一[13]。然而,关于初始乳酸水平与ECMO撤机结局的相关性,现有研究结论尚不一致[6, 19]。本研究结果显示,初始乳酸水平与VA-ECMO撤机失败无显著相关性,与部分研究报道一致[6, 20]。这种不一致性可能与VA-ECMO上机时机、患者基础状态及CS病因存在差异有关。对于接受VA-ECMO的患者,上机后乳酸水平的动态变化可能比单一的初始值更具预后价值[21]。Dettling等[7]研究表明,24 h乳酸清除是撤机失败的独立保护因素(OR=0.21,P < 0.001),但未深入探讨两者间的具体关系。另有研究显示[22],不同生存结局患者的LCR在ECMO支持后12 h即出现显著差异。基于此,本研究将预测窗口提前至ECMO支持后的12 h这一更早节点。结果显示,12 h LCR同样与撤机失败显著相关。具体而言,12 h LCR每增加10%,CS患者撤机失败风险降低14%,中、高LCR组的撤机失败风险较低LCR组分别显著降低76%和87%。在校正相关混杂因素后,该结果仍稳健。这提示12 h LCR或可作为CS患者更早期的预后评估工具。
本研究首次通过RCS分析发现,12 h LCR与撤机失败风险呈显著非线性负相关,风险随LCR升高呈“先慢、后快、再趋缓”的下降趋势。这为临床早期风险分层评估提供了直观依据:当12 h LCR处于低位(尤其为负值)时,属高危状态,撤机失败风险高且下降缓慢;当LCR升至一定水平,风险快速下降;而当LCR达较高水平后,患者状态趋于稳定,风险已较低,随LCR升高风险下降再次趋缓,此时LCR升高的临床获益幅度较快速下降阶段有所减小。值得注意的是,仍需大样本研究验证该非线性关系并进一步明确具体阈值。亚组分析显示,12 h LCR与VA-ECMO撤机结局的相关性可能在不同人群中存在差异。本研究发现,在初始乳酸水平≥4 mmol/L或上机前发生CA的患者中,12 h LCR与撤机结局的关联性似乎更强。这与Park等[11]的发现相呼应,该研究显示LCR在基础乳酸水平较高(> 5 mmol/L)的CS患者中对住院死亡率更具预测价值。然而,本研究亚组样本量较小,可能存在样本分布不均衡,该结果应被视为探索性发现,需大样本研究加以验证。此外,在不同原发病因(是否为心梗相关)的亚组中,12 h LCR与撤机结局的相关性保持稳定。本研究ROC曲线分析显示12 h LCR对撤机成功具有中等预测能力,与在术后低心排人群中得到的结果相近[6]。
CS所致的高乳酸血症主要源于心输出量下降导致的组织灌注不足和微循环功能障碍。此外,应激状态下儿茶酚胺和其他炎性介质释放导致的丙酮酸生成增加,以及伴随出现的肝肾功能损伤所致的乳酸清除能力下降,亦是重要因素[10, 23]。相较于单次乳酸水平,LCR更能反映机体组织灌注改善和无氧代谢的纠正程度[18, 24]。CS可导致全身大循环和微循环严重障碍[25],尽管VA-ECMO能够快速改善大循环血流动力学,但可能无法同步改善微循环[26]。研究显示,难治性CS患者的大部分微循环参数在VA-ECMO支持后12 h有改善[27]。本研究观察到的12 h LCR与撤机结局的非线性关系,可能反映了不同CS患者VA-ECMO支持下微循环与代谢的恢复差异:LCR为低或负清除率时,提示尽管大循环已获得机械支持,但微循环和线粒体功能障碍可能依然存在[28],治疗反应不佳;而当LCR超过一定阈值,组织灌注和代谢得到有效恢复与纠正,细胞氧利用提升,乳酸水平下降,机体从“难治性休克”向“可逆状态”过渡,治疗反应良好;当LCR处于高位区间时,患者生理状态趋于稳定,撤机成功率高。LCR对CS患者预后影响的具体机制,仍需高质量研究深入探索。
本研究的局限性:(1)本研究为单中心、回顾性研究,存在一定选择和混杂偏倚,受样本量限制,未能校正所有潜在的混杂因素(如其他影响乳酸代谢的基础疾病、血管活性药物剂量等时间动态协变量),对非线性关系、亚组分析仅做探讨,需更大样本、前瞻性研究加以验证;(2) LCR计算可能受治疗干预影响;(3)撤机失败定义(撤机后48 h内死亡)可能受撤机后管理影响。
12 h LCR可能与CS患者VA-ECMO撤机失败风险显著负相关,且存在非线性关系,或可作为早期预警工具评估VA-ECMO撤机结局,且在高初始乳酸或心脏骤停亚组中价值可能更大,但仍需更多大样本、前瞻性的研究加以验证。
利益冲突 所有作者声明无利益冲突
作者贡献声明 张闪:研究设计与实施、数据收集与统计分析、论文撰写;董进中:数据统计分析、作图;范震:病例筛选与质控;乐健伟:研究指导、论文审阅;陈国栋:研究指导;李丹辉:论文审阅、论文修改
| [1] | Lang CN, Kaier K, Zotzmann V, et al. Cardiogenic shock: incidence, survival and mechanical circulatory support usage 2007-2017-insights from a national registry[J]. Clin Res Cardiol, 2021, 110(9): 1421-1430. DOI:10.1007/s00392-020-01781-z |
| [2] | Lüsebrink E, Binzenhöfer L, Adamo M, et al. Cardiogenic shock[J]. Lancet, 2024, 404(10466): 2006-2020. DOI:10.1016/S0140-6736(24)01818-X |
| [3] | Zeymer U, Westermann D. Veno-arterial extracorporeal membrane oxygenation[J]. Curr Opin Crit Care, 2025, 31(4): 473-479. DOI:10.1097/MCC.0000000000001295 |
| [4] | Ostadal P, Rokyta R, Karasek J, et al. Extracorporeal membrane oxygenation in the therapy of cardiogenic shock: results of the ECMO-CS randomized clinical trial[J]. Circulation, 2023, 147(6): 454-464. DOI:10.1161/CIRCULATIONAHA.122.062949 |
| [5] | Ellouze O, Soudry Faure A, Radhouani M, et al. Levosimendan in venoarterial ECMO weaning. Rational and design of a randomized double blind multicentre tria[J]. ESC Heart Fail, 2021, 8(4): 3339-3347. DOI:10.1002/ehf2.13427 |
| [6] | Charbonneau F, Chahinian K, Bebawi E, et al. Parameters associated with successful weaning of veno-arterial extracorporeal membrane oxygenation: a systematic review[J]. Crit Care, 2022, 26(1): 375. DOI:10.1186/s13054-022-04249-w |
| [7] | Dettling A, Kellner C, Sundermeyer J, et al. Incidence and predictors of weaning failure from veno-arterial extracorporeal membrane oxygenation therapy in patients with cardiogenic shock[J]. Eur J Heart Fail, 2025, 27(5): 832-841. DOI:10.1002/ejhf.3583 |
| [8] | Gharipour A, Razavi R, Gharipour M, et al. The incidence and outcome of severe hyperlactatemia in critically ill patients[J]. Intern Emerg Med, 2021, 16(1): 115-123. DOI:10.1007/s11739-020-02337-9 |
| [9] | Thevathasan T, Gregers E, Rasalingam Mørk S, et al. Lactate and lactate clearance as predictors of one-year survival in extracorporeal cardiopulmonary resuscitation - An international, multicentre cohort study[J]. Resuscitation, 2024, 198: 110149. DOI:10.1016/j.resuscitation.2024.110149 |
| [10] | Yuzefpolskaya M, Schwartz S, Ladanyi A, et al. The role of lactate metabolism in heart failure and cardiogenic shock: clinical insights and therapeutic implications[J]. J Card Fail, 2026, 32(1): 115-125. DOI:10.1016/j.cardfail.2025.01.011 |
| [11] | Park IH, Yang JH, Jang WJ, et al. Clinical significance of lactate clearance in patients with cardiogenic shock: results from the RESCUE registry[J]. J Intensive Care, 2021, 9(1): 63. DOI:10.1186/s40560-021-00571-7 |
| [12] | Zhang QF, Zhang SL, Li G, et al. Prognostic value of lactate clearance, fluid balance, and APACHE Ⅱ score in patients with cardiogenic shock receiving extracorporeal membrane oxygenation[J]. Front Cardiovasc Med, 2025, 12: 1557909. DOI:10.3389/fcvm.2025.1557909 |
| [13] | Sinha SS, Morrow DA, Kapur NK, et al. 2025 concise clinical guidance: an ACC expert consensus statement on the evaluation and management of cardiogenic shock: a report of the American college of cardiology solution set oversight committee[J]. J Am Coll Cardiol, 2025, 85(16): 1618-1641. DOI:10.1016/j.jacc.2025.02.018 |
| [14] | Naidu SS, Baran DA, Jentzer JC, et al. SCAI SHOCK Stage Classification Expert Consensus Update: a Review and Incorporation of Validation Studies: This statement was endorsed by the American College of Cardiology (ACC), American College of Emergency Physicians (ACEP), American Heart Association (AHA), European Society of Cardiology (ESC) Association for Acute Cardiovascular Care (ACVC), International Society for Heart and Lung Transplantation (ISHLT), Society of Critical Care Medicine (SCCM), and Society of Thoracic Surgeons (STS) in December 2021[J]. J Am Coll Cardiol, 2022, 79(9): 933-946. DOI:10.1016/j.jacc.2022.01.018 |
| [15] | 中国医师协会体外生命支持专业委员会. 成人体外膜氧合循环辅助专家共识[J]. 中华医学杂志, 2018, 98(12): 886-894. DOI:10.3760/cma.j.issn.0376-2491.2018.12.003 |
| [16] | 中华人民共和国国家卫生健康委员会. 成人体外膜肺氧合技术操作规范(2024年版)[S/OL]. (2024-11-26)[2025-11-24]. https://www.nhc.gov.cn/wjw/c100376/202411/f978f85e6c724b3fae3d50336abbf332/files/1732873199940_40343.pdf. |
| [17] | Evans L, Rhodes A, Alhazzani W, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021[J]. Crit Care Med, 2021, 49(11): e1063-e1143. DOI:10.1097/CCM.0000000000005337 |
| [18] | 中国医疗保健国际交流促进会急诊医学分会, 北京医院国家老年医学中心, 中华医学会急诊医学分会, 等. 血乳酸在急危重症应用的急诊专家共识[J]. 临床急诊杂志, 2025, 26(10): 553-563. DOI:10.13201/j.issn.1009-5918.2025.10.002 |
| [19] | Hsu HR, Sekhar P, Grover J, et al. Predictors of successful weaning from veno-arterial extracorporeal membrane oxygenation (V-a ECMO): a systematic review and meta-analysis[J]. PLoS One, 2025, 20(3): e0310289. DOI:10.1371/journal.pone.0310289 |
| [20] | Sawada K, Kawakami S, Murata S, et al. Predicting parameters for successful weaning from veno-arterial extracorporeal membrane oxygenation in cardiogenic shock[J]. ESC Heart Fail, 2021, 8(1): 471-480. DOI:10.1002/ehf2.13097 |
| [21] | Scolari FL, Schneider D, Fogazzi DV, et al. Association between serum lactate levels and mortality in patients with cardiogenic shock receiving mechanical circulatory support: a multicenter retrospective cohort study[J]. BMC Cardiovasc Disord, 2020, 20(1): 496. DOI:10.1186/s12872-020-01785-7 |
| [22] | Slottosch I, Liakopoulos O, Kuhn E, et al. Lactate and lactate clearance as valuable tool to evaluate ECMO therapy in cardiogenic shock[J]. J Crit Care, 2017, 42: 35-41. DOI:10.1016/j.jcrc.2017.06.022 |
| [23] | Müller J, Radej J, Horak J, et al. Lactate: the fallacy of oversimplification[J]. Biomedicines, 2023, 11(12): 3192. DOI:10.3390/biomedicines11123192 |
| [24] | Wang JF, Ji MX. The 6-hour lactate clearance rate in predicting 30-day mortality in cardiogenic shock[J]. J Intensive Med, 2024, 4(3): 393-399. DOI:10.1016/j.jointm.2024.01.003 |
| [25] | Merdji H, Levy B, Jung C, et al. Microcirculatory dysfunction in cardiogenic shock[J]. Ann Intensive Care, 2023, 13(1): 38. DOI:10.1186/s13613-023-01130-z |
| [26] | Govender K, Jani VP, Cabrales P. The disconnect between extracorporeal circulation and the microcirculation: a review[J]. ASAIO J, 2022, 68(7): 881-889. DOI:10.1097/MAT.0000000000001618 |
| [27] | Chommeloux J, Montero S, Franchineau G, et al. Microcirculation evolution in patients on venoarterial extracorporeal membrane oxygenation for refractory cardiogenic shock[J]. Crit Care Med, 2020, 48(1): e9-e17. DOI:10.1097/CCM.0000000000004072 |
| [28] | Pahuja M, Yerasi C, Lam PH, et al. Review of pathophysiology of cardiogenic shock and escalation of mechanical circulatory support devices[J]. Curr Cardiol Rep, 2023, 25(4): 213-227. DOI:10.1007/s11886-023-01843-4 |
 2026, Vol. 35
2026, Vol. 35