肺栓塞(pulmonary embolism, PE)作为心肺血管系统的急危重症,发病率呈逐年增高趋势,近十年来,住院率增加了6倍,其并发症的管理成为临床研究的重点[1-2]。急性肾损伤(acute kidney injury, AKI)作为PE患者常见且预后不良的并发症,发生率在住院患者中可达15%~20%,且肾损伤的严重程度与PE的严重程度和死亡率呈正相关,并显著增加医疗负担[3-4]。研究数据显示,PE患者中并发AKI与不并发AKI的早期全因死亡率分别为15%(95%CI: 9%~22%)和5%(95%CI: 3%~8%)(RR 1.76, 95%CI: 1.61~1.92)[5-6]。早期识别高危人群并实施有效干预,对于改善PE患者的预后具有重要意义。然而,目前临床对PE并发AKI的危险因素及预测模型研究存在局限性,现有研究多基于传统危险因素(如年龄、肌酐水平)构建预测模型,缺乏对并发症(如心力衰竭、脑卒中)与PE协同作用的系统分析[7-8]。本研究基于首都医科大学附属北京安贞医院的临床数据,分析PE患者并发AKI的临床特征及危险因素,构建PE患者并发AKI的预测模型,为早期制定干预策略提供参考。
1 资料与方法 1.1 研究对象本研究为病例对照研究,选取2020年1月至2024年12月在首都医科大学附属北京安贞医院住院治疗的119例PE并发AKI患者为病例组,以同院同期诊断为单纯PE的737例住院患者为对照组。纳入标准为:①年龄≥18岁;②PE符合《肺栓塞(2019版)》中的诊断标准[9];③依据国际公认的肾脏病指南(kidney disease: improving global outcomes, KDIGO),符合AKI的诊断标准[10],AKI定义为急性肾损伤,诊断标准:血清肌酐在48 h内升高≥26.52 µmol/L或7 d内肌酐升至基线值的≥1.5倍或尿量 < 0.5 mL·kg-1·h-1持续6 h以上。排除标准为:①临床资料不完整;②妊娠;③并发严重感染性疾病及免疫功能极度低下。本研究通过首都医科大学附属北京安贞医院伦理委员会审核(审批号:2024-05)。
1.2 研究方法对所有患者进行详细的病史采集,并利用患者出院的病案首页、入院的电子病历、病程记录单收集临床资料(诊断符合相关指南标准):①一般资料:姓名、性别、体重指数(body mass index, BMI)、吸烟史、饮酒史、既往疾病史(高血压[11]、糖尿病[12]、高脂血症[13]、冠心病[14]、心力衰竭[15]、脑卒中[16]);②入院24 h内首次血常规实验室指标:白细胞、血红蛋白、中性粒细胞数、淋巴细胞数、单核细胞数、嗜酸细胞数、嗜碱细胞数、血糖、糖化血红蛋白、胱抑素C、血清白蛋白、活化部分凝血活酶时间(activated partial thromboplastin time, APTT)、凝血酶原时间(prothrombin Time, PT)。
1.3 统计学方法选用SPSS 25.0软件进行数据统计分析。计量资料经Shapiro-Wilk正态性检验,符合正态分布的计量资料以均数±标准差(x±s)表示,组间比较采用两独立样本t检验;非正态分布的计量资料以中位数和四分位数[M(Q1, Q3)]表示,组间比较用Mann-Whitney U检验。计数资料以频数(率)[n(%)]表示,组间比较采用χ2检验。多因素比较采用Logistic回归分析,基于Logistic回归分析结果构建风险预测模型。通过受试者工作特征曲线(receiver operating characteristic, ROC)下面积(area under the curve, AUC)以评价模型的预测性能。P < 0.05为差异有统计学意义。
2 结果 2.1 两组患者基本临床特征研究共收集了2020年1月1日至2024年12月31日期间的737例单纯PE的患者及119例PE并发AKI的患者。男性PE患者AKI发生率为54.62%,女性PE患者为45.38%,差异无统计学意义(P > 0.05)。与对照组患者比较,病例组患者年龄较大,且既往并发高血压、糖尿病、高脂血症、心力衰竭、脑卒中病史比例以及入院时中性粒细胞数更高,而血红蛋白、淋巴细胞数更低(均P < 0.05)。与对照组患者比较,病例组患者BMI、既往并发冠心病病史、吸烟史、饮酒史及白细胞、单核细胞数、嗜酸细胞数、嗜碱细胞数差异无统计学意义(P > 0.05),见表 1。
2.2 PE患者并发AKI危险因素的多因素Logistic分析以PE患者是否并发AKI作为因变量,以单因素内差异有统计学意义的条目作为自变量。以上述单因素分析筛选得到的差异变量纳入Logistic模型进行多因素分析,结果显示,既往并发高血压、糖尿病、心力衰竭病史及入院时血红蛋白水平低是PE患者并发AKI的危险因素(均P < 0.05)。见表 2。
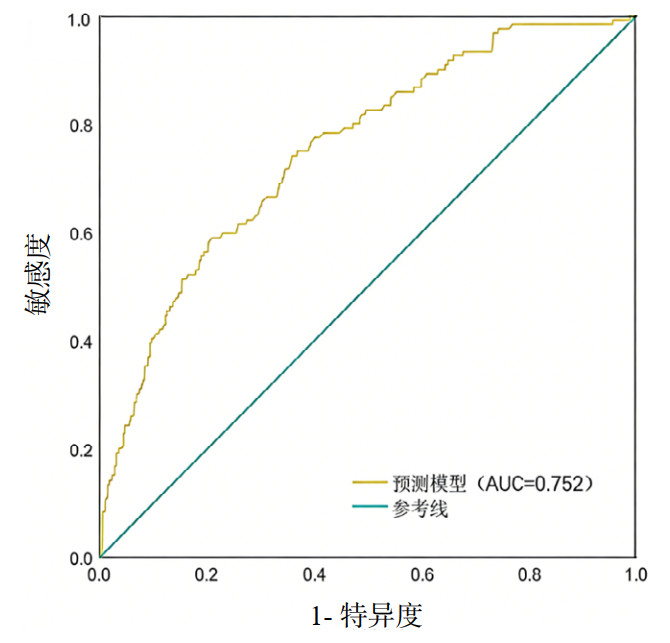
2.3 PE患者并发AKI风险预测模型的构建及预测价值根据多因素Logistic分析结果,利用筛选出的四个变量建立PE患者并发AKI风险预测模型,并对该模型进行验证,通过绘制ROC曲线进行分析,结果显示,既往并发高血压、糖尿病、心力衰竭、入院时血红蛋白减低预测PE患者并发AKI风险的AUC分别为0.623、0.581、0.611、0.378,预测模型AUC为0.752(95%CI: 0.714~0.805),敏感度为67.2%,特异度为73.0%,提示已构建的模型具有较好的预测效能。见图 1。
3 讨论PE与AKI是临床中两类具有紧密联系的疾病,二者在发病机制、病理生理演变及临床管理中展现出复杂的双向关联[17]。首先,PE会导致肺部气体交换障碍,引发低氧血症,长期或严重的低氧血症可导致全身组织缺氧,从而引发AKI[18];大面积PE可以导致右心室压力增加,进而影响心脏的整体泵血功能,减少肾血流灌注,导致AKI[19];PE引起的循环系统不稳定可以激活肾素-血管紧张素-醛固酮系统(renin-angiotensin-aldosterone system, RAAS),导致血管收缩、血压升高,可导致肾功能恶化[20]。其次,AKI患者往往伴有多种心肺血管风险因素,如高血压、糖尿病等,这些因素都会增加PE的发生风险[21];AKI患者体内尿毒素易蓄积,加剧血管内皮功能障碍,促进血栓形成,间接增加了PE的风险[22]。因此,在处理这两种疾病时,需要全面考虑患者的全身状况,进行个体化治疗。本研究基于首都医科大学附属北京安贞医院临床数据,通过多因素分析与逻辑回归模型构建,揭示了既往并发高血压、糖尿病、心力衰竭病史及入院时血红蛋白减低是PE患者并发AKI的独立危险因素,为临床实践中早期识别和干预高危患者提供了科学依据。
3.1 心力衰竭与PE-AKI的关系从危险因素来看,心力衰竭是PE并发AKI的独立危险因素。三者之间存在着复杂的相互关系,它们不仅各自独立影响患者的健康状况,而且彼此之间也能通过多种机制产生交互影响。首先,心力衰竭患者心脏泵血功能下降,导致血液循环效率降低,血液流动缓慢,容易在静脉系统中形成血栓,并导致肾脏的有效灌注压降低,导致肾血流量减少,进而促进AKI的发生、发展[23];其次,PE会导致右心室压力和后负荷增加,进一步加重心脏负担,可能导致心衰发生[24];最后,PE患者并发心力衰竭时,右心功能不全可能进一步加重体循环淤血,导致肾脏静脉高压和肾间质水肿,形成“心肾综合征”的恶性循环[25]。因此,PE患者应当进行血流动力学优化,加强容量管理,降低心脏负荷,通过无创心输出量监测指导容量管理,必要时及早启动连续性肾脏替代等治疗手段。
3.2 高血压与糖尿病的损伤效应本研究同样证实了:高血压与糖尿病是PE患者并发AKI的独立危险因素。首先,长期高血压导致肾小球高滤过和肾小管间质纤维化,而PE引发的肺动脉高压通过反射性体循环血管收缩,进一步减少肾血流量,形成“肾灌注不足—RAAS激活—肾小管损伤”的恶性循环[26]。其次,糖尿病通过糖基化终末产物沉积损伤肾小球基底膜,并通过氧化应激加剧内皮功能障碍。在PE患者中,高血糖与炎症因子的协同作用可能加速肾小管上皮细胞凋亡,导致AKI发生[27]。最后,高血压和糖尿病作为心血管疾病的共病,常伴随全身血管内皮功能障碍和慢性炎症状态,其全身血管调节功能受损,进一步加剧肾脏缺血-再灌注损伤[28]。对于PE患者需要监测血压、血糖,控制在靶目标范围内,对于糖尿病患者可考虑应用钠-葡萄糖协同转运蛋白2(sodium-glucose cotransporter 2, SGLT2)抑制剂(如达格列净)抑制肾小管葡萄糖重吸收,减轻氧化应激损伤。
3.3 入院时血红蛋白水平本研究通过多因素Logistic回归分析,明确了入院时血红蛋白减低是PE患者并发AKI的独立危险因素。血红蛋白是体内运送氧气的重要蛋白,其水平较低可能会导致组织器官的氧气输送量减少,并可能通过以下机制参与AKI的发生:①贫血导致全身组织低氧,激活缺氧诱导因子,促进促炎因子释放,加剧肾小管损伤[29];②缺铁性贫血可能通过铁调素升高引发线粒体功能障碍,导致肾细胞能量代谢异常[30];③贫血患者血液携氧能力下降,迫使肾脏代偿性增加红细胞生成素分泌,加剧肾小管缺氧损伤[31]。对于贫血患者,可考虑及早启动静脉铁剂联合促红细胞生成素治疗,必要时进行血制品输注。
综上所述,既往并发高血压、糖尿病、心力衰竭病史及入院时血红蛋白减低是PE患者并发AKI的独立危险因素,基于以上四项指标构建的预测模型,对早期识别PE患者并发AKI的效能较好,能指导个体化预防措施的制定。模型中涉及的变量获取便利,尤其适用于急诊快速风险评估,其“快速、低成本”的特点契合中国基层医疗需求,为临床早期预警与精准干预提供了科学依据。
本研究局限性:①回顾性设计可能存在选择偏倚;②未纳入动态生物标志物(如连续肾功能监测)及影像学指标(如超声心动图右心功能参数)以优化模型;③缺乏多中心外部验证。未来要实现对PE并发AKI的精准预测和有效防控,还需要多学科协作,进行更加深入的基础研究和临床试验,不断优化和完善现有模型。
| 指标 | PE并发AKI (n=119) | 单纯PE (n=737) | Z/t/χ2/值 | P值 |
| 性别(n, %) | 1.811 | 0.178 | ||
| 男性 | 65(54.62) | 350(47.49) | ||
| 女性 | 54(45.38) | 387(52.51) | ||
| 年龄(x±s, 岁) | 68.55±13.22 | 63.79±14.43 | 3.372 | 0.001 |
| BMI(x±s) | 24.82±4.16 | 24.63±4.12 | 0.444 | 0.657 |
| 既往史(n, %) | ||||
| 吸烟史 | 67 (56.30) | 374 (50.75) | 1.054 | 0.305 |
| 饮酒史 | 54 (45.38) | 337 (45.73) | 0.001 | 0.978 |
| 高血压 | 87 (73.11) | 358 (48.58) | 23.734 | < 0.001 |
| 糖尿病 | 39 (32.77) | 122 (16.55) | 16.604 | < 0.001 |
| 高脂血症 | 55 (46.22) | 267 (36.23) | 3.942 | 0.047 |
| 冠心病 | 45 (37.82) | 226 (30.66) | 2.102 | 0.147 |
| 心力衰竭 | 44 (36.97) | 109 (14.79) | 32.858 | < 0.001 |
| 脑卒中 | 29 (24.37) | 80 (10.85) | 15.647 | < 0.001 |
| 实验室指标 | ||||
| 白细胞(x±s, ×109/L) | 7.55±3.31 | 7.05±3.30 | 1.527 | 0.127 |
| 血红蛋白(x±s, g/L) | 119.31±24.97 | 128.74±21.05 | 3.901 | < 0.001 |
| 中性粒细胞数[M(Q1, Q3, ), ×109/L] | 4.75 (3.66, 6.57) | 4.25 (3.13, 5.61) | 2.426 | 0.015 |
| 淋巴细胞数[M(Q1, Q3, ), ×109/L] | 1.24 (0.92, 1.69) | 1.46 (1.09, 1.88) | 2.917 | 0.004 |
| 单核细胞数[M(Q1, Q3, ), ×109/L] | 0.41 (0.32, 0.52) | 0.39 (0.29, 0.51) | 1.512 | 0.131 |
| 嗜酸细胞数[M(Q1, Q3, ), ×109/L] | 0.11 (0.03, 0.21) | 0.09 (0.04, 0.16) | 1.226 | 0.220 |
| 嗜碱细胞数[M(Q1, Q3, ), ×109/L] | 0.02 (0.01, 0.03) | 0.02 (0.01, 0.03) | 0.061 | 0.952 |
| 糖化血红蛋白(x±s, %) | 5.34±2.21 | 4.93±2.07 | 2.786 | 0.057 |
| 胱抑素C(x±s, mg/L) | 1.01±0.65 | 0.77±0.58 | 1.659 | 0.221 |
| 血清白蛋白(x±s, g/L) | 37.42±8.73 | 40.24±12.69 | 2.028 | 0.107 |
| APTT(x±s, s) | 32.54±12.78 | 29.78±11.54 | 3.459 | 0.276 |
| PT(x±s, s) | 12.23±6.74 | 11.36±7.63 | 2.547 | 0.387 |
| 注:PE为肺栓塞,AKI为急性肾损伤,BMI为体重指数,APTT为活化部分凝血活酶时间,PT为凝血酶原时间 | ||||
| 指标 | B | S.E. | Wald | OR (95%CI) | P值 |
| 年龄 | 0.005 | 0.009 | 0.277 | 1.005 (0.987~1.022) | 0.598 |
| 高血压 | 0.954 | 0.251 | 14.476 | 2.596 (1.588~4.244) | < 0.001 |
| 糖尿病 | 0.565 | 0.249 | 5.159 | 1.760 (1.081~2.865) | 0.023 |
| 高脂血症 | 0.157 | 0.230 | 0.468 | 1.170 (0.746~1.837) | 0.494 |
| 心力衰竭 | 1.354 | 0.241 | 31.577 | 3.874 (2.416~6.213) | < 0.001 |
| 脑卒中 | 0.461 | 0.279 | 2.724 | 1.586 (0.917~2.741) | 0.099 |
| 血红蛋白 | -0.017 | 0.005 | 12.099 | 0.983 (0.974~0.993) | 0.001 |
| 中性粒细胞数 | 0.035 | 0.033 | 1.123 | 1.036 (0.971~1.105) | 0.289 |
| 淋巴细胞数 | -0.299 | 0.184 | 2.629 | 0.742 (0.517~1.064) | 0.105 |
| 注:PE为肺栓塞,AKI为急性肾损伤 | |||||
|
| 图 1 PE患者并发AKI风险预测模型的ROC曲线 Fig 1 ROC curve of combined AKI risk prediction model for PE patients |
|
|
利益冲突 所有作者声明无利益冲突
作者贡献声明 杨赓、冯龙:研究设计、数据收集与整理、统计分析、初稿撰写;杨赓、郭志霞、王睿、陈德成:研究构思与指导、方法学支持、结果解读、论文修改与审校;郭志霞、张泽华、王睿、陈德成:临床资料提供、病例纳入标准制定、数据质量控制;冯龙、张泽华、王睿、陈德成:实验室指标审核、文献检索与综述、图表制作;全体作者:审阅并最终批准稿件,对文章内容负责
| [1] | Zuin M, Bikdeli B, Ballard-Hernandez J, et al. International clinical practice guideline recommendations for acute pulmonary embolism: harmony, dissonance, and silence[J]. J Am Coll Cardiol, 2024, 84(16): 1561-1577. DOI:10.1016/j.jacc.2024.07.044 |
| [2] | Henkin S, Ujueta F, Sato A, et al. Acute pulmonary embolism: evidence, innovation, and horizons[J]. Curr Cardiol Rep, 2024, 26(11): 1249-1264. DOI:10.1007/s11886-024-02128-0 |
| [3] | Panahi L, Udeani G, Horseman M, et al. Review of medical therapies for the management of pulmonary embolism[J]. Medicina, 2021, 57(2): 110. DOI:10.3390/medicina57020110 |
| [4] | Xing XQ, Liu J, Deng YS, et al. Impact of renal function on the prognosis of acute pulmonary embolism patients: a systematic review and meta-analysis[J]. Expert Rev Respir Med, 2022, 16(1): 91-98. DOI:10.1080/17476348.2021.1862653 |
| [5] | Wang DY, Fan GH, Liu X, et al. Renal insufficiency and short-term outcomes of acute pulmonary embolism: a systemic review and meta-analysis[J]. Thromb Haemost, 2020, 120(7): 1025-1034. DOI:10.1055/s-0040-1712459 |
| [6] | Berghaus TM, Schwaiblmair M, von Scheidt W. Renal biomarkers and prognosis in acute pulmonary embolism[J]. Heart, 2012, 98(16): 1185-1186. DOI:10.1136/heartjnl-2012-302298 |
| [7] | Zhan Y, Fu XW, Bi WH, et al. Risk factors for venous thromboembolism in patients with chronic kidney disease: a systematic review and meta-analysis[J]. Ren Fail, 2024, 46(2): 2431149. DOI:10.1080/0886022X.2024.2431149 |
| [8] | Wang G, Xu JT, Lin XX, et al. Machine learning-based models for predicting mortality and acute kidney injury in critical pulmonary embolism[J]. BMC Cardiovasc Disord, 2023, 23(1): 385. DOI:10.1186/s12872-023-03363-z |
| [9] | Essien EO, Rali P, Mathai SC. Pulmonary embolism[J]. Med Clin North Am, 2019, 103(3): 549-564. DOI:10.1016/j.mcna.2018.12.013 |
| [10] | Authors N. KDIGO 2024 clinical practice guideline for the evaluation and management of chronic kidney disease[J]. Kidneys, 2024, 13(2): 140-171. DOI:10.22141/2307-1257.13.2.2024.456 |
| [11] | 中国高血压防治指南修订委员会, 高血压联盟(中国), 中国医疗保健国际交流促进会高血压分会, 等. 中国高血压防治指南(2024年修订版)[J]. 中华高血压杂志(中英文), 2024, 32(7): 603-700. DOI:10.16439/j.issn.1673-7245.2024.07.002 |
| [12] | 《中国老年型糖尿病防治临床指南》编写组. 中国老年2型糖尿病防治临床指南(2022年版)[J]. 中国糖尿病杂志, 2022, 30(1): 2-51. DOI:10.3760/cma.j.cn112138-20211027-00751 |
| [13] | Wierzbicki AS, Kim EJ, Esan O, et al. Hypertriglyceridaemia: an update[J]. J Clin Pathol, 2022, 75(12): 798-806. DOI:10.1136/jclinpath-2021-207719 |
| [14] | 胸痛中心专家委员会, 中华医学会心电生理和起搏分会, 中国医师协会心律学专业委员会, 等. 冠状动脉粥样硬化性心脏病猝死防治专家共识(2024)[J]. 中华心血管病杂志(网络版), 2024, 7(1): 1-18. DOI:10.3760/cma.j.cn116031.2024.1000177 |
| [15] | Heidenreich PA, Bozkurt B, Aguilar D, et al. 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines[J]. Circulation, 2022, 145(18): e895-e1032. DOI:10.1161/CIR.0000000000001063 |
| [16] | 中华人民共和国国家卫生健康委员会. 脑血管病防治指南(2024年版)[J]. 磁共振成像, 2025, 16(1): 1-8. DOI:10.12015/issn.1674-8034.2025.01.001 |
| [17] | Murgier M, Bertoletti L, Bikdeli B, et al. Prognostic impact of acute kidney injury in patients with acute pulmonary embolism data from the RIETE registry[J]. J Thromb Thrombolysis, 2022, 54(1): 58-66. DOI:10.1007/s11239-022-02633-5 |
| [18] | Gorgis S, Yang BY, Zhen-Yu Tong M, et al. Refractory hypoxemia in acute-on-chronic submassive pulmonary embolism[J]. Ann Am Thorac Soc, 2023, 20(11): 1654-1658. DOI:10.1513/AnnalsATS.202302-126CC |
| [19] | Teerapuncharoen K, Bag R. Chronic thromboembolic pulmonary hypertension[J]. Lung, 2022, 200(3): 283-299. DOI:10.1007/s00408-022-00539-w |
| [20] | Shah IK, Merfeld JM, Chun J, et al. Pathophysiology and management of pulmonary embolism[J]. Int J Angiol, 2022, 31(3): 143-149. DOI:10.1055/s-0042-1756204 |
| [21] | Düsing P, Zietzer A, Goody PR, et al. Vascular pathologies in chronic kidney disease: pathophysiological mechanisms and novel therapeutic approaches[J]. J Mol Med, 2021, 99(3): 335-348. DOI:10.1007/s00109-021-02037-7 |
| [22] | Rapp N, Evenepoel P, Stenvinkel P, et al. Uremic toxins and vascular calcification-missing the forest for all the trees[J]. Toxins, 2020, 12(10): 624. DOI:10.3390/toxins12100624 |
| [23] | Singh G, Bamba H, Inban P, et al. The prognostic significance of pro-BNP and heart failure in acute pulmonary embolism: a systematic review[J]. Disease-a-Month, 2024, 70(10): 101783. DOI:10.1016/j.disamonth.2024.101783 |
| [24] | Katterle KR, Niedoba MJ, Pasadyn VE, et al. Impact of baseline heart failure on acute pulmonary embolism risk stratification and clinical outcomes[J]. Am J Cardiol, 2023, 200: 26-31. DOI:10.1016/j.amjcard.2023.05.008 |
| [25] | Arrigo M, Huber LC. Pulmonary embolism and heart failure: a reappraisal[J]. Card Fail Rev, 2021, 7: e03. DOI:10.15420/cfr.2020.26 |
| [26] | Totoń-Żurańska J, Mikolajczyk TP, Saju B, et al. Vascular remodelling in cardiovascular diseases: hypertension, oxidation, and inflammation[J]. Clin Sci, 2024, 138(13): 817-850. DOI:10.1042/CS20220797 |
| [27] | Fang XY, Zhang YJ, Wu HR, et al. Mitochondrial regulation of diabetic endothelial dysfunction: Pathophysiological links[J]. Int J Biochem Cell Biol, 2024, 170: 106569. DOI:10.1016/j.biocel.2024.106569 |
| [28] | Petrie JR, Guzik TJ, Touyz RM. Diabetes, hypertension, and cardiovascular disease: clinical insights and vascular mechanisms[J]. Can J Cardiol, 2018, 34(5): 575-584. DOI:10.1016/j.cjca.2017.12.005 |
| [29] | Nader E, Romana M, Connes P. The red blood cell-inflammation vicious circle in sickle cell disease[J]. Front Immunol, 2020, 11: 454. DOI:10.3389/fimmu.2020.00454 |
| [30] | Papagiannaki M. Understanding and managing iron deficiency anaemia[J]. Nurs Stand, 2025, 40(3): 61-66. DOI:10.7748/ns.2025.e12430 |
| [31] | Yang C, Yokomori R, Chua LH, et al. Mitochondria transfer mediates stress erythropoiesis by altering the bioenergetic profiles of early erythroblasts through CD47[J]. J Exp Med, 2022, 219(12): e20220685. DOI:10.1084/jem.20220685 |
 2026, Vol. 35
2026, Vol. 35