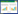患者男性,68岁, 因“恶心呕吐、剑突下及后背部疼痛6 d,加重3 d。”于2024年8月17日收入院。患者既往有难治性类风湿关节炎(rheumatoid arthritis, RA)病史7余年,曾多次因关节疼痛发作于我院治疗。患者于6 d前饮酒后出现恶心呕吐,呕吐物为胃内容物,随即出现剑突下及后背部疼痛, 呈持续性钝痛,自行口服胃药后胃部疼痛好转,未进一步治疗。3 d前患者自觉后背部持续疼痛不缓解且较前加重,深呼吸后明显,偶有咳嗽咳痰,痰呈白黏痰,易咳出,遂就诊于本院急诊,进行相关辅助检查化验。血常规:白细胞计数14.80×109/L, 单核细胞计数1.26×109/L, 中性粒细胞计数11.99×109/L;超敏肌钙蛋白T 0.492 ng/mL;肌酸激酶252 U/L、肌酸激酶同工酶22.4 U/L。心电图:①窦性心律;②广泛导联ST段抬高伴PR段压低、部分导联TP段下移。心脏超声:①室间隔增厚;②二、三尖瓣反流(轻度);③左室舒张功能减低(轻度);④心包积液(少量)(见图 2)。
|
| 图 1 患者心电图改变 |
|
|
|
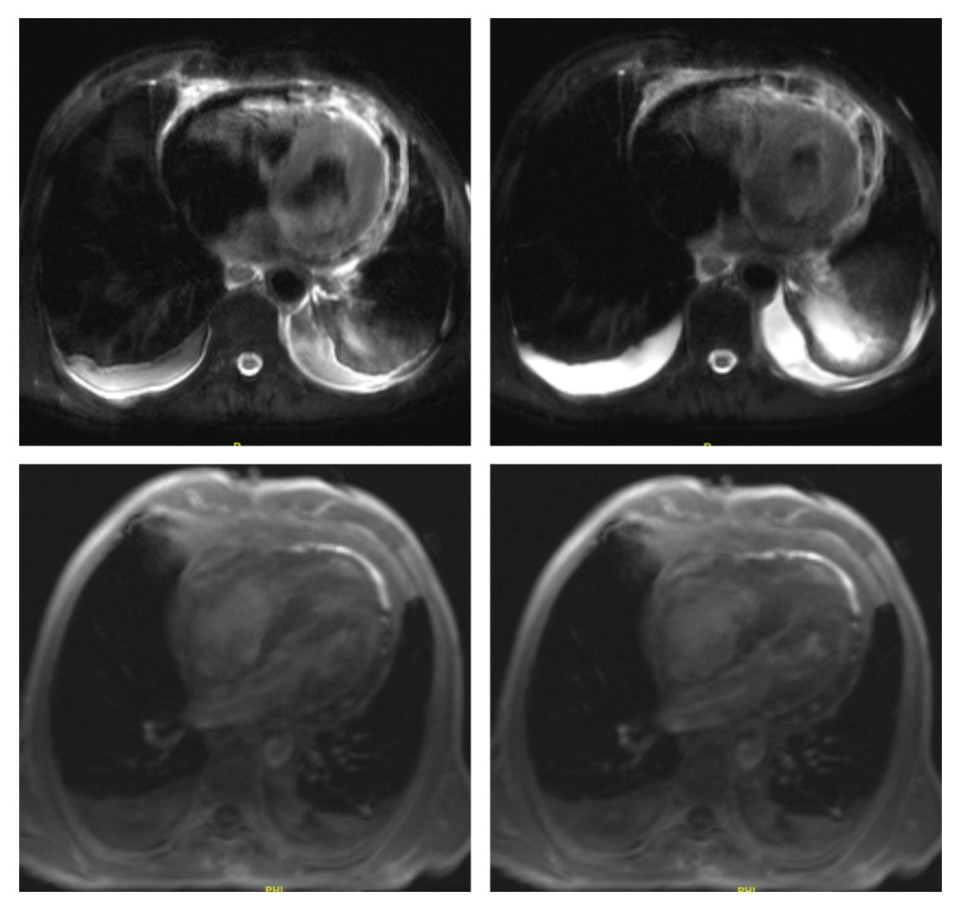
| 图 2 心脏磁共振检查图像 |
|
|
急诊医师结合患者疼痛症状、心肌标志损伤物升高及心电图广泛ST段抬高,误诊为急性心肌梗死,给予抗血小板、抗凝、抗心肌缺血等对症治疗后症状未见明显缓解, 遂行急诊冠脉造影术,见主支血管通畅未见狭窄,收入院治疗。查体:体温36.3℃,血压101/84 mmHg(1 mmHg=0.133 kPa),心率84次/min,双手掌指关节、近端指间关节肿胀伴压痛,余未见明显异常。患者入院第二天检验情况:血沉104 mm/h;超敏肌钙蛋白T 0.415 ng/mL;肌酸激酶93 U/L、肌酸激酶同工酶10 U/L;C-反应蛋白175.2 mg/L;白介素-6 221.27 pg/mL;类风湿全项:抗波形蛋白抗体MCV 287.48 U/mL抗环胍氨酸肽Ⅱ代抗体616.15 U/mL类风湿因子IgA>200 RU/mL类风湿因子IgM 350 IU/mL。心脏磁共振显示:双房增大,右心室增大,心包厚度约为5.2 mm,考虑急性心包炎累及心肌(见图 2)。根据临床表现及上述检查诊断为“心包心肌炎合并心包缩窄”,进一步完善检查,排除结核、肿瘤、创伤性炎症等相关的缩窄性心包炎,结合患者RA病史,考虑心包心肌炎合并心包缩窄与RA相关。经积极的药物治疗(营养心肌、改善心功能),患者症状明显改善,于2024年8月25日出院。
2 讨论心包炎的病因多种多样,大致分为感染性原因(病毒、细菌、真菌或寄生虫)和非感染性原因(自身免疫、肿瘤、代谢、创伤/医源性、药物相关和先天性畸形)[1]。缩窄性心包炎是一种罕见的晚期并发症,其特征是慢性心包炎,导致心包的增厚和钙化。缩窄性心包炎是类风湿关节炎的心脏并发症,临床中较为少见,可见于血清阳性的活动性RA患者,也可发生于血清阴性的RA患者,男性患者为发病的高危人群[2-3],通常由免疫介导机制和慢性炎症组合引起。RA的诊断和类风湿心包炎之间的中位间隔时间为9年,但范围从2个月到30年不等。在RA中,无症状心包炎的患病率为30%~50%,而急性心包炎的发生率不到10%[2]。2015年欧洲心脏病学会心包疾病诊断和管理指南[4]指出,符合以下四项标准中的至少两项就可以诊断急性心包炎:①胸痛、②心包摩擦音、③心电图上新发或广泛ST段抬高或PR压低、④影像学上有心包积液(新发或恶化)的证据。本例患者既往RA病史,此次以剑突下及后背部疼痛为主诉,疼痛症状与吸气有关,心电图可见PR段压低及Spodick征,炎症指标(血沉、白细胞计数)升高,心脏核磁即胸部CT可见心包积液,心包心肌炎合并心包缩窄诊断明确。
本例病例的启示如下。首先,临床怀疑和相关的辅助检查(如超声心动图、心脏磁共振等)在疑似心包疾病的诊断中发挥关键作用。本例患者主要以剑突下及后背部疼痛为主诉,查体未查到心脏相关阳性体征,辅助检查中心肌标志损伤物升高、心电图广泛ST段抬高,再加上本例患者当时于急诊做的床旁心彩超,由于彩超医师的经验限制,并未观察到心包增厚及钙化,最后导致误诊为急性ST段抬高型心肌梗死。值得注意的是,部分心包炎患者会以右心衰竭为首发症状,如外周水肿、腹水、胸腔积液等,查体可见Kussmaul征和闻及心包敲击音,此时应加强怀疑心包炎。第二,本例患者临床症状、心电图及相关辅助检查与急性ST段抬高型心肌梗死相似,患者心电图除了ST段抬高外,部分导联还有PR段压低及Spodick征即TP段下斜,这是急性心包炎早期特征性心电图的改变。一项关于心包炎与急性ST段抬高型心肌梗死的研究显示,29%的心包炎患者存在Spodick征,而急性ST段抬高型心肌梗死患者中仅有5%[5]。因此,PR段压低及Spodick征是鉴别两者的重要依据,应当引起重视。当然,Spodick征有时在诊断心包炎时存在一定的隐匿性。如在心率过快时,由于P波和T波的靠近使T-P段消失,因此TP段下移表现为阴性[6]。第三,急性心包炎通常隐藏于胸痛患者中,本例患者心肌酶与肌钙蛋白均升高,考虑是由于急性心包炎累及心肌所致,这与心脏核磁的结果也一致。最后,对于缩窄性心包炎的治疗,药物治疗仅用于缓解症状,而心包切除术是唯一确定的治疗方法[7]。本例患者无右心衰竭症状,相关检查提示处于急性心包炎的早期,患者手术意愿不强烈,因此未行心包切除术。
总之,尽管RA不是心包炎常见的原因,但对于RA患者,尤其是没有其他潜在易感因素的男性患者中,应警惕此类疾病的发生。此外,Spodick征通常被临床医生忽视,急诊科医师应在胸痛患者中快速区分心包炎,以减少不必要的冠脉介入。
利益冲突 所有作者声明无利益冲突
| [1] | Goldar G, Garraud C, Sifuentes AA, et al. Autoimmune pericarditis: multimodality imaging[J]. Curr Cardiol Rep, 2022, 24(11): 1633-1645. DOI:10.1007/s11886-022-01785-3 |
| [2] | Kontzias A, Barkhodari A, Yao QP. Pericarditis in systemic rheumatologic diseases[J]. Curr Cardiol Rep, 2020, 22(11): 142. DOI:10.1007/s11886-020-01415-w |
| [3] | Sanghavi N, Ingrassia JP, Korem S, et al. Cardiovascular manifestations in rheumatoid arthritis[J]. Cardiol Rev, 2024, 32(2): 146-152. DOI:10.1097/CRD.0000000000000486 |
| [4] | Adler Y, Charron P, Imazio M, et al. 2015 ESC Guidelines for the diagnosis and management of pericardial diseases. Task force for the diagnosis and management of pericardial diseases of the European Society of Cardiology (ESC)[J]. G Ital Cardiol (Rome), 2015, 16(12): 702-738. DOI:10.1714/2088.22592 |
| [5] | 陈军, 郭继鸿. Spodick征(209)[J]. 临床心电学杂志, 2022, 31(1): 74. |
| [6] | Abdelazeem B, Kandah E, Borcheni M, et al. Spodick's sign: a case report and review of literature[J]. Cureus, 2020, 12(11): e11606. DOI:10.7759/cureus.11606 |
| [7] | Vitali C, Minniti A, Pignataro F, et al. Management of sjögren's syndrome: present issues and future perspectives[J]. Front Med, 2021, 8: 676885. DOI:10.3389/fmed.2021.676885 |
 2025, Vol. 34
2025, Vol. 34